Значение словосочетания «возбуждённое состояние атома»
1. энергетически нестабильное, неустойчивое состояние атома, образуемое из основного состояния при переходе одного или нескольких электронов (из-за получения энергии извне) с занятых орбиталей на свободные или занятые лишь одним электроном
Все значения словосочетания «возбуждённое состояние атома»
Значение слова «возбуждённый»
ВОЗБУЖДЁННЫЙ, —ая, —ое. 1. Прич. страд. прош. от возбудить.
Все значения слова «возбуждённый»
Значение слова «атом»
А́ТОМ, -а, м. Наименьшая частица химического элемента, которая является носителем его химических свойств.
Все значения слова «атом»
Предложения со словосочетанием «возбуждённые атомы»
-
Теорией о спонтанном возникновении фотонов в излучении возбуждённых атомов – эффект без причины – учёные как кувалдой могли размахивать в спорах о кантианской причинности природы.
-
Эта ядерная реакция экзотермическая – лишняя освободившаяся энергия, как и в случае возбуждённого атома, сбрасывается в виде ядерного гамма-излучения.
-
Одним из источников этого монополя может быть быстрое торможение электрона в электрическом поле возбуждённого атома при его переходе на одно из низших состояний.
- (все предложения)
Ассоциации к слову «возбуждённый»
- возбуждение
- возбудитель
- (ещё ассоциации…)
Ассоциации к слову «атом»
- химия
- частицы
- физика
- молекула
- микрочастица
- (ещё ассоциации…)
Сочетаемость слова «возбуждённый»
- возбуждённое состояние
- возбуждённый гул голосов
- выглядел возбуждённым
- (полная таблица сочетаемости…)
Сочетаемость слова «атом»
- мирный атом
- атом водорода
- ядро атома
- атом распадается
- состоять из атомов
- (полная таблица сочетаемости…)
Морфология
- Разбор по составу слова «возбуждённый»
- Разбор по составу слова «атом»
Правописание
- Как правильно пишется слово «возбуждённый»
- Как правильно пишется слово «атом»
На букву В Со слова «возбуждённые»
Фраза «возбуждённые атомы»
Фраза состоит из двух слов и 17 букв без пробелов.
- Синонимы к фразе
- Написание фразы наоборот
- Написание фразы в транслите
- Написание фразы шрифтом Брайля
- Передача фразы на азбуке Морзе
- Произношение фразы на дактильной азбуке
- Остальные фразы со слова «возбуждённые»
- Остальные фразы из 2 слов

Видеоурок по химии «Валентные возможности атомов. Степень окисления»

Как можно увидеть атом?

Тема 1.18 Возбужденное состояние атома

Физика света. Фильм 4. Свет и атомы

Квантовый мир Документальный фильм National Geographic HD Документальные фильмы 2020

Почему вещи твердые Если атомы пустые!
Синонимы к фразе «возбуждённые атомы»
Какие близкие по смыслу слова и фразы, а также похожие выражения существуют. Как можно написать по-другому или сказать другими словами.
Фразы
- + абсолютный нуль температуры −
- + быстрые нейтроны −
- + векторная сумма −
- + диэлектрическая проницаемость −
- + зависит от длины волны −
- + заряд ядра −
- + заряжённые частицы −
- + излучать фотоны −
- + ионная связь −
- + калибровочные бозоны −
- + ложный вакуум −
- + межзвёздное облако −
- + оптический диапазон −
- + процесс сжатия −
- + сдвиг фаз −
- + силовые линии пространства −
- + слабое ядерное взаимодействие −
- + спектр поглощения −
- + структура вещества −
- + тепловое равновесие −
- + физические поля −
- + химический потенциал −
- + эквивалентная масса −
- + электронное нейтрино −
Ваш синоним добавлен!
Написание фразы «возбуждённые атомы» наоборот
Как эта фраза пишется в обратной последовательности.
ымота еыннёджубзов 😀
Написание фразы «возбуждённые атомы» в транслите
Как эта фраза пишется в транслитерации.
в латинской🇬🇧 vozbuzhdyonnye atomy
Как эта фраза пишется в пьюникоде — Punycode, ACE-последовательность IDN
xn--90abhede9bad6c6e3c xn--80ayfp1c
Как эта фраза пишется в английской Qwerty-раскладке клавиатуры.
djp,e;l`yystfnjvs
Написание фразы «возбуждённые атомы» шрифтом Брайля
Как эта фраза пишется рельефно-точечным тактильным шрифтом.
⠺⠕⠵⠃⠥⠚⠙⠡⠝⠝⠮⠑⠀⠁⠞⠕⠍⠮
Передача фразы «возбуждённые атомы» на азбуке Морзе
Как эта фраза передаётся на морзянке.
⋅ – – – – – – – ⋅ ⋅ – ⋅ ⋅ ⋅ ⋅ ⋅ – ⋅ ⋅ ⋅ – – ⋅ ⋅ ⋅ – ⋅ – ⋅ – ⋅ – – ⋅ ⋅ – – – – – – – – ⋅ – –
Произношение фразы «возбуждённые атомы» на дактильной азбуке
Как эта фраза произносится на ручной азбуке глухонемых (но не на языке жестов).
Передача фразы «возбуждённые атомы» семафорной азбукой
Как эта фраза передаётся флажковой сигнализацией.
Остальные фразы со слова «возбуждённые»
Какие ещё фразы начинаются с этого слова.
- возбуждённые возгласы
- возбуждённые голоса
- возбуждённые крики
- возбуждённые лица
- возбуждённые люди
- возбуждённые зрители
- возбуждённые гости
- возбуждённые мужские голоса
- возбуждённые глаза
- возбуждённые дети
- возбуждённые молодые люди
- возбуждённые соски
- возбуждённые разговоры
- возбуждённые солдаты
- возбуждённые горожане
- возбуждённые нервы
- возбуждённые умы
- возбуждённые воины
- возбуждённые лошади
- возбуждённые студенты
- возбуждённые чувства
- возбуждённые пассажиры
- возбуждённые туристы
- возбуждённые выкрики
Ваша фраза добавлена!
Остальные фразы из 2 слов
Какие ещё фразы состоят из такого же количества слов.
- а вдобавок
- а вдруг
- а ведь
- а вот
- а если
- а ещё
- а именно
- а капелла
- а каторга
- а ну-ка
- а приятно
- а также
- а там
- а то
- аа говорит
- аа отвечает
- аа рассказывает
- ааронов жезл
- аароново благословение
- аароново согласие
- аб ово
- абажур лампы
- абазинская аристократия
- абазинская литература
Комментарии

14:40
Что значит фраза «возбуждённые атомы»? Как это понять?..
Ответить

16:59

×
Здравствуйте!
У вас есть вопрос или вам нужна помощь?
Спасибо, ваш вопрос принят.
Ответ на него появится на сайте в ближайшее время.
А Б В Г Д Е Ё Ж З И Й К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Ъ Ы Ь Э Ю Я
Транслит Пьюникод Шрифт Брайля Азбука Морзе Дактильная азбука Семафорная азбука
Палиндромы Сантана

Народный словарь великого и могучего живого великорусского языка.
Онлайн-словарь слов и выражений русского языка. Ассоциации к словам, синонимы слов, сочетаемость фраз. Морфологический разбор: склонение существительных и прилагательных, а также спряжение глаголов. Морфемный разбор по составу словоформ.
По всем вопросам просьба обращаться в письмошную.
Атомно-молекулярное учение
Мы приступаем к изучению химии — мира молекул и атомов. В этой статье мы рассмотрим базисные понятия и разберемся с электронными
формулами элементов.
Атом (греч. а — отриц. частица + tomos — отдел, греч. atomos — неделимый) — электронейтральная частица вещества микроскопических
размеров и массы, состоящая из положительно заряженного ядра (протонов) и отрицательно заряженных электронов (электронные орбитали).
Описываемая модель атома называется «планетарной» и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом

Протон (греч. protos — первый) — положительно заряженная (+1) элементарная частица, вместе с нейтронами образует ядра атомов
элементов. Нейтрон (лат. neuter — ни тот, ни другой) — нейтральная (0) элементарная частица, присутствующая в ядрах всех
химических элементов, кроме водорода.
Электрон (греч. elektron — янтарь) — стабильная элементарная частица с отрицательным электрическим зарядом (-1), заряд атома —
порядковый номер в таблице Менделеева — равен числу электронов (и, соответственно, протонов).
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20)
в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.

Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило:
порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим
электроны занимают различные энергетические уровни.
Энергетические уровни подразделяются на несколько подуровней:
- Первый уровень
- Второй уровень
- Третий уровень
- Четвертый уровень
Состоит из s-подуровня: одной «1s» ячейки, в которой помещаются 2 электрона (заполненный электронами — 1s2)
Состоит из s-подуровня: одной «s» ячейки (2s2) и p-подуровня: трех «p» ячеек (2p6), на которых
помещается 6 электронов
Состоит из s-подуровня: одной «s» ячейки (3s2), p-подуровня: трех «p» ячеек (3p6) и d-подуровня:
пяти «d» ячеек (3d10), в которых помещается 10 электронов
Состоит из s-подуровня: одной «s» ячейки (4s2), p-подуровня: трех «p» ячеек (4p6), d-подуровня:
пяти «d» ячеек (4d10) и f-подуровня: семи «f» ячеек (4f14), на которых помещается 14
электронов

Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число
электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а
также узнаете об исключении, которое только подтверждает данные правила.
Подуровни: «s», «p» и «d», которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или
атомным орбиталям, движутся электроны, создавая определенный «рисунок».
S-орбиталь похожа на сферу, p-орбиталь напоминает песочные часы, d-орбиталь — клеверный лист.

Правила заполнения электронных орбиталей и примеры
Существует ряд правил, которые применяют при составлении электронных конфигураций атомов:
- Сперва следует заполнить орбитали с наименьшей энергией, и только после переходить к энергетически более высоким
- На орбитали (в одной «ячейке») не может располагаться более двух электронов
- Орбитали заполняются электронами так: сначала в каждую ячейку помещают по одному электрону, после чего орбитали дополняются
еще одним электроном с противоположным направлением - Порядок заполнения орбиталей: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было
бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе.
Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Без практики теория мертва, так что приступает к тренировке. Нам нужно составить электронную конфигурацию атомов углерода и
серы. Для начала определим их порядковый номер, который подскажет нам число их электронов. У углерода — 6, у серы — 16.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.

Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил.
А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся
одним электроном дополнили первую ячейку.
Таким образом, электронные конфигурации наших элементов:
- Углерод — 1s22s22p2
- Серы — 1s22s22p63s23p4
Внешний уровень и валентные электроны
Количество электронов на внешнем (валентном) уровне — это число электронов на наивысшем энергетическом уровне, которого достигает элемент. Такие электроны называются валентными: они могут быть спаренными или неспаренными. Иногда
для наглядного представления конфигурацию внешнего уровня записывают отдельно:
- Углерод — 2s22p2 (4 валентных электрона)
- Сера -3s23p4 (6 валентных электронов)
Неспаренные валентные электроны способны к образованию химической связи. Их число соответствует количеству связей, которые данный атом может образовать с другими атомами. Таким образом неспаренные валентные электроны тесно связаны с валентностью — способностью атомов образовывать определенное число химических связей.

- Углерод — 2s22p2 (2 неспаренных валентных электрона)
- Сера -3s23p4 (2 неспаренных валентных электрона)
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных
электронов. Ниже будет дано наглядное объяснение этой задаче.

Запишем получившиеся электронные конфигурации магния и скандия:
- Магний — 1s22s22p63s2
- Скандий — 1s22s22p63s23p64s23d1
В целом несложная и интересная тема электронных конфигураций отягощена небольшим исключением — провалом электрона, которое только подтверждает общее
правило: любая система стремится занять наименее энергозатратное состояние.
Провал электрона
Провалом электрона называют переход электрона с внешнего, более высокого энергетического уровня, на предвнешний, энергетически более
низкий. Это связано с большей энергетической устойчивостью получающихся при этом электронных конфигураций.
Подобное явление характерно лишь для некоторых элементов: медь, хром, серебро, золото, молибден. Для примера выберем хром, и рассмотрим
две электронных конфигурации: первую «неправильную» (сделаем вид, будто мы не знаем про провал электрона) и вторую правильную, написанную
с учетом провала электрона.
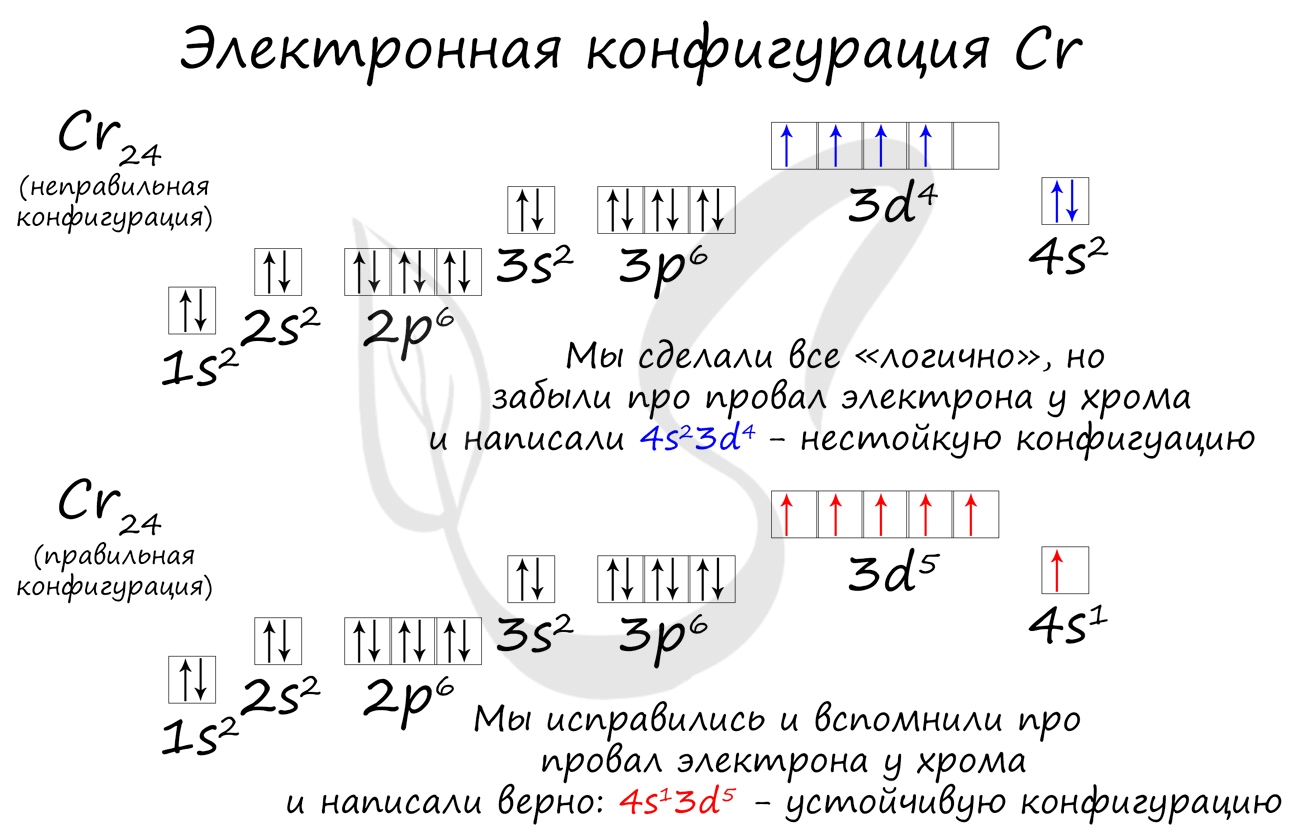
Теперь вы понимаете, что кроется под явлением провала электрона. Запишите электронные конфигурации хрома и меди самостоятельно еще раз и
сверьте с представленными ниже.

Основное и возбужденное состояние атома
Основное и возбужденное состояние атома отражаются на электронных конфигурациях. Возбужденное состояние связано с движением электронов
относительно атомных ядер. Говоря проще: при возбуждении пары электронов распариваются и занимают новые ячейки.
Возбужденное состояние является для атома нестабильным, поэтому долгое время в нем он пребывать не может. У некоторых атомов: азота,
кислорода , фтора — возбужденное состояние невозможно, так как отсутствуют свободные орбитали («ячейки») — электронам некуда перескакивать, к тому
же d-орбиталь у них отсутствует (они во втором периоде).
У серы возможно возбужденное состояние, так как она имеет свободную d-орбиталь, куда могут перескочить электроны. Четвертый энергетический
уровень отсутствует, поэтому, минуя 4s-подуровень, заполняем распаренными электронами 3d-подуровень.
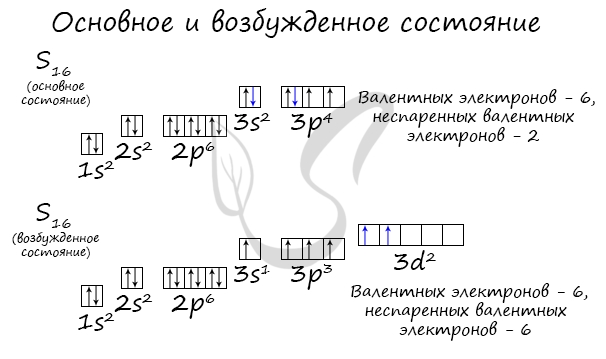
По мере изучения основ общей химии мы еще не раз вернемся к этой теме, однако хорошо, если вы уже сейчас запомните, что возбужденное состояние
связано с распаривание электронных пар.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Содержание
- 1 Русский
- 1.1 Тип и синтаксические свойства сочетания
- 1.2 Произношение
- 1.3 Семантические свойства
- 1.3.1 Значение
- 1.3.2 Синонимы
- 1.3.3 Антонимы
- 1.3.4 Гиперонимы
- 1.3.5 Гипонимы
- 1.4 Этимология
- 1.5 Перевод
- 1.6 Библиография
Русский[править]
Тип и синтаксические свойства сочетания[править]
возбуждённое состояние атома
Устойчивое сочетание (термин). Используется в качестве именной группы.
Произношение[править]
- МФА: [vəzbʊˈʐdʲɵnːəɪ̯ə səstɐˈjænʲɪɪ̯ə ˈatəmə]
Семантические свойства[править]
Значение[править]
- энергетически нестабильное, неустойчивое состояние атома, образуемое из основного состояния при переходе одного или нескольких электронов (из-за получения энергии извне) с занятых орбиталей на свободные или занятые лишь одним электроном ◆ Отсутствует пример употребления (см. рекомендации).
Синонимы[править]
Антонимы[править]
Гиперонимы[править]
- возбуждённое состояние
Гипонимы[править]
- первое возбужденное состояние
Этимология[править]
Перевод[править]
| Список переводов | |
Библиография[править]
|
|
Статья нуждается в доработке.
Это незаконченная статья. Вы можете помочь проекту, исправив и дополнив её.
(См. Общепринятые правила). |
Содержание
- Основное отличие — основное состояние от возбужденного состояния
- Что такое основное состояние
- Что такое возбужденное состояние
- Разница между основным состоянием и возбужденным состоянием
Основное отличие — основное состояние от возбужденного состояния
Атомы состоят из атомного ядра и электронов, которые находятся в движении вокруг этого ядра. Электроны не имеют определенного местоположения в атоме; у них есть только «вероятность» быть где-то вокруг ядра. Согласно этим вероятностям, ученые обнаружили дискретные энергетические уровни, которые с наибольшей вероятностью содержат электроны. Эти энергетические уровни содержат электроны, имеющие определенное количество энергии. Энергетические уровни, которые находятся рядом с атомным ядром, имеют более низкую энергию по сравнению с более дальними энергетическими уровнями. Когда атому дается определенное количество энергии, он переходит в возбужденное состояние из основного состояния из-за движения электрона с более низкого энергетического уровня на более высокий энергетический уровень. Основное различие между основным состоянием и возбужденным состоянием состоит в том, что Основное состояние — это состояние, в котором электроны в системе находятся на минимально возможных уровнях энергии, тогда как возбужденное состояние — это любое состояние системы, которое имеет более высокую энергию, чем основное состояние.
Ключевые области покрыты
1. Что такое основное состояние
— определение, объяснение
2. Что такое возбужденное состояние
— определение, объяснение
3. В чем разница между основным состоянием и возбужденным состоянием
— Сравнение основных различий
Ключевые слова: атом, атомное ядро, электрон, уровень энергии, возбужденное состояние, основное состояние, вакуумное состояние
Что такое основное состояние
Основное состояние относится к состоянию, в котором все электроны в системе (атом, молекула или ион) находятся на минимально возможных уровнях энергии. Следовательно, известно, что основное состояние не имеет энергии по сравнению с возбужденным состоянием, поскольку электроны находятся на нулевом энергетическом уровне. Основное состояние также называется вакуумное состояние.
Когда энергия подается на атом в основном состоянии, он может перейти в возбужденное состояние, поглощая энергию. Но время жизни возбужденного состояния меньше, поэтому атом возвращается в основное состояние, испуская поглощенную энергию, как показано на следующем рисунке.
Рисунок 1: Эмиссия поглощенной энергии
Следовательно, основное состояние является очень стабильным по сравнению с возбужденным состоянием и имеет более длительный срок службы. В атомах основного состояния расстояние между электронами и атомным ядром имеет наименьшее возможное расстояние. Электроны находятся ближе к атомному ядру.
Что такое возбужденное состояние
Возбужденное состояние атома относится к состоянию, которое имеет более высокую энергию, чем основное состояние этого атома. Здесь один или несколько электронов находятся не на самом низком уровне энергии. Электроны перешли на более высокий энергетический уровень, поглощая энергию извне. Но, чтобы перейти в возбужденное состояние, предоставленное количество энергии должно быть равно разности энергий между двумя уровнями энергии. В противном случае возбуждение не произошло бы.
Однако возбужденное состояние не является стабильным, поскольку более высокие уровни энергии не являются стабильными, и атомы имеют тенденцию возвращаться в основное состояние, испуская поглощенную энергию. Это излучение приводит к образованию электромагнитного спектра, который имеет эмиссионные линии.
Рисунок 2: Излучение поглощенной энергии из возбужденного состояния
Время жизни возбужденного состояния очень короткое, так как возбужденное состояние нестабильно из-за его высокой энергии. Здесь расстояние между атомным ядром и электронами не является наименьшим возможным расстоянием.
Разница между основным состоянием и возбужденным состоянием
Определение
Основное состояние: Основное состояние относится к состоянию, в котором все электроны в системе (атом, молекула или ион) находятся на минимально возможных уровнях энергии.
Возбужденное состояние: Возбужденное состояние — это любое состояние системы, которое имеет более высокую энергию, чем основное состояние.
энергии
Основное состояние: Известно, что основное состояние системы имеет «нулевую» энергию.
Возбужденное состояние: Возбужденное состояние системы обладает высокой энергией.
стабильность
Основное состояние: Основное состояние очень стабильно.
Возбужденное состояние: Возбужденное состояние крайне нестабильно.
Продолжительность жизни
Основное состояние: Основное состояние имеет длительный срок службы.
Возбужденное состояние: Возбужденное состояние имеет короткий срок службы.
Расстояние от атомного ядра
Основное состояние: Расстояние между электроном основного состояния и атомным ядром является наименьшим возможным расстоянием.
Возбужденное состояние: Расстояние между возбужденным состоянием электрона и атомным ядром больше, чем у основного состояния.
Расположение электронов
Основное состояние: В основном состоянии электроны находятся на минимально возможных уровнях энергии.
Возбужденное состояние: В возбужденном состоянии электроны находятся на более высоких энергетических уровнях.
Заключение
Основное состояние и возбужденное состояние системы связаны с движением электронов между двумя уровнями энергии. Основное различие между основным состоянием и возбужденным состоянием состоит в том, что основное состояние является состоянием, тогда как электроны в системе находятся на минимально возможных уровнях энергии, тогда как возбужденное состояние — это любое состояние системы, которое имеет более высокую энергию, чем основное состояние.
Ссылка:
1. «Основное состояние». OChemPal,




