Полные аналоги: 16
| Название | Форма выпуска | Владелец рег. уд. | ||
|
Айронгард |
Р-р д/в/в введения 20 мг/мл: амп. 2 мл или 5 мл 5 шт. рег. №: ЛП-005775 |
ФАРМАСИНТЕЗ (Россия) |
||
|
Айрондекст |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 5 шт. рег. №: ЛП-004509 |
ФАРМАЦЕВТИЧЕСКИЕ ПРОЕКТЫ (Россия) Произведено: GLAND PHARMA (Индия) |
||
|
АлвиферГем |
Р-р д/в/в введения 20 мг/мл: 5 мл амп. 5 или 10 шт. рег. №: ЛП-006931 |
АЛВИЛС (Россия) Произведено: ВИФИТЕХ (Россия) |
||
|
Аргеферр® |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 5 или 25 шт. рег. №: ЛСР-008788/10 |
GENFA MEDICA (Швейцария) Произведено и расфасовано: P.L. RIVERO Y CIA (Аргентина) Упаковка и выпускающий контроль качества: P.L. RIVERO Y CIA (Аргентина) ПРОТЕРА (Россия) |
||
|
Бинноферум® |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 5 или 10 шт. рег. №: ЛП-(000812)-(РГ-RU ) Предыдущий рег. №: ЛП-006021 |
БИННОФАРМ (Россия) |
||
|
Велферрум® |
Р-р д/в/в введения 100 мг/5 мл: амп. 5 мл 5 шт. рег. №: ЛП-002843 |
ВЕЛФАРМ (Россия) |
||
|
Железа (III) Гидроксид сахарозный комплекс |
Р-р д/в/в введения 20 мг/мл: 2 мл или 5 мл амп. 10 шт. рег. №: ЛП-006159 |
АльТро (Россия) Произведено: ЭКОФАРМПЛЮС (Россия) |
||
|
Железа (III) Гидроксид сахарозный комплекс |
Р-р д/в/в введения 20 мг/мл: амп. 5 мл 1, 3, 5, 10, 20, 25 или 50 шт. рег. №: ЛП-007337 |
ЭЛЛАРА (Россия) |
||
|
Железа (III) гидроксид сахарозный комплекс |
Р-р д/в/в введения 20 мг/мл: амп. 5 мл 5 или 10 шт. рег. №: ЛП-006554 |
БРЫНЦАЛОВ-А (Россия) |
||
|
Железа (III) Гидроксид сахарозный комплекс |
Р-р д/в/в введения 20 мг/мл: амп. 5 мл 5 шт. рег. №: ЛП-005089 |
БИОКАД (Россия) |
||
|
Железа (III) Гидроксид сахарозный комплекс |
Р-р д/в/в введения 20 мг/мл: амп. 5 мл 5 шт. рег. №: ЛП-006141 |
ДЖОДАС ЭКСПОИМ (Россия) Произведено: STANEX DRUGS & CHEMICALS PVT. LTD. (Индия) |
||
|
Железа [III] гидроксид сахарозный комплекс |
Р-р д/в/в введения 20 мг/мл: 2 мл или 5 мл амп. 5 шт. рег. №: ЛП-004118 |
ФАРМСТАНДАРТ-УфаВИТА (Россия) |
||
|
Ликферр 100® |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 3, 5, 6 или 24 шт.; , фл. 5 мл 1, 3 или 5 шт. рег. №: ЛСР-008006/10 |
ФармФирма Сотекс (Россия) Произведено: SAMRUDH PHARMACEUTICALS (Индия) Упаковано: ФармФирма Сотекс (Россия) контакты: ФармФирма Сотекс ЗАО (Россия) |
||
|
Ликферр 100® |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 3, 5, 6 или 24 шт.; фл. 5 мл 1, 3 или 5 шт. рег. №: ЛСР-008006/10 |
ФармФирма Сотекс (Россия) Произведено: EMCURE PHARMACEUTICALS (Индия) HELP (Греция) контакты: ФармФирма Сотекс ЗАО (Россия) |
||
|
Трикомбия |
Р-р д/в/в введения 20 мг/1 мл: амп. 2 мл 5 или 10 шт.; 5 мл 5, 10 или 25 шт. рег. №: ЛП-007512 |
ГРОТЕКС (Россия) |
||
|
Феррум Сандоз® |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 5 или 25 шт. рег. №: ЛП-005616 |
SANDOZ (Словения) Произведено: RAFARM (Греция) |
Информация о групповых и нозологических аналогах предназначена
только для
специалистов.
Групповые и нозологические аналоги не являются полными аналогами препаратов, решение об их использовании может быть принято только специалистом при назначении терапии в отсутствие препаратов первой линии.
Групповые аналоги: 4
| Название | Форма выпуска | Владелец рег. уд. | ||
|
Железа [III] Гидроксид декстран |
Раствор для внутривенного и внутримышечного введения 50 мг/мл рег. №: ЛП-008740 |
ВЕЛФАРМ (Россия) |
||
|
Космофер |
Р-р д/в/в и в/м введения 50 мг/мл: амп. 5 шт. рег. №: ЛС-002435 |
PHARMACOSMOS A/S (Дания) Произведено и упаковано: SOLUPHARM PHARMAZEUTISCHE ERZEUGNISSE (Германия) Выпускающий контроль качества: PHARMACOSMOS A/S (Дания) |
||
|
Монофер |
Р-р д/в/в введения 100 мг/1 мл: амп. 2 мл 5 или 10 шт., амп. 5 мл 2 или 5 шт. рег. №: ЛП-001499 |
PHARMACOSMOS A/S (Дания) Произведено и упаковано: SOLUPHARM PHARMAZEUTISCHE ERZEUGNISSE (Германия) Выпускающий контроль качества: PHARMACOSMOS A/S (Дания) |
||
|
Феринжект® |
Р-р д/в/в введения 50 мг/1 мл: фл. 2 мл 1 или 5 шт., 10 мл 1, 2 или 5 шт. рег. №: ЛСР-008848/10 |
VIFOR (International) (Швейцария) Произведено: IDT BIOLOGIKA (Германия) Выпускающий контроль качества: VIFOR (International) (Швейцария) контакты: ВИФОР (ИНТЕРНЭШНЛ) Инк. (Швейцария) |
Нозологические аналоги: 30
| Название | Форма выпуска | Владелец рег. уд. | ||
|
Актиферрин |
Капли д/приема внутрь 4.72 г+3.56 г/100 мл: фл. 30 мл с пробкой-капельницей рег. №: П N015041/03 |
Teva Pharmaceutical Industries (Израиль) Произведено: MERCKLE (Германия) контакты: ТЕВА (Израиль) |
||
|
Актиферрин |
Сироп 3.42 г+2.58 г/100 мл: фл. 1 шт. рег. №: П N015041/01 |
Teva Pharmaceutical Industries (Израиль) Произведено: MERCKLE (Германия) |
||
|
Биофер |
Таб. жевательные 100 мг+0.35 мг: 30 или 60 шт. рег. №: ЛСР-002336/09 |
MICRO LABS (Индия) контакты: МИКРО ЛАБС ЛИМИТЕД (Индия) |
||
|
Гематоген Л |
Пастилки жевательные: 6 или 10 шт. рег. №: ЛС-001818 |
ВОЗРОЖДЕНИЕ И РАЗВИТИЕ (Россия) |
||
|
Гематоген Новый |
Пастилки жевательные: 30 г рег. №: Р N000560/01 |
ВОЗРОЖДЕНИЕ И РАЗВИТИЕ (Россия) |
||
|
Гематоген Новый |
Пастилки жевательные: 50 г рег. №: Р N000560/01 |
ВОЗРОЖДЕНИЕ И РАЗВИТИЕ (Россия) |
||
|
Гематоген С |
Пастилки жевательные: 30 г рег. №: Р N000559/01 |
ВОЗРОЖДЕНИЕ И РАЗВИТИЕ (Россия) |
||
|
Гематоген С |
Пастилки жевательные: 50 г рег. №: Р N000559/01 |
ВОЗРОЖДЕНИЕ И РАЗВИТИЕ (Россия) |
||
|
Гематоген С Вита |
Плитки: 20 г, 30 г, 40 г или 50 г рег. №: Р N002929/01 |
ГЕНЕСС (Россия) Произведено: ГЕНЕСС (Россия) |
||
|
Гематоген С Вита |
Плитки: 20 г, 30 г, 40 г или 50 г рег. №: Р N002929/01 |
ГЕНЕСС (Россия) Произведено: ГЕНЕСС (Россия) ПК ФАРМ-ПРО (Россия) |
||
|
Гематоген с кедровым орехом |
Плитки: 50 г рег. №: Р N002928/01 |
ГЕНЕСС (Россия) |
||
|
Гино-Тардиферон® |
Таб. с модифицир. высвобождением, покр. пленочной оболочкой, 256.3 мг+350 мкг: 30 шт. рег. №: ЛС-000300 |
PIERRE FABRE MEDICAMENT (Франция) Произведено: Pierre Fabre Medicament Production (Франция) |
||
|
Мальтофер® |
Капли д/приема внутрь 50 мг/1 мл: фл. 30 мл с дозатором рег. №: П N011981/01 |
VIFOR (International) (Швейцария) Произведено: VIFOR (Швейцария) Выпускающий контроль качества: VIFOR (International) (Швейцария) контакты: ВИФОР (ИНТЕРНЭШНЛ) Инк. (Швейцария) |
||
|
Мальтофер® |
Сироп 10 мг/1 мл: фл. 150 мл в компл. с мерн. колпачком рег. №: П N011981/04 |
VIFOR (International) (Швейцария) Произведено: VIFOR (Швейцария) Выпускающий контроль качества: VIFOR (International) (Швейцария) контакты: ВИФОР (ИНТЕРНЭШНЛ) Инк. (Швейцария) |
||
|
Мальтофер® |
Таб. жевательные 100 мг: 30 шт. рег. №: П N011981/03 |
VIFOR (International) (Швейцария) Произведено: VIFOR (Швейцария) Выпускающий контроль качества: VIFOR (International) (Швейцария) контакты: ВИФОР (ИНТЕРНЭШНЛ) Инк. (Швейцария) |
||
|
Мальтофер® Фол |
Таб. жевательные 100 мг+0.35 мг: 30 шт. рег. №: П N011982/01 |
VIFOR (International) (Швейцария) Произведено: VIFOR (Швейцария) Выпускающий контроль качества: VIFOR (International) (Швейцария) контакты: ВИФОР (ИНТЕРНЭШНЛ) Инк. (Швейцария) |
||
|
Сорбифер Дурулес |
Таб., покр. пленочной оболочкой: 30 или 50 шт. рег. №: ЛП-(000080)-(РГ-RU ) Предыдущий рег. №: П N011414/01 |
EGIS Pharmaceuticals (Венгрия) |
||
|
Тардиферон® |
Таб. с пролонгир. высвобождением, покр. пленочной оболочкой, 80 мг: 30 шт. рег. №: ЛП-(000332)-(РГ-RU ) Предыдущий рег. №: П N013865/01 |
PIERRE FABRE MEDICAMENT (Франция) Произведено: Pierre Fabre Medicament Production (Франция) |
||
|
Тотема® |
Р-р д/приема внутрь: амп. 10 мл 20 шт. рег. №: П N015590/01 |
Laboratoire INNOTECH INTERNATIONAL (Франция) Произведено: INNOTHERA CHOUZY (Франция) |
||
|
Фенюльс® |
Капс.: 10, 30, 90 или 100 шт. рег. №: П N016072/01 |
SUN PHARMACEUTICAL INDUSTRIES (Индия) Произведено: NATCO PHARMA (Индия) |
||
|
Фер-Ромфарм |
Р-р д/в/м введен. 100 мг/2 мл: амп. 5 или 10 шт. рег. №: ЛП-002807 |
S.C. ROMPHARM Company (Румыния) |
||
|
Ферлатум |
Р-р д/приема внутрь 800 мг/15 мл: фл. 10 или 20 шт. рег. №: П N013855/01 |
ITALFARMACO (Италия) Произведено: ITALFARMACO (Испания) контакты: ИТАЛФАРМАКО С.п.А. (Италия) |
||
|
Ферлатум ФОЛ |
Р-р д/приема внутрь 800 мг/15 мл и порошок 235 мкг/100 мг: фл. с колпачком-контейнером 10 или 20 шт. рег. №: ЛСР-004031/07 |
ITALFARMACO (Италия) Произведено: ITALFARMACO (Испания) ABC FARMACEUTICI (Италия) Выпускающий контроль качества: ITALFARMACO (Испания) контакты: ИТАЛФАРМАКО С.п.А. (Италия) |
||
|
Ферретаб® Комп. |
Капс. пролонгированного действия 152.1 мг+0.5 мг: 30 шт. рег. №: П N013723/01 |
ACINO PHARMA (Швейцария) Произведено: G.L. PHARMA (Австрия) |
||
|
Ферро-Фольгамма Нео® |
|
Таб. с модифицированным высвобождением, покр. оболочкой, 36.77 мг+0.8 мг: 20, 30, 50 или 100 шт. рег. №: ЛП-(000586)-(РГ-RU ) |
WOERWAG PHARMA (Германия) Произведено: LOMAPHARM (Германия) контакты: ВЕРВАГ ФАРМА ООО (Россия) |
|
|
Феррогематоген |
Пастилки жевательные: 50 г рег. №: Р N003265/01 |
ФАРМСТАНДАРТ-УфаВИТА (Россия) |
||
|
Ферромальт |
Капли д/приема внутрь 50 мг/мл рег. №: ЛП-008751 |
АЛВИЛС (Россия) |
||
|
Феррум ЛЕК® |
Р-р д/в/м введен. 100 мг/2 мл: амп. 5 или 50 шт. рег. №: П N014059/01 |
SANDOZ (Словения) |
||
|
Феррум Лек® |
Сироп 50 мг/5 мл: фл. 100 мл в компл. с мерной ложкой рег. №: П N012698/02 |
SANDOZ (Словения) Произведено: GENVEON ILAC SANAYI VE TICARET (Турция) |
||
|
Феррум ЛЕК® |
Таб. жевательные 100 мг: 30 или 50 шт. рег. №: П N012698/01 |
SANDOZ (Словения) |
Классификация аналогов
-
Полные аналоги – препараты, имеющие в составе идентичные активные вещества и схожие формы
выпуска. -
Групповые аналоги (доступны специалистам) – препараты, содержащие активные вещества
со схожим механизмом действия и имеющие схожие формы выпуска. -
Нозологические аналоги (доступны специалистам) – могут быть использованы специалистами
при назначении терапии в отсутствие препаратов «первой линии».
Полные аналоги Венофер® по формам выпуска
|
Айронгард (PHARMASYNTEZ AO Россия) |
Р-р д/в/в введения 20 мг/мл: амп. 2 мл или 5 мл 5 шт. |
|
Айрондекст (Pharmaceutical Projects ООО Россия) |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 5 шт. |
|
АлвиферГем (ALVILS OOO Россия) |
Р-р д/в/в введения 20 мг/мл: 5 мл амп. 5 или 10 шт. |
|
Аргеферр® (GENFA MEDICA Швейцария) |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 5 или 25 шт. |
|
Бинноферум® (BINNOPHARM AO Россия) |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 5 или 10 шт. |
|
Велферрум® (VELPHARM OOO Россия) |
Р-р д/в/в введения 100 мг/5 мл: амп. 5 мл 5 шт. |
|
Железа (III) Гидроксид сахарозный комплекс (AlTro Россия) |
Р-р д/в/в введения 20 мг/мл: 2 мл или 5 мл амп. 10 шт. |
|
Железа (III) Гидроксид сахарозный комплекс (ELLARA OOO Россия) |
Р-р д/в/в введения 20 мг/мл: амп. 5 мл 1, 3, 5, 10, 20, 25 или 50 шт. |
|
Железа (III) гидроксид сахарозный комплекс (BRINTSALOV-A PAO Россия) |
Р-р д/в/в введения 20 мг/мл: амп. 5 мл 5 или 10 шт. |
|
Железа (III) Гидроксид сахарозный комплекс (BIOCAD AO Россия) |
Р-р д/в/в введения 20 мг/мл: амп. 5 мл 5 шт. |
|
Железа (III) Гидроксид сахарозный комплекс (JODAS EXPOIM OOO Россия) |
Р-р д/в/в введения 20 мг/мл: амп. 5 мл 5 шт. |
|
Железа [III] гидроксид сахарозный комплекс (PHARMSTANDARD-UfaVITA OAO Россия) |
Р-р д/в/в введения 20 мг/мл: 2 мл или 5 мл амп. 5 шт. |
|
Ликферр 100® (PharmFirma Sotex ZAO Россия) |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 3, 5, 6 или 24 шт.; , фл. 5 мл 1, 3 или 5 шт. |
|
Ликферр 100® (PharmFirma Sotex ZAO Россия) |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 3, 5, 6 или 24 шт.; фл. 5 мл 1, 3 или 5 шт. |
|
Трикомбия (GROTEX OOO Россия) |
Р-р д/в/в введения 20 мг/1 мл: амп. 2 мл 5 или 10 шт.; 5 мл 5, 10 или 25 шт. |
|
Феррум Сандоз® (SANDOZ d.d. Словения) |
Р-р д/в/в введения 20 мг/1 мл: амп. 5 мл 5 или 25 шт. |
| 💯 Аналоги | Есть |
| 💯 Полные аналоги | 16 |
| 💯 Групповые аналоги | 4 |
| 💯 Нозологические аналоги | 30 |
Выберите тип аналогов (синонимов), чтобы получить список препаратов.
Аналоги по действующему веществу — препараты, которые содержат одно и то же активное вещество, но выпускаются под разными торговыми наименованиями.
Для того чтобы подобрать полный аналог по действующему веществу, необходимо также выбрать дозировку и лекарственную форму.
Аналоги по фармгруппе — препараты, которые содержат разные действующие вещества, но относятся к одной фармакологической группе и применяются по одинаковым
показаниям.
Аналоги по АТХ — препараты, относящиеся к одному уровню АТХ-классификации.
Состав
В одном миллилитре препарата Венофер содержится: 540 мг гидроксида железа (III) в форме сахарозного комплекса, вода очищенная для инъекций, гидроксид натрия.
Форма выпуска
Лекарство выпускают в виде раствора в ампулах по 2 мл, по 5 ампул в контурной упаковке, 1 упаковка в картонной пачке.
Раствор однородный, коричневый.
Фармакологическое действие
Противоанемическое.
Фармакодинамика и фармакокинетика
Действующее вещество представляет собой многоядерные центры атомов железа, с валентностью 3, окруженные снаружи большим количеством не ковалентно связанных молекул сахарозы. Комплекс оказывается достаточно тяжелым, порядка 43 кД, что не позволяет ему быстро выводиться из организма с помощью почек. Комплекс достаточно стабилен, не склонен выделять ионы железа. Молекулы железа в комплексе сходны с естественной составляющей гемоглобина ферритином. Данный комплекс был разработан для обеспечения контролируемого освоения железа, его транспорта и сохранения ферритина и трансферрина в организме.
После первого укола препарата максимальная концентрация железа в крови достигается через 10 минут после инъекции.
Период полувыведения составляет 6 часов. Уровень распределения железа в жидких средах достаточно низкий.
Сахарат железа нестабилен, поэтому за сутки происходит перенос около 31 мг железа.
В первые 4 час, порядка 5% железа выводится через почки. Спустя сутки уровень железа в крови становится прежним, около 75% сахарозы выводится из плазмы.
Показания к применению
Венофер могут назначить:
- для быстрого восстановления уровня железа в организме при железодефицитной анемии;
- лицам, которые не переносят и не в состоянии принимать железосодержащие средства в виде таблеток;
- если имеются повреждения, перфорации или заболевания ЖКТ, при которых прием таблетированной формы невозможен.
Противопоказания
Лекарство не назначают:
- при прочих видах анемий (гемолитической, мегалобластической, при нарушении эритропоэза или гипоплазии костного мозга);
- если у пациента аллергия на какой-либо из компонентов средства;
- в первом триместре беременности;
- при гемосидерозе, гемохроматозе, перенасыщении организма железом;
- при нарушениях процессов утилизации железа в организме (отравление свинцом, талассемия, сидероахрестическая анемия, кожная порфирия).
Побочные эффекты
Наиболее распространенные побочные эффекты от приема средства: дисгевзия, озноб, снижение артериального давления, тошнота, покраснение и воспаление в месте введения. Очень редко могут развиться анафилактоидные реакции.
Также возникали:
- привкус металла во рту, головокружение и головная боль;
- миалгия, спазмы мышц, рвота, тошнота, понос;
- крапивница и высыпания на коже, эритема;
- тахикардия, одышка, брадикардия, ощущение сердцебиения, снижение АД, циркуляторный коллапс, бронхоспазм;
- лихорадка, приливы, тяжесть в груди, потливость.
Редко наблюдались парестезии, артралгия, артериальная гипертензия, потеря или спутанность сознания, боль в спине, отечность суставов, зуд на коже, астения, ощущение жара, ангиоэдема и сильное утомление пациента.
Если во время введения препарата произошло случайное вытекание средства под кожу, могут проявиться: боль и воспаление в месте укола, некроз тканей, кожа приобретет коричневый оттенок.
Инструкция по применению Венофера (Способ и дозировка)
Лекарство можно вводить исключительно внутривенно, непосредственно в вену или капельно.
Перед тем, как произвести первую инъекцию, следует ввести тест-дозу. Необходимо держать наготове реанимационный набор. Если в течение 15 минут не проявились, какие-либо из нежелательных реакций, можно вводить оставшуюся часть раствора.
Тестовая доза для взрослых и лиц, с весом более 14 кг – 20 мг железа, для детей – 1,5 мг на кг веса.
Как правило, дозировка средства для взрослых составляет 5-10 мл Венофера, от 1 до 3 раз в 7 дней.
Для детей от трех лет назначают не более 0,15 мг препарат на один кг веса, 1-3 раза в 7 дней.
Инструкция по применению Венофера, внутривенное капельное введение средства
Данный вид инъекции является более безопасным и эффективным, снижается вероятность попадания раствора под кожу, снижается риск развития артериальной гипотензии.
Перед инфузией препарат разводят в р-ре натрия хлорида (0,9 %) в соотношении 1 к 20-ти. Так 1 мл средства разводят в 20 мл хлорида натрия, 5 мл – в 100 мл, 25 мл – в 500 мл.
Скорость введения раствора определяется по схеме:
- 100 мг железа – 15 минут;
- 200 мг – 30 мин.;
- вводить 300 мг железа рекомендуется на протяжении 90 минут;
- 400 мг – 2,5 часа;
- 500 мг – 3,5 часа.
Максимальная допустимая разовая дозировка составляет 7 мг железа на один килограмм веса пациента. Вводить ее следует не менее, чем за 3,5 часа.
Внутривенное струйное введение
Инъекция производится неразведенным препаратом со скоростью 1 мл в минуту, однако максимальное кол-во лекарства составляет 10 мл за один укол.
При таком способе ввода также необходимо производить тестовую инъекцию. Для взрослых – 1 мл, для детей – 1,5 мг железа на кг, в течение минуты.
Расчет дозировки производится по формуле: масса тела (кг) х Hb (г/л) х 0,24 + депонированное железо (мг), где
- Hb (при весе менее 35кг) = 130 грамм на литр; депонированное железо = 15 мг на кг;
- при весе более 35 мг, Hb=150 г/л, депонированное железо = 500 мг.
Если терапевтическая доза выше, чем высчитанная суточная, то прием средства следует производить кратно.
Улучшения в показателях крови и состоянии больного должны наступить через 7-14 дней после начала лечения. Если этого не произошло, то диагноз нужно пересмотреть.
Расчет дозировки после больших кровопотерь или сдачи крови (донорской)
Если известно, какое количество крови было потеряно, то необходимая дозировка рассчитывается как кол-во единиц потерянной крови, умноженное на 200. Если же было снижено Hb, то используется та же формула, при условии, что не нужно восполнять депо железа.
Передозировка
В результате передозировки проявляются симптомы острой перегрузки железом – гемосидероза.
В качестве терапии показано использование симптоматических средств, веществ, связывающих хелаты (дефероксамина) внутривенно.
Взаимодействие
Не рекомендуется сочетать Венофер с железосодержащими таблетками, может снизиться абсорбция железа. Лечение такого рода препаратами должно проводиться не скорее, чем через 5 суток после последнего укола.
Условия продажи
Для приобретения ампул с лекарством может потребоваться рецепт.
Условия хранения
Препарат нельзя замораживать и хранить при температуре выше 27 градусов. Хранить в оригинальной упаковке.
Срок годности
36 месяцев.
Использовать раствор рекомендуется сразу после вскрытия ампулы.
После смешивания вещества с физ. раствором его можно хранить при температуре 18-20 градусов не более 12 часов.
Особые указания
Принимать средство можно только пациентам, которым диагноз был поставлен в соответствии с результатами анализов.
Не стоит использовать просроченные ампулы, если лекарство выпало в осадок, помутнело, ампула повреждена.
В связи с высоким риском развития анафилактоидных реакций у больных с поливалентной аллергией, дефицитом фолиевой кислоты, бронхиальной астмой и экземой, лечить данную группу пациентов с помощью инъекций Венофера нужно осторожно.
Рекомендуется соблюдать дозировку и скорость введения препарата, во избежание сильного понижения давления у пациентов или же усиления побочных эффектов.
Аналоги Венофера
Совпадения по коду АТХ 4-го уровня:
Существует ряд аналогов средства: Аргеферр, Ферролек-Здоровье, Декстрафер, Феринжект, Суфер, ФерМед, Железа Сахарата-железное вино, Феррум Лек, Фермед, Ликферр 100, Мальтофер.
При беременности и лактации
Лекарство нельзя использовать на первом триместре беременности.
Во время проведения исследований на животных, не было выявлено отрицательного воздействия средства на развитие плода, эмбриона, роды или его постнатальное развитие.
Перед тем, как назначить лекарство беременной, следует внимательно соотнести отношение риск/польза.
Сахарат железа не проникает в грудное молоко. Во время кормления грудью средство можно принимать только после консультации с врачом.
Отзывы о Венофере
Отзывов о средстве крайне мало. Препарат достаточно эффективен при борьбе с железодефицитной анемией в условиях стационара. Из побочных реакций чаще всего жалуются на отечность в ногах, тошноту и головокружение, которые проходят через некоторое время после инъекции.
Цена Венофера
Купить Венофер в Москве можно за 2972 рубля за 5 ампул.
Средняя цена Венофера составляет порядка 1900-2500 рублей.
- Интернет-аптеки РоссииРоссия
ЛюксФарма* специальное предложение
-
Венофер 100мг/5мл 5 шт. р-р для внутривенного введения
ЗдравСити
-
Венофер раствор для в/в введ. фл. 20мг/мл 5мл 5штАй Ди Ти Биологика ГмбХ/БИПСО ГмбХ
Аптека Диалог
-
Венофер (р-р в/в 20мг/мл 5мл фл. №5)Vifor/АйДиТи Биологика
показать еще
Венофер, инструкция по применению
- Производитель
- Страна происхождения
- Группа препаратов
- Действующее вещество
- Формы выпуска
- Упаковка
- Состав
- Дозировка
- Показания к применению
- Передозировка
- Противопоказания
- Побочные действия
- Способ применения
- Применение при беременности и кормлении грудью
- Фармакологическое действие
- Синонимы
- Фармакокинетика
- Взаимодействие с другими лекарствами
- Лекарственная форма
- Условия хранения
- Срок годности
- Особые условия
- Условия отпуска из аптек
Лекарственный препарат Венофер используется при железодефицитных состояниях, когда в короткий срок нужно устранить симптомы нехватки железа в организме. Средство зарекомендовало себя как безопасное и высокоэффективное. Побочные реакции у больных вызывает редко.
Производитель
Изготовлением медикамента занимается швейцарская фармацевтическая компания Vifor International Inc.
Страна происхождения
Швейцария.
Группа препаратов
Лекарство относится к фармакологическим группам «Макро- и микроэлементы», «Препараты железа (стимуляторы гемопоэза)».
Код АТХ: B03AC.
Действующее вещество
Активное соединение медикамента — железа (III) гидроксид сахарозный комплекс (Ferric (III) hydroxide sacharose complex).
Формы выпуска
Приобрести Венофер в аптеке можно только в виде водного раствора коричневого цвета, предназначенного для внутривенного введения. В форме таблеток или крема он не производится.
Упаковка
Средство разливают в стеклянные бесцветные ампулы. В контурной ячейковой упаковке находится 5 ампул. В картонной коробке одна контурная основа и подробная инструкция по применению.
Состав
Медикамент образуют:
- главное действующее вещество — железа (III) гидроксид сахарозный комплекс. Является высокоэффективным источником железа;
- вспомогательные компоненты: натрия гидроксид и вода для инъекций (не более 1 мл).
Дозировка
В официальном описании указано, что вводить раствор можно исключительно в вену (капельно или струйно) или венозный участок диализной системы. Запрещается делать инъекции в мышцу. Нельзя одномоментно вводить всю назначенную врачом дозу.
До начала терапии Венофером определяется тестовая дозировка. Если во время ее введения возникли нежелательные побочные реакции, дальнейшее использование лекарства запрещено.
Расчет терапевтической дозы осуществляется с учетом возникшего дефицита железа по особой формуле. При этом берутся во внимание показатели содержания гемоглобина в крови пациента и его массы тела. Формула выглядит следующим образом: «общий дефицит железа (мг) = масса тела (кг) х целевое содержание гемоглобина — фактическое содержание гемоглобина) [г/л] х 0,24 + депонированное железо [мг]».
Показания к применению
Лечиться препаратом нужно при:
- остром дефиците микроэлемента в организме;
- персональной непереносимости пероральных препаратов железа, невозможности соблюдать назначенный режим лечения;
- наличии прогрессирующего воспалительного заболевания кишечника, если железо в виде таблеток оказалось неэффективным.
Передозировка
Прием высоких доз лекарства Венофер может обусловить острую перегрузку железом. Тогда у пациента проявляются признаки гемосидероза. Имеются в виду гипохромная анемия, дыхательная недостаточность, кровотечения разной интенсивности, появление пигментных пятен и геморрагической сыпи.
Лечение передозировки должно быть симптоматическим. Если нужно, пациенту вводят средства, которые связывают железо.
Противопоказания
Запрещается использовать медикамент при индивидуальной непереносимости любого из соединений, входящих в его состав, при высокой чувствительности к железо-сахарозному комплексу. Также лекарство не подойдет, если анемия спровоцирована не дефицитом железа. Его нельзя применять при врожденных нарушениях реакции утилизации микроэлемента, наличии симптомов перегрузки железом. В I триместре беременности лечиться Венофером также запрещается.
С осторожностью препарат назначают лицам с:
- экземой;
- бронхиальной астмой;
- поливалентной аллергией;
- дефицитом фолиевой кислоты;
- инфекционными заболеваниями;
- высоким уровнем ферритина в сыворотке крови;
- печеночной недостаточностью;
- аллергией на парентеральные лекарства, содержащие железо.
Важно учитывать, что введение средства внутривенно может оказывать нежелательное влияние на течение имеющейся вирусной/бактериальной инфекции.
Побочные действия
Не все больные одинаково хорошо переносят терапию средством. У некоторых лекарство Венофер вызывает нежелательные побочные реакции. Так, со стороны центральной нервной системы возможны головокружения, головные боли, обмороки, парестезии. Со стороны сердечно-сосудистой системы в редких случаях возникают скачки кровяного давления, тахикардия, «приливы» крови к лицу. Иногда наблюдаются сбои в работе органов дыхательной системы. Тогда пациент жалуется на одышку и бронхоспазм.
Среди других возможных побочных реакций:
- боли в животе, эпигастральной области, тошнота, рвота, нарушения стула;
- кожные высыпания, изменение пигментации кожных покровов, усиленная потливость, зуд, эритема;
- болевые ощущения в области спины, артралгия, отеки суставов, дискомфорт в верхних и нижних конечностях, миалгия;
- отек лица, гортани, опасные анафилактоидные реакции;
- повышенная утомляемость, астения, бледность, озноб, повышение температуры тела.
Иногда место введения препарата Венофер воспаляется и становится болезненным на ощупь.
Способ применения
Средство можно вводить только в вену — путем капельной инфузии или медленной инъекции. Также разрешено его вливать непосредственно в венозный участок диализной системы. Нельзя ставить уколы в мышцу.
Перед применением раствора следует изучить ампулу на предмет отсутствия повреждений или наличия осадка. Можно использовать исключительно однородный состав коричневого цвета, в котором нет никакого осадка.
Каждая ампула предназначена для одноразового использования. Неиспользованные излишки следует утилизировать. Хранить их запрещено.
Во время лечения лекарством Венофер пациент должен находиться под постоянным врачебным контролем. Если возникнут симптомы анафилактической реакции, нужно сразу же прервать инфузионную терапию.
За больным необходимо наблюдать как минимум в течение получаса после каждого введения средства. Это позволит своевременно выявить опасные симптомы и купировать их.
Применение при беременности и кормлении грудью
Запрещается лечение медикаментом в первые 12 акушерских недель беременности. На сегодняшний день не проведены контролируемые исследования, которые бы позволили сделать вывод о возможности безопасного использования средства будущими мамами. В ходе тестирований на животных негативное влияние Венофера на эмбрион/плод выявлено не было.
В период грудного вскармливания лечиться препаратом можно. Считается, что поступление неметаболизированного сахарата железа в грудное молоко маловероятно. Лекарство не представляет опасности для детей, находящихся на грудном вскармливании.
Фармакологическое действие
Медикамент, разработанный для устранения железодефицитных состояний. Многоядерные центры железа (III) гидроксида окружены снаружи большим количеством нековалентно связанных молекул сахарозы. В итоге формируется комплекс, молекулярная масса которого около 43 кД.
Его выведение почками в неизмененном виде невозможно. Состав стабилен и в физиологических условиях не выделяет ионы железа. Железо в комплексе связано со структурами, сходными с естественным ферритином.
Синонимы
Среди аналогов препарата в аптеке представлено средство Ликферр100. Это тоже раствор для внутривенного введения, содержащий железа III гидроксид сахарозный комплекс. Его выпуском занимается отечественная фармацевтическая организация «Сотекс».
Фармакокинетика
При однократном введении в вену 100 мг железа максимальная концентрация микроэлемента, составляющая 538 мкмоль, наблюдается через 10 минут. Vd центральной камеры практически полностью соответствует объему сыворотки — примерно 3 л. Vd в равновесном состоянии — 8 л. Это доказывает низкое распределение микроэлемента в жидких средах организма.
За счет невысокой стабильности железа сахарата, в сравнении с трансферрином, фиксируется конкурентный обмен железа в пользу трансферрина. В итоге за сутки переносится около 31 мг железа (III).
Период полувыведения препарата — около 6 часов. В первые 4 часа за счет работы почек выводится менее 5% соединения от общего клиренса. Через 24 часа концентрация железа в сыворотке возвращается к исходному (до введения) значению. Около 75% сахарозы покидает сосудистое русло.
Взаимодействие с другими препаратами
Нельзя вводить Венофер вместе с другими лекарственными формами железа. Медикамент снижает всасывание микроэлемента из желудочно-кишечного тракта. Прием пероральных средств, включающих железо, можно начинать через 5 суток после введения последней инъекции.
Разрешается смешивать раствор в одном шприце только со стерильным физраствором. Нельзя добавлять к нему никакие другие препараты, так как существует высокий риск преципитации или иных нежелательных взаимодействий.
Совместимость лекарства с ампулами, изготовленными не из стекла, не изучена.
Лекарственная форма
Раствор для инфузий.
Условия хранения
Лекарство нужно хранить при температуре окружающей среды от 4 до 25 °C. Оно не подлежит замораживанию. Вскрытая ампула храниться не может.
Срок годности
С момента выпуска медикамент годен на протяжении 3 лет. Затем его следует утилизировать.
Особые условия
Можно использовать Венофер только в том случае, если диагноз «анемия» подтвержден лабораторной диагностикой.
Нужно учитывать, что препараты железа, вводимые в вену, способны вызывать опасные для здоровья и жизни анафилактоидные реакции.
При использовании высоких доз медикамента возрастает риск проявления побочных реакций. Иногда они бывают тяжелыми, провоцируют резкое падение кровяного давления.
Условия отпуска из аптек
Заказать Венофер в аптеке можно по врачебному рецепту.
Венофер — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
Торговое название:
Венофер® (Venofer®)
Международное непатентованное или группировочное название:
железа(III) гидроксид сахарозный комплекс
Лекарственная форма:
раствор для внутривенного введения
Состав:
1 мл препарата содержит:
Активное вещество:
железо(Ш) 20 мг
в виде железа(Ш) гидроксид сахарозного комплекса 510-570 мг
Вспомогательные вещества:
натрия гидроксид 0-5 мг
в виде 10 % раствора натрия гидроксида q.s. до доведения pH 10,5-11,0
вода для инъекций 580-640 мг
Описание
Водный раствор коричневого цвета.
Фармакотерапевтическая группа:
противоанемическое средство, препарат железа для парентерального введения.
Код АТХ:
В03АС
Фармакологические свойства
Фармакодинамика
Механизм действия
Активный компонент препарата Венофер® — железо-сахарозный комплекс — состоит из ядра многоядерного гидроксида железа(Ш), окруженного большим количеством нековалентно связанных молекул сахарозы. Средняя молекулярная масса этого комплекса примерно равна 43 кДа. Структура многоядерного железосодержащего ядра сходна со структурой ядра белка ферритина — физиологического депо железа. Этот комплекс предназначен для создания управляемого источника утилизируемого железа для белков, отвечающих за транспорт и депонирование железа в организме (соответственно трансферрина и ферритина).
После внутривенного введения многоядерное железосодержащее ядро этого комплекса захватывается преимущественно ретикулоэндотелиальной системой печени, селезенки и костного мозга. На следующем этапе железо используется для синтеза гемоглобина, миоглобина и других железосодержащих ферментов, либо хранится преимущественно в печени в форме ферритина.
Фармакокинетика
Распределение
Феррокинетика железо-сахарозного комплекса, меченного 52Fe и 59Fe, оценивалась у пациентов с анемией и хронической почечной недостаточностью. В течение первых 6-8 часов 52Fe захватывался печенью, селезенкой и костным мозгом. Считается, что захват радиоактивной метки селезенкой, богатой макрофагами, является типичным для захвата железа ретикулоэндотелиальной системой.
После внутривенного введения однократной дозы препарата Венофер®, содержащей 100 мг железа, здоровым добровольцам максимальные суммарные концентрации железа в сыворотке достигались через 10 минут после инъекции, при этом средняя концентрация составляла 538 μ моль/л. Объем распределения центральной камеры полностью соответствовал объему плазмы (около 3 л).
Биотрансформация
После инъекции сахароза по большей части распадается, а многоядерное железосодержащее ядро захватывается преимущественно ретикулоэндотелиальной системой печени, селезенки и костного мозга. Через 4 недели после введения утилизация железа эритроцитами составляет от 59 до 97 %.
Выведение
Средняя молекулярная масса железо-сахарозного комплекса примерно равна 43 кДа, что достаточно много для предотвращения выведения через почки.
Выведение железа почками в первые 4 часа после инъекции дозы препарата Венофер®, содержащей 100 мг железа, составляло менее 5 % от введенной дозы. Через 24 часа суммарная концентрация железа в сыворотке снижалась до уровня перед введением. Выведение сахарозы почками составляло около 75 % от введенной дозы.
Показания к применению
Венофер® применяется для лечения железодефицитных состояний в следующих случаях:
- при клинической потребности в быстром восполнении запасов железа;
- у пациентов, которые не переносят пероральные препараты железа или не соблюдают режим лечения;
- при наличии активного воспалительного заболевания кишечника, когда пероральные препараты железа неэффективны.
Противопоказания
Применение препарата Венофер® противопоказано в следующих случаях:
- повышенная чувствительность к железо-сахарозному комплексу, раствору железосахарозного комплекса или к любому из компонентов данного лекарственного препарата;
- анемия, не обусловленная дефицитом железа;
- наличие признаков перегрузки железом или врожденные нарушения процессов его утилизации;
- I триместр беременности.
С осторожностью
Пациентам с бронхиальной астмой, экземой, поливалентной аллергией, аллергическими реакциями на иные парентеральные препараты железа и лицам, имеющим низкую железосвязывающую способность сыворотки и/или дефицит фолиевой кислоты Венофер® нужно назначать с осторожностью. Также осторожность требуется при введении препаратов железа пациентам с печеночной недостаточностью, с острыми или хроническими инфекционными заболеваниями и лицам, у которых повышены показатели ферритина сыворотки крови в связи с тем, что парентерально вводимое железо может оказывать неблагоприятное действие при наличии бактериальной или вирусной инфекции.
Применение во время беременности и в период грудного вскармливания
Умеренное количество данных по применению препарата Венофер® беременными женщинами во II и III триместрах беременности не выявило каких-либо угроз для матери или новорожденного.
Однако Венофер® следует применять во время II и III триместра беременности только тогда, когда потенциальная польза для матери превышает потенциальный риск для плода.
Применение препарата в первом триместре беременности противопоказано.
Результаты исследований на животных не выявили прямых или опосредованных вредных воздействий на течение беременности, развитие эмбриона/плода, роды или постнатальное развитие.
Количество данных по выделению железа с грудным молоком человека после внутривенного введения железо-сахарозного комплекса ограничено. В рамках небольшого клинического исследования здоровые, кормящие грудью матери с дефицитом железа получали 100 мг железа в виде железо-сахарозного комплекса. Через 4 дня после лечения содержание железа в грудном молоке не повышалось, и разницы в сравнении с контрольной группой (n=5) не наблюдалось. Нельзя исключить тот факт, что железо из препарата Венофер® может поступать новорожденному/младенцу с молоком матери, поэтому следует проводить оценку соотношения риска и пользы.
Способ применения и дозы
Применение
Препарат Венофер® вводится только внутривенно: путем капельной инфузии, или медленной инъекции, или непосредственно в венозный участок диализной системы.
Перед использованием ампулы/флаконы следует осмотреть на предмет отсутствия осадка или повреждений. Использовать следует только ампулы/флаконы с однородным, не содержащим осадка раствором коричневого цвета.
Каждая ампула/флакон препарата Венофер® предназначены исключительно для одноразового использования. Любые остатки неиспользованного лекарственного препарата или его отходы следует утилизировать в соответствии с локальными требованиями.
Введение препарата Венофер® должно осуществляться под наблюдением медицинского персонала, имеющего опыт диагностики и лечения анафилактических реакций, в условиях специализированного отделения. Должна быть обеспечена возможность проведения противошоковой терапии, включающая 0,1 % раствор эпинефрина (адреналина), антигистаминные и/или кортикостероидные препараты. Тест-доза не является надежным прогностическим фактором развития в последующем реакций гиперчувствительности, в связи с чем ее предварительное введение не рекомендуется.
Во время введения препарата и непосредственно после введения пациенты должны находиться под наблюдением врача. При появлении первых признаков анафилактических реакций применение препарата должно быть немедленно прекращено.
Необходимо наблюдать за каждым пациентом в течение как минимум 30 минут после каждого введения препарата Венофер® в терапевтической дозе на предмет отсутствия нежелательных явлений.
Внутривенная капельная инфузия
Венофер® разводится только стерильным 0,9 % (масса/объем) раствором натрия хлорида (NaCl). Разведенный раствор должен быть прозрачным, коричневого цвета. Разведение следует производить непосредственно перед инфузией, а полученный раствор следует вводить следующим образом:
Разведение препарата до более низких концентраций железа недопустимо по причинам, связанным со стабильностью раствора.
Внутривенная инъекция
Венофер® может вводиться путем медленной внутривенной инъекции со скоростью 1 мл неразведенного раствора в минуту и его доза не должна превышать 10 мл (200 мг железа) на инъекцию.
Инъекция в венозный участок диализной системы
Венофер® можно вводить во время сеанса гемодиализа непосредственно в венозный участок диализной системы при соблюдении тех же условий, что и для внутривенной инъекции.
Дозы
Для каждого пациента следует индивидуально рассчитывать кумулятивную дозу препарата Венофер®, которую нельзя превышать.
Расчет дозы
Общая кумулятивная доза препарата Венофер®, эквивалентная общему дефициту железа (мг), определяется на основании содержания гемоглобина (Hb) и массы тела (МТ). Дозу препарата Венофер® следует индивидуально рассчитывать для каждого пациента в соответствии с общим дефицитом железа, рассчитанным по нижеприведенной формуле Ганзони, например:
Общий дефицит железа [мг] = масса тела [кг] х (целевое содержание гемоглобина -фактическое содержание гемоглобина) [г/л] х 0,24* + депонированное железо [мг]
При массе тела менее 35 кг: целевое содержание гемоглобина = 130 г/л, а количество депонированного железа = 15 мг/кг массы тела
При массе тела 35 кг и больше: целевое содержание гемоглобина = 150 г/л, а количество депонированного железа = 500 мг
* Коэффициент 0,24 = 0,0034 (содержание железа в гемоглобине = 0,34 %) х 0,07 (масса крови ~ 7 % от массы тела) х 1000 (перевод [г] в [мг])
Общее количество препарата Венофер®, которое следует ввести (в мл) = Общий дефицит железа [мг] / 20 мг железа/мл
Общее количество препарата Венофер® (мл), которое следует ввести, в зависимости от массы тела, фактического содержания гемоглобина и целевого содержания гемоглобина* :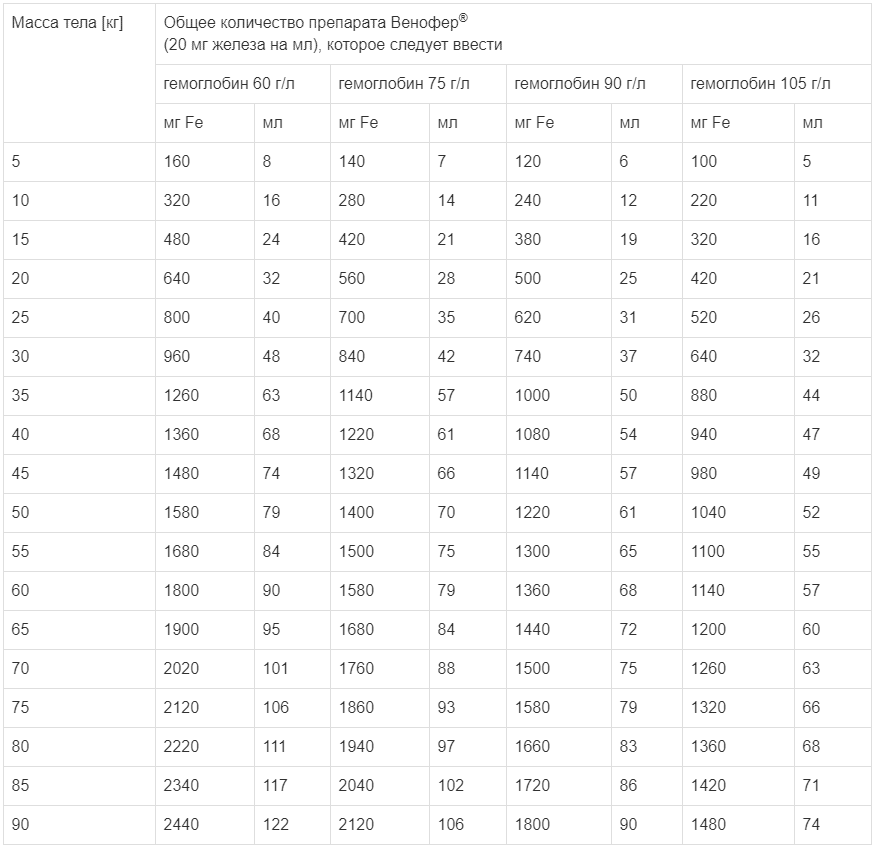
* При массе тела менее 35 кг: Целевое содержание гемоглобина = 130 г/л
При массе тела 35 кг и больше: Целевое содержание гемоглобина = 150 г/л
Для перевода гемоглобина (ммоль) в гемоглобин (г/л) умножьте первое значение на 16. Если общая необходимая доза превышает максимальную дозволенную однократную дозу, ее следует разделить на несколько введений.
Если через 1-2 недели не наблюдается ответа со стороны гематологических параметров, первоначальный диагноз следует пересмотреть.
Расчет дозы для восполнения запасов железа после кровопотери или при сдаче аутологичной крови
Дозу препарата Венофер®, необходимую для компенсации дефицита железа, можно рассчитать по следующим формулам:
Если количество потерянной крови известно: введение 200 мг железа (10 мл препарата Венофер®) должно приводить приблизительно к такому же повышению концентрации гемоглобина, что и переливание 1 порции крови (400 мл с концентрацией гемоглобина = 150 г/л).
Количество железа, которое необходимо восполнить [мг] = количество порций потерянной крови х 200 мг
или
Необходимый объем препарата Венофер® [мл] = количество порций потерянной крови х 10 мл
Если содержание гемоглобина ниже желаемого: формула предполагает, что депо железа пополнять не требуется.
Количество железа, которое необходимо восполнить [мг] = масса тела [кг] х 0,24 х (целевое содержание гемоглобина — фактическое содержание гемоглобина) [г/л]
Пример:
При массе тела = 60 кг и снижении содержания гемоглобина = 10 г/л
⇒≈150 мг железа необходимо восполнить
⇒ необходимо 7,5 мл препарата Венофер®
Максимальная переносимая разовая и недельная дозы указаны ниже в разделах «Стандартные дозы» и «Максимальная переносимая разовая и недельная дозы».
Стандартные дозы
Пациенты взрослого и пожилого возраста
5-10 мл препарата Венофер® (100-200 мг железа) 1-3 раза в неделю.
Время введения препарата и способ разведения указаны в разделе «Применение».
Дети
Имеется лишь умеренное количество данных о применении препарата у детей в рамках исследований. В случае клинической необходимости применения не рекомендуется превышать дозу 0,15 мл препарата Венофер® (3 мг железа) на кг массы тела не чаще 3 раз в неделю.
Время введения препарата и способ разведения указаны в разделе «Применение».
Максимально переносимая разовая и недельная дозы
Пациенты взрослого и пожилого возраста
Максимальная переносимая доза в сутки, вводимая в виде инъекции не чаще 3 раз в неделю:
- 10 мл препарата Венофер® (200 мг железа), вводимые в течение минимум 10 минут.
Максимальная переносимая доза в сутки, вводимая в виде инфузии не чаще 1 раза в неделю:
- Пациенты с массой тела более 70 кг: 500 мг железа (25 мл препарата Венофер®), вводимые в течение минимум 3,5 часов.
- Пациенты с массой тела 70 кг и менее: 7 мг железа/кг массы тела, вводимые в течение минимум 3,5 часов.
Следует строго придерживаться времени инфузии, указанного в разделе «Применение», даже если пациент не получил максимальной переносимой разовой дозы.
Побочное действие
Наиболее частой нежелательной лекарственной реакцией (НЛР), регистрировавшейся в рамках клинических исследований препарата Венофер®, являлось изменение вкусовых ощущений, которое наблюдалось с частотой 4,5 явления на 100 субъектов. Наиболее важными серьезными нежелательными лекарственными реакциями, связанными с применением препарата Венофер®, являлись реакции гиперчувствительности, которые наблюдались в рамках клинических исследований с частотой 0,25 явления на 100 субъектов.
В таблице ниже представлены нежелательные лекарственные реакции, зарегистрированные после применения препарата Венофер® в рамках клинических исследований, а также в пострегистрационном периоде.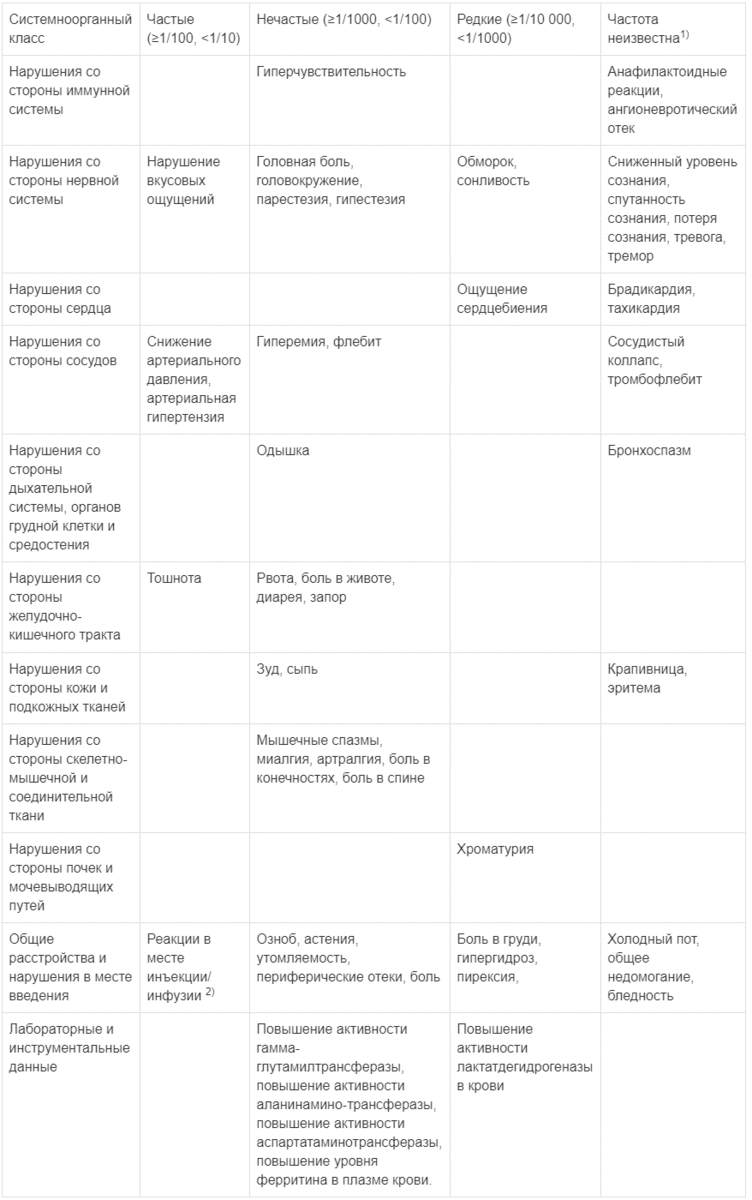
1)Спонтанные сообщения, полученные в пострегистрационном периоде
2)Наиболее частые: боль в месте инъекции/инфузии, экстравазация в месте инъекции/инфузии, раздражение в месте инъекции/инфузии, реакция в месте инъекции/инфузии, изменение окрашивания кожи в месте инъекции/инфузии, кровоподтек в месте инъекции/инфузии, зуд в месте инъекции/инфузии.
Передозировка
Передозировка может вызывать перегрузку железом, которая может проявляться симптомами гемосидероза. Передозировку следует лечить с использованием хелатирующего средства для связывания железа или в соответствии со стандартами медицинской практики.
Взаимодействие с другими лекарственными средствами
Как и при применении всех парентеральных препаратов железа, препарат Венофер® не рекомендуется применять одновременно с пероральными препаратами железа, поскольку всасывание перорального железа может снижаться, поэтому терапию пероральными препаратами железа следует начинать не ранее, чем через 5 дней после последней инъекции.
Венофер можно смешивать только со стерильным 0,9 % (масса/объем) раствором натрия хлорида. При смешивании с другими растворами или лекарственными препаратами имеется риск выпадения осадка и/или взаимодействия. Совместимость с контейнерами из других материалов, помимо стекла, полиэтилена и поливинилхлорида, не изучена.
Особые указания
Парентерально вводимые препараты железа могут вызывать аллергические или анафилактоидные реакции, которые потенциально могут быть летальными, поэтому в наличии должны иметься противоаллергические препараты, а также оборудование для проведения сердечно-легочной реанимации и соответствующих процедур. После предшествовавших неосложненных введений парентеральных комплексов железа также отмечались реакции гиперчувствительности. После каждой инъекции препарата Венофер® за всеми пациентами следует наблюдать на предмет отсутствия нежелательных явлений в течение как минимум 30 минут.
Пациентам, имеющим в анамнезе бронхиальную астму, экзему, другие виды атопических аллергий или аллергические реакции на другие парентеральные препараты железа, препарат Венофер® следует применять с осторожностью, поскольку такие пациенты в особенности могут иметь риск развития аллергической реакции.
Пациентам с нарушением функции печени парентеральное железо следует применять только после тщательной оценки соотношения риска и пользы. Пациентам с нарушением функции печени, когда перегрузка железом является провоцирующим фактором, не следует применять парентеральное железо. Для того чтобы избежать перегрузки железом, рекомендуется проводить тщательный мониторинг уровня железа в организме.
Парентеральное железо следует применять с осторожностью при наличии острой или хронической инфекции. Пациентам с бактериемией рекомендуется прекратить применение препарата Венофер®. У пациентов с хронической инфекцией следует провести оценку соотношения риска и пользы.
Следует избегать проникновения препарата в околовенозное пространство, поскольку это может привести к появлению боли, развитию воспаления и окрашиванию кожи в коричневый цвет. В случаях непреднамеренного проникновения препарата в околовенозное пространство лечение следует проводить в соответствии со стандартами медицинской практики.
Венофер® следует применять только в тех случаях, когда показание к применению подтверждено результатами соответствующих исследований (например, уровень ферритина в сыворотке, уровень насыщения трансферрина, содержание гемоглобина (Hb), эритроцитарные показатели — MCV, MCH, MCHC).
Срок годности после первого вскрытия контейнера
С микробиологической точки зрения, препарат следует использовать незамедлительно.
Срок годности после разведения 0,9 % раствором натрия хлорида (NaCl)
Химическая и физическая стабильность после разведения при комнатной температуре (15-25 °С) составляет 12 часов. Однако с микробиологической точки зрения, препарат следует использовать сразу после разведения. Если препарат не был использован сразу же после разведения, тот, кто использует данный раствор, несёт ответственность за условия и время хранения после разведения, которое в любом случае не должно превышать 3 часов при комнатной температуре, кроме тех случаев, когда разведение было выполнено в контролируемых и надлежащих асептических условиях.
Влияние на способность управлять транспортными средствами или работать с другими механизмами
Данных о влиянии на способность управлять транспортными средствами или работать с другими механизмами не имеется. Однако некоторые нежелательные реакции (такие, как головокружение, спутанность сознания и прочие (указаны в разделе «Побочное действие»)) могут оказывать негативное влияние на способность управлять транспортными средствами или работать с другими механизмами. Пациентам, у которых отмечаются данные нежелательные реакции, рекомендовано воздержаться от управления транспортными средствами или работы с другими механизмами до полного исчезновения данных симптомов.
Форма выпуска
Раствор для внутривенного введения 20 мг/мл.
По 5 мл препарата в бесцветные, прозрачные стеклянные ампулы (тип I по Евр. Ф.), имеющие насечку на шейке ампулы и технические цветные метки в виде одного или двух ободков и точки.
По 5 мл препарата в бесцветные, прозрачные стеклянные флаконы (тип I по Евр. Ф.), закрытые эластичной пробкой и алюминиевым колпачком с отрывным элементом.
По 5 ампул или флаконов в контурной ячейковой упаковке из поливинилхлорида вместе с инструкцией по применению упаковывают в картонную пачку.
Условия хранения
В оригинальной упаковке при температуре не выше 25 °С.
Препарат не подлежит замораживанию.
Хранить в местах, недоступных для детей.
Срок годности
3 года.
Не применять по истечении срока годности.
Условия отпуска
По рецепту.
Юридическое лицо, на имя которого выдано регистрационное удостоверение / Компания, осуществляющая выпускающий контроль качества
Вифор (Интернэшнл) Инк.
Рехенштрассе 37, 9014 Ст. Галлен, Швейцария
Vifor (International) Inc.
Rechenstrasse 37, 9014 St. Gallen, Switzerland
Производитель
БИПСО ГмбХ, Роберт-Гервиг-Штрассе 4, 78224 Зинген, Германия
(BIPSO GmbH, Robert-Gerwig-Strasse 4, 78224 Singen, Germany)
АйДиТи Биологика ГмбХ, Ам Фармапарк, 06861 Дессау-Росслау, Германия
(IDT Biologika GmbH, Am Pharmapark, 06861 Dessau-Rosslau, Germany)
Организация, принимающая претензии потребителей
ООО «Такеда Фармасьютикалс»
119048, г. Москва, ул. Усачева, д. 2, стр. 1
Купить Венофер в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)

