Оглавление
Ключевые слова
- Болезнь малых ножек подоцита;
- болезнь минимальных изменений;
- нефротический синдром;
- стероидзависимый нефротический синдром;
- стероидрезистентный нефротический синдром;
- стероидчувствительный нефротический синдром;
Список сокращений
БМИ – болезнь минимальных изменений
БРА – блокаторы рецепторов ангиотензина
ГН – гломерулонефрит
СЗ СЧНС – стероидзависимая форма стероид-чувствительного нефротического синдрома
и-АПФ – ингибиторы ангиотензинпревращающего фермента
КНИ – кальцинейрина ингибиторы
ММФ – микофенолат мофетил
МК – микофеноловая кислота
МП – метилпреднизолон
НС – нефротический синдром
ОРВИ – острая респираторная вирусная инфекция
РААС – ренин-ангиотензин-альдостероновая система
рСКФ – расчетная скорость клубочковой фильтрации
СРНС – стероидрезистентный нефротический синдром
ФСГС – фокально-сегментаоный гломерулосклероз
ЧР – часто-рецидивирующий
NPHS1 – ген нефрина
NPHS2 – ген подоцина
PLCE1 – фосфолипаза С эпсилон 1
TRPC-6 – потенциал- зависимый временный рецептор катионов 6
NEPH1 – нефриноподобный белок 1
CD2AP – CD2-ассоциированный протеин
ZO-1 – белок плотных контактов (zonula occludens 1)
WT-1 – белок опухоли Вильмса 1
LMX1B – LIM гомеобокс фактор транскрипции 1бета (LIM homeobox transcription factor 1, beta)
SMARCAL1 – подобный, ассоциированный с матриксом; актин- зависимый регулятор хроматина, белок 1 подсемейства альфа
INF2 – инвертированный формин 2.
Термины и определения
Ангиотензин (ангио- + лат. Tensio напряжение; син.: ангиотонин, гипертензин) — биологически активный полипептид, образующийся из ангиотензиногена, повышающий артериальное давление в результате сужения кровеносных сосудов.
Ангиотензин I — неактивная форма а., представляющая собой декапептид, образующийся из ангиотензиногена под действием ренина; предшественник ангиотензина II.
Ангиотензин II — активная форма а., представляющая собой октапептид, образующийся из ангиотензина I под действием пептидазы.
Ангиотензиноген (ангиотензин + греч. -genes порождающий; син. Гипертензиноген) — сывороточный глобулин, образующийся в печени и являющийся предшественником ангиотензина.
Биопсия — микроскопическое исследование прижизненно иссеченных или изъятых другим способом тканей и органов с диагностической целью.
Биоптат — материал, полученный путем биопсии.
Гиперкортицизм – синдром, обусловленный избыточным содержанием в крови кортикостероидов.
Гиперхолестеринемия (hypercholesterinaemia; гипер- + холестерин + греч. Haima кровь; син. Холестеринемия) — повышенное содержание холестерина в крови.
Гипоальбуминемия (hypoalbuminaemia; гипо- + альбумин + греч. Haima кровь) — уменьшенное содержание альбуминов в сыворотке крови; наблюдается при поражениях паренхимы печени, нефротическом синдроме и т. Д.
Гиповолемия (oligaemia; олиг- + греч. Haima кровь) — уменьшенное общее количество крови.
Гипопротеинемия (hypoproteinaemia; гипо- + протеинемия) — пониженное содержание белка в сыворотке крови, наблюдается при его недостаточном поступлении в организм или значительных потерях.
Гломерула (glomerula)- клубочек, часть функциональной единицы почек-нефрона, ответственный за фильтрационную функцию почек.
Гломерулонефрит (glomerulonephritis; гломеруло- + нефрит; син. Брайтова болезнь — устар.) — двустороннее диффузное воспаление почек с преимущественным поражением клубочков.
Гломерулопатия — состояние, при котором отмечается патологические изменения в клубочковом аппарате почек любого генеза
Денситометрия (денсито- + греч. Metreo измерять, определять) —измерение оптической плотности фотопластинки или фотопленки, слоя геля, бумаги и т. Д.; используется, напр., при анализе рентгено- и хроматограмм.
Кушинга синдром (н. W. Cushing; син. Иценко — кушинга синдром) — сочетание характерных изменений внешнего вида больного (ожирение с преимущественным отложением жира на животе и задней части шеи, лунообразное яйцо, гирсутизм, наличие атрофических полос на коже) с артериальной гипертензией, остеопорозом, мышечной слабостью, снижением переносимости глюкозы, у женщин — также с нарушениями менструального цикла; наблюдается при гиперфункции коры надпочечников (чаще при наличии гормонально-активной опухоли), а также при длительном лечении препаратами адренокортикотропного или кортикостероидных гормонов.
Нефротический синдром (НС) — клинико-лабораторный симптомокомплекс, характеризующийся протеинурией, гипоальбуминемией , диспротеинемией, гиперлипидемией, отеками, в том числе полостными.
Протеинурия (proteinuria; протеины + греч. uron моча; син. альбуминурия — устар.) — повышенное содержание белка в моче.
Подоцит — видоизмененный эпителий в структуре клубочкового аппарата почек.
Подоцитопатия — состояние, характеризующееся видоизменением структуры подоцита, обусловленное различными механизмами(иммунными и неиммунными).
Стероидчувствительный НС — наличие эффективности стероидной терапии с достижением полной клинико-лабораторной ремиссии.
Стероидрезистентный НС — отсутствие эффективности стероидной терапии в дозе 60 мг/м2/сут (2 мг/кг/сут) в течение 8 недель, или в дозе 60 мг/м2/сут (2 мг/кг/сут) в течение 6 недель и трех последовательных пульсов метилпреднизолона в дозе 1000 мг/1,73м2 при разовом введении.
Стероидзависисмый НС — развитие рецидива НС при снижении дозы преднизолона или в течение 2 недель после отмены преднизолона.
Фильтрация клубочковая (син. фильтрация гломерулярная) — совокупность процессов перехода веществ, содержащихся в крови, через стенку капилляра клубочка почки в полость его капсулы, что приводит к образованию первичной мочи.
1. Краткая информация
1.1 Определение
Болезнь минимальных изменений (БМИ) – это непролиферативная гломерулопатия, не имеющая каких-либо морфологических критериев при световой микроскопии, обусловленная повреждением (иммунным или неиммунным) подоцитов (подоцитопатия), которое диагностируется исключительно при ультраструктурном анализе в виде диффузного слияния ножковых отростков подоцитов. Повреждение подоцита определяет формирование в клинике заболевания нефротического синдрома (НС).
1.2 Этиология и патогенез
Определенного этиологического фактора при болезни минимальных изменений нет. Однако при многих состояниях может возникнуть нефротический синдром с минимальными изменениями (см. табл.1)
Таблица 1
Состояния, ассоциированные с БМИ
Аллергия:
Пыльца
Грибы
Коровье молоко
Домашняя пыль
Укусы пчел, медуз
Шерсть кошки
Лекарственные препараты:
Нестероидные противовоспалительные препараты
Ампициллин
Препараты золота
Препараты лития
Ртуть-содержащие препараты
Триметадион
Злокачественные заболевания:
Болезнь Ходжкина
Неходжкинская лимфома
Рак толстой кишки
Карцинома легких
Другие:
Вирусная инфекция
Болезнь Кимуры
Сахарный диабет
Миастения Грависа
Вакцинация
В патогенезе БМИ следует рассматривать два механизма развития:
Иммуноопосредованный:
В настоящее время исследования in vivo и in vitro продемонстрировали высокую активность Т-лимфоцитов в ответ на антигенную стимуляцию. В последующем происходит дифференцировка Т-клеток с преимущественным образованием Тh2, экспрессирующих IL-4 и IL-13. Более того активация NFkB транскрипционного фактора наблюдается при всех случаях рецидивов НС при БМИ. Антагонистом NFkB является IkB, концентрация которого под влиянием глюкокортикоидов увеличивается. Эффективность ритуксимаба при лечении БМИ предполагает роль В-клеток в патогенезе БМИ. Одной из гипотез развития протеинурии при БМИ является повреждение щелевой диафрагмы, регулируемое экспрессией CD80 (В7-1) на подоцитах – трансмембранного протеина, экспрессирующегося на антиген-презентирующих клетках (АПК), натуральных киллерах и В-лимфоцитах. CD80 определяет ко-стимулирующий сигнал для Т-лимфоцитов, связываясь с последними посредством соединения с их рецепторами CD28. Данный механизм отмечается при представлении антигена АПК Т-клеткам с последующей их активацией. Однако связывание CD28 на Т-лимфоцитах с CTLA-4 – протеина, экспрессируемого на Foxp3+ регуляторных Т-клетках (Treg) ингибирует активацию последних. Мутация в гене Foxp3 у больных БМИ приводит к снижению активации Treg клеток, тем самым способствуя развитию протеинурии.
Неиммунный:
Структура подоцита изменяется в результате изменения структурных белков подоцитов, обусловленное мутациями генов. До 66% случаев НС на первом году жизни у детей составляет генетически обусловленный НС. Частота генетических форм НС у детей при идиопатическом НС неизвестна. Однако следует помнить морфологический диагноз БМИ у детей с генетически обусловленным НС носит транзиторный характер, так как в последующем он трансформируется в ФСГС. Неиммунный характер формирования БМИ определяет развитие стероид-резистентной формы БМИ.
1.3 Эпидемиология
- БМИ составляет 76,6 % всех морфологических вариантов первичного гломерулонефрита (ГН) у детей.
- Наибольшая встречаемость у детей раннего возраста.
- БМИ чаще отмечается у мальчиков в соотношении 2:1
- Возможны семейные формы, обусловленные мутациями генов структурных белков подоцита.
- Рецидивов в трансплантате нет.
1.4 Коды по МКБ-10
N04.0 — Нефротический синдром с незначительными гломерулярными нарушениями
1.5 Классификация
Официально утвержденной классификации болезни минимальных изменений нет. Однако с учетом этиологического фактора можно разделить данную патологию на две формы:
Первичная (идиопатическая) БМИ
Основой развития идиопатического нефротического синдрома у детей является дисфункция Т-клеточного звена иммунной системы или генетические мутации. Однако БМИ может быть ассоциирована с множеством других патологических состояний таких, как аллергия, онкопатология, лекарственные воздействия.
Генетически обусловленная БМИ (гены):
- Щелевой диафрагмы и цитоскелета подоцитов – NPHS1, NPHS2, TRCP6, CD2AP, ACTN4, INF2;
- Фосфолипазы – PLCE1;
- Гломерулярной базальной мембраны – LAMB2;
- Факторов транскрипции – WT1, LMX1B;
- Лизосомных белков – SCARB2;
- Митохондриальных белков – COQ2;
- Посредника реструктуризации ДНК-нуклеосомы — SMARCAL1.
2. Диагностика
Дифференциальную диагностику проводят с другими формами ГН, дебютировавшими НС (НГ). Дифференциальная диагностика проводится в случае развития стероидзависимой и стероидрезистентной формы НС. (1В)
Клинические проявления БМИ не различаются при идиопатическом и вторичном вариантах заболевания. В этой связи дифференциальная диагностика этих форм должна базироваться на исключении всех возможных вторичных причин БМИ (см. классификацию) (НГ).
Детальное морфологическое исследование ткани почки, включающее световую, иммуногистохимическую и электронную микроскопию, обязательно для диагностики БМИ (НГ).
Морфологические критерии БМИ
Световая микроскопия:
На светооптическом уровне – при БМИ клубочек выглядит не поврежденным, иногда может присутствовать минимальная мезангиальная пролиферация (до 3-х клеток), что создает трудности в дифференциации с минимальными изменениями при мезангиопролиферативном гломерулонефрите. У детей с часторецидивирующим БМИ некоторые клубочки могут быть инволютированы.
Клетки канальцев инфильтрированы белками и липидами из-за увеличенной реабсорбции. Наличие атрофии и фиброза канальцев должны вызвать подозрение на наличие фокально-сегментарного гломерулосклероза.
Иммуногостохимия:
При иммуногистохимическом исследовании отмечается отсутствие отложения иммуноглобулионов и компонентов комплемента.
Электронная микроскопия:
Диффузное «сглаживание» ножек подоцитов является гистологическим маркером БМИ при сочетании с вышеизложенной световой микроскопией и иммуногистохимическим исследованием.
2.1 Жалобы и анамнез
Диагноз БМИ устанавливается на основании клинико-лабораторной картины НС и быстрому положительному ответу на стероидную терапию (НГ). Морфологическая диагностика является резервным методом при атипичном клиническом ответе на терапию.
- Клиническая диагностика идиопатической БМИ должна базироваться на развитии НС у детей раннего и дошкольного возраста (HГ).
- Наличие в анамнезе состояний, ассоциированных с БМИ (табл. 1) и ранний возраст дебюта НС следует рассматривать как факторы, определяющие развитие БМИ.
- Развитие НС на первом году жизни и в подростковом возрасте должны насторожить врача в пользу генетически обусловленного НС или другой морфологической формы НС.
- Клиническим синдромом БМИ является внезапно развившийся НС (протеинурия, гипоальбуминурия, гиперлипидемия). Отягощенный аллергологический анамнез и аллергические проявления у детей с БМИ наблюдаются в 30-70% случаев в отличие от других форм гломерулонефрита. Триггерными факторами могут быть ОРВИ, детские инфекции, атопические реакции (см. выше табл.1).
2.2 Физикальное обследование
Артериальная гипертензия наблюдается крайне редко и характеризуется кратковременностью. Повышение артериального давления при БМИ связано с компенсаторным механизмом на выраженную гиповолемию. При резкой гиповолемии возможно развитие нефротического криза с болями в животе, кожной эритемой и сердечно-сосудистым шоком с циркуляторной недостаточностью.
- Рекомендовано обратить внимание на отеки.
Уровень убедительности рекомендаций С (уровень достоверности –4)
Комментарии: Первым клиническим симптомом, заметным для больного и окружающих, являются отеки. Они могут развиться постепенно или же стремительно, достигнув степени анасарки. Периферические отеки выявляются в области век, лица, поясничной области и половых органов, могут распространяться на всю подкожную клетчатку, растягивая кожу до образования стрий. В это время у больных могут образовываться транссудаты в серозные полости: одно- или двусторонний гидроторакс, асцит, гидроперикард; возможно развитие отека легких.
2.3 Лабораторная диагностика
- Рекомендовано проведение клинического анализа крови и определение гематокритного показателя.
Уровень убедительности рекомендаций С (уровень достоверности –4)
Комментарии:
- Возможна умеренная анемия;
- Повышенный гематокрит (> 44%);
- Тромбоцитоз;
- Вторичный лейкоцитоз на фоне приема глюкокортикостероидов.
- Выраженное повышение СОЭ.
- Рекомендовано проведение биохимического анализа крови.
Уровень убедительности рекомендаций С (уровень достоверности –4)
Комментарии:
- Гипопротеинемия (<55г/л);
- Гиопаальбуминемия(<25г/л);
- Гиперхолестеринемия (>5,7ммоль/л);
- Диспротеинемия (повышение ?2-фракций глобулинов и снижение ?-глобулинов).
- Рекомендовано проведение общего анализа мочи.
Уровень убедительности рекомендаций С (уровень достоверности –4)
Комментарии:
-
- Выраженная протеинурия (> 3г/л);
- Редко микрогематурия до 10 эр. в п /зрения;
- Цилиндрурия (гиалиновые).
- Рекомендовано определение суточной экскреции белка для уточнения степени протеинурии.
Уровень убедительности рекомендаций С (уровень достоверности –4)
Комментарии: Протеинурия> 1г/м2/сутки или >40 мг/м2/сут. При невозможности определения суточной экскреции белка для уточнения степени протеинурии может быть использовано определение отношения уровня экскретируемого белка к креатинину в разовой порции мочи. Этот коэффициент достоверно коррелирует с уровнем суточной протеинурии/1,73м2 Экскреция белка (г/сут/1,73м2) = (белок г/л*0,088) /креатинин мочи (ммоль/л)
- Рекомендовано проведение коагулограммы.
Уровень убедительности рекомендаций С (уровень достоверности –4)
Комментарии:
- Гиперпротромбинемия;
- Гиперфибриногенемия;
- Повышения D-димеров;
- Снижение антитромбина III.
- Рекомендованы иммунологические исследования.
Уровень убедительности рекомендаций С (уровень достоверности – 4)
Комментарии: Возможно повышение IgE, Низкий уровень IgG.
- Рекомендованы определение СКФ методом Шварца.
Уровень убедительности рекомендаций С (уровень достоверности – 4)
- Рекомендованы проба Реберга для оценки клиренса эндогенного креатинина.
Уровень убедительности рекомендаций С (уровень достоверности – 4)
Комментарии: Возможно снижение клубочковой фильтрации и клиренса эндогенного креатинина в активную стадию на фоне выраженной гиповолемии.
- Рекомендовано генетическое (гены см. выше) исследование в случае, если НС наблюдается до 1 года и при стероидрезистентной форме.
Уровень убедительности рекомендаций С (уровень достоверности – 4)
2.4 Инструментальная диагностика
- Рекомедовано проведение ЭКГ- электрографические признаки гидроперикарда.
Уровень убедительности рекомендаций С (уровень достоверности – 4)
- Рекомедовано проведение Эхо-ЭКГ — эхографические признаки гидроперикарда.
Уровень убедительности рекомендаций С (уровень достоверности – 4)
- Рекомендовано проведение ультразвукового исследования почек.
Уровень убедительности рекомендаций С (уровень достоверности – 4)
Комментарии: Увеличение размеров почек, гипоэхогенность коркового слоя;
- Рекомендовано денситометрия поясничного отдела позвоночника или рентгенография трубчатых костей для оценки степени деминерализации костной ткани;
Уровень убедительности рекомендаций С (уровень достоверности – 4)
- Рекомендована пункционная биопсия почек (по показаниям) в случае, если дебют заболевания раннее 1 года и старше 12 лет, стероидрезистентная форма.
Уровень убедительности рекомендаций С (уровень достоверности – 4)
3. Лечение
Показания к госпитализации:
- Все дети в активную стадию должны быть госпитализированы в стационар. Длительность пребывания в стационаре в среднем 14-21 день.
Дети в стадии ремиссии могут наблюдаться в амбулаторных условиях.
3.1 Лечение первого эпизода стероидчувствительного нс при БМИ (НГ)
При развитии НС у детей до года до начала кортикостероидной терапии следует проводить нефробиопсию.
Немедикаментозное лечение
- Не рекомендовано ограничение двигательной активности.
Уровень убедительности рекомендаций С (уровень достоверности –4)
- Рекомендована сбалансированная диета, количество потребляемого белка- 1,5-2 г/кг и сохранение калоража пищи за счет полиненасыщенных жиров. Бессолевая или с низким содержанием соли (<2гNa / день) только в период выраженных отеков. При тяжелых отеках: ограничение потребления жидкости.
Уровень убедительности рекомендаций С (уровень достоверности –4)
Медикаментозное лечение
- Рекомендовано назначать кортикостероидную терапию (преднизолон) на период не менее 12 недель.
Уровень убедительности рекомендаций B (уровень достоверности –1)
- Рекомендовано применять преднизолон внутрь ежедневно в 1 или 2 приема (1B) в начальной дозе 60 мг/м2/24 ч или 2 мг/кг/24 ч, максимально до 60 мг/24 ч (1D) в течение 4–6 недель (1C) с последующим переходом на прием препарата через день (альтернирующий прием), начиная с дозы 40 мг/м2 или 1,5 мг/кг (максимум 40 мг через день) в один прием (1D) с постепенным снижением дозы в течение 2–3 мес. (1B).
Уровень убедительности рекомендаций B-D (уровень достоверности –1)
Комментарии: Общая длительность терапии должна составлять 4-5мес (1B).
3.2 Лечение рецидивирующей формы НС при БМИ
Кортикостероидная терапия у детей с редкими рецидивами стероидчувствительного НС при БМИ.
- У детей с редкими рецидивами стероидчувствительного нефротического синдрома (СЧНС) рекомендовано проводить лечение преднизолоном в дозе 60 мг/м2 или 2 мг/кг (максимально 60 мг/24 ч) в 1 или 2 приема до тех пор, пока не будет констатирована полная ремиссия в течение 3 дней.
Уровень убедительности рекомендаций D (уровень достоверности –2)
- После достижения ремиссии рекомендовано назначается преднизолон в дозе 40 мг/м2 или 1,5 мг/кг (максимально 40 мг) через день в течение как минимум 4 недель.
Уровень убедительности рекомендаций С (уровень достоверности –2)
Кортикостероидная терапия у детей с часто рецидивирующими и стероидзависимыми формами стероидчувствительного НС при БМИ.
- При рецидивах часто рецидивирующей (ЧР) и стероидзависимой формы (СЗ) СЧНС рекомендовано назначать преднизолон ежедневно до тех пор, пока полная ремиссия не будет констатирована в течение не менее 3 дней, и затем преднизолон в альтернирующем режиме в течение не менее чем 3 мес.
Уровень убедительности рекомендаций С (уровень достоверности –2)
- У детей с ЧР и СЗ СЧНС рекомедовано рассмотреть возможность назначение преднизолона в альтернирующем режиме в самых низких дозах, необходимых для поддержания ремиссии, во избежание серьезных побочных эффектов. В случае неэффективности данной схемы возможен ежедневный прием в минимальной суточной дозе, необходимой для поддержания ремиссии без серьезных побочных эффектов.
Уровень убедительности рекомендаций D (уровень достоверности –2)
- У детей с ЧР и СЗ СЧНС, получающих преднизолон в режиме через день, на период эпизодов респираторных и других инфекций рекомендовано назначать преднизолон ежедневно, с целью уменьшения риска обострений.
Уровень убедительности рекомендаций С (уровень достоверности –2)
3.3 Лечение ЧР и СЗ СЧНС кортикостероидсберегающими препаратами
Алкилирующие препараты при лечении часто рецидивирующей и стероидзависимой формы стероидчувствительного НС при БМИ. Эффективность составляет от 30% до 50%.Основные осложнения терапии: цитопения, инфекционные поражения, токсический гепатит, геморрагический цистит, гонадотоксичность.
Показаниями у биопсии почки у детей с СЧНС являются (НГ):
- отсутствие эффекта при рецидивах после первоначального ответа на кортикостероиды;
- высокий индекс подозрения в отношении иной основной патологии;
- ухудшение функции почек у детей, получающих КНИ.
- Рекомендовано назначать стероидсберегающие препараты у детей с ЧР и СЗ СЧНС в тех случаях, когда развиваются побочные эффекты кортикостероидной терапии.
Уровень убедительности рекомендаций В (уровень достоверности –1)
- При ЧР (1B) и СЗ (2C) СЧНС рекомендовано использовать в качестве стероидсберегающих препаратов алкилирующие агенты — циклофосфамид или хлорамбуцил.
Уровень убедительности рекомендаций С (уровень достоверности –2)
- Назначать циклофосфамид в дозе 2 мг/кг/24 ч в течение 8–12 нед (максимальная кумулятивная доза 168 мг/кг).
Уровень убедительности рекомендаций С (уровень достоверности –2)
- Не рекомендовано начинать терапию циклофосфамидом до тех пор, пока не будет достигнута ремиссия с помощью кортикостероидов (2D).
Уровень убедительности рекомендаций D (уровень достоверности –2)
- Рекомедовано назначать хлорамбуцил в дозе 0,1–0,2 мг/кг/24 ч в течение 8 нед (максимальная кумулятивная доза 11,2 мг/кг) в качестве альтернативы циклофосфамиду.
Уровень убедительности рекомендаций С (уровень достоверности –2)
- На фоне приема алкилирующих препаратов глюкокортикостероидная терапия должна быть окончена не более чем за 2 недели до окончания курса алкилирующих препаратов.
Уровень убедительности рекомендаций С (уровень достоверности –2)
- Не рекомендовано проводить второй курс алкилирующих препаратов.
Уровень убедительности рекомендаций D (уровень достоверности –2)
Левамизол при лечении часто рецидивирующей и стероидзависимой формы стероидчувствительного НС при БМИ
- При лечении ЧР и СЗ СЧНС (1В) рекомедовано назначить левамизол в дозе 2,5 мг/кг через день (2B) в течение как минимум 12 мес (2C), так как у большинства детей при отмене левамизола возникают рецидивы. Препарат назначать под контролем уровня нейтрофилов.
Уровень убедительности рекомендаций В (уровень достоверности –2)
Ингибиторы кальцинейрина (циклоспорин или такролимус) при лечении часто рецидивирующей и стероидзависимой формы стероидчувствительного НС при БМИ.
- Рекомендовано назначать КНИ в течение как минимум 12 мес, так как у большинства детей при отмене КНИ развиваются обострения.
Уровень убедительности рекомендаций С (уровень достоверности –2)
- Рекомендовано применять циклоспорин А в начальной дозе 4–6 мг/ кг/24 ч в 2 приема.
Уровень убедительности рекомендаций С (уровень достоверности –2)
Комментарии: Начало терапии при достижении ремиссии на фоне глюкокортикоидной терапии и переходе на альтернирующий режим. Контроль эффективности дозы осуществляется путем измерения концентрации препарата в сыворотке крови. Определение концентрации циклоспорина А возможно в двух точках: в точке С0 – определение базального уровня циклоспорина до утреннего приема препарата(или через 12 часов от вечернего приема); в точке C2— определение концентрации через 2 часа после утреннего приема препарата. Эффективная концентрация циклоспорина А при ЧР и СЗ СЧНС при БМИ следующая:
С0— 80-100нг/мл
С2 – 700-800нг/мл
Эффективность терапии- 80-90%.
- Рекомендовано применять такролимус в начальной дозе 0,1 мг/кг/24 ч в 2 приема вместо циклоспорина А в случае выраженных косметических побочных эффектов циклоспорина.
Уровень убедительности рекомендаций D (уровень достоверности –2)
Комментарии: Принцип назначения такролимус такой как циклоспорина А, т.е. контроль эффективности дозы определяется базальным уровнем концентрации препарата в сыворотке крови.
Эффективная концентрация такролимуса в т. С0 – 5-8 нг/мл.
Эффективность терапии- 60-80%.
Основные осложнения терапии: нефротоксичность. При снижении скорости клубочковой фильтрации (СКФ) на 30% дозу КНИ уменьшают вдвое, при снижении СКФ на 50% — отменяют препарат. При длительности терапии более 2,5-3 лет рекомендуется проведение нефробиопсии для выявления возможных морфологических признаков токсичности (повреждение эпителия канальцев, склероз интерстиция и стенок артериол). Также среди побочных действий ЦСА – гепатотоксичность, гиперурикемия, гипертрихоз, гиперкалиемия, гипомагнезиемия, гиперплазия десен.
- Для уменьшения токсичности следует мониторировать концентрацию ингибиторов кальцинейрина в сыворотки крови (КНИ).
Уровень убедительности рекомендаций НГ
- Рекомендовано назначать КНИ в течение как минимум 12 мес, так как у большинства детей при отмене КНИ развиваются обострения.
Уровень убедительности рекомендаций С (уровень достоверности – 2)
Микофенолаты при лечении часто рецидивирующей и стероидзависимой формы стероидчувствительного НС при БМИ
- Рекомендовано назначать микофенолат мофетил в начальной дозе 1200 мг/м2/24 ч или микофеноловую кислоту начальной дозе 720 мг/м2 в 2 приема в течение как минимум 12 мес, так как у большинства детей при отмене микофенолатов развиваются рецидивы (2C).
Уровень убедительности рекомендаций С (уровень достоверности – 2)
Комментарии: Эффективность терапии составляет 50-60%.
Ритуксимаб при лечении часто рецидивирующей и стероидзависимой формы стероидчувствительного НС при БМИ.
- Рекомендовано применять ритуксимаб только у тех детей со СЗ СЧНС, у которых частые рецидивы возникают несмотря на применение оптимальых комбинаций преднизолона и кортикостероидсберегающих препаратов или у тех, у которых развиваются серьезные побочные эффекты этой терапии.
Уровень убедительности рекомендаций С (уровень достоверности – 2)
Комментарии: Введение препарата возможно только в условиях стационара в дозе 375мг/2 внутривенно с еженедельным введением в течение 4 недель.
- Не рекомендовано использовать мизорибин? в качестве кортикостероидсберегающего препарата при ЧР и СЗ СЧНС при БМИ.
Уровень убедительности рекомендаций С (уровень достоверности – 2)
- Не рекомендовано использовать азатиоприн в качестве кортикосте-роидсберегающего препарата при ЧР и СЗ СЧНС при БМИ.
Уровень убедительности рекомендаций В (уровень достоверности – 1)
3.4 Лечение стероидрезистентной формы НС при БМИ
Для оценки детей со СРНС требуется (НГ):
- диагностическая биопсия почки;
- оценка функции почек по СКФ и рСКФ;
- количественная оценка экскреции белка.
- Рекомендовано констатировать стероидную резистентность после 8 недель стероидной терапии без эффекта или 3 пульсов-терапии метил преднизолоном в дозе 20-30мг/кг, но не более 1г/сут. после 6 недель.
Уровень убедительности рекомендаций D (уровень достоверности – 2)
- Рекомендовано использовать КНИ в качестве инициальной терапии у детей со СРНС.
Уровень убедительности рекомендаций В (уровень достоверности – 1)
- Рекомендовано роводить терапию КНИ в течение как минимум 6 мес. и прекращать ее, если к этому времени не достигнута частичная или полная ремиссия ПУ.
Уровень убедительности рекомендаций С(уровень достоверности – 2)
- Рекомендовано продолжить терапию КНИ в течение как минимум 12 мес., если через 6 мес. достигнута хотя бы частичная ремиссия (2C).
Уровень убедительности рекомендаций С (уровень достоверности – 2)
Комментарии: Эффективная доза КНИ определяется определением их концентраций в сыворотке крови.
При СРНС эффективная лечебная концентрация циклоспорина А и такролимуса составляют:
ЦисА:
т. С0— 100-120нг/мл
т. С2— 1000-1200нг/мл
Так.:
т.С0— 6-8нг/мл соответственно
- Рекомендовано комбинировать терапию малыми дозами кортикостероидов с терапией КНИ.
Уровень убедительности рекомендаций D (уровень достоверности – 2)
- Всем детям со СРНС рекомендовано проводить лечение иАПФ или БРА детям со СРНС как в качестве гипотензивной, так и в качестве нефропротективной терапии.
Уровень убедительности рекомендаций В (уровень достоверности – 1)
- При высокой активности СРНС рекомендовано использовать пульс-терапию метилпреднизолоном (МП) в сочетании с КНИ: схема Вальдо (табл. 2).
Уровень убедительности рекомендаций В (уровень достоверности – 1)
Комментарии: Таблица 2 — Схема Вальдо
|
Неделя |
МП 30 мг/кг в/в |
Преднизолон |
Циклоспорин А |
|
1-2 |
3 раза в неделю |
— |
— |
|
3-8 |
1 раз в неделю |
2 мг/кг через день |
6 мг/кг/24ч |
|
9-29 |
— |
1 мг/кг через день |
3 мг/кг/24ч |
|
30-54 |
— |
0,5 мг/кг через день |
3 мг/кг/24ч |
У детей, не достигших ремиссии на терапии КНИ:
- Рекомендовано использовать микофенолата мофетил и высокие дозы кортикостероидов или комбинацию этих препаратов у детей, не достигших полной или частичной ремиссии на КНИ и кортикостероидах.
Уровень убедительности рекомендаций D (уровень достоверности – 2)
- Не рекомендовано назначать циклофосфамид детям со СРНС.
Уровень убедительности рекомендаций В (уровень достоверности – 2)
- У пациентов с рецидивом нефротического синдрома после достижения полной ремиссии возобновить терапию с использованием одной из следующих схем:
- кортикостероиды внутрь;
- вернуться к тому иммуносупрессивному препарату, который ранее был эффективен;
- использовать альтернативный иммуноспурессивный препарат для уменьшения кумулятивной токсичности.
Уровень убедительности рекомендаций D (уровень достоверности – 2)
3.6 Симптоматическая терапия
- Рекомендована диуретическая терапия для лечения больных с отеками.
Уровень убедительности рекомендаций В (уровень достоверности – 1)
Комментарии: Диуретическая терапия широко используются для лечения больных с отеками:
- Гидрохлоротиазид: 2 -4 мг / кг/сут;
- Верошпирон: 2 ~ 4 мг /кг;
- В/в декстраны: 10 ~ 15мл/кг, с последующим введением фурасемида (Лазикс) 2-4мг/кг, спустя 30 ~ 60мин;
- В/в альбумин (20%-до 5 мл/кг) +лазикс;
Показания для в/в альбумина:
- Тяжелые отеки;
- Асцит;
- Гидроторакс и гидроперикард;
- Генитальные отеки;
- Низкий уровень альбумина ( <20г/л).
3.7 Лечение осложнений:
Гипертония:
- Рекомендовано назначать с гипотензивной и нефропротективной целью ингибиторы ангиотензин-превращающего фермента (иАПФ): фозиноприл или эналаприл индивидуальный подбор дозы, в среднем: 0,1- 0,3 мг/кг по фозиноприлу и блокаторы рецепторов ангиотензина (БРА).
Уровень убедительности рекомендаций В (уровень достоверности – 1)
- Рекомендовано применять И АПФ и БРА при отсутствии эффекта от ранее проводимых всех видов иммуносупрессивной терапии.
Уровень убедительности рекомендаций В (уровень достоверности – 1)
Гиперкоагуляция:
- Рекомендовано проводить антикоагулянтную терапию с целью профилактики венозных и артериальных тромбозов. проводится в активную стадию заболевания под контролем коагулограммы.
Уровень убедительности рекомендаций В (уровень достоверности – 1)
Комментарии: В условиях стационара лучше использовать антикоагулянты с коротким периодам выведения для дальнейшей быстрой коррекции: гепарин в суточной дозе 150-200 Ед/кг/сутки подкожно в 4 приема или фраксипарин 170 МЕ/кг/сут подкожно 1 раз в сутки. Антикоагулянтная терапия проводиться под контролем коагулограммы. При стабилизации дозу гепарина снижают (начинают со снижения дозы, а затем кратности введения).Антиагреганты-дипиридамол (курантил) в дозе 5-8 мг/кг/сутки или тиклодипин (тиклид) 8 мг/кг/сутки, у подростков возможно использование клопидогрела (плавикса) в дозе 75 мг 1 раз в сутки.
Коррекция остеопении и остеопороза:
- Рекомендован витамин D3 в дозе 1000-3000 МЕ в сутки в сочетании с препаратами кальция. 1000–1500 мг/сут (по элементарному кальцию).
Уровень убедительности рекомендаций В (уровень достоверности – 1)
Профилактика язвенной болезни
- На фоне приема лечебной дозы глюкокортикостероидов с целью профилактики язвенной болезни рекомендовано назначать ингибиторы протонной помпы или блокаторы Н2— гистаминовых рецепторов в возрастной дозе.
Уровень убедительности рекомендаций В (уровень достоверности – 1)
4. Реабилитация
Реабилитация больных БМИ не проводится.
5. Профилактика и диспансерное наблюдение
5.1. Профилактика
5.1.1 Первичная профилактика не проводится.
5.1.2 Профилактика обострения заболевания
У больных с установленным БМИ в эпидемический период проводится профилактика ОРВИ с использованием немедикаментозных и медикаментозных методов профилактики (НГ).
- В случае развития ОРВИ у больного с БМИ на фоне приема иммуносупрессивных препаратов с целью профилактики обострения процесса рекомендовано назначать антибактериальную терапию.
Уровень убедительности рекомендаций С (уровень достоверности –4)
- Рекомендация 42. Для уменьшения риска серьезных инфекций у детей с СЧ БМИ следует (НГ):
- проводить детям противопневмококковую вакцинацию.
- проводить вакцинацию против гриппа ежегодно детям, и всем, кто проживает с ними совместно.
- отложить вакцинацию живыми вакцинами до тех пор, пока доза преднизолона не будет снижена до 1 мг/кг/24ч (<20 мг/24ч) или до 2 мг/кг через день (<40 мг через день).
- живые вакцины противопоказаны детям, получающим кортикостероид-сберегающие иммуносупрессивные препараты.
- для уменьшения риска инфицирования детей с подавленными иммунитетом иммунизировать здоровых лиц, проживающих совместно с детьми живыми вакцинами, но обеспечить отсутствие контакта детей с выделениями мочевой, пищеварительной и дыхательной систем вакцинированных лиц в течение 3-6 недель после вакцинации.
- при контакте с ветряной оспой – не привитым детям, получающим иммуносупрессанты, при возможности назначать противозостерный иммуноглобулин.
Уровень убедительности рекомендаций С (уровень достоверности –4)
5.2 Диспансерное наблюдение
- Длительность наблюдения не менее 5 лет(2С).
- Наблюдение проводится участковым педиатром и нефрологом. Частота осмотра представлена в таблице 3.
- В комплекс диспансерного наблюдения входят определения режима, диеты, санаторно-курортное лечение.
- Диета у больного с БМИ должна быть гипоаллергенной, с исключением экстративных веществ, и сбалансированная по калоражу согласно возрасту.
- Режим – ограничений двигательной активности нет.
- Обязательное проведение санации очагов инфекции, с этой целью проводится осмотр стоматологом и отолорингологом. Частота осмотра представлена в табл. 3
- В перечень лабораторных исследований в период диспансерного наблюдения у больного с БМИ входят: общий анализ мочи, клинический анализ крови, определение суточной экскреции белка, количественный анализ мочи (Амбурже или Нечипоренко), проба Зимницкого, биохимический анализ крови, функциональная с определением СКФ или клиренса эндогенного креатинина. Частота исследований представлены в таблице 3.
- Снятие с учета через 5 лет полной ремиссии после обследования в нефрологическом стационаре, стационаре одного дня, диагностическом центре.
Таблица 4. Примерная схема диспансерного наблюдения детей с острым гломерулонефритом (по М.В. Эрману, 1997)
|
Частота осмотров специалистами |
Дополнительные методы обследования |
Основные пути оздоровления |
|
· Педиатр 1-ый год: В первые 3 мес. — 2 раз/месяц С 3 до 12 мес. — 1 раз/месяц Затем 1 раз в 2-3 мес.
1-ый год: 1 раз в 3 мес. Затем 1-2 раза в год
1 раз в 6 мес.
|
1. Анализ мочи Первые 6 мес. — 1раз в 10-14 дней, затем 1 раз в мес.
|
Режим Диета Реабилитация в местном нефрологическом санатории При интеркуррентных заболеваниях симптоматическая терапия. Анализы мочи при заболевании, выздоровлении через 2-3 мес. Медицинский отвод от прививок на го |
Критерии оценки качества медицинской помощи
|
№ |
Критерии качества |
Уровень достоверности доказательств |
Уровень убедительности рекомендаций |
|
1 |
Выполнено определение уровня суточной протеинурии и оценка биохимических показателей НС (уровень альбумина сыворотки крови, уровень холестерина сыворотки крови |
А |
1 |
|
2 |
Выполнена оценка скорости клубочковой фильтрации |
В |
1 |
|
3 |
Выполнено ультразвуковое исследование почек |
С |
4 |
|
4 |
Выполнен общий анализ мочи с микроскопией мочевого осадка |
С |
4 |
Список литературы
- Детская нефрология. /Под ред. Н. Сигела /Пер.А. Александровского, Д. Буйнова, А. Вермеля, А. Засядько, Д. Колода, Е. Макаренко, А. Мишарина, Ю. Ольшанской, А. Рылова, Н. Первухова. М.: Практика 2006; 336.
- Детская нефрология. /Под ред. Э. Лойманна, А.Н. Цыгина, А.А. Саркисяна. М.: Литтерра — 2010.
- Детская нефрология Руководство для врачей. /Под ред. М.С. Игнатовой, 3-е изд. М.: МИА 2011;696.
- Диагностика и лечение нефротического синдрома у детей: Руководство для врачей. М.С. Игнатова, О.В. Шатохина. М.: МИА 2009; 300.
- Клиническая нефрология.
http://www.sma.org.sg/handheld/express/guidelines/01_06.htm
/Под ред. Папаян А.В., Савенковой Н.Д. С-П.: Сотис 2008; 712.
- Нефрология детского возраста. Руководство для врачей. М.В. Эрман М.: Спецлит 2010; 683.
- Davin J.-C., Rutjes N.W. Nephrotic Syndrome in Children: From Bench to Treatment. International Journal of Nephrology. 2011;8:1-6.
- Dorresteijn E.M., Kist-van Holthe J.E., Levtchenko E.N. et al. Mycophenolate mofetil versus cyclosporine for remission maintenance in nephrotic syndrome. Pediatric Nephrology, 2008; 23(11):2013–2020.
- Eddy A.A., Symons J.M. Nephrotic syndrome in childhood. Lancet 2003; 362(9384):629–639.
- Garin EH, Mu W, Arthur JM, Rivard CJ, Araya CE, Shimada M, et al. Urinary CD80 is elevated in minimal change disease but not in focal segmental glomerulosclerosis. Kidney Int. 2010;78: 296-302.
- Hinkes B.G., Mucha B., Vlangos C.N. et al. Nephrotic syndrome in the first year of life: two thirds of cases are caused by mutations in 4 genes (NPHS1, NPHS2, WT1, and LAMB2). Pediatrics, 2007; 119(4): e907–e919.
- Hodson E.M., Willis N.S., Craig J.C. Interventions for idiopathic steroid-resistant nephrotic syndrome in children. Cochrane Database of Systematic Reviews, 2010;11: Article ID CD003594.
- Hodson E.M., Willis N.S., Craig J.C. Non-corticosteroid treatment for nephrotic syndrome in children. Cochrane Database of Systematic Reviews, 2008; 1: Article ID CD002290.
- Ishimoto T, Cara-Fuentes G, Wang H, Shimada M, Wasserfall CH, Winter WE, Rivard CJ, Araya CE, Saleem MA, Mathieson PW, Johnson RJ, Garin EH. Serum from minimal change patients in relapse increases CD80 expression in cultured podocytes. Pediatr Nephrol. 2013 Sep;28(9):1803-1812.
- Ishimoto T, Shimada M, Gabriela G, Kosugi T, Sato W, Lee PY, Lanaspa MA, Rivard C, Maruyama S, Garin EH, Johnson RJ. Toll-like receptor 3 ligand, polyIC, induces proteinuria and glomerular CD80, and increases urinary CD80 in mice. Nephrol Dial Transplant. 2013; 28(6):1439-1446.
- Kimata H., Fujimoto M., Furusho K. Involvement of interleukin (IL)-13, but not IL-4, in spontaneous IgE and IgG4 production in nephrotic syndrome. European Journal of Immunology, 1995; 25(6): 1497–1501.
- Lai K.W., Wei C.L., Tan L.K. et al. Overexpression of interleukin-13 induces minimal-change-like nephropathy in rats Journal of the American Society of Nephrology, 2007; 18(5):1476–1485.
- Machuca E., Benoit G., Antignac C., Genetics of nephrotic syndrome: connecting molecular genetics to podocyte physiology. Human Molecular Genetics, 2009;18(R2): R185–R194.
- Nephrotic syndrome in children: prediction of histopathology from clinical and laboratory characteristics at time of diagnosis. A report of the International Study of Kidney Disease in Children. Kidney International. 1978;13(2):159-165.
- Niaudet P. Steroid-sensitive nephrotic syndrome in children in Paediatric Nephrology. /E.D. Avner, W.E. Harmon and P. Neasden, Eds. 2004; 543–556, Lippincott Williams and Wilkins, Philadelphia, Pa, USA.
- Reiser J, Mundel P. Danger signaling by glomerular podocytes defines a novel function of inducible B7-1 in the pathogenesis of nephrotic syndrome. J Am Soc Nephrol. 2004;15:2246-2248.
- Reiser J, von Gersdorff G, Loos M, Oh J, Asanuma K, Giardino L, et al. Induction of B7-1 in podocytes is associated with nephrotic syndrome. J Clin Invest. 2004;113:1390-1397.
- Siegel N.J., Gur A., Krassner L.S., Kashgarian M. Minimal-lesion nephrotic syndrome with early resistance to steroid therapy. J Pediatr 1975;87(3):377–380.
- Wing K, Onishi Y, Prieto-Martin P, Yamaguchi T, Miyara M, Fehervari Z, et al. CTLA-4 control over Foxp3 regulatory T cell function. Science. 2008; 322: 271-275.
- Yap H.K., Cheung W., Murugasu B.,. Sim S.K, Seah C.C., Jordan S.C. Th1 and Th2 cytokine mRNA profiles in childhood nephrotic syndrome: evidence for increased IL-13 mRNA expression in relapse. Journal of the American Society of Nephrology, 1999;10(3):529–537.
- Yu CC, Fornoni A, Weins A, Hakroush S, Maiguel D, Sageshima J, et al. Abatacept in B7?1?positive proteinuric kidney disease. N Engl J Med 2013;369:2416?2423.
Приложение А1. Состав рабочей группы
Рабочая группа:
- Петросян Э.К. – д.м.н., профессор, нефролог
- Длин. В.В. – д.м.н., профессор, нефролог
Конфликтов интересов: нет
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций являются:
-
-
-
- Врач-педиатр;
- Врач-нефролог.
-
-
-
Для рекомендаций сила указана как уровень 1, 2 или «нет степени» (табл.5), качество доказательной базы обозначено как А, В, С (табл.6).
Таблица 5. Оценка силы рекомендаций (составлена в соответствии с клиническими рекомендациями KDIGO).
Уровень
Оценка рекомендаций
Со стороны пациентов
Со стороны врача
Дальнейшее направление использования
Уровень 1 «Эксперты рекомендуют»
Подавляющее большинство пациентов, оказавшихся в подобной ситуации, предпочли бы следовать рекомендуемым путем, и лишь небольшая часть из них отвергли бы этот путь
Подавляющему большинству своих пациентов врач будет рекомендовать следовать именно этим путем
Рекомендация может быть принята в качестве стандарта действия медицинского персонала в большинстве клинических ситуаций
Уровень 2
«Эксперты полагают»
Большая часть пациентов, оказавшихся в подобной ситуации, высказались бы за то, чтобы следовать рекомендуемым путем, однако значительная часть отвергла бы этот путь
Для разных пациентов следует подбирать различные варианты рекомендаций, подходящие именно им. Каждому пациенту необходима помощь в выборе и принятии решения, которое будет соответствовать ценностям и предпочтениям данного пациента
Рекомендации, вероятно, потребуют обсуждения с участием всех заинтересованных сторон до принятия их в качестве клинического стандарта
«Нет градации»
(НГ)
Данный уровень применяется в тех случаях, когда в основу рекомендации укладывается здравый смысл исследователя-эксперта или тогда, когда обсуждаемая тема не допускает адекватного применения системы доказательств, используемых в клинической практике.
Таблица 6. Оценка качества доказательной базы (составлена в соответствии с клиническими рекомендациями KDIGO).
Качество доказательной базы
Значение
А – высокое
Эксперты уверены, что ожидаемый эффект близок к рассчитываемому
В — среднее
Эксперты полагают, что ожидаемый эффект близок к рассчитываемому эффекту, но может и существенно отличаться
С – низкое
Ожидаемый эффект может существенно отличаться от рассчитываемого эффекта
D – Очень низкое
Ожидаемый эффект очень неопределенный и может быть весьма далек от рассчитываемого
Приложение Б. Алгоритмы ведения пациента
Алгоритм ведения больных с БМИ (дети)
«Диагностика»
н
нет да
нет да
Нет Да
«Лечение»
нет да
нет да нет да
Приложение В. Информация для пациентов
- Рекомендация II1. Для своевременной диагностики рецидива заболевания с целью мониторирования протеинурии рекомендовано использовать в домашних условиях определения белка с помощью тест-полосок.
- Рекомендация II2. На фоне заболевания ОРВИ доза глюкокортикостероидов снижать не следует, а при стероидзависимой форме возможен переход на ежедневный прием в той же дозе коротким курсом (на период заболевания),с последующим переходом на альтернирующий прием.
- Рекомендация II3. При обострении заболевания не следует самостоятельно подбирать дозу иммуносупрессивных препаратов. Коррекция лечения должна проводиться либо в специализированном стационаре, либо в амбулаторных условиях врачом-специалистом.
- Рекомендация II4. Отдых проводить в климатических условиях близких к климату проживания.
Приложение Г.
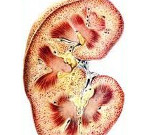
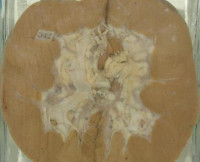
Липоидный нефроз — самостоятельная форма поражения почек только у детей с минимальными (подоцитарными) гломерулярными изменениями.
Липоидный нефроз — заболевание детей раннего возраста (преимущественно 2-4 лет), чаще мальчиков. Липоидный нефроз — это заболевание почек, при котором морфологически имеются только минимальные изменения. Эксперты ВОЗ определяют липоидный нефроз как минимальные изменения «болезнь малых отростков подоцитов», которые подвергаются диспластическим изменениям, мембрана и мезангий реагируют вторично.
При электронной микроскопии выявляются лишь минимальные изменения в клубочках почки с повреждением или исчезновением малых отростков (педикул) подоцитов, смещением их и распластыванием по базальной мембране капилляров клубочков.
Иммуногистохимическое исследование биоптатов почек при липоидном нефрозе дает отрицательный результат и помогает дифференцировать липоидный нефроз и другие типы гломерулонефрита. Важнейшим доказательством является по данным иммунофлюоресценции отсутствие при липоидном нефрозе отложений, содержащих IgG, IgM, комплемента и соответствующего антигена.
Причины липоидного нефроза неизвестны.
В патогенезе липоидного нефроза играет роль дисфункция в системе Т-клеточного иммунитета, повышение активности субпопуляции Т-супрессоров и гиперпродукция цитокинов. В сыворотке крови у больных обнаруживается повышенная активность ИЛ-2, ИЛ-4, ИЛ-8, ИЛ-10. Интерлейкин-8 играет важную роль в патогенезе нарушения селективности гломерулярного фильтра. Происходит утрата зарядно-селективной функции клубочкового фильтрационного барьера, вследствие чего повышается проницаемость капилляров для белка, особенно отрицательно заряженных альбуминов. Развивается протеинурия (в основном альбуминурия). Повышенная фильтрация гломерулярными капиллярами белка приводит к функциональному перенапряжению канальцевого аппарата. В связи с повышением реабсорбции отфильтрованного белка возникает резорбтивная тубулярная недостаточность.
Развивающаяся гипоальбуминемия приводит к снижению онкотического давления плазмы крови и создает возможность для нее транссудации из сосудистого русла в интерстициальное пространство. Это, в свою очередь, ведет к снижению объема циркулирующей крови (ОЦК). Снижение ОЦК приводит к снижению перфузионного давления в почках, что активирует ренин-ангиотензин-альдостероновую систему (РААС). Активация РААС стимулирует реабсорбцию натрия в дистальных канальцах. Сниженный ОЦК стимулирует высвобождение и антидиуретического гормона (АДГ), который усиливает реабсорбцию воды в собирательных трубочках почки. Кроме того, нарушению транспортных процессов в собирательных трубочках канальцев почек и образованию отеков способствует и атриальный натрийуретический пептид.
Реабсорбируемые натрий и вода поступают в интерстициальное пространство, что усиливает отеки при липоидном нефрозе.
Дополнительным патогенетическим фактором в развитии отеков при липоидном нефрозе является функциональная недостаточность лимфатической системы почек, то есть нарушенный лимфоотток.
Выраженные отеки при липоидном нефрозе появляются тогда, когда уровень сывороточного альбумина становится ниже 25 г/л. Развивающаяся гипопротеинемия стимулирует синтез белка в печени, в том числе липопротеинов. Однако катаболизм липидов снижен вследствие понижения в плазме крови уровня липопротеинлипазы, основной ферментной системы, влияющей на удаление липидов. В результате развивается гиперлипидемия и дислипидемия: повышение содержания в крови холестерина, триглицеридов, фосфолипидов.
Потеря белка почками ведет к нарушению иммунных реакций — потере IgG, IgA с мочой, снижению синтеза иммуноглобулинов и развитию вторичного иммунодефицита. Больные липоидным нефрозом дети подвержены вирусным и бактериальным инфекциям. Этому способствует и потеря витаминов, микроэлементов. Массивная протеинурия отражается на транспорте тиреоидных гормонов.
Развитию болезни и рецидивов почти всегда предшествуют ОРВИ или бактериальные инфекции. С возрастом, когда происходит созревание тимуса, наклонность к рецидивам липоидного нефроза отчетливо снижается.
Симптомы липоидного нефроза. Липоидный нефроз развивается постепенно (исподволь) и вначале незаметно для родителей ребенка и окружающих его лиц. В начальный период могут быть выражены слабость, утомляемость, снижение аппетита. Появляется пастозность на лице и ногах, однако об этом родители вспоминают ретроспективно. Отеки нарастают и становятся заметными — это и служит поводом обращения к врачу. Отеки распространяются на область поясницы, половых органов, нередко развивается асцит и гидроторакс. При липоидном нефрозе отеки рыхлые, легко перемещаются, ассиметричны. Кожа бледная, появляются признаки гипополивитаминозов А, С, В1, В2. На коже могут образовываться трещины, отмечается сухость кожных покровов. При больших отеках появляются одышка, тахикардия, выслушивается функциональный систолический шум на верхушке сердца. Артериальное давление нормальное. На высоте образования отеков появляется олигурия с высокой относительной плотностью мочи (1,026-1,028).
При исследовании мочи выраженная протеинурия, содержание белка 3-3,5 г/сут до 16 г/сут и более. Цилиндрурия. Эритроциты — единичные. В начале заболевания может быть лейкоцитурия, связанная с основным процессом в почках, она является показателем активности процесса. Клубочковая фильтрация по эндогенному креатинину выше нормы или нормальная. Уровень альбумина в крови ниже 30-25 г/л, иногда содержание альбумина составляет у больного 15-10 г/л. Степень снижения альбумина в крови определяет тяжесть течения липоидного нефроза и выраженность отечного синдрома. В крови увеличено содержание всех основных липидных фракций. Они могут достигать очень высоких цифр: холестерин выше 6,5 ммоль/л и до 8,5-16 ммоль/л; фосфолипиды 6,2-10,5 ммоль/л. Белок сыворотки крови ниже 40-50 г/л. Характерна повышенная СОЭ 60-80 мм/час.
Течение липоидного нефроза волнообразное, характерны спонтанные ремиссии и рецидивы заболевания. Обострение могут вызывать ОРВИ, бактериальные инфекции; у детей с аллергическими реакциями может играть роль соответствующий аллерген.
Ремиссию диагностируют при достижении уровня альбумина крови 35 г/л, при отсутствии протеинурии. Рецидив липоидного нефроза диагностируют при появлении значительной протеинурии в течение 3 дней.
Лечение липоидного нефроза.
Режим — постельный в активной фазе, при выраженных отеках на 7-14 дней. В дальнейшем в режиме не предусматривается ограничений, наоборот, рекомендуется активный двигательный режим с целью улучшения процессов обмена, крово- и лимфообращения. Больному необходимо обеспечить доступ свежего воздуха, гигиенические процедуры, ЛФК.
Диета должна быть полноценной с учетом возраста. При наличии аллергии — гипоаллергенная. Количество белка с учетом возрастной нормы, при выраженной протеинурии — добавление количества белка, теряемого за сутки с мочой. Жиры преимущественно растительные. При выраженной гиперхолестеринемии снизить потребление мяса, предпочтение отдать рыбе и птице. Бессолевая диета — 3-4 нед с последующим постепенным введением натрия хлорида до 2-3 г. Гипохлоридная диета (до 4-5 г) рекомендуется больному на многие годы. Жидкость не ограничивается, так как функция почек не нарушена, тем более, что ограничение жидкости на фоне гиповолемии и лечения глюкокортикостероидами (ГКС) ухудшает реологические свойства крови и может способствовать возникновению тромбозов. В период схождения отеков и приема максимальных доз глюкокориткостероидов необходимо назначение продуктов, содержащих калий — печеный картофель, изюм, курага, чернослив, бананы, тыква, кабачки.
В период ремиссии ребенок не нуждается в ограничении диеты и физической активности.
Медикаментозная лечение липоидного нефроза Лечение дебюта липоидного нефроза в основном сводится к назначению глюкокортикостероидов, терапия которыми является патогенетической. На фоне глюкокориткостероидов вначале назначают антибиотики. Используются полусинтетические пенициллины, амоксиклав, а при наличии у больного в анамнезе аллергических реакций на пенициллин — цефалоспорины III и IV поколения.
Преднизолон назначается из расчета 2 мг/кг/сут в 3 или 4 приема ежедневно до 3-4 последовательных отрицательных анализов суточной мочи на белок. Обычно это происходит на 3-4-й неделях от начала лечения. Затем назначается 2 мг/кг через день в течение 4-6 нед; далее 1,5 мг/кг через день — 2 нед; 1 мг/кг через день — 4 нед; 0,5 мг/кг через день — 2 нед с последующей отменой преднизолона. Курс 3 мес. Прогнозирование результатов лечения глюкокориткостероидами может быть проведено по оценке развития диуретического ответа через 4-7 дней от начала лечения. При быстром развитии стероидного диуреза можно полагать, что лечение будет успешным. При отсутствии стероидного ответа на диурез или при позднем его развитии (на 3-4 нед) лечение в большинстве случаев неэффективно. Следует искать причину отсутствия эффекта, возможна дисплазия почек. Проводится обследование на возможность скрытых очагов инфекции и санация очагов инфекции.
При стероидорезистентности — отсутствие эффекта от лечения глюкокориткостероидами в течение 4-8 нед — назначается циклофосфан 1,5-2,5 мг/кг/сут в течение 6-16 нед в сочетании с преднизолоном 0,5-1 мг/кг/сут; в дальнейшем курс поддерживающей терапии в половинной дозе цитостатика еще в течение 3-6 мес непрерывно.
При участии в рецидивировании липоидного нефроза атопии у детей с отягощенным аллергическим анамнезом рекомендуют использовать в лечении интал, задитен.
При ОРВИ используют реаферон, интерферон, анаферон детский.
Диспансерное наблюдение осуществляют педиатр и врач-нефролог, они при необходимости корригируют лечение. Необходимы консультации ЛОР-врача и стоматолога 2 раза в год.

Липоидный нефроз (Болезнь подоцитов, Идиопатический нефротический синдром детей)
Липоидный нефроз – это заболевание, характеризующееся дистрофическим поражением клубочков с развитием нефротического синдрома. На начальных стадиях симптомы не определяются, в дальнейшем развиваются отеки подкожной жировой клетчатки, слабость, сильная жажда, нарушения аппетита. Диагностика производится на основании результатов лабораторных исследований (общие и биохимические анализы крови и мочи), осмотра больного, УЗИ почек. В спорных случаях назначается биопсия ткани органа для последующего гистологического изучения. Лечение заключается в разработке специальной диеты, применении кортикостероидных и диуретических средств, инфузионной терапии.
Общие сведения
Липоидный нефроз (болезнь подоцитов, идиопатический нефротический синдром детей, ИНСД) – редкое заболевание неясной этиологии, первично поражающее пациентов в возрасте до 4-5 лет. Аналогичные изменения в почках возникают у взрослых с инфекционными состояниями (туберкулез, дифтерия, сифилис) или интоксикацией организма тяжелыми металлами. Согласно статистическим данным, мальчики страдают от первичной патологии в два раза чаще девочек, вторичные формы не имеют особенностей в половом распределении.
Причина состояния кроется в нарушенной работе подоцитов – клеток, покрывающих капилляры в клубочках нефрона. Именно с этим связано синонимичное название заболевания. Среди всех поражений почечной системы доля данного нефроза колеблется в пределах 0,4-0,6%, при этом количество взрослых составляет около 20% от всех заболевших.
Липоидный нефроз
Причины
Этиология первичного липоидного нефроза на сегодняшний момент неизвестна. Предполагается влияние преимущественно эндогенных факторов. Изучение патогенетических процессов выявило нарушение некоторых звеньев Т-клеточного иммунитета, приводящее к повышенному выделению специфических цитокинов. У ряда больных помимо почечных нарушений отмечаются аллергические патологии и поражения кожи (псориаз).
Примерно у 70% пациентов с идиопатическим нефрозом обнаруживаются особые формы генов главного комплекса гистосовместимости — HLA-B8 и HLA-DR7. Эти серотипы также ассоциируют с определенными разновидностями псориаза. Основная зона их распространения – Северная и Западная Европа – соответствует области наибольшей встречаемости ИНСД.
Вторичное поражение почечной ткани, аналогичное липоидному нефрозу, обычно возникает на фоне хронических патологий инфекционного, опухолевого или интоксикационного генеза. Причиной заболевания также считается аномальная активность иммунной системы, приводящая к избирательному поражению подоцитов клубочков.
Считается, что у лиц с вторичными формами нефроза имеется генетическая предрасположенность к нефротическому состоянию, а системная патология выступает провоцирующим фактором, увеличивая вероятность опосредованного повреждения почек. Нередко отличить липоидные изменения от некоторых форм гломерулонефрита можно только при исследовании ультраструктуры почек посредством электронной микроскопии.
Патогенез
Установлено, что липоидный нефроз обусловлен нарушениями в Т-клеточном сегменте иммунной системы. При идиопатическом нефротическом синдроме детей эти аномалии являются первичными, обусловлены генетическими факторами. Некоторые системные заболевания также могут аномальным образом активировать иммунитет. В результате происходит резкое увеличение популяции Т-супрессоров на фоне значительного выделения цитокинов и интерлейкинов (ИЛ).
Особенно пагубно на клубочки нефрона воздействуют повышенные концентрации ИЛ-8, который уменьшает заряд мембран подоцитов. В результате увеличивается проницаемость стенок капилляров для белков, главным образом – альбуминов, имеющих отрицательный заряд. Попадая в канальцевую систему, протеины закупоривают ее и способствуют деградации эпителиальных клеток, в конечном итоге нефрон полностью перестает выполнять свои функции.
Потеря значительных количеств белка потенцирует изменение реологических свойств плазмы крови. Снижение онкотического давления наряду с нарушением реабсорбции воды и ионов натрия в почках становится причиной отеков. В качестве компенсаторной реакции для улучшения вязкости крови развивается гиперлипидемия. Массовое «выключение» нефронов приводит к хронической почечной недостаточности. С мочой теряются не только альбумины, но и другие протеины, в частности иммуноглобулины классов A и G. Этим обусловлено снижение сопротивляемости организма инфекциям вплоть до вторичного иммунодефицита.
Классификация
Изучение причин липоидного нефроза и разработка принципов классификации данного состояния продолжаются. В настоящее время в практической урологии выделяют две основные группы патологии – идиопатический и вторичный нефроз. Первый тип возникает преимущественно у детей, некоторыми исследователями считается «истинным» липоидным нефрозом. Второй вариант заболевания развивается у взрослых при системных патологиях – отдельные авторы относят его к разновидностям гломерулонефрита. Минимальные гломерулярные нарушения у взрослых по этиологическому признаку разделяют на следующие виды:
- Инфекционного характера. Включают формы нефроза, возникающие под воздействием туберкулеза, сифилиса, дифтерии, малярии и других заболеваний. Инфекции считаются самой распространенной причиной ЛН у лиц старше 16 лет.
- Опухолевого характера. Определенные виды онкологических заболеваний (лимфомы, лимфогранулематоз) способны приводить к иммунным нарушениям с выделением больших количеств цитокинов. Результатом становится поражение подоцитов, характерное для липоидного нефроза.
- Интоксикационного характера. К этой группе относят дистрофические поражения клубочков, вызванные хроническим отравлением тяжелыми металлами – чаще всего ртутью или свинцом.
Приведенная выше классификация считается спорной. Изучение патологии осложняется тем, что для достоверного определения болезни подоцитов необходимо ультрамикроскопическое исследование. По клиническим и гистологическим (посредством световой микроскопии) данным липоидный нефроз очень сильно похож на ряд воспалительных поражений почечной ткани – например, мембранозный гломерулонефрит.
Симптомы липоидного нефроза
Клиническая картина обычно неясная, на начальном этапе заболевание ничем себя не проявляет. Первыми симптомами становятся слабость, разбитость, повышенная утомляемость, нарушения аппетита. Затем возникают отеки, сначала обычно на нижних конечностях, потом на лице, шее, в области поясницы. При тяжелом течении к ним присоединяется накопление жидкости в полостях тела – асцит, гидроторакс, проявляющиеся увеличением живота, затруднением дыхания. Кожные покровы бледные, отечные, ткани рыхлые, на них долго остаются следы от пальцев или других оказывающих давление предметов.
У детей симптомы идиопатического нефротического синдрома аналогичны клинической картине у взрослых. Развитию заболевания часто предшествует перенесенная вирусная инфекция или ангина. Вначале родители отмечают снижение двигательной активности ребенка, сонливость, капризность, нередко – отказ от пищи. После этого появляются отеки и признаки асцита.
Особенностью детской разновидности патологии является возникновение недостатка витаминов А, С, В1. Полигиповитаминоз сопровождается сухостью кожи, образованием кровоизлияний из-за ломкости капилляров, трещинами в углах рта. Возможны неврологические нарушения – чаще всего, снижение кожной чувствительности. Моча при любой форме заболевания приобретает бурый цвет и мутность, ее суточное количество снижается (олигурия).
Липоидный нефроз характеризуется волнообразным течением, периоды обострений с развитием отеков и иных нарушений чередуются с эпизодами спонтанной ремиссии. В межприступный период патология не проявляется, ее наличие можно определить только по протеинурии в результатах общего анализа мочи. При частых обострениях у больных развивается иммунодефицит, обусловленный потерей глобулинов крови. Его признаками являются пневмонии, бронхиты, частые гнойничковые поражения кожи. Характерно появление кожных трещин в области отеков с последующим развитием рожистого воспаления.
Осложнения
На высоте обострения липоидный нефроз опасен развитием шока из-за тяжелых электролитных нарушений и снижения объема циркулирующей крови. Возможны проблемы с дыханием из-за пневмоторакса, усугубленного респираторной инфекцией. Определенную угрозу несут бактериальные поражения кожи, часто принимающие тяжелый характер, существует риск развития сепсиса. При высокой частоте приступов заболевания отмечается гипохромная анемия. При отсутствии лечения со временем возможно формирование вторично-сморщенной почки, что становится причиной ХПН. По некоторым данным, липоидное поражение в отдаленной перспективе повышает риск возникновения амилоидоза.
Диагностика
Диагноз «липоидный нефроз» чаще применяют в современной педиатрической практике. У взрослых аналогичная клиническая картина зачастую определяется врачами-нефрологами как «минимальные гломерулярные изменения». Однако в большинстве случаев речь идет об одном и том же процессе – поражении подоцитов и клубочков при отсутствии иммунных комплексов. Для выявления патологии используют множество диагностических методик, часть из которых направлена на исключение иных почечных патологий со схожим течением. Алгоритм определения данного нефроза включает в себя следующие этапы:
- Осмотр и опрос. При осмотре выявляется отечность подкожной клетчатки различной локализации несимметричного характера, одутловатое лицо, суженные глазные щели. На ощупь отеки рыхлые, неэластичные, легко смещаются, кожные покровы над ними иногда имеют трещины и иные повреждения. При расспросе определяется слабость, отсутствие аппетита, утомляемость, повышенная жажда.
- Лабораторные исследования. Наиболее показательным признаком заболевания является наличие протеинурии в анализах мочи. Потери белка могут составлять до 16 грамм в сутки. Биохимический анализ крови подтверждает гипоальбуминемию до 20-30 г/л, гиперлипидемию за счет увеличения уровня холестерина и фосфолипидов. Показатели креатинина и общего азота при отсутствии осложнений обычно находятся в пределах нормы.
- Ультразвуковые исследования. УЗИ почек обнаруживает увеличение размеров органов, ослабление дифференциации между мозговым и корковым веществом. На поздних этапах развития патологии при многолетнем течении может выявляться сморщивание и уменьшение почек.
- Гистологические исследования. Взятие биопсии тканей почки с последующим микроскопическим исследованием считается золотым стандартом в диагностике данного нефроза. Определяются дистрофические изменения в клубочках, в эпителии проксимальных канальцев обнаруживаются отложения липидов. При иммунногистохимическом исследовании иммунные комплексы отсутствуют – важный признак отличия заболевания от гломерулонефрита.
При вторичном характере патологии производят определение наличия инфекционных, опухолевых или интоксикационных состояний и их тяжести. Дифференциальную диагностику проводят с мембранозным и другими типами гломерулонефрита, амилоидозом почек, пиелонефритом. Отличительной особенностью липоидного нефроза является относительное сохранение фильтрационной способности мочевыделительной системы на протяжении длительного времени.
Лечение липоидного нефроза
Терапевтические мероприятия направлены на устранение отеков, восполнение недостатка протеинов, профилактику инфекционных осложнений. Необходимо ослабить дистрофические процессы в почках, замедлить прогрессирование заболевания. С этой целью разрабатывается сложное комплексное лечение, включающее в себя не только использование лекарственных средств, но и специальную диету. Основными компонентами терапии болезни в нефрологии являются:
- Диета. В рационе больных должны преобладать белки, суточная потребность в которых возрастает до 2,5 грамм в сут. на килограмм массы тела. Для снижения отечности рекомендуется уменьшить потребление поваренной соли (не более 1-2 грамм в день). При выраженной гиперлипидемии следует использовать продукты, содержащие мало жиров (птица, белая рыба, овощи).
- Назначение диуретиков. Мочегонные средства применяют для устранения отеков, особенно в острый период заболевания. При этом важно следить за электролитным составом плазмы крови во избежание осложнений.
- Иммуносупрессивная терапия. Глюкокортикостероиды являются практически единственной группой препаратов для этиотропного лечения липоидного нефроза. Они эффективно снижают активность иммунитета и продукцию цитокинов, ослабляя пагубное воздействие ИЛ-8 на подоциты.
- Лечение инфекционных осложнений. При наличии гнойничкового поражения кожи, пневмонии, ОРЗ назначают антибактериальные или противовирусные средства. При бактериальном заражении эффективны антибиотики и сульфаниламидные препараты.
- Инфузионная терапия. Для улучшения реологических свойств крови показано капельное вливание специальных коллоидных растворов. При угрожающей гипопротеинемии возможно переливание донорской плазмы.
Особенностью лечения патологии у взрослых является одновременное устранение провоцирующего заболевания. В таком случае врач должен учитывать все возможные варианты взаимодействия лекарственных средств из разных групп. В период ремиссии больным рекомендуется санаторно-курортное лечение в регионах с теплым и сухим климатом.
Прогноз и профилактика
При своевременном выявлении липоидного нефроза у ребенка и активном лечении прогноз заболевания относительно благоприятный. Длительность течения может достигать 20 лет, в период обострений пациент временно теряет работоспособность по причине выраженных отеков и сопутствующих нарушений. При вторичном типе состояния прогноз во многом зависит от особенностей течения провоцирующей болезни.
Специфическая профилактика нефроза отсутствует, рекомендуется в полном объеме лечить заболевания, способные стимулировать такое поражение почек. Больным в бессимптомной стадии для предотвращения развития приступа следует придерживаться диеты, избегать переохлаждений и контактов с источниками инфекций. Необходимо регулярно проходить обследование у нефролога с контролем уровня белка в моче для профилактики осложнений.
Липоидный нефроз — лечение в Москве

Хронический гломерулонефрит диагностируют в любом возрасте, он может быть следствием неизлеченного острого нефрита, но чаще развивается как первично хроническое заболевание.
Классификация
В педиатрической практике традиционно выделяют гематурическую, нефротическую и смешанную формы хронического гломерулонефрита. При постановке диагноза необходимо уточнить морфологический вариант заболевания. В соответствии с морфологической классификацией хронического гломерулонефрита различают следующие формы.
- Минимальные изменения клубочков.
- Фокально-сегментарный гломерулярный склероз (гиалиноз).
- Мембранозный гломерулонефрит (мембранозная нефропатия).
- Мезангиопролиферативный гломерулонефрит.
- Мезангиокапиллярный (мембранопролиферативный гломерулонефрит).
- Фибропластический гломерулонефрит (финал всех типов).
Этиология
Причину заболевания удаётся установить не во всех случаях. Предполагают роль нефритогенных штаммов стрептококка, персистирующих вирусов (гепатита В, цитомегаловируса, вирусов Коксаки, Эпстайна-Барр, гриппа и др.), генетически детерминированных особенностей иммунитета (например, дефект в системе комплемента или клеточного иммунитета). Возникновению заболевания способствуют врождённые почечные дисплазии.
Патогенез
Выделяют иммунологически обусловленные и иммунологически не обусловленные варианты заболевания. Иммунологически обусловленные могут быть иммунокомплексного, реже аутоантительного генеза. Большинство форм первичного хронического гломерулонефрита относят к иммунокомплексным гломерулопатиям. Их патогенез напоминает таковой при остром гломерулонефрите. Участие иммунологических процессов при гломерулонефрите с минимальными изменениями — предмет дискуссий. Несмотря на то что у многих больных заболевание можно рассматривать как аллергическую реакцию на вакцинацию, лекарственные препараты и другие факторы, при исследовании клубочков иммуногистохимическим методом не обнаруживают специфических изменений. При помощи электронной микроскопии выявляют редукцию малых отростков подоцитов, свидетельствующую о метаболических изменениях в клетках. Патология подоцитов приводит к нарушению целостности клубочкового фильтра. В результате белки и липиды в избыточном количестве проникают в первичную мочу и, реабсорбируясь, накапливаются в каналыдевом эпителии. Развивается белковая и жировая дегенерация тубулярных клеток, отчётливо видимая при световой микроскопии, что в прежнее время дало повод называть патологический процесс «липоидным нефрозом».
Клиническая картина хронического гломерулонефрита зависит от его формы.
Нефротическая форма
У детей от 1 до 5 лет нефротической форме хронического гломерулонефрита обычно соответствует морфологический вариант с минимальными изменениями в клубочках. Обсуждают возможность перехода минимальных изменений клубочков в фокально-сегментарный гломерулосклероз, так как основное изменение при последнем — также поражение подоцитов. Для нефротической формы хронического гломерулонефрита характерны массивная протеинурия (более 3 г/сут), отёки, гипо- и диспротеинемия, гиперлипидемия. При нефрите с минимальными изменениями нефротическии синдром не сопровождается ни гематурией, ни артериальной гипертензией. Поэтому он носит такие названия, как «чистый», или «идиопатический», или «первичный», нефротическии синдром. При этом протеинурия может достигать 20-30 г/сут и более, но она почти всегда селективна и представлена главным образом альбуминами. Значительная потеря белка с мочой приводит к гипопротеинемии и диспротеинемии (в основном гипоальбуминемии), а это в свою очередь определяет снижение онкотического давления плазмы, вследствие чего вода переходит в ткани. Уменьшается ОЦК, снижается клубочковая фильтрация, появляются отёки (большей частью диффузные, с водянкой полостей). Отёки придают больным характерный вид. Кожа белого цвета, холодная на ощупь. Больные ошущают жажду, сухость во рту, слабость. Вследствие скопления жидкости в плевральных полостях могут быть жалобы на кашель и одышку. Появляется тахикардия, при отсутствии асцита выявляют увеличение печени. Наряду с развитием гипоальбуминемии повышается концентрация липидов в сыворотке крови. Количество мочеиспусканий и объём мочи уменьшаются, но относительная плотность мочи повышена. Осадок скудный и в основном содержит цилиндры, жир и жироперерождённый эпителий. Эритроциты выявляют редко и очень непродолжительное время. Макрогематурии не бывает. СОЭ резко увеличена. Во время обострения количество IgE или IgM и фибриногена может быть повышено. Концентрация компонента комплемента СЗ всегда в норме. Прогноз благоприятный. Большинство детей выздоравливают.
У детей школьного возраста при нефротической форме хронического гломерулонефрита обычно обнаруживают мембранозный и мезангиопролиферативный морфологические варианты. Для мембранозного варианта характерны наличие субэпителиальных депозитов и утолщение гломерулярной базальной мембраны при отсутствии значительной пролиферации эндотелиальных и мезангиальных клеток. Мезангиопролиферативный вариант наблюдают реже. Для него характерны пролиферация мезангиальных клеток и матрикса. Болезнь может развиваться исподволь с появления протеинурии и постепенного нарастания отёков. Возможно и бурное начало с нефротического синдрома. Протеинурия низко селективна, что свидетельствует о тяжёлом поражении капилляров клубочков. Гематурия выражена в различной степени — от микро- до макрогематурии. Обнаруживают гипокомплементемию — показатель активности патологического процесса. Течение заболевания волнообразное, азотовыделительная функция почек длительно остаётся сохранной, однако у половины больных через 5-10 лет нефрит приводит к развитию хронической почечной недостаточности. Ремиссии нефротического варианта чаще отмечают у больных с мембранозным гломерулонефритом.
Гематурическая форма
Основное проявление этой формы — стойкая гематурия. Возможны небольшая протеинурия и анемия. Самочувствие больных обычно не нарушается. В некоторых случаях отмечают пастозность век. Морфологически это мезангиопролиферативный гломерулонефрит (вариант с отложением в клубочках IgA и компонента комплемента СЗ).
Один из вариантов гематурической формы хронического гломерулонефрита — болезнь Берже (IgA-нефропатия). Заболевание диагностируют у детей любого возраста. Мальчики болеют в 2 раза чаще девочек. Характерна рецидивирующая макрогематурия, возникающая при ОРВИ, сопровождающихся лихорадкой, в первые дни или даже часы болезни («синфарингитная гематурия»), реже — после других заболеваний или вакцинации. В качестве возможного этиологического фактора обсуждают роль глютена. У некоторых больных в сыворотке обнаруживают повышенные титры антител класса IgA к пищевому белку глиадину. Течение IgA-нефропатии относительно благоприятное. Большинство больных выздоравливают. Исход в хроническую почечную недостаточность бывает редко. Резистентность к терапии отмечают у детей с болезнью Берже. Прогностически неблагоприятно развитие нефротического синдрома и артериальной гипертензии.
Смешанная форма
Развивается у детей старшего возраста и имеет тяжёлое, неуклонно прогрессирующее течение, торпидное к терапии. При смешанной форме возможны все морфологические варианты (кроме минимальных изменений). Чаще других выявляют мезангиокапиллярный вариант, характеризующийся пролиферацией мезангиальных клеток и утолщением или двуконтурностью стенки капилляров за счёт проникновения в них мезангиальных клеток. Прогрессирование патологического процесса приводит к развитию склероза и формированию фибропластического гломерулонефрита — финалу большинства форм хронического гломерулонефрита. Развивается склероз капиллярных петель клубочка, формируются фиброэпителиальные и фиброзные полулуния, утолщение и склероз капсулы клубочка.
Заболевание нередко начинается с острого нефротического синдрома с внезапным развитием гематурии, выраженной неселективной протеинурии, отёков и стойкой артериальной гипертензии. Болезнь может проявиться быстро нарастающей почечной недостаточностью. Особенность смешанной формы — гипокомплементемия со снижением концентрации СЗ и/или С4 компонентов комплемента. Прогноз неблагоприятный, довольно быстро у детей развивается хроническая почечная недостаточность.
Лечение
На современном этапе оптимальным считают лечение с учётом морфологического варианта хронического гломерулонефрита, однако это не всегда возможно, особенно у детей, и приходится ориентироваться на клинические проявления болезни. Лечение назначают в зависимости от активности патологического процесса. В активный период заболевания при наличии отёков, макрогематурии и выраженного повышения артериального давления показан постельный режим. Его расширяют по мере угасания клинических проявлений патологического процесса. Диету назначают с учётом состояния азотовыделительной функции почек. При её сохранности ребёнок получает белки в количестве, соответствующем возрастной норме (2-3 г/кг/сут), при азотемии — 1 г/кг/сут. При выраженной гиперлипидемии необходимо сократить приём жиров. При отёках и артериальной гипертензии назначают гипохлоридную диету. Объём жидкости дозируют в зависимости от диуреза. Однако в стадии полиурии подобные ограничения не нужны и даже вредны.
С учётом патогенеза гломерулонефрита применяют препараты, воздействующие как на иммунные механизмы (глюкокортикоиды, цитостатики), так и на неиммунные [антикоагулянты (гепарин по 200-400 ЕД/кг/сут в течение 2-4 нед и более), антиагреганты (дипиридамол по 3-5 мг/кг), ингибиторы АПФ (эналаприл, лизиноприл)], также назначают гиполипидемические препараты [ловастатин, флувастатин (лескол) и др.].
- При впервые возникшем нефротическом синдроме с минимальными изменениями клубочков лечение рекомендуют начинать с преднизолона в дозе 2-3 мг/кг массы тела или 60 мг/м2. Препарат в указанной дозе назначают на 4-8 нед. При нефротическом синдроме, чувствительном к гормональной терапии (у большинства детей), наступает клинико-лабораторная ремиссия. Рецидив, развившийся после отмены глюкокортикоидов, свидетельствует о гормональной зависимости нефротического синдрома. Лечение первого рецидива проводят так же, как терапию в начале болезни. При частых рецидивах добавляют цитостатики — циклофосфамид по 2 мг/кг, хлорамбуцил (лейкеран, хлорбутин) по 0,1-0,2 мг/кг, снижая при этом дозу преднизолона до 40 мг/м2 и переводя больного на альтернирующий режим приёма препарата (через день). Отсутствие эффекта от гормональной терапии в течение 8 нед указывает на резистентность нефротического синдрома к гормональной терапии. В этом случае лечение проводят цитостатиками или селективным иммунодепрессантом циклоспорином в дозе 3-5 мг/кг.
- Больным с фокально-сегментарным гломерулярным склерозом в настоящее время длительным курсом (до 6 мес) назначают глюкокортикоиды и цитостатики, что позволяет добиться ремиссии у больных, ранее считавшихся бесперспективными.
- При наиболее тяжёлой смешанной форме хронического гломерулонефрита используют 4-компонентную схему лечения (глюкокортикоиды + цитостатики + антиагреганты + антикоагулянты). При отсутствии эффекта от указанной терапии проводят сеансы плазмафереза с пульс-терапией метилпреднизолоном в дозе 10-20 мг/кг и/или циклофосфамидом по 5-15 мг/кг с последующим переводом больного на приём иммуносупрессивных препаратов внутрь.
- При гематурической форме хронического гломерулонефрита (мезангиопролиферативном гломерулонефрите) и IgA-нефропатии при сохранной функции почек, небольшой протеинурии (менее 1 г/сут) с эпизодами «синфарингитной макрогематурии» можно назначить ингибиторы АПФ (с нефропротективной целью) и дипиридамол. В случае развития нефротического синдрома целесообразно использовать глюкокортикоиды и цитостатики. НПВС, широко используемые ранее при гематурической форме хронического гломерулонефрита, в настоящее время в связи с побочными действиями применяют редко.
- При фибропластическом варианте гломерулонефрита (выраженных склеротических изменениях в клубочках) глюкокортикоиды не показаны.
Профилактика
Профилактика хронического гломерулонефрита направлена на предупреждение рецидивов заболевания (ограничение физической нагрузки, исключение стрессовых состояний, охлаждения, предохранение от интеркуррентных заболеваний, санация очагов хронической инфекции, вакцинопрофилактика по индивидуальному плану). Больным показано диспансерное наблюдение с контролем за функцией почек.
Прогноз
Прогноз прежде всего зависит от клинико-морфологических особенностей нефрита. Наиболее неблагоприятно течение смешанной формы хронического гломерулонефрита. Хроническая почечная недостаточность может развиться в сроки от нескольких месяцев до 15-20 лет после начала заболевания. При терминальной стадии хронической почечной недостаточности показаны гемодиализ и трансплантация почки.
Оригинал статьи www.eurolab.ua Иллюстрации с сайта: © 2011 Thinkstock.
Источник: Детские болезни. Баранов А.А. // 2002.