Портальное
кровообращение (синоним воротное
кровообращение) — система кровоснабжения
брюшных органов, получающих артериальную
кровь из чревной и мезентериальных
артерий.
Из чревной, мезентериальных
и селезеночной артерий кровь под
давлением 110— 120 мм рт. ст. поступает в
так называемую первую сеть капилляров
портального русла, расположенную в
кишечнике, желудке, поджелудочной железе
и селезенке. Оттуда под давлением 15—20
мм рт. ст. она направляется в венулы,
вены и далее в воротную вену , где давление
составляет 10—15 мм рт. ст. Из воротной
вены кровь поступает в так называемую
вторую сеть капилляров портального
русла, расположенную в печени, т. е. в
печеночные синусоиды, давление в которых
колеблется в пределах 6— 12 мм рт. ст.
Оттуда кровь по системе печеночных
вен попадает в нижнюю полую вену, покидая
портальное русло Одна из ветвей чревной
артерии — печеночная артерия —
направляется к печени , где артериальные
капилляры впадают непосредственно в
печеночные венулы и синусоиды, т. е. во
вторую капиллярную сеть. Кровь, притекающая
по этой артерии, предназначена для
снабжения печени кислородом и
соответственно минует первую капиллярную
сеть. Разность давлений в начальной и
конечной частях портального русла,
составляющая 100—110 мм рт. ст., обеспечивает
поступательный ток кровиПортальное
русло является основным депо крови в
организме. В осуществлении функции
депонирования важную роль играют
диффузный сосудистый сфинктер,
расположенный в области печени и
регулирующий отток крови из портального
русла, а также мускулатура мезентериальных
артерий, тонус которой регулирует
величину притока крови в портальное
русло.
Особенности кровообращения в
печени тесно связаны со строением
внутрипеченочных сосудов. Так, в ткани
печени существует широкий артериовенозный
анастомоз между разветвлениями воротной
вены и печеночной артерии. Значение
этого анастомоза в норме состоит в том,
что к печеночным клеткам поступает не
чистая портальная или артериальная
кровь, а смесь портальной и артериальной
крови, оптимальная для осуществления
печеночными клетками их обменной
функции. Следовательно, в печени
существует взаимозамещаемость портального
и артериального кровотока. На этом
основаны хирургические операции,
применяемые при лечении портальной
гипертонии.
Мелкие внутрипеченочные
сосуды — терминальные венулы портальной
системы, синусоиды, центральные вены,
разветвления печеночной артерии —
обладают большой вазомоторной активностью
Третья часть внутренней поверхности
синусоидов печени покрыта так называемыми
купферовскими клетками, которые, являясь
частью ретикулоэндотелиальной системы
, фагоцитируют бактерий и фиксируют в
своей протоплазме чужеродные вещества.
Воротная
вена образуется из слияния верхней
брыжеечной, v. mesenterica superior, и селезеночной,
v. splenica (lienalis), вен. Место их слияния, то
есть место формирования v. portae. находится
позади головки поджелудочной железы.
В воротную вену впадают v. pancreaticoduodenalis
superior, v. prepylorica и правая и левая желудочные
вены, vv. gastricae dextra et sinistra. Последняя
нередко впадает в селезеночную вену.
Нижняя брыжеечная вена, v. mesenterica inferior,
как правило, впадает в селезеночную,
реже — в верхнюю брыжеечную вену. Из-под
головки поджелудочной железы воротная
вена идет кверху позади двенадцатиперстной
кишки и входит в промежуток между
листками печеночно-дуоденальной связки.
Там она располагается позади печеночной
артерии и общего желчного протока. Длина
воротной вены колеблется от 2 до 8 см. На
расстоянии 1,0—1,5 см от ворот печени или
в воротах она разделяется на правую и
левую ветви, r. dexter et r. sinister.
Компенсаторным
механизмом при нарушенном оттоке
становится коллатеральный кровоток по
анастомозам с ветвями полых вен
(портокавальные анастомозы).
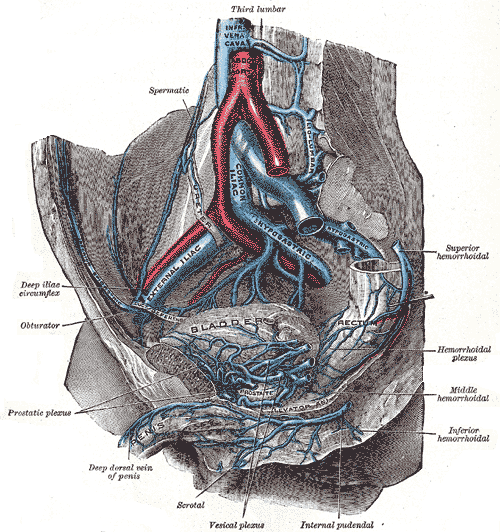
Портокавальными
анастомозами являются: 1) анастомозы
между венами желудка (система v. portae) и
венами пищевода (система v. cava superior); 2)
анастомозы между верхней (v. portae) и средней
(v. cava inferior) венами прямой кишки; 3) между
околопупочными венами (v. portae) и венами
передней брюшной стенки (v. cava superior и
inferior); 4) анастомозы верхней и нижней
брыжеечных, селезеночной вен (v. portae) с
венами забрюшинного пространства
(почечные, надпочечные, вены яичка или
яичника и другие, впадающие в v. cava
inferior).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
19.02.201643.77 Mб117Kaplan.pdf
- #
- #
- #
- #
- #
- #
- #
Портальное кровообращение (синоним воротное кровообращение) — это система кровоснабжения брюшных органов, получающих артериальную кровь из чревной и мезентериальных артерий.
Из чревной, мезентериальных и селезеночной артерий кровь под давлением 110— 120 мм рт. ст. поступает в так называемую первую сеть капилляров портального русла, расположенную в кишечнике, желудке, поджелудочной железе и селезенке. Оттуда под давлением 15—20 мм рт. ст. она направляется в венулы, вены и далее в воротную вену (см.), где давление составляет 10—15 мм рт. ст. Из воротной вены кровь поступает в так называемую вторую сеть капилляров портального русла, расположенную в печени, т. е. в печеночные синусоиды, давление в которых колеблется в пределах 6— 12 мм рт. ст. Оттуда кровь по системе печеночных вен попадает в нижнюю полую вену, покидая портальное русло (цветн. таблица).
Схема портального кровообращения: 1 — v. lienalis; 2 — v. mesenterica Inf.; 3 — v. mesenterica sup.; 4 — v. portae; 5 — ветвление сосудов в печени; 6 — vv. hepaticae; 7 — v. cava inf.
Одна из ветвей чревной артерии — печеночная артерия — направляется к печени (см.), где артериальные капилляры впадают непосредственно в печеночные венулы и синусоиды, т. е. во вторую капиллярную сеть. Кровь, притекающая по этой артерии, предназначена для снабжения печени кислородом и соответственно минует первую капиллярную сеть. Разность давлений в начальной и конечной частях портального русла, составляющая 100—110 мм рт. ст., обеспечивает поступательный ток крови. У человека через портальное русло протекает в среднем 1,5 л крови в 1 мин. Время движения крови от начала мезентериальных артерий через обе капиллярные сети до печеночных вен — 20 сек.; от начала печеночной артерии через сосуды печени до печеночных вен — 11 сек.
Портальное русло является основным депо крови в организме. В осуществлении функции депонирования важную роль играют диффузный сосудистый сфинктер, расположенный в области печени и регулирующий отток крови из портального русла, а также мускулатура мезентериальных артерий, тонус которой регулирует величину притока крови в портальное русло.
Соотношение тонуса сосудов, по которым происходят отток и приток крови, определяет количество ее в портальном русле. В норме эта величина составляет около 20% общего количества крови, содержащейся в организме, но при некоторых патологических состояниях может увеличиваться до 60% и более.
Важный отдел портального русла — кровообращение в печени, к которой но воротной вене притекает примерно 80% крови г по печеночной артерии — 20% . Особенности кровообращения в печени тесно связаны со строением внутрипеченочных сосудов. Так, в ткани печени существует широкий артериовенозный анастомоз между разветвлениями воротной вены и печеночной артерии. Значение этого анастомоза в норме состоит в том, что к печеночным клеткам поступает не чистая портальная или артериальная кровь, а смесь портальной и артериальной крови, оптимальная для осуществления печеночными клетками их обменной функции. Если перевязать печеночную артерию, то печень будет снабжаться кровью, притекающей только по воротной вене. Если создать порто-кавальный анастомоз Экка (фистула Экка), направив таким образом портальный кровоток в обход печени, то печень будет полностью снабжаться артериальной кровью. Сколько-нибудь выраженного нарушения обменных и желчевыделительных функций печени ни в том, ни в другом случае не наблюдается. Следовательно, в печени существует взаимозамещаемость портального и артериального кровотока. На этом основаны хирургические операции, применяемые при лечении портальной гипертонии.
Мелкие внутрипеченочные сосуды — терминальные венулы портальной системы, синусоиды, центральные вены, разветвления печеночной артерии — обладают большой вазомоторной активностью. Адреналин вызывает спазм синусоидов, раскрытие выходных сфинктеров и выбрасывание крови из печени в общее русло кровообращения. Введение гипертонического раствора NaCl или 40% раствора глюкозы вызывает спазм внутрипеченочных сосудов, а спустя 20 мин.— их расширение. Холодовое раздражение рецепторов кожи, травма отдаленных органов и тканей, кровопотеря ведут к спазму внутрипеченочных сосудов; приложение к коже тепла — к их расширению. Третья часть внутренней поверхности синусоидов печени покрыта так называемыми купферовскими клетками, которые, являясь частью ретикулоэндотелиальной системы (см.), фагоцитируют бактерий и фиксируют в своей протоплазме чужеродные вещества.
Нервная регуляция портального кровообращения осуществляется вегетативными центрами под определенной степенью коркового контроля. Во всех отделах портального русла имеются многочисленные барорецепторы, раздражение которых при растяжении портальных сосудов повышенным давлением приводит к повышению артериального давления в большом круге кровообращения. Симпатическая иннервация портального русла берет начало от невронов боковых столбов III — XI грудных сегментов спинного мозга. При возбуждении симпатических центров происходит резкое сужение разветвлений воротной вены и синусоидов печени; соответственно возрастает портальное давление. Возбуждение системы блуждающего нерва приводит к противоположному результату.
[анатомическое (vena) portae воротная вена] — условная зона системы кровообращения, ограниченная местом отхождения от аорты чревного ствола и верхней брыжеечной артерии и местом впадения печеночных вен в нижнюю полую вену. Представляет собой область кровообращения печени, желудка, кишечника, поджелудочной железы и селезенки (рис. 1). В клинической практике термин «портальное кровообращение» используется в более узком смысле — для обозначения кровообращения в системе воротной вены.
Кровь в системе П. к. проходит через две сети капилляров. К первой из них относят капилляры, расположенные в стенках органов пищеварения, и капилляры селезенки. Вторая сеть капилляров находится в паренхиме печени и обеспечивает обменную и экскреторную функции непосредственно печени. Из воротной вены кровь попадает в нижнюю полую вену и возвращается к сердцу, пройдя через печень, где осуществляется обезвреживание токсических продуктов, образующихся в желудочно-кишечном тракте в процессе пищеварения. В печень поступает кровь из двух систем сосудов (артериальная — из собственной печеночной артерии, венозная — из воротной вены) с единым дренированием через печеночные вены.
Существенной особенностью кровообращения в печени является широкая сеть разветвлений воротной вены и собственной печеночной артерии, образующей в дольках печени синусоидных капилляров, мембраны которых непосредственно контактируют печеночные клетки (гепатоциты). Из синусоидных капилляров кровь оттекает в центральные вены, затем в печеночные и нижнюю полую вену.
Нейрогуморальная и гемодинамическая регуляция П. к. осуществляется через систему сфинктеров, расположенных по ходу портального русла (рис. 2). Эта система в норме обеспечивает приспособление кровотока к деятельности органов брюшной полости, а также выполняет функцию депонирования крови в портальном русле и печени. Входные сфинктеры расположены в местах перехода мелких разветвлений воротной вены и артериол в синусоидные капилляры, а выходные сфинктеры — в области впадения синусоидных капилляров в центральную вену и центральной вены в междольковую. Роль дополнительного сфинктера портального русла играет мышечный слой средней оболочки стенок артерий и артериол, входящих в систему П. к. Тонус этого слоя и определяет величину притока крови в портальное русло.
Одним из основных условий нормального кровообращения (Кровообращение) в любой сосудистой системе является разность давления между различными ее точками. В системе П. к. артериальная кровь под давлением 110—120 мм рт. ст. поступает в первую сеть капилляров, где оно понижается до 10—15 мм рт. ст. В воротной вене давление составляет 5—10 мм рт. ст., а в печеночных венах — 0—5 мм рт. ст. Таким образом, разность давления в начальном и конечном отделах портального русла, обеспечивающая поступательное движение крови, составляет свыше 100 мм рт. ст. Внеорганные сосуды печени также имеют мышечный слой, что способствует пропульсивному движению крови. Возможно, что ток портальной крови происходит также за счет ритмичных сокращений селезенки.
Иннервацию и нервную регуляцию П. к. осуществляет чревное сплетение, содержащее как симпатические, так и парасимпатические волокна. Важную роль в регуляции П. к. играет эндокринная система. Введение адреналина или норадреналина в общий кровоток вызывает сужение афферентных сосудов печени и синусоидных капилляров, спазм входных сфинктеров и расслабление выходных сфинктеров. Одновременно повышается давление в воротной вене. Серотонин заметно суживает сосуды системы воротной вены, АКТГ значительно увеличивает печеночный кровоток. Ацидоз, гипоксия, гипотермия и другие факторы ухудшают микроциркуляцию в печени.
К наиболее информативным и распространенным методам исследования П. к. относятся спленопортография, интраоперационная портография и спленопортоманометрия, позволяющие судить о гемодинамике портального русла и локализации патологического процесса, блокирующего портальный кровоток. Особенности артериального кровообращения отражают целиакография (см. Ангиография) и реогепатография. Зондирование печеночных вен (измерение давления, контрастирование) дает информацию о состоянии выводящей системы портального русла.
Нарушение кровотока в системе П. к. обусловлено изменением количества притекающей крови, сопротивления ее оттоку, бокового давления на стенки сосудов и реологических свойств крови.
Поступление крови в воротную вену может увеличиваться в процессе пищеварения, однако в этом случае оно превышает кровоток в покое не более чем на 50%. Существенно возрастает кровенаполнение венозных сосудов органов брюшной полости при воспалительных процессах, например перитоните. Уменьшение поступления крови в воротную вену возможно при резких изменениях положения тела (ортостатический коллапс), при ишемии кишечника в результате кровопотери, тяжелой механической травмы и др.
Нарушения оттока крови из системы сосудов воротной вены, приводящие обычно к повышению давления в ней (см. Портальная гипертензия), могут быть вызваны сердечной недостаточностью, сужением или тромбозом печеночных вен, а также возрастанием сопротивления кровотоку в сосудах печени в результате изменений их тонуса под влиянием нервных и особенно гуморальных факторов или сужения их просвета, например при развитии цирроза печени (Цирроз печени). Повышение внутрибрюшного давления при асците, метеоризме, атонии кишечника и др. также сопровождается нарушениями портального кровотока. Изменения реологических свойств крови, например увеличение ее динамической вязкости, способствует замедлению кровотока в воротной вене.
При затруднении оттока крови через печеночные вены или возрастании ее притока в печени может депонироваться до 20% общего объема крови. Сосуды печени, выполняя функцию шлюзов, играют большую роль в регуляции системной гемодинамики (Гемодинамика). Задержка крови в синусоидных капиллярах печени увеличивает экстравазацию жидкости в перисинусоидальные пространства, что имеет значение для регуляции водно-солевого обмена (Водно-солевой обмен). В депонировании крови в портальном русле принимают участие селезенка и сосуды кишечника.
Расстройства П. к. сопровождаются нарушениями обменных процессов в печени и ее функций. Так, при наложении экковского соустья (анастомоз между нижней полой и воротной веной с одновременной перевязкой выше него воротной вены) кровоток через печень и потребление кислорода уменьшаются на 50%; это заметно влияет на белковый обмен, прежде всего на синтез мочевины.
При выраженных расстройствах кровоснабжения печени, в первую очередь артериального, и развитии глубокой гипоксии значительно нарушаются энергетический обмен и сопряженные с ним процессы переаминирования и синтеза белков, особенно плазмы крови.
Библиогр.: Заболевания органов пищеварения, под ред. А.С. Логинова, с. 28, М., 1977; Селезнев С.А. Печень в динамике травматического шока, Л., 1971, библиогр.; Фолков Б. и Нил Э. Кровообращение, пер. с англ., М., 1976.

Рис. 1. Схематическое изображение артерий и вен, входящих в систему портального кровообращения: 1 — брюшная аорта; 2 — чревный ствол; 3 — верхняя брыжеечная артерия; 4 — нижние брыжеечные артерия и вена; 5 — верхняя брыжеечная вена; 6 — селезеночная вена; 7 — воротная вена; 8 — печеночная вена; 9 — ветвление воротной вены в печени; 10 — печеночные вены; 11 — нижняя полая вена.
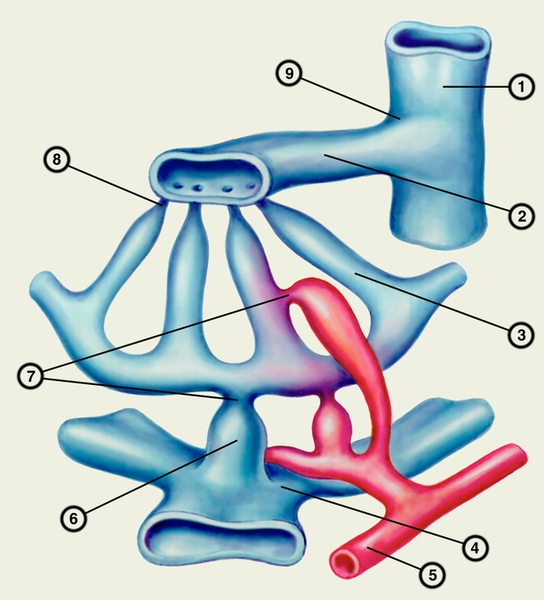
Рис. 2. Схематическое изображение системы сфинктеров на уровне внутрипеченочного кровообращения: 1 — междольковая вена; 2 — центральная вена; 3 — синусоидный капилляр; 4 — воротная вена; 5 — печеночная артерия; 6 — входной венозный сфинктер; 7 — входные артериальные сфинктеры; 8 — выходной сфинктер в месте впадения синусоидного капилляра в центральную вену; 9 — выходной сфинктер в области соединения центральной и междольковой вен.
1. Малая медицинская энциклопедия. — М.: Медицинская энциклопедия. 1991—96 гг. 2. Первая медицинская помощь. — М.: Большая Российская Энциклопедия. 1994 г. 3. Энциклопедический словарь медицинских терминов. — М.: Советская энциклопедия. — 1982—1984 гг.
УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Введение
Кардиосовместимая допплерография — новое направление в ультразвуковой диагностике. Основное его содержание состоит в синхронизированном с ЭКГ сопоставлении показателей регионарной или органной гемодинамики с параметрами функции сердца, т.е. с показателями системной гемодинамики. Способы исследования сосудов печени и обработки результатов кардиосовместимой допплерографии могут иметь значение для выявления нарушений микроциркуляции и прогнозирования развития осложнений. Депонирование крови в дополнительных сосудистых резервуарах обычно недоступно для непосредственной ультразвуковой визуализации. Однако новое направление позволяет решать подобные диагностические задачи, в том числе связанные с диагностикой сосудистых заболеваний, а также с имеющими риск развития внезапными, подчас фатальными синдромами (геморрагическим или окклюзионным).
Кардиосовместимая допплерография портальной системы печени как одного из регионов системы большого круга кровообращения включает в себя оценку синхронно с ЭКГ портального потока в комплексе с определением варианта центральной гемодинамики.
Вариант или тип сердечной (центральной) гемодинамики оценивается с помощью соотношения индексов удельного периферического сосудистого сопротивления (УПС) в обоих кругах кровообращения и ударных индексов (УИ) левого и правого желудочков по данным постоянноволновой допплерографии. Анализ трансаортального потока с определением ударного индекса левого желудочка (УИлж) проводится на уровне клапанов аорты, а значение ударного индекса правого желудочка (УИпж) рассчитывается по транспульмональному потоку на уровне клапанов легочной артерии.
Выделение типа центральной гемодинамики необходимо для сравнения с показателями периферического сосудистого кровотока. Суть такого подхода заключается в том, что показатели гемодинамики сосудов большого круга кровообращения (линейные, объемные скоростные количественные характеристики потоков и их индексы) сопоставляются, вопервых, с уровнем УИ левого желудочка сердца, т.е. с количеством крови, выбрасываемой ЛЖ в аорту за 1 сокращение и, вовторых, с удельным периферическим сосудистым сопротивлением за 1 кардиоцикл (УПС-1).
На основании проведенного кросс-корреляционного анализа УИлж и УПС-1 выделяются следующие типы центральной гемодинамики:
- нормокинетический тип со значением УИ 33-45 мл/м²; УПС-1 — 55-75 ед. Уиггерса;
- гиперкинетический тип — УИ более 45 мл/м², УПС-1 менее 55 ед.;
- гипокинетический тип — УИ менее 33 мл/м², УПС-1 более 60 ед.;
- застойный тип — УИ менее 25 мл/м², УПС-1 выше 88 ед., повышенное среднее давление в легочной артерии более 18 мм рт. ст.;
- гиповолемический тип — УИ менее 25 мл/м², УПС-1 выше 80 ед., нормальное давление в легочной артерии;
- неопределенный тип-значения УИ и УПС-1 не укладываются ни в один определенный тип. Как правило, это наблюдается на фоне лекарственной терапии кардиотониками или вазоактивными препаратами. Обычно это такие соотношения УИлж и УПС-1, при которых оба показателя достоверно повышены либо оба понижены.
Наиболее интересным и сложным звеном регионального спланхнического кровообращения является гемодинамика печени, в частности, портальный кровоток.
Воротная вена (ВВ) собирает кровь от непарных органов брюшной полости. Воротная вена образуется при слиянии селезеночной, верхней и нижней брыжеечной вен, а иногда и желудочных вен. Портальная система представлена висцеральной венозной сосудистой сетью брюшной полости и таза. Она располагается между двумя капиллярными сетями: пищеварительной и печеночной. Анатомически воротная система подразделяется на главную, представленную воротной веной и ее ветвями, и добавочную портальную систему, представленную венами Саппей.
Воротную вену целесообразно исследовать с оценкой кровотока в дуплексном режиме, т.е. с использованием импульсной допплерографии и цветового допплеровского картирования (ЦДК) в нескольких отделах:
- во внепеченочном сегменте, т.е. в области локации головки поджелудочной железы, где селезеночная вена вливается в более крупный отдел-основной ствол воротной вены;
- в месте вхождения воротной вены в ворота печени, где она практически сразу делится на две ветви-правую и левую, направляющиеся в соответствующие доли печени;
- в ветвях 2-3-го порядка правой и левой ветвей воротной вены.
В норме диаметр воротной вены колеблется и зависит от фаз дыхания, приема пищи, положения тела и степени физической активности. Так, он значительно увеличивается при вдохе и уменьшается на выдохе.
L. Bolondi и соавт. (1982) установлено, что на уровне мезентерико-воротного слияния колебание диаметра воротной вены между глубоким вдохом и полным выдохом составляет в норме 30-50%.
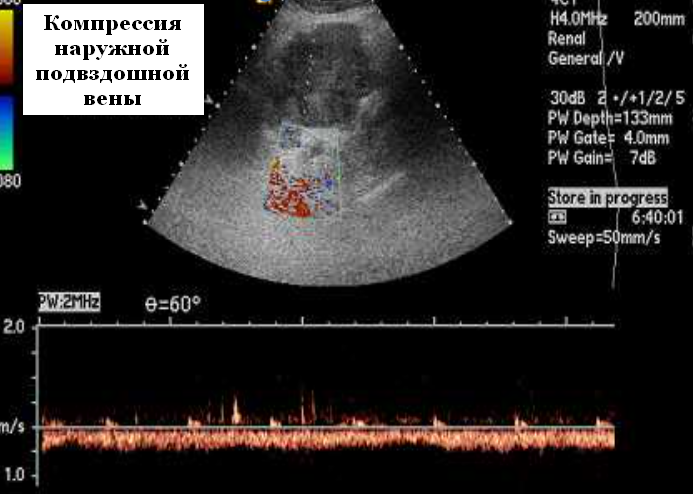
Качественный анализ спектра допплеровского сдвига частот в воротной вене выявляет непрерывный, близкий к ламинарному, поток с незначительными колебаниями, связанными с актом дыхания. Он не зависит в норме от ритма сердечной деятельности (рис. 1).
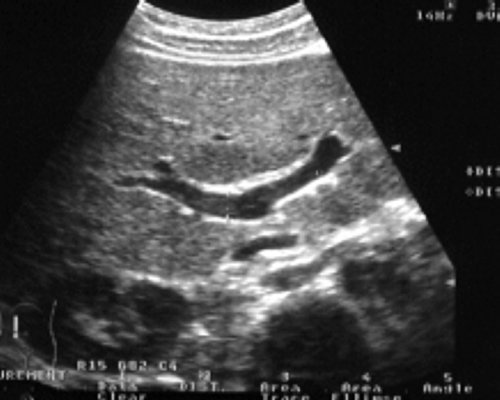
Рис. 1. Локация основного ствола в воротах печени (внутрипеченочный отдел), правой и левой ветвей воротной вены.
Количественный анализ кровотока в воротной вене включает определение средней линейной и объемной скоростей кровотока. Средняя линейная скорость кровотока в воротной вене колеблется от 15,0+4,4 см/с до 12,4+3,5 см/с и соответственно объемная скорость кровотока — от 578±312 мл/мин до 426±240 мл/мин. При анализе этих показателей после физической нагрузки отмечено снижение линейной скорости кровотока с 12,4±3,5 см/с до 11,1±3,4 см/с, а объемная скорость кровотока — с 426±24,0 мл/мин до 324±15,6 мл/мин. В течение последующих 10 мин значения этих показателей в норме возвращаются к исходным. Moriyasi и соавт. (1992) показали, что объемный воротный кровоток у здоровых людей варьирует в широких пределах — от 605 до 1173 см³/мин. Причем пиковая скорость и объемный кровоток в воротной вене меняются в пределах 10-15% и 14-20% соответственно.
Г.И. Кунцевич и соавт. (1994), проводя оценку портального кровообращения у здоровых лиц до и после приема пищи, установила, что в воротной вене и в селезеночной вене (СВ) уже через 5-10 мин происходит прирост линейной скорости кровотока на 90% в воротной вене и на 70% — в СВ. Параллельно с этим регистрируется увеличение объемной скорости кровотока, достигающей максимального прироста 110- 120% через 30 мин в воротной вене и через 40 мин — в СВ. У мужчин объемный кровоток в воротной вене составляет около 1000-1200 мл/мин.
Непосредственно в воротах печени воротной вены делится на две ветви, соответствующие правой и левой долям. Распределение портального кровотока в печени непостоянно. Возможно преобладание кровотока либо в правой, либо в левой доле печени, возможен и коллатеральный переток крови из системы одной долевой ветви в другую (рис. 2-5).
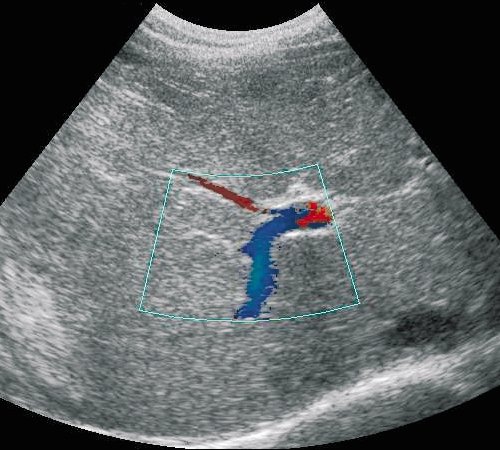
Рис. 2. ЦДК. Кровоток в правой передней ветви воротной вены (синее кодирование).
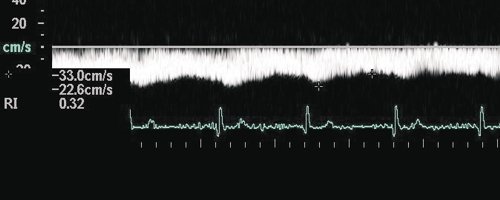
Рис. 3. Импульсная допплерография. Близкий к ламинарному воротный кровоток с элементами пульсации.
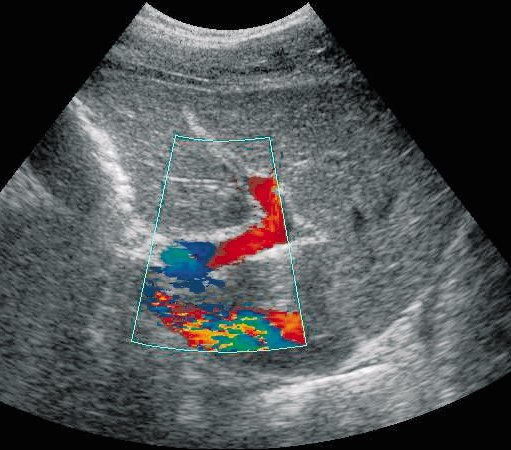
Рис. 4. ЦДК. Латеральная ветвь левой воротной вены. Видно продолжение направления сепарации круглой связки печени с остатком пупочной вены.
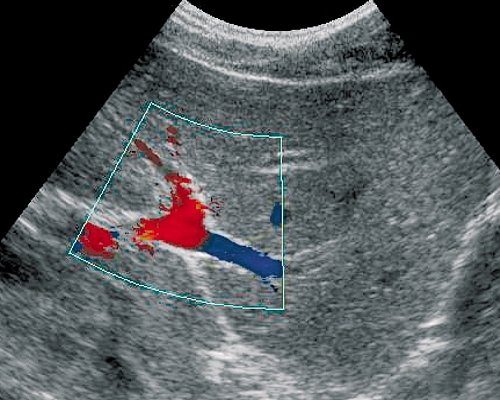
Рис. 5. ЦДК. Медиальная ветвь левой воротной вены (синее кодирование потока крови).
Правая ветвь воротной вены разделяется на переднюю и заднюю, а левая-на медиальную и латеральную. В области бифуркации левая ветвь соединена с круглой связкой печени (облитерированная пупочная вена). Это важная анатомическая особенность, так как слияние круглой связки печени и левой ветви воротной вены определяет наиболее частую локализацию околопупочных портосистемных коллатералей, возникающих при портальной гипертензии. У здорового человека кровоток в венах портальной системы направлен вперед, в сторону печени. Такое направление называется гепатопетальным. Кровоток из печени назад из воротной вены называется гепатофугальным (рис. 6).
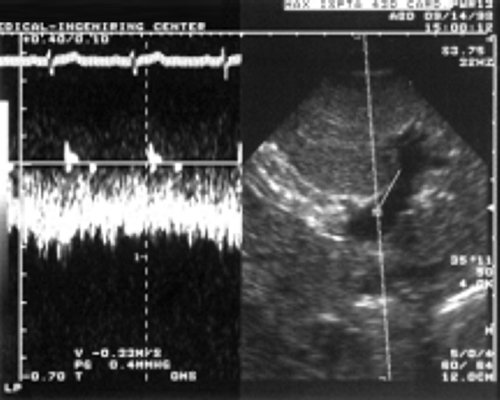
Рис. 6. Гепатофугальный кровоток в воротной вене. Направление из левой ветви вниз, в основной ствол воротной вены.
Направление потока легко определяется методом цветового допплеровского картирования. Следует отметить, что в местах ветвления воротной вены кровоток окрашивается в зависимости от направления потока по отношению к УЗ-лучу.
В норме у здорового человека гепатопетальный поток отмечается в любом отделе портальной венозной системы. Паренхиматозные процессы часто лежат в основе сосудистых аномалий. В свою очередь, первичные сосудистые поражения оказывают непосредственное влияние на паренхиму печени. При циррозе печени с прогрессирующим нарастанием портальной гипертензии возникают аномальные кровотоки в воротной вене как в отдельных исследуемых ее участках, так и в основном стволе.
Выделяют следующие виды аномальных потоков в воротной вене:
- реверсивный (гепатофугальный поток)-полностью изменивший направление поток. Это относительно редкая аномалия. Реверсивный поток часто сочетается с наличием коллатералей. Изолированный реверсивный поток в правой ветви воротной вены движется только из расширенной параумбиликальной вены. Изолированный реверсивный поток в левой ветви воротной вены часто связан с функционирующим параумбиликальным кровообращением или сочетается с отсутствием потока в желудочной вене. Гепатофугальный реверсивный поток в селезеночной вене имеет связь со спленоренальными коллатералями;
- полное отсутствие (аннулирование) потока в основном стволе воротной вены выявляется реже, чем отсутствие его в отдельных ветвях. Это является признаком выраженной портальной гипертензии, но без явных коллатералей. Когда поток в основной портальной вене реверсивный, то кровь, текущая во внутрипеченочные воротные ветви, должна поступать из артерий печени через шунты. Существует два типа таких шунтов. Транссинусоидальный шунт связан с тем, что кровь течет от печени к воротам на долевом уровне. Переднепортальный шунт возникает из увеличенной центрально расположенной венозной сосудистой коммуникации. Этот шунт обычно проводит поток в печень. Аннулирование потока в основном стволе происходит при синдроме Бадда-Киарри и при наличии портокавального шунта «бок в бок»;
- преходящее аннулирование потока в портальных венах возможно при трикуспидальной регургитации. Механизм этого явления до конца не понятен и может быть связан, например, с ритмичным увеличением синусоидального давления в систолу желудочков сердца;
- пульсирующий поток (двунаправленный) — фазный; при нем гепатофугальный и гепатопетальный потоки уравновешены. При цветовом допплеровском картировании поток поочередно кодируется красным и синим цветом, отражая изменение фаз направления потока. Разновидность двунаправленного кровотока при цветовом допплеровском картировании — винтовой поток при тромбозе воротной вены. Он может быть полностью гепатопетальным;
- двухцветная воротная вена — одновременная регистрация в одном участке воротной вены двух разнонаправленных потоков — в печень и из печени;
- застывший или неподвижный поток описан как отражение допплеровских сигналов от негустой крови в воротной вене. Он может выявляться после хирургического или естественного спленоренального шунтирования, иногда при циррозе печени, как правило, без коллатералей.
Среди всех видов аномальных кровотоков в воротной вене наиболее важным, с точки зрения кардиосовместимой допплерографии при дифференциальной диагностике первичных и вторичных печеночных болезней, является пульсирующий кровоток (рис. 7).
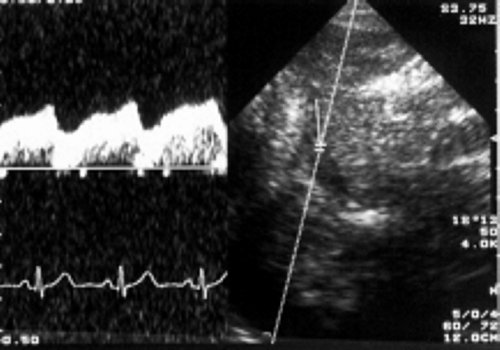
Рис. 7. Вариант пульсирующего кровотока в воротной вене.
Такая пульсация кровотока в воротной вене напрямую связана с деятельностью правого сердца через печеночные синусоиды. Она возникает при повышении давления в правом предсердии и при повышении центрального венозного давления (ЦВД). Поэтому пульсирующий допплеровский спектр кровотока «привязан» к комплексу QRS на ЭКГ. В этом случае минимальная скорость воротного потока соответствует систоле желудочков сердца. Он оценивается по так называемой шкале градаций пульсации потока в воротной вене. При нормальном давлении в правом предсердии, т.е. до 10 мм. рт. ст., отмечаются: 1-я и редко 2-я градации. При повышении давления в ПП градации увеличиваются. При наличии трикуспидальной недостаточности отмечаются 4-я или 5-я градации. Следует обратить внимание на отсутствие корреляции между степенью трикуспидальной недостаточности и шкалой пульсации в воротной вене. Феномену пульсирующего кровотока в воротной вене часто сопутствует спленомегалия. Оценка портальной гемодинамики в рамках кардиосовместимой допплерографии проводится при сопоставлении показателей кровотока в воротной вене с уровнем функционирования левого желудочка (УИ, СИ, УПС за 1 кардиоцикл). Пульсирующий кровоток в воротной вене требует анализа, аналогичного анализу артериального кровотока с учетом RI и PI в сочетании с оценкой функции правого предсердия и транстрикуспидального кровотока.
Для практического использования предложена следующая «шкала градаций пульсирующего кровотока в воротной вене»:
- 1-я — монофазный постоянный кровоток, не связанный с сердечной деятельностью. Это вариант нормального потока. Показатель пульсации в норме превышает 0,55. Этот показатель пульсации рассчитывается как соотношение минимальной скорости кровотока в воротной вене к максимальной. Если он меньше или равен 0,54, такой поток является пульсирующим;
- 2-я — систолический пульсирующий кровоток легкой степени. Амплитуда пульсации менее 1/3 основного спектра;
- 3-я — систолический пульсирующий кровоток средней степени. Амплитуда пульсации от 1 до 2/3 основного спектра;
- 4-я — выраженный систолический пульсирующий кровоток с разрывом основного спектра. В систолу желудочков сердца скорость кровотока в воротной вене падает, а допплеровский спектр располагается на изолинии;
- 5-я — реверсивный систолический кровоток. В этом случае в систолу желудочков появляется ретроградный (ниже изолинии) кровоток. Разница между максимальной и минимальной скоростями потоков составляет 50-60 см/с. Это классический вариант двунаправленного потока.
Т. Hosoki и соавт. (1990) обследовали с помощью подобной методики больных с патологией печени, застойной сердечной недостаточностью и здоровых. У больных с сердечной недостаточностью (СН) показатель пульсации-от максимума до минимума скорости в воротной вене — колебался от 0 до 0,54. При этом среднее значение постоянной части спектра составляло 0,45. У некоторых больных с выраженной СН показатель пульсации достигал 0,58; у больных с синдромом Бадда-Киарри он достигал 0,99, у больных с хроническим гепатитом и циррозом он варьировал от 0,91 до 0,81. Считается, что пульсирующий кровоток в воротной вене по мере своего увеличения является механическим фактором, влияющим на функцию правого предсердия. Он усугубляет застойную сердечную недостаточность.
Исследование воротной вены имеет особое значение для изучения сосудистой патологии спланхнического региона. Характер изменений воротного кровотока был детально изучен при сосудистой патологии, связанной с препятствием продвижения крови по сосуду в различных отделах портального кровообращения. Тем не менее остаются не совсем понятными изменения кровотока при диффузных поражениях печени первичного и вторичного характера.
Цель работы — изучение характера кровотока в воротной вене при патологии сердца и при диффузной патологии печени в зависимости от уровня функционирования сердца, а также уточнение его клинического и прогностического значения.
Материалы и методы
Обследованы 287 человек. Все больные разделены на 4 группы: 1 группа — 56 пациентов с ишемической болезнью сердца и стенокардией 1-2 функционального класса (NYHA) без недостаточности кровообращения; 2-я группа — 48 пациентов с ишемической болезнью сердца, атеросклеротическим и постинфарктным кардиосклерозом, стенокардией 3-4 ФК (NYHA) c недостаточностью кровообращения 2Б (по Василенко-Стражеско); 3 группа — 93 больных с хроническими вирусными гепатитами (В,С) с индексами Кноделля до 4-6 баллов с минимальными степенями активности по классификации 1994 г. (Лос-Анджелес); 4 группа — 51 больной с достоверно установленным циррозом печени с портальной гипертензией и степенью тяжести по шкале Чайлд-Пью от А до В. К 5 контрольной группе отнесены 39 практически здоровых лиц.
Допплерография воротной вены проводилась из субкостального доступа в области внутрипеченочного отдела основного ствола воротной вены, а также в начальной части бифуркации в правой ветви воротной вены и/или во внутрипеченочных ветвях синхронно с ЭКГ маркером систолы и диастолы. Кровоток в воротной вене оценивался по методике Т. Hosoki и соавт. (1990). При этом запись кровотока проводилась при задержке дыхания в среднем между вдохом и выдохом положении с установкой контрольного объема в центре воротной вены под углом, не превышающим 45°, и шириной контрольного объема 3-10 мм.
Эзофагогастродуоденоскопия проводилась всем обследованным по общепринятой методике для выявления ранних вариксов в этом участке пищеварительного тракта — наиболее частом месте локализации портосистемных шунтов.
Методы количественного анализа
Исходные показатели:
ДВВ-диаметр воротной вены (норма в среднем 8,9 мм);
ПСВВ — площадь сечения воротной вены (норма 0,6 см²);
Vmean — средняя скорость кровотока;
Vmax — максимальная или пиковая линейная скорость (норма 15 см/с);
Vmin — минимальная линейная или диастолическая скорость потока.
В формате кардиосовместимой допплерографии на основании этих измерений рассчитываются следующие показатели:
ИОКВВ — индекс объемного кровотока в воротной вене;
Vmax/ДВВ, т.е. «индекс застоя» — отношение линейной скорости потока к диаметру воротной вены (или площади сечения воротной вены).
Объемная скорость в воротной вене рассчитывается по формуле:
F = A · Vmean · 60 (л/мин),
где А = 0,25·ПИ·(d1хd2), а d1 и d2 — размеры эллипсоидного сечения воротной вены.
Для сопоставления этого показателя с системной гемодинамикой целесообразно пользоваться индексом объемного кровотока, нормированным на поверхность тела. Учитывая факт отсутствия зависимости от сердечной деятельности этого показателя в норме, следует вводить в расчет фактор времени, т.е. коэффициент — 60 (Sabba C., 1990).
Для оценки объемного венозного портального кровотока (венозного притока) в печень используются следующие скоростные индексы:
ИОКВВ — индекс объемного кровотока в воротной вене за 1 мин:
ИОКВВ (мл/мин · м²) = 1,055 · ПСВВ (см²) · Vвв (см/с) · 60 / BSA (м²) = 63,3 · ПСВВ (см²) · Р (см/с) / BSA (м²),
где Р — линейная скорость кровотока в воротной вене.
ИОКВВ у здоровых равен в среднем 333 мл/м² (324,4±6,9 мл/м²).
Для стандартизации полученных расчетов общепринятым считается измерение кровотока в правой ветви воротной вены на расстоянии 3-4 см от ворот печени. Объемный воротный кровоток, выраженный в процентах к минутному объему сердца (VоВВ%МОС), в норме равен 13-20%.
Корреляционный и кросс-корреляционный анализ полученных результатов в каждой группе проводился с учетом коэффициента корреляции Пирсона:
rxy = СУММА(dx · dy) / КОРЕНЬ [СУММА (dx² · dy²)].
В анализе полученных данных участвовали лишь достоверные результаты с учетом значения критерия «t» для 3-х степеней вероятности и стандартные коэффициенты «r», которые считаются достоверными.
Результаты исследования
Качественный анализ допплерэхограмм в импульсном режиме и цветовом допплеровском картировании портального кровообращения у больных ишемической болезнью сердца и у больных с диффузными поражениями печени выявил наличие разной степени выраженности пульсирующего характера кровотока. Высокие градации пульсирующего портального кровотока у больных 2 группы коррелировали с наличием трикуспидальной регургитации, что вполне согласуется с данными литературы. У 7 больных 4 группы также установлен пульсирующий характер портального потока. Однако, по нашим наблюдениям, он не коррелирует с тяжестью цирроза печени. У 5 больных при цветовом допплеровском картировании выявлена «двухцветная воротная вена». Как известно, наличие этого признака ассоциируется с портальной гипертензией выше 10-15 мм рт. ст. В 4 случаях из 47 у больных 4 группы было обращено внимание при импульсной допплерографии на реверсию портального кровотока ниже изолинии.
По данным ЭГДС, мелкие низкие эзофагальные вариксы выявлены у 73,5% больных 4-й группы (причем у 4-х — с признаками бывших геморрагий), мелкие «ранние» вариксы — у 23,3% больных 3-й группы и у 13,7% больных 2-й группы. У всех лиц контрольной и 1-й групп эзофагальных вариксов не выявлено.
Количественный анализ индексов объемного портального кровообращения показал, что индекс объемного кровотока в воротной вене (ИОКВВ) у больных 4-й группы оказался самым низким, составив 293,1 мл/мин/м² (для сравнения, в контрольной группе он составил 324,5 мл/мин/м², у больных 1-й (387,5 мл/мин/м²), 2-й (377,0 мл/мин/м²) и 3-й (366,0 мл/мин/м²) групп он оказался достоверно выше, чем у больных с циррозом печени. Из этого следует, что по сравнению с 1-й, 2-й и 3-й группами при достоверно наибольшем значении площади сечения воротной вены у больных 4-й группы (1,39 см²) и при достоверно наименьшей линейной скорости потока (6,3 см/с) объемный кровоток у этих больных недостоверно меньше, чем в контрольной группе. Однако все же он меньше, чем в первых трех группах. Это подтверждается при анализе второго индекса объемного портального кровотока, выраженного в % к минутному объему сердца. По результатам этого исследования, только 12,5% минутного объема сердца составляет портальный объемный поток у больных циррозом печени с портальной гипертензией, тогда как в контрольной группе-13,3% минутного объема сердца, а у больных 3-й группы с хроническим вирусным гепатитом — 15,6% минутного объема сердца.
В 1-й группе у больных ишемической болезнью сердца без недостаточности кровообращения портальный кровоток составил в среднем 16% минутного объема сердца, а во 2-й группе — более 1/5 минутного объема сердца — 22,0%. Это достоверно больше, чем у больных циррозом с портальной гипертензией и в контрольной группе.
Таким образом, результаты исследования объемного портального кровотока, нормированного на минутный объем сердца, выявляют принципиальное отличие портального кровообращения печени при ишемической болезни сердца с недостаточностью кровообращения и при циррозе печени с портальной гипертензией. При сердечной недостаточности недостоверно снижается артериальный печеночный поток при достоверном нарастании венозного портального кровотока, а у больных циррозом печени с портальной гипертензией отмечается достоверное снижение относительного артериального и венозного портального притока крови к печени. Причина этого явления — «застой» или повышение давления (гидродинамический затвор или преграда портальному потоку) в системе портального кровообращения. Ранее существовало представление, что при нарастании портальной гипертензии у больных с циррозом печени развивается так называемый гипердинамический синдром. Эти результаты кардиосовместимой допплерографии портального кровообращения показывают истинное соотношение гемодинамик печени и сердца.
Анализ портального кровообращения у больных с различными типами центральной гемодинамики
Нормокинетический тип. Портальный венозный поток у больных с разной патологией сердца и печени, но с одинаковыми значениями УИ при нормокинетическом типе центральной гемодинамики имеет закономерности, представленные в табл. 1.
Таблица 1. Портальное кровообращение печени при нормокинетическом типе центральной гемодинамики.
| Группа/показатель | ДСВВ, мм | Р, см/с | VoBB%MOC | ИОКВВ, мл/м² |
|---|---|---|---|---|
| 1/Ишемическая болезнь сердца без недостаточности кровообращения, n=58 | 9,5 ± 1,1 | 16,1 ± 1,3 | 16,1 ± 1,5 | 389,8 ± 8,0 |
| 2/Ишемическая болезнь сердца с недостаточностью кровообращения, n=5 | 11,1 ± 1,3 | 11,9 ± 1,6 | 15,8 ± 1,5 | 399,1 ± 19,2 |
| 3/Хронический вирусный гепатит, n=56 | 9,3 ± 1,1 | 15,2 ± 1,2 | 14,2 ± 1,6 | 355,1 ± 10,7 |
| 4/Цирроз с портальной гипертензией, n=26 | 13,3 ± 1,2 | 6,4 ± 0,1 | 13,2 ± 1,4 | 297,1 ± 9,5 |
| 5/Контроль, n=51 | 8,9 ± 1,1 | 15,1 ± 1,3 | 13,9 ± 1,4 | 333,9 ± 9,7 |
Доля портального кровотока относительно минутного объема сердца достоверно не отличается ни в одной из групп относительно контроля и между собой. В контрольной группе объемный портальный поток сопоставим в среднем с 13,9% минутного объема сердца; в 4-й группе у больных с циррозом печени и портальной гипертензией — 13,2% минутного объема сердца; в 3-й группе у больных хроническим вирусным гепатитом — 14,2% минутного объема сердца; в 1-й группе при ишемической болезни сердца без недостаточности кровообращения — 16,1% минутного объема сердца; во 2-й группе у больных ишемической болезнью сердца с недостаточностью кровообращения — 15,8% минутного объема сердца.
Анализ абсолютных значений объемного портального кровообращения выявил тенденцию к снижению его у больных циррозом печени и портальной гипертензией и к увеличению — у больных с ишемической болезнью сердца. Так, в контрольной группе ИОКВВ составил в среднем 333,9 мл/мин/м², в 1-й и 2-й группах повышается в среднем до 389,8 мл/мин/м² и 399,1 мл/мин/м². В 3-й группе ИОКВВ составил в среднем 355,1 мл/мин/м², в 4-й — снижается несколько менее остальных, в среднем до 297,1 мл/мин/м².
Более чувствительным параметром оказалась средняя амплитуда линейной скорости потока в воротной вене. У больных с циррозом печени она снижается до 6,4 см/с, т.е. в 2,5 раза по сравнению с контролем, где она составляет в среднем 15,1 см/с. У больных 1-й и 3-й групп она составила соответственно 16,1 и 15,2 см/с, а во 2-й группе несколько ниже, чем в контрольной и 1-й и 3-й группах, но выше, чем у больных 4-й группы, составляя в среднем 11,9 см/с.
Как известно, поперечное сечение воротной вены в норме имеет овальный профиль. При портальной гипертензии оно становится округлым и диаметр увеличивается более 12 мм. В 4-й группе переднезадний диаметр воротной вены увеличен в среднем до 13,3 мм по сравнению с контролем (8,9 мм). В 1-й и 3-й группах этот размер достоверно не отличается от контроля, составляя соответственно 9,4 и 9,3 мм. У больных 2-й группы диаметр воротной вены составил в среднем 11,1 мм, что больше, чем в контроле, но меньше, чем у больных циррозом.
Таким образом, оказалось, что абсолютный и относительный объемный портальный кровотоки у больных с нормокинетическим типом центральной гемодинамики, у больных с ишемической болезнью сердца с недостаточностью кровообращения и у больных с циррозом печени с портальной гипертензией существенно не отличаются от контрольной и от остальных групп.
Гипокинетический тип. Сравнение функции ЛЖ у больных с гипокинетическим типом центральной гемодинамики выявило ведущую причину снижения у них УИ, во-первых, вследствие снижения сократительных свойств миокарда ЛЖ, во-вторых, из-за нарастания объемной перегрузки ЛЖ и появления митральнопапиллярной дисфункции с митральной регургитацией. Анализ портального кровообращения у больных с гипокинетическим типом центральной гемодинамики показал, что у больных с хроническим вирусным гепатитом на фоне диффузного поражения печени выявлено и относительное и абсолютное нарастание портального кровотока (табл. 2).
Таблица 2. Портальное кровообращение печени при гипокинетическом типе центральной гемодинамики.
| Группа/показатель | ДСВВ, мм | Р, см/с | VoBB%MOC | ИОКВВ, мл/м² |
|---|---|---|---|---|
| 1/Ишемическая болезнь сердца без недостаточности кровообращения, n=20 | 9,3 ± 1,1 | 15,6 ± 1,5 | 17,7 ± 1,8 | 361,9 ± 18,7 |
| 2/Ишемическая болезнь сердца с недостаточностью кровообращения, n=22 | 10,6 ± 1,1 | 12,7 ± 1,2 | 19,1 ± 1,6 | 382,7 ± 11,7 |
| 3/Хронический вирусный гепатит, n=19 | 9,9 ± 1,2 | 15,0 ± 1,3 | 20,9 ± 1,9 | 404,1 ± 19,8 |
| 4/Цирроз с портальной гипертензией, n=14 | 13,2 ± 1,2 | 6,4 ± 1,1 | 12,4 ± 1,6 | 305,7 ± 10,2 |
| 5/Контроль, n=30 | 8,5 ± 1,1 | 14,4 ± 1,3 | 12,4 ± 1,5 | 293,5 ± 9 |
Так, ИОКВВ в 3-й группе составляет в среднем 404,1 мл/мин/м², в контроле — 293,5 мл/мин/м², в 4-й группе у больных с циррозом печени ИОКВВ не отличается от контроля, составляя 305,7 мл/мин/м². В 1-й и 2-й группах ИОКВВ недостоверно выше, чем в контрольной, составляя в 1-й 362 мл/мин/м², а во 2-й — 382,7 мл/мин/м². В то же время увеличенное УПС-1 затрудняет возврат венозной крови к сердцу через периферию и, наоборот, переключает этот возврат через печень, особенно у больных хроническим вирусным гепатитом с гипокинетическим типом центральной гемодинамики.
Гиперкинетический тип центральной гемодинамики. Этот вариант центральной гемодинамики не выявлен у больных ишемической болезнью сердца с клинически выраженной недостаточности кровообращения и у больных с циррозом печени с портальной гипертензией (табл. 3).
Таблица 3. Портальное кровообращение печени при гиперкинетическом типе центральной гемодинамики.
| Группа/показатель | ДСВВ, мм | Р, см/с | VoBB%MOC | ИОКВВ, мл/м² |
|---|---|---|---|---|
| 1/Ишемическая болезнь сердца без недостаточности кровообращения, n=11 | 9,7 ± 1,1 | 15,2 ± 1,9 | 13,5 ± 1,1 | 396,1 ± 29,2 |
| 2/Ишемическая болезнь сердца с недостаточностью кровообращения, n=0 | — | — | — | — |
| 3/Хронический вирусный гепатит, n=11 | 9,0 ± 1,3 | 14,7 ± 1,5 | 11,5 ± 1,9 | 338,1 ± 33,6 |
| 4/Цирроз с портальной гипертензией, n=0 | — | — | — | — |
| 5/Контроль, n=9 | 9,5 ± 1,1 | 15,4 ± 1,8 | 12,7 ± 1,8 | 398,9 ± 25,2 |
Сравнительный анализ показал, что абсолютный и относительный портальный кровоток несколько снижен у больных хроническим вирусным гепатитом с гиперкинетическим типом относительно контрольной и 1-й групп.
Застойный тип центральной гемодинамики. Этот вариант кровообращения был выявлен лишь у больных 2-й группы, поэтому проводить сравнительный анализ с другими группами невозможно — подобный вариант центральной гемодинамики может не развиваться у больных с диффузными поражениями печени либо подобные больные могут не попасть в данную выборку. Возможно, более обширная статистика позволит получить ответы на вопросы.
У больных ишемической болезнью сердца с застойным типом центральной гемодинамики ранее был описан феномен «пульсирующего портального потока» различной степени выраженности и достоверно не связанного с передаточной пульсацией от соседних артериальных стволов. У всех больных этой группы мы также отметили пульсирующий характер потока при задержке дыхания в среднем положении. Поэтому значение средней линейной скорости портального потока рассчитывали (табл. 4) как средний интеграл 3-5 измерений пульсирующих комплексов (площадь под кривой, огибающей пульсирующий спектр потока в воротной вене).
Таблица 4. Портальное кровообращение печени при застойном типе центральной гемодинамики.
| Группа/показатель | ДСВВ, мм | Р, см/с | VoBB%MOC | ИОКВВ, мл/м² |
|---|---|---|---|---|
| 2/Ишемическая болезнь сердца с недостаточностью кровообращения | 10,7 ± 1,1 | 12,2 ± 1,2 | 25,9 ± 1,4 | 267,0 ± 9,4 |
Параметры воротной вены, линейной скорости портального потока и абсолютное значение объемного портального венозного притока к печени у больных с застойным типом центральной гемодинамики практически не отличаются от гипокинетического типа. Однако на фоне резкого снижения насосной функции ЛЖ у больных с застойным типом центральной гемодинамики отмечается достоверный рост относительного портального кровообращения. Если ИОКВВ у больных с застойным типом составляет в среднем 367,04+9,38 мл/мин/м², т.е. практически столько же, сколько при гипокинетическом типе (соответственно 382,7+11,7 мл/мин/м²), то относительный объемный воротный кровоток в % к минутному объему сердца увеличен в среднем до 25,9+1,4% минутного объема сердца по сравнению с 19,1+0,6% минутного объема сердца у больных с гипокинетическим типом.
Гиповолемический тип центральной гемодинамики. В нашем исследовании этот вариант центральной гемодинамики выявлен лишь у больных 3-й и 4-й групп. Этот факт, возможно, свидетельствует о формировании условий к большему депонированию крови в явных и скрытых вариксах и иных участках венозной системы спланхнического кровообращения. Кроме того, относительная малочисленность этих групп не позволяет сделать достоверные заключения.
Тем не менее параметры портального венозного притока к печени у больного 4-й группы существенно хуже, чем в 3-й группе. Так, диаметр воротной вены больше, линейная скорость портального потока, абсолютный и объемный относительный портальный поток более чем в два раза меньше, чем в 3-й группе (табл. 5).
Таблица 5. Портальное кровообращение печени при гиповолемическом типе центральной гемодинамики.
| Группа/показатель | ДСВВ, мм | Р, см/с | VoBB%MOC | ИОКВВ, мл/м² |
|---|---|---|---|---|
| 3/хронический вирусный гепатит | 10,1 ± 1,3 | 14,5 ± 1,6 | 26,3 ± 1,9 | 432,5 ± 24,1 |
| 4/цирроз с портальной гипертензией | 12,8 | 5,9 | 10,7 | 217,5 |
Неопределенный тип. Размеры воротной вены и значения линейной скорости портального венозного потока-притока у больных с неопределенным типом центральной гемодинамики полностью совпадают с нормокинетическим типом (табл. 6).
Таблица 6. Портальное кровообращение печени при неопределенном типе центральной гемодинамики.
| Группа/показатель | ДСВВ, мм | Р, см/с | VoBB%MOC | ИОКВВ, мл/м² |
|---|---|---|---|---|
| 1/Ишемическая болезнь сердца без недостаточности кровообращения, n=3 | 9,9 ± 1,1 | 15,7 ± 1,3 | 13,5 ± 1,4 | 447,7 ± 53,0 |
| 2/Ишемическая болезнь сердца с недостаточностью кровообращения, n=2 | 10,9 ± 1,7 | 12,8 ± 1,7 | 21,5 ± 1,9 | 377,8 ± 54,1 |
| 3/Хронический вирусный гепатит, n=4 | 9,2 ± 1,3 | 14,9 ± 1,5 | 13,9 ± 1,6 | 365,4 ± 24,6 |
| 4/Цирроз с портальной гипертензией, n=6 | 13,100 ± 1,3 | 6,1 ± 0,2 | 9,5 ± 1,4 | 258,6 ± 12,6 |
| 5/Контрольная, n=9 | 8,7 ± 1,1 | 14,9 ± 1,7 | 13,4 ± 1,1 | 300,1 ± 18,4 |
Анализ объемного кровотока в воротной вене, нормированного на поверхность тела, показал, что абсолютное значение ИОКВВ у больных ишемической болезнью сердца без недостаточности кровообращения, т.е. в 1-й группе выше, а относительное значение в % к минутному объему сердца меньше, чем при нормокинетическом типе. Наоборот, у больных 2-й и 4-й групп, т.е. у больных ишемической болезнью сердца с недостаточностью кровообращения и у больных с циррозом печени и портальной гипертензией ИОКВВ меньше, а объемный кровоток в общей печеночной артерии в % к минутному объему сердца выше, чем при нормокинетическом типе. У лиц контрольной группы с неопределенным и нормокинетическим типами отмечено полное совпадение кровотока в ОПА.
Результаты коррелляционного анализа
Выявлена очень высокая прямо пропорциональная взаимосвязь допплеровского СИлж с диаметром печеночной вены (r=0,966 при р<0,001), с диаметром воротной вены (r=0,955 при р<0,001) и в большей степени с диаметром общей печеночной артерии (r=0,989 при р<0,001). Иными словами, чем больше допплеровский СИ, тем больше диаметры основных сосудистых стволов притока и оттока крови от печени.
Средняя линейная скорость в воротной вене достаточно высоко коррелирует с допплеровским СИлж (r=0,795 при р<0,001). Тесная взаимосвязь между венозным портальным и артериальным притоком к печени в ОПА проявляется при анализе средней линейной скорости в воротной вене, диаметра ОПА (r=0,798), индекса PI (r=0,795), индекса RI (r=0,793), пола (r=0,788), косвенного индекса митральной регургитации (r=0,792) и типа центральной гемодинамики (r=0,756) с одинаково высокой достоверностью при р<0,001.
В нашем исследовании доказано с высокой достоверностью, что у мужчин чаще, чем у женщин, встречаются более высокие градации типа центральной гемодинамики (нормо- и гиперкинетический) (r=0,971). И, наоборот, низкие градации типа центральной гемодинамики достоверно чаще встречаются у женщин.
Абсолютное значение индекса объемного кровотока в воротной вене не коррелирует с допплеровским и эхокардиографическим УИлж, УИпж, ИМПП и относительными (в % к минутному объему сердца) объемными потоками в ОПА (артериальный приток к печени) и в печеночных венах (интегральный венозный отток крови от печени).
Таким образом, полученные результаты свидетельствуют о существовании тесной взаимосвязи между венозным портальным кровообращением печени, с одной стороны, а с другой — о существовании тесной взаимосвязи между функцией сердца и кровообращением печени.
Обсуждение
Представленные в этой работе результаты показывают важность исследования сосудов спланхнического региона методом кардиосовместимой допплерографии. Этот подход к диагностике и дифференциальной диагностике нарушений кровообращения печени позволяет наиболее точно выявлять патологию и строить на основании этого прогноз развития фатальных осложнений.
Проведение сравнительных исследований в группах без учета типа центральной гемодинамики, как правило, дает неубедительные результаты. Из-за этого многие опубликованные результаты зарубежных авторов дают противоречивые, а иногда сомнительные выводы. Особенно следует быть осторожным при анализе таких результатов нарушения печеночной гемодинамики, как феномена «гипердинамического синдрома» при циррозе печени с портальной гипертензией, при кардиальном фиброзе печени с портальной гипертензией при сердечной недостаточности с трикуспидальной регургитацией. Наиболее прост в практическом применении «индекс застоя в печени» для диагностики портальной гипертензии как соотношение линейной скорости портального потока и диаметра воротной вены.
Установление типа центральной гемодинамики у больных с диффузным поражением печени, особенно гипокинетического и гиповолемического, имеет важное прогностическое и диагностическое значение в раннем выявлении скрытых эзофагальных вариксов.
Истинные допплеровские критерии определения типа центральной гемодинамики позволяют доказать, что застойный тип не выявляется у больных 1-й, 3-й и 4-й групп. В то же время гиповолемический тип не характерен для ишемической болезни сердца. Гиперкинетический тип не характерен как для цирроза печени с портальной гипертензией, так и для ишемической болезни сердца с недостаточностью кровообращения. Неопределенный тип выявлен во всех группах, но он малочислен и обусловлен скорее всего сопутствующим приемом кардиотоников и вазоактивных лекарственных веществ.
Импульсно-волновая допплерография портального потока, как, впрочем, и других венозных потоков спланхнического региона в рамках кардиосовместимой допплерографии, должна проводиться синхронно с ЭКГ для диагностики реверсивных и сдвиговых потоковых феноменов.
Выводы
При сердечной недостаточности со сниженным артериальным притоком крови к печени нарастает венозный портальный поток. При циррозе печени и портальной гипертензии снижается и артериальный и венозный портальный приток крови к печени.
При циррозе печени с гипокинетическим типом центральной гемодинамики по сравнению с нормокинетическим типом более выражены признаки портальной гипертензии и шунтирования крови через печень, минуя периферию. Гипокинетический и особенно гиповолемический типы центральной гемодинамики у больных с портальной гипертензией являются маркерами существующих портокавальных шунтов, что может служить неблагоприятным фактором возникновения кровотечений из вариксных сосудов. Косвенные признаки «артериализации печени» наиболее отчетливо выражены у больных хроническим вирусным гепатитом с гипокинетическим и гиповолемическим типами центральной гемодинамики.
На фоне резкого снижения насосной функции левого желудочка у больных с застойным типом центральной гемодинамики отмечается достоверный рост относительного портального кровообращения в % к минутному объема сердца в среднем до 25,9% по сравнению с 19,1% у больных с гипокинетическим типом центральной гемодинамики.
Абсолютные значения индексов венозного портального потока к печени увеличиваются по мере роста насосной производительности ЛЖ. Средняя линейная скорость портального потока коррелирует с допплеровским СИлж (r=0,795 при р<0,001).
Литература
- Кунцевич Г.И., Белолапотко Е.А., Сидоренко Г.В. Оценка состояния портального кровообращения у больных циррозом печени по данным дуплексного сканирования / Визуализация в клинике. — Декабрь. — 1994. — С. 33-38.
- Лелюк В.Г., Лелюк С.Э. Ультразвуковая ангиология. -Реальное время, 1999. — 286 с.
- Митьков В.В. Ультразвуковая диагностика (практическое руководство). Допплерография. — Видар: М., 1999.
- Милягин В.А. Нарушения внутрипеченочного кровообращения при хронических заболеваниях печени, их механизмы и коррекция / Дисс. д-ра мед. наук. — Пермь, 1989.
- Пыков М.И. Современные возможности лучевой диагностики в педиатрической практике / Дисс. докт. мед. наук. — М., 1997.
- Берестень Н.Ф., Цыпунов А.О. Допплерография периферических сосудов / Sonoace international, 1999, N 4.
- Берестень Н.Ф. Допплерэхография в комплексной оценке нарушений печеночной и сердечной гемодинамики / Дисс. докт. мед. наук. — М., 2000.
- Alpem M.B., Rubin J.M., Williams D.M. et al. Porta hepatis: duplex Doppler US with angiographic correlation, Radiology, 1987; 162:53.
- Barbara L. The value of Doppler US in the study of hepatic hemodynamics. Consensus conference, J. Hepatol.,1990; 10: 353-355.
- Bolondi L., Gandolfi L., Arienti V. et al. Ultrasonography in the diagnosis of portal hypertension: diminished response of portal, vessels to respiration, Radiology, 1982; 142: 167-172.
- Bolondi L., Gaiani S., Mazziotta A. et al. Morphological and hemodynamic changes in the portal venous system after distal splenorenal shunt: an ultrasound and pulsed Doppler study, Hepatology, 1988; 8:652-57.
- Bolondi L., Gaiani S., Barbara L. Accuracy and reproducibility of portal flow measurement by Doppler US, J. Hepatol., 1991; 13:269-73.
- De Vries P.J., Van Hattum J., Hoekstra J.B. et al. Duplex Doppler measurement of portal venous flow in normal sabjects. Inter and intra-observer variability J. Hepatol, 1991; 13:358-363.
- Duerinckx A., Grant E., Perella RR. et al. The pulsatile portal vеin in cases of congestive heart failure: correlation of duplex Doppler findings with right atrial pressure, Radiol., 1990; 176:655-658.
- Hosoki T., Arisawa J., Marukawa T. et al. Portal blood flow in congestive heart failure: pulsed duplex sonographic findings, Radiol., 1990; 733-736.
- Lafortune M., Marleau D., Breton G. et al. Portal venous system measurements in portal hypertension Radiology, 1984; 151:27-30.
- Nelson R.C., Sheburne G.M., Spencer H.B. et al. Splenic venous flow exceeding portal venous flow at Doppler sonography: relationship to portosystemic varices, AJR, 1993; 161:563-567.
- Ohnishi K., Saito M., Sato S. Portal hemodynamics in idiopathic portal hypertension (Banti syndrome) comparison with chronic persistent hepatitis and normal subjects, Gastroent., 1987; 92:751-758.
- Sabba C., Ferraioli G.G., Genecin P. et al. Evaluation of postprandial hyperemia in superior mesenteric artery and portal vein in healthy and cirrhotic humans: an operator-blind echo-doppler study Hepatology, 1991; 13:714-718.
- Zoli M., Iervese T., Merkel C. et al. Prognostic significance of portal hemodinamics in patients with compensated cirrhosis, J. Hepatol., 1993; 17:56-61.
УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Обзор общего кровообращения поможет понять компоненты венозной системы. Под малым кругом кровообращения понимается кровообращение в легких. Неоксигенированная кровь течет по легочным артериям в легкие. Вновь насыщенная кислородом кровь течет в левое предсердие через легочные вены. Системное кровообращение описывает центральное или периферическое кровообращение. Портальное кровообращение относится к возвращению крови из внутренних органов в печень, где она затем перемещается в нижнюю полую вену (НПВ), которая транспортирует кровь в правое предсердие сердца. Под глубокими венами понимаются глубокие вены верхних и нижних конечностей. Эти сосуды прилегают к артериям и имеют то же название, что и сопутствующая артерия. Глубокие вены расположены глубоко в тканях под фасцией и окружены мышцами. Количество сосудов может варьироваться при сравнении вен с артериями. Глубокие вены имеют прямое сообщение с НПВ и ВПВ.
Поверхностная венозная система расположена между слоями поверхностной фасции под кожным покровом. Эти сосуды возвращают кровь из этих областей и сообщаются с глубокими венами через перфорантные (перфорирующие) или коммуникантные вены. Перфорантные вены соединяют поверхностную систему с глубокой. Их называют перфорирующими венами, потому что они перфорируют фасцию при соединении двух систем.
Вены верхней конечности
Глубокая венозная система верхней конечности расположена ниже фасции, окружена мышцами и прилегает к сопутствующей артерии. Начиная с руки, глубокие ладонные вены сопровождают глубокую ладонную дугу, сообщаясь с глубокими локтевыми венами. Они соединяются с лучевыми венами на запястье. Межкостные вены сопровождают переднюю и заднюю межкостные артерии. Они начинаются на запястье и соединяются с лучевой и локтевой венами.
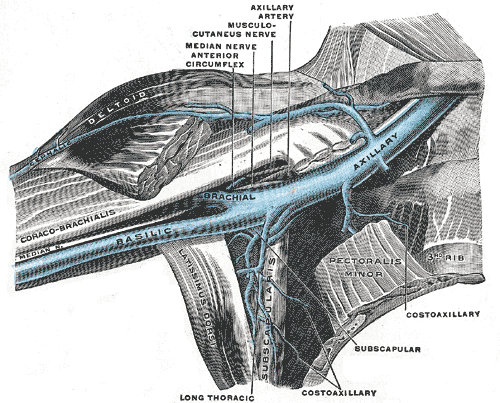
Общая локтевая вена — это короткий ствол, образованный передней и задней локтевыми венами, и их анатомия вариабельна. Когда присутствует ответвление, то она присоединяется к медиальной подкожной вене, образуя медиальную вену поверхностной системы. Лучевая и локтевая вены соединяются в локтевом суставе, образуя плечевую вену. Лучевая и локтевая вены различаются по течению как над, так и под фасцией. Плечевая вена начинается от передней локтевой ямки. Он проходит рядом с плечевой артерией по всей длине плечевой кости. Она заканчивается образованием подмышечной вены.
Подмышечная вена расположена на уровне подмышечной впадины и содержит около двух клапанов. Подключичная вена является продолжением подмышечной вены. Он идет от внешней границы первого ребра к внутреннему концу яремной вырезки. Она соединяется с внутренней яремной веной, образуя безымянную (плечеголовную) вену.
В отличие от артерий, здесь две безымянные вены, по одной с каждой стороны. Правая безымянная вена начинается у внутреннего медиального конца ключицы. Она соединяется с левой безымянной веной чуть ниже первого ребра, образуя верхнюю полую вену. Она также получает кровь из правой позвоночной вены, правой внутренней молочной железы, правой нижней щитовидной железы и иногда из правой верхней межреберной вены. Левая безымянная вена больше правой безымянной вены. Он проходит слева направо через верхнюю переднюю часть грудной клетки. Она соединяется с правой безымянной веной, образуя верхнюю полую вену.
Верхняя полая вена получает кровь из безымянных вен и транспортирует ее к сердцу. Она начинается чуть ниже первого ребра с правой стороны, входит в перикард и заканчивается в правом предсердии сердца.
Поверхностная система вен верхних конечностей
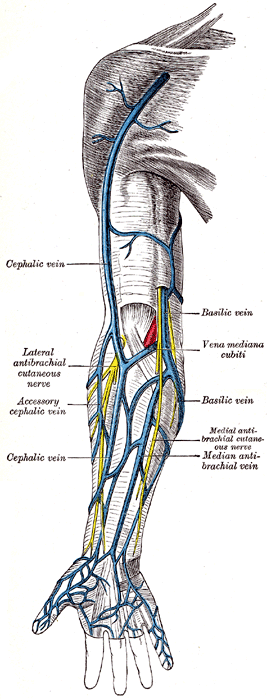
Обсуждение поверхностной системы верхней конечности начнется с руки. Поверхностные вены располагаются на тыльной поверхности кистей рук. Внутреннее и внешнее сплетения соединяются, образуя поверхностную арку на тыльной стороне кисти. Срединная вена проходит по внутренней стороне предплечья и соединяется с передними локтевыми и лучевыми венами. В локтевой ямке она соединяет латеральную (v.cefalica)) и медиальную (v.basilica) вены. Срединная латеральная вена проходит через бороздку между мышцей длинного супинатора и двуглавой мышцей, затем сливается с лучевой и латеральной венами. Срединная локтевая вена соединяет базиликовую и головную вены на уровне локтя.
Медиальная вена — самая крупная поверхностная вена верхней конечности. Он проходит медиально вверх по руке и перфорирует глубокую фасцию, переходя в подмышечную вену. Латеральная (головная) вена проходит вдоль боковой стороны руки и соединяется с глубокой системой выше подмышечной вены, образуя подключичную вену. Головная (латеральная) вена может оканчиваться у подмышечной вены у некоторых пациентов.
Глубокая система вен нижних конечностей
Глубокая венозная система нижних конечностей транспортирует кровь от ног к сердцу по нижней полой вене. Общие подвздошные вены начинаются примерно на 4 м поясничном позвонке на уровне бифуркации НПВ. Они разделяются на внутреннюю и наружную подвздошные вены и не содержат клапанов. Внутренние подвздошные вены отводят кровь от таза и соединяются с наружными подвздошными венами, чтобы отдать кровь в общие подвздошные вены.
Внутренние подвздошные вены обычно не содержат клапанов. Левая наружная подвздошная вена проходит по внутренней стороне соответствующей артерии. Правая наружная подвздошная вена проходит по внутренней стороне подвздошной артерии, а затем продолжается по пути позади артерии. В наружные подвздошные вены поступает кровь из глубоких надчревных и огибающих вен. Эти вены содержат до двух клапанов. Общая бедренная вена расположена на уровне паховой связки в паховой складке и лежит медиальнее общей бедренной артерии. Область сафено-бедренного соединения находится там, где большая подкожная вена впадает в общую бедренную вену. Общая бедренная вена делится на бедренную (ранее известную как поверхностная бедренная) и глубокие бедренные вены.
Бедренная вена прилегает к поверхностной бедренной артерии. Он начинается чуть ниже паховой связки и распространяется по всей длине бедра. В дистальной части он проходит кзади через приводящий канал, образуя подколенную вену. Примерно у 25% населения бедренные вены дублируются. Этот сосуд содержит до 4 клапанов. Подколенная вена располагается в подколенной ямке, прилегающей к подколенной артерии. Она получает кровь из икроножных вен от икроножной мышцы, суставных вен и малых подкожных вен. Двойная подколенная вена встречается примерно у 25% населения. В подколенной вене примерно 4 клапана.
Передние большеберцовые вены образованы венами тыльной стороны стопы и проходят между большеберцовой и малоберцовой костью над межкостной перепонкой. На каждую артерию голени приходится как минимум две вены. В большеберцовых и малоберцовых венах клапаны расположены примерно через каждые 2 см по длине сосудов. Задние большеберцовые вены образованы наружными и внутренними подошвенными венами. Они расположены кзади от медиальной лодыжки, продолжаясь вдоль медиальной стороны голени, образуя большеберцовый и малоберцовый ствол примерно на три пальца ниже колена. В задние большеберцовые вены также поступает кровь из подошвенных пазух икроножной мышцы. Малоберцовые вены проходят вдоль заднебокового ствола на том же уровне, что и задние большеберцовые вены.
Поверхностная венозная система нижних конечностей
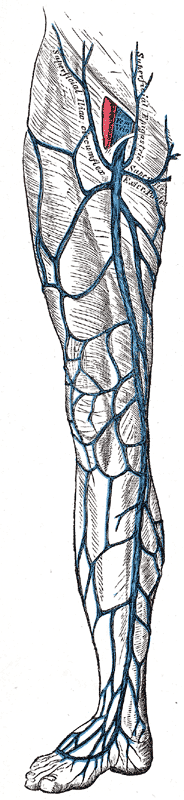
Поверхностная венозная система нижней конечности состоит из большой и малой подкожных вен. Большая подкожная вена (длинная подкожная вена), сокращенно БПВ, начинается спереди от медиальной лодыжки и проходит по внутренней стороне голени за большеберцовой костью. Он заканчивается у общей бедренной вены чуть ниже паховой связки. В большую подкожную вену кровь поступает из перфорирующих вен голеностопного сустава и множества других притоков. Есть много анатомических вариаций нормальной анатомии. В большой подкожной вене от 10 до 12 клапанов.
Малая подкожная вена (короткая подкожная вена) или МПВ, начинается на наружной тыльной стороне стопы и проходит за боковой лодыжкой, заканчиваясь подколенной веной. Он содержит примерно от 3 до 9 клапанов. Перфорантные вены соединяют глубокую и поверхностную венозные системы, прободая глубокую фасциальную поверхность. Обычно поток должен перемещаться из поверхностной системы в глубокую.
В ноге обычно более 100 перфораторов, но четыре основные группы наиболее клинически значимы для лечения венозной недостаточности БПВ. Один из них — перфоратор Хантера, расположенный в середине верхней части бедра. Задние большеберцовые перфораторы (Cockett’s) соединяют заднюю большеберцовую вену с задней арочной веной в области лодыжки. Перфораторы Бойда (паратибиальные) соединяют БПВ с задними большеберцовыми венами в верхней части голени, а перфораторы Додда (бедренный канал), которые соединяют БПВ с бедренной веной в медиальной части бедра выше колена.
Вена Джакомини — это название, данная вена часто встречается при расширении малой подкожной вены за пределы подколенной вены, и прилегает к глубокой вене бедра. Эта вена может иметь альтернативный путь, поверхностно изгибаясь вокруг ноги, чтобы присоединиться к БПВ его заднемедиальной ветвью в верхней части бедра.
Центральные вены
Нижняя полая вена (НПВ) начинается на уровне 4-го поясничного позвонка и проходит по правой стороне позвоночника и заканчивается в правом предсердии сердца. Он получает кровь из вен нижних конечностей, почек и печени. Система воротной вены образована слиянием селезеночной, нижней брыжеечной и верхней брыжеечных вен. Портальная вена расположена кпереди от нижней полой вены, переходя в печень, где она разветвляется на правую и левую воротные вены. По воротной вене кровь насыщена кислородом на 75%. Он получает кровь из селезенки, поджелудочной железы, желудка и других органов брюшной полости. Почечные вены переносят кровь от почек к НПВ. Левая почечная вена проходит кпереди от аорты и кзади от верхней брыжеечной артерии, прежде чем оканчивается в нижней полой вене. Правая почечная вена проходит непосредственно от почки в НПВ. Почечные вены в большинстве случаев проходят кпереди от почечной артерии.
Микроскопическая венозная анатомия
Венозные капилляры состоят из однослойной эндотелиальной стенки, которая обеспечивает всасывание газов и биохимических соединений в кровь. Кровь течет из капиллярного русла в венулы. Венулы состоят из двух слоев: внешней адвентиции и эндотелия. Адвентиция намного тоньше и менее прочна по сравнению с артериями. Это позволяет венам расширяться при изменении положения или силы тяжести. Стенки артерий и вен питаются внутренними сосудами, называемыми Vasa Vasorum.
Венозная гемодинамика
Вены выполняют четыре основные функции:
- Вены регулируют температуру тела.
- Вены контролируют скорость возврата крови к сердцу и тем самым регулируют сердечный выброс.
- Вены хранят от 2/3 до3/4 общего объема крови тела.
- Вены действуют как магистраль для транспортировки крови от органа или конечности к сердцу.
Понимание функции вен помогает понять структуру. Расположение вен помогает регулировать температуру. Поверхностные вены, перевязанные под кожей, отлично подходят для охлаждения, а вены глубоко внутри мышц согревают кровь. Способность вен сжиматься или набухать без значительного изменения давления также важна для терморегулирования. Кровь может оставаться там, где может происходить обмен тепловой энергией. Эта способность удерживать большое количество крови помогает выполнять все четыре функции, и поэтому вены называют емкостными сосудами.
Венозное сопротивление. Три основных фактора, способствующих кровотоку в верхних и нижних конечностях, включают:
- Сердечное сокращение.
- Внутрипросветное артериальное давление.
- Периферическое сопротивление в капиллярном ложе
Для кровотока необходим градиент давления, и кровь будет течь только из области высокого давления в область низкого давления. Потеря энергии происходит при градиенте давления. Другие факторы, способствующие потере энергии, включают вязкость, объем крови, длину и диаметр сосуда. У пациента в вертикальном положении также возникает внутрипросветный градиент венозного давления около 15 мм / рт.ст., но постоянно снижается до нуля на уровне правого предсердия. Градиент давления существует через капиллярные русла с самым высоким давлением в артериолах и самым низким давлением в венулах. Эта разница давлений позволяет крови проходить через ткань. Кровь течет из венулы в вену из-за большего размера вены и более низкого сопротивления.
Соотношение давление / объем. Стенки вен не очень эластичны, в отличие от очень эластичных стенок артерий, так как они не имеют такого количества эластичных волокон, как стенки артерий. Стенки вен имеют больше коллагеновых волокон. Если провести аналогию с тканью, стенки жилок похожи на тканый хлопковый перкаль. Артериальные стенки похожи на трикотажный полиэфирный спандекс. Это не значит, что вены жесткие. Вы можете сжать вену на тыльной стороне ладони, чтобы увидеть, насколько вены сжимаются. Они спадаются или меняют форму иначе, чем артерии.
Представьте себе артерию и вену в поперечном сечении, расширенные и круглые. По мере уменьшения объема в каждом сосуде артерия остается круглой, а вена принимает продолговатую форму в поперечном сечении. Когда происходит это изменение объема, артериальное давление падает, а венозное давление нет. Изменения внутрипросветного венозного давления мало различаются с большими изменениями венозного объема.
Гидростатическое давление. Гравитация также заставляет клетки крови двигаться к ногам у стоящего пациента. Ранее мы рассматривали концепцию полной энергии жидкости, один из компонентов которой является потенциальной энергией. Потенциальная энергия состоит из гравитационной потенциальной энергии и внутрисосудистого давления. Давайте посмотрим на внутрисосудистое давление. Как в артериях, так и в венах внутрисосудистое давление складывается из статического давления наполнения, динамического давления от сокращения левого желудочка и гидростатического давления. В отличие от системы артериального давления, динамическое давление от выброса левого желудочка не имеет значения, тогда как гидростатическое давление весьма важно для оценки венозного внутрисосудистого давления. Когда кровь течет к венулам, возникает значительное сопротивление венозному возврату в сердце из-за гидростатического давления.
Под гидростатическим давлением обычно понимается внешнее давление во всех направлениях внутри жидкости. Он имеет одинаковое значение как для артерий, так и для вен на любом уровне. Он рассчитывается как произведение удельного веса крови, ускорения свободного падения и вертикального расстояния от сердца. Поскольку гравитационное ускорение на этой планете относительно фиксировано, а удельный вес крови относительно постоянен, гидростатическое давление становится основным фактором внутрисосудистого венозного давления. Чем дальше вертикальное расстояние от сердца, тем больше внешняя сила, действующая на стенки вены. Наибольшее расстояние по вертикали достигается у лодыжек стоящего пациента. Соответственно, это создает наибольшее гидростатическое давление. Величина гидростатического давления в поднятой руке может быть аналогична таковой в ноге из-за аналогичного вертикального расстояния, но над сердцем эта сила имеет отрицательное значение, а под сердцем — положительное значение. Когда пациент лежит на спине, расстояние по вертикали от сердца незначительно, как и сила, обусловленная гидростатическим давлением во всем теле.
Отек из-за заболевания вен в основном возникает в дистальных отделах нижних конечностей. Неслучайно именно здесь наибольшее гидростатическое давление, а для вен — самое высокое внутрисосудистое давление. Отек возникает, когда внутрисосудистое давление превышает давление ткани. Когда человек стоит, давление в артериях и венах увеличивается. Это приводит к вытеснению жидкости через стенки капилляров в окружающую ткань.
Венозная кровь возвращается к сердцу за счет сокращения икроножной мышцы (вено-моторный насос). Эффективность помпы зависит от силы венозного сокращения и работоспособности венозных клапанов, которые направляют поток в одном направлении: к сердцу. Он работает путем отвода крови из глубоких мышечных пазух в глубокие вены бедра, вперед и вверх в сердце. По мере того, как кровь выводится из вен голени, внутримуральное и трансмуральное давление падает. Это уменьшает количество жидкости, поступающей в ткани, окружающие капилляры. Если сокращение мышц слабое, из ноги выводится меньше крови. Другой фактор, влияющий на отказ насоса икроножных мышц, — это некомпетентные венозные клапаны. Икроножные мышцы качают с большой силой, выталкивая большое количество крови из ноги, но, если клапан не удерживает кровь в голени, сила тяжести будет тянуть кровь обратно вниз. Чистого оттока из ноги не будет. Фактически, кровь будет поступать в ногу через артерии быстрее, чем она может выйти из ноги через вены, и это приведет к отеку.
С эффективным мышечным насосом мы ожидаем отсутствия потока или слабого потока во время отдыха, увеличения прямого потока при сокращении и отсутствия потока или низкого потока при расслаблении. При неэффективной мышечной помпе из-за венозной недостаточности мы ожидаем рефлюкса в состоянии покоя, увеличения кровотока при сокращении и рефлюкса при расслаблении. Кровь поднимается вверх, а затем снова падает.
Эффекты дыхания. Сжимаемость вен можно рассматривать с точки зрения градиентов давления. Существует градиент между внутренним давлением, выталкивающим наружу, и давлением ткани, давящим снаружи вены. Трансмуральное давление — это разница или градиент между интрамуральным и тканевым давлением. Выталкивание из-за увеличения интрамурального давления приводит к увеличению трансмурального давления и расширению вены. Снижение интрамурального давления снижает трансмуральное давление в вене. Если давление ткани превышает интрамуральное давление, вена спадается.
Давайте посмотрим, как это относится к венам живота и нижних конечностей, когда лежащий на спине пациент делает вдох. При вдохе диафрагма опускается, вызывая повышение абдоминального давления и давления тканей вокруг нижней полой вены. Трансмуральное давление падает, и НПВ спадается. Поскольку НПВ коллапсирует, общая бедренная вена испытывает повышенное сопротивление потоку. Здесь повышается интрамуральное давление, как и трансмуральное давление, заставляя вену расширяться. Если предположить, что венозные клапаны расположены дистальнее общей бедренной вены (бедренная вена и подколенная вена), в венах голени не должно быть изменений давления или объема.
Фазность. Соответствующая форма волны отражает эти изменения давления и дает фазовую форму волны. При вдохе увеличивается давление в брюшной полости и увеличивается сопротивление потоку, поэтому профиль скорости становится меньше. Затем с выдохом трансмуральное давление выше, и профиль скорости немного ускоряется назад к сердцу. Заболевание вен возникает, когда кровоток по венам затруднен. Это может произойти в конечной точке венозного кровотока или в правом предсердии. Все, что вызывает повышение давления в правом предсердии или центрального венозного давления, будет препятствовать току в сердце. Они могут быть вызваны регургитацией трехстворчатого клапана, стенозом трехстворчатого клапана и застойной сердечной недостаточностью. Двигаясь от сердца к венам нижних конечностей, мы видим, что коллабирование НПВ или подвздошных вен во время пробы Вальсальвы или на вдохе затрудняет венозный кровоток в нижних конечностях. Экстравазальное сжатие этих вен образованием в малом тазу или ручное сжатие дает те же результаты. Все это примеры пониженного трансмурального давления, поскольку внешнее давление ткани, вызывающее коллапс вены, превышает интрамуральное давление, удерживающее вену в расширенном состоянии. Венозный тромб проксимальнее интересующей точки на нижней конечности также будет препятствовать венозному току.
Еще статьи по теме: