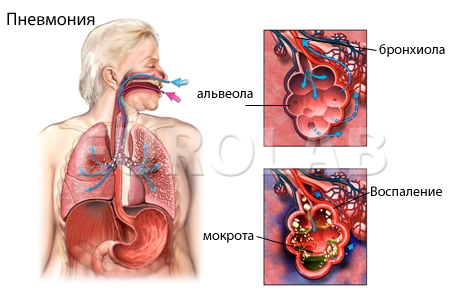
Пневмония (профиль: терапевтический, этап: стационар)
Утратил силу — Архив
Также:
H-Т-036
Версия: Архив — Клинические протоколы МЗ РК — 2007 (Приказ №764)
Категории МКБ:
Бронхопневмония неуточненная (J18.0)
Общая информация
Краткое описание
Внебольничная пневмония – острое инфекционное заболевание, возникшее во внебольничных условиях, сопровождающееся симптомами инфекции нижних дыхательных путей (лихорадка, кашель, выделение мокроты, возможно гнойной, боли в груди, одышка) и рентгенологическими свидетельствами “свежих” очагово-инфильтративных изменений в легких при отсутствии очевидной диагностической альтернативы.
Код протокола: H-Т-036 «Пневмония»
Для стационаров терапевтического профиля
Коды по МКБ -10:
J13 Пневмония, вызванная Streptococcus pneumoniae
J14 Пневмония, вызванная Haemophilus influenzae
J15 Бактериальная пневмония, не классифицированная в других рубриках
J16 Пневмония, вызванная другими инфекционными возбудителями, не классифицированная в других рубриках
J18 Пневмония без уточнения возбудителя
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 500 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
В основу классификации положены условия развития заболевания и иммунологический статус больного.
Различают:
1. Внебольничная пневмония — приобретенная вне лечебного учреждения (синонимы: домашняя, амбулаторная).
2. Нозокомиальная пневмония — приобретенная в лечебном учреждении (синонимы: госпитальная, внутрибольничная).
3. Аспирационная пневмония.
4. Пневмония у лиц с тяжелыми дефицитами иммунитета (врожденный иммунодефицит, ВИЧ-инфекция, ятрогенная иммуносупрессия) и уточнение локализации и наличия осложнений.
Критерии тяжести течения пневмонии:
1. Легкое течение: невыраженные симптомы интоксикации, температура тела субфебрильная, отсутствуют дыхательная недостаточность и нарушения гемодинамики, легочная инфильтрация в пределах 1 сегмента, лейкоциты 9,0-10,0х109/л, нет сопутствующих заболеваний.
2. Средняя степень тяжести течения: умеренно выраженные симптомы интоксикации, повышение температуры тела до 38°С, легочный инфильтрат в пределах 1-2 сегментов, ЧДД — до 22/мин., ЧСС — до 100 уд.мин., осложнения отсутствуют.
3. Тяжелое течение пневмонии: тяжелое состояние больного, выраженные симптомы интоксикации, температура тела > 38,0°С, дыхательная недостаточность II-III ст., нарушения гемодинамики (АД — <90/60 мм рт. ст., ЧСС — более 100 уд./мин., септический шок, потребность в вазопрессорах), лейкопения менее 4,0 х 109/л или лейкоцитоз 20,0х109/л с количеством незрелых нейтрофилов более 10%; многодолевая, двусторонняя пневмоническая инфильтрация, быстрое прогрессирование процесса (увеличение зоны инфильтрации на 50% и более за 48 часов наблюдения, плевральный выпот, абсцедирование, азот мочевины >10,7ммоль/л, ДВС-синдром, сепсис, недостаточность других органов и систем, нарушения сознания, обострение сопутствующих заболеваний.
Факторы и группы риска
Факторы риска затяжного течения ВП:
— возраст старше 55 лет;
— алкоголизм;
— сопутствующие инвалидизирующие заболевания внутренних органов;
— тяжелое течение ВП;
— мультилобарная инфильтрация;
— вирулентные возбудители заболевания (Legionella pneumophila, Staphylococcus aureus, грамотрицательные энтеробактерии);
— курение;
— клиническая неэффективность проводимой терапии (сохраняющиеся лейкоцитоз, лихорадка);
— вторичная бактериемия.
Диагностика
Диагностические критерии
Жалобы и анамнез:
— острая лихорадка в начале заболевания (t > 38оС);
— кашель с мокротой.
Физикальное обследование
Физические признаки:
— фокус крепитации и/или мелкопузырчатые хрипы;
— жесткое бронхиальное дыхание;
— укорочение перкуторного звука.
Лабораторные исследования: лейкоцитоз > 10 х 109/л и/или палочкоядерный сдвиг (>10%).
Инструментальные исследования
Диагноз ВП является определенным при наличии у пациента рентгенологически подтвержденной очаговой инфильтрации легочной ткани.
Показания к консультации специалистов:
— фтизиатр – для исключения туберкулеза легких;
— онколог – при подозрении на новообразование;
— кардиолог – для исключения сердечно-сосудистой патологии.
Перечень основных диагностических мероприятий:
— общий анализ крови;
— биохимический анализ крови – креатинин, электорлиты, печеночные ферменты;
— микробиологическая диагностика:
— микроскопия мазка, окрашенного по Грамму;
— культуральное исследование мокроты для выделения возбудителя и оценки его чувствительности к антибиотикам;
— ЭКГ;
— рентгенография грудной клетки в двух проекциях.
Перечень дополнительных диагностических мероприятий
— коагулограмма;
— газы артериальной крови;
— ПЦР крови на присутствие атипичной микрофлоры (хламидии, микоплазмы, легионеллы, аспергиллы, ЦМВ и др.);
— исследование гемокультуры (оптимально проводить забор двух проб венозной крови из разных вен);
— ПЦР мокроты на присутствие атипичной микрофлоры (хламидии, микоплазмы, легионеллы, аспергиллы, ЦМВ и др.);
— исследование ANA, ENA, ANCA для исключения ИБЛ;
— спирометрия;
— плевральная пункция с цитологическим, биохимическим, микробиологическим исследованием плеврального выпота;
— ФБС с биопсией слизистой при подозрении на новообразование;
— КТ грудного сегмента по показаниям для исключения туберкулеза, новообразований, иммунопатологических и других состояний;
— биопсия легкого (трансторакальная, трансбронхиальная, открытая) по показаниям для исключения иммунопатологических состояний (ИБЛ).
Дифференциальный диагноз
| Туберкулез легких | Наличие при микроскопии по Цилю-Нильсену хотя бы в одном из мазков кислотоустойчивых бацилл позволяет верифицировать диагноз. |
| Новообразования |
Первичный рак легкого Эндобронхиальные метастазы Аденома бронха Лимфома |
| Тромбоэмболия легочной артерии и инфаркт легкого | Признаки венозного тромбоэмболизма |
| Гранулематоз Вегенера |
Сочетанное поражение легких (чаще сегментарные или лобарные инфильтративные изменениия), верхних
дыхательных путей и почек, вовлечение в патологический процесс ЦНС или периферической нервной системы, кожи суставов. Признаки гранулематозного воспаления при гистологическом исследовании биоптатов пораженных органов. |
| Волчаночный пневмонит |
Преимущественная распространенность заболевания среди женщин. Прогрессирующий характер течения. Полиорганность поражения (кожный, суставной, почечный, неврологический и другие синдромы) Наличие в сыворотке крови АНАТ и АТ к ДНК |
|
Аллергический бронхо- легочный аспергиллез |
Бронхоспастический синдром. Транзиторные легочные инфильтраты. Центральные (проксимальные) бронхоэктазы. Эозинофилия периферической крови. Значительное повышение общего сывороточного IgE АТ к Аг Aspergillus fumigatus в сыворотке крови. Кожная гиперчувствительность немедленного типа к Аг Aspergillus. |
| Облитерирующий бронхиолит с организующейся пневмонией |
Развивается у лиц в возрасте 60-70 лет Выраженный положительный эффект при терапии системными ГКС Тельца Масона (гранулематозные «пробки» в просвете дистальных бронхов, распространяющиеся внутрь альвеолярных ходов и альвеол) при гистологическом исследовании |
| Эозинофильная пневмония |
В анамнезе у пациентов симптомокомплекс бронхиальной астмы или признаки атопии. Эозинофилия периферической крови. Повышение уровня сывороточного IgE. Билатеральная альвеолярная инфильтрация преимущественно в периферических и базальных отделах легких при рентгенологическом исследовании. |
| Саркоидоз |
Развивается преимущественно в возрасте от 20 до 40 лет. Полиорганность поражения ( в патологический процесс вовлекаются почки, эндокринная система, кожа и др.). Билатеральная прикорневая и/или медиастинальная аденопатия. Признаки гранулематозного воспаления при гистологическом исследовании. |
|
Лекарственная (токсическая) пневмопатия |
Регресс инфильтративных изменений в легких на фоне отмены ЛС и назначения системных ГКС. Наиболее часто токсическая реакция со стороны легких ассоциируется с приемом амиодарона, метотрексата. |
Лечение
Цели лечения:
— эрадикация возбудителя;
— купирование симптомов заболевания;
— нормализация лабораторных показателей и функциональных нарушений;
— разрешение инфильтративных изменений в легочной ткани;
— профилактика осложнений заболевания.
Немедикаментозное лечение
Отсутствуют доказательные данные, подтверждающие целесообразность назначения при внебольничной пневмонии таких физиотерапевтических методов лечения, как ДМВ, УВЧ, магнитотерапия, электро- и фонофорез.
Дыхательная гимнастика в случае экспекторации мокроты в объеме ≥ 30 мл/сут.
Медикаментозное лечение
1. Антибактериальная терапия ВП в амбулаторных условиях.
1.1. Пациенты в возрасте < 60 лет, сопутствующие заболевания отсутствуют. ЛС выбора:
— азитромицин внутрь 0,5 г 1 раз в сутки – 1-е сутки, далее 0,25 г 1 раз в сутки в течение 4 суток или
— амоксициллин внутрь по 0,5-1,0 г 3 раза в сутки, 7-10 суток или
— кларитромицин внутрь по 0,5 г 2 раза в сутки, 7-10 суток или
— рокситромицин внутрь по 0,15 г 2 раза в сутки, 7-10 суток.
Альтернативные ЛС:
— доксициклин внутрь по 0,1 г 2 раза в сутки 7-10 суток или
— левофлоксацин внутрь 0,5 г 1 раз в сутки 7-10 суток.
1.2. Пациенты в возрасте ≥ 60 лет и/или имеются сопутствующие заболевания. ЛС выбора:
— амоксициллин/клавуланат внутрь до или во время еды по 500 мг/125 мг или 875 мг/125 мг 3 раза в сутки или по 1 г 2 раза в сутки, 7-10 суток или
— цефуроксим внутрь после еды по 0,5 г 2 раза в сутки, 7-10 суток.
— левофлоксацин внутрь 0,5 г 1 раз в сутки, 7-10 суток или
— цефтриаксон в/м 1-2 г 1 раз в сутки, 7-10 суток.
2. Антибактериальная терапия ВП в стационарных условиях.
2.1. Лечение пневмонии легкой и средней степени тяжести. ЛС выбора:
— амоксициллин/клавуланат в/в по 1,2 г 3 раза в сутки, 3-4 суток или
— цефотаксим в/в или в/м по 1-2 г 2-3 раза в сутки, 3-4 суток или
— цефтриаксон в/в или в/м 1-2 г 1 раз в сутки, 3-4 суток или
— цефуроксим в/в или в/м по 0,75 г 3 раза в сутки, 3-4 суток или
— цефуроксим аксетил — таблетки, покрытые оболочкой, 250 мг.
Альтернативные ЛС: левофлоксацин в/в 0,5 г 1 раз в сутки, 3-4 суток.
Через 3-4 дня лечения при достижении клинического эффекта (нормализация температуры тела, уменьшение выраженности интоксикации и других симптомов заболевания) возможен переход с парентерального на пероральный способ применения антибиотика. Общая длительность лечения составляет 7-10 суток. Допускается изначальное применение пероральных противомикробных ЛС.
2.2. Лечение тяжелой ВП. ЛС выбора:
— азитромицин 0,5 г 1 раз в сутки, в течение 7-10 суток или
— кларитромицин в/в по 0,5 г 2 раза в сутки, в течение 10 суток или
— спирамицин 1,5 млн МЕ 3 раза в сутки + амоксициллин/клавуланат в/в по 1,2 г 3 раза в сутки, 10 суток или
— цефтриаксон в/в 1-2 г 1 раз в сутки, 10 суток или
— цефепим в/в 1-2 г 2 раза в сутки, 10 суток или
— цефотаксим в/в по 1-2 г 2-3 раза в сутки, 10 суток.
— левофлоксацин в/в 0,5 г 1-2 раза в сутки, 10 суток или
— офлоксацин в/в по 0,4 г 2 раза в сутки 10 суток + цефотаксим в/в по 1-2 г 2-3 раза в сутки, 10 суток или
— цефтриаксон в/в 1-2 г 1 раз в сутки, 10 суток.
2.3. Лечение пневмонии, вызванной P. Aeruginosa:
— имипенем в/в по 0,5 г 3-4 раза в сутки или
— меропенем в/в по 0,5 г 3-4 раза в сутки или
— цефепим в/в или в/м 1-2 г 2 раза в сутки или
— цефоперазон/сульбактам в/в по 2-4 г 2 раза в сутки или
— цефтазидим в/в или в/м 1-2 г 2-3 раза в сутки ± амикацин в/м или в/в 15-20 мг/кг 1 раз в сутки, 10 суток.
Длительность лечения при применении любого из вышеперечисленных препаратов определяется индивидуально.
При наличии клинических и/или эпидемиологических данных о микоплазменной или хламидийной этиологии заболевания продолжительность терапии должна составлять 14 суток.
При ВП, вызванной S. aureus и Enterobacteriaceae, длительность антибактериальной терапии составляет 14-21 сутки.
При легионеллезной пневмонии длительность лечения составляет 21 сутки.
3. Симптоматическая терапия ВП. Отхаркивающие средства:
— амброксол внутрь по 30 мг х 3 раза в сутки в течение 2 суток, далее по 30 мг 2 раза в сутки, 7-10 суток или
— ацетилцистеин внутрь по 200 мг 3-4 раза в сутки, 7-10 суток или
— бромгексин внутрь по 8-16 мг 3 раза в сутки 7-10 суток; в/м или в/в по 16 мг 2-3 раза в сутки, 7-10 суток или
— карбоцистеин внутрь по 750 мг 3 раза в сутки, 7-10 суток.
Для лечения и профилактики возникновения микоза при длительной массивной антибиотикотерапии – итраконазол 200 мг 2 раза в день, в течение 7 дней.
4. Дополнительные лечебные мероприятия (лечение осложнений ВП).
Бронхообструктивный синдром:
— бронходилатационная терапия — ипратропия бромид 1,0 + Sol. NaCl 0,9% 4,0 через небулайзер 3-4 раза в сутки или
— ипратропия бромид (MDI) 1 -2 дозы х 3-4 раза в сутки или
— салметерол (MDI) 1 доза х 2 раза в сутки
Плевральный выпот: торакоцентез (при наличии свободно смещаемой жидкости с толщиной слоя более 1 см на латерограмме) с эвакуацией всей или большей части жидкости.
— ЛС выбора: амоксициллин/клавуланат, ампициллин/сульбактам, цефоперазон/сульбактам;
— альтернативные ЛС: линкосамиды+аминогликозиды или цефалоспорины III-IV поколений; фторхинолоны+метронидазол; карбапенемы.
Эмпиема плевры:
— ЛС выбора: цефалоспорины II-IV поколений;
— альтернативные ЛС: линкосамиды, ванкомицин, ко-тримоксазол, фторхинолоны, ампициллин/сульбактам;
— торакотомическое дренирование;
— торакоскопия + декортикация.
Острая дыхательная недостаточность:
— оксигенотерапия с помощью носовых канюль или лицевой маски;
— неинвазивная вентиляция легких — при ЧД > 25 в мин., признаках дисфункции дыхательной мускулатуры, PaO2/FiO2 < 250 мм рт.ст., PaCO2 > 50 мм рт.ст., или рН < 7,33;
— ИВЛ при остановке дыхания, нарушении сознания, психомоторном возбуждении, нестабильности гемодинамики ( систолическое АД< 70 мм рт.ст., ЧСС < 50 /мин.), частоте дыхания > 35 в мин., PaO2/FiO2 < 150 мм рт.ст., повышении PaCO2 > 20% от исходного уровня, изменениях ментального статуса.
Острый респираторный дистресс-синдром:
— адекватная доставка кислорода к тканям;
— ИВЛ.
Сепсис, септический шок:
— антибактериальная терапия: амоксициллин/клавуланат в/в + макролид в/в; цефотаксим + макролид в/в; цефтриаксон + макролид в/в; цефепим в/в + макролид в/в; левофлоксацин (таваник) 500 мг 2 раза в сутки в/в;
— введение инфузионных сред до достижения уровня ЦВД 8-14 мм рт.ст., давления заклинивания капилляров легочной артерии — 14-18 мм рт.ст.;
— сосудистые и инотропные ЛС;
— респираторная поддержка – ИВЛ при сочетании септического шока с острым респираторным дистресс-синдромом, нарушением сознания, прогрессирующей полиорганной недостаточностью;
— иммуноглобулины (IgG и IgG+IgM) в/в.
Дальнейшее ведение:
— рентгенологический контроль через 2-3 недели от начала болезни;
— в случае неразрешающейся пневмонии и при наличии факторов риска затяжного течения заболевания — рентгенологический контроль через 4 недели;
— в случае неразрешающейся пневмонии и при отсутствии факторов риска затяжного течения заболевания — КТ грудного сегмента, ФБС.
Перечень основных медикаментов:
1 Амоксициллин 500 мг, 1000 мг, табл.; 250 мг; 500 мг, капс.; 250 мг/5 мл пероральная суспензия *
2 Амоксициллин+клавулановая кислота табл. 500 мг/125 мг, 875 мг/125 мг *
3 Азитромицин 250 мг, 500 мг, капс*
4 Кларитромицин 250 мг, 500 мг табл*
5 Рокситромицин 50 мг табл *
6 Цефуроксим 250 мг, 500 мг табл; порошок для приготовления инъекционного раствора во флаконе 750 мг *
7 Цефуроксим аксетил — гранулы для приготовления суспензии для приема внутрь во флаконе 125мг/5мл, таблетки, покрытые оболочкой 125 мг, 250 мг *
8 Цефепим 1000 мг, порошок для приготовления инъекционного раствора
9 Цефотаксим 250 мг, 500 мг, 1000 мг, во флаконе, порошок для приготовления инъекционного раствора *
10 Цефтриаксон 250 мг, 500 мг, 1 000 мг, во флаконе, порошок для приготовления инъекционного раствора *
11 Спирамицин гранулы для суспензии 1,5 млн ЕД, 375 тыс ЕД, 750 тыс ЕД порошок для инфузий 1,5 млн ЕД *
12 Цефоперазон/сульбактам
13 Цефтазидим — порошок для приготовления раствора для инъекций во флаконе 500 мг, 1 гр, 2 г *
14 Амикацин 10 мг *
15 Амброксол 30 мг табл.; 15 мг/2 мл амп.; 15 мг/5 мл, 30 мг/5 мл сироп *
16 Ацетилцистеин 2% 2мл, амп.*
17 Бромгексин
18 Карбоцистеин 250 мг, 500 мг, табл.
Перечень дополнительных медикаментов:
1 Левофлоксацин 250 мг, 500 мг табл.*
2 Винкомицин*
3 Ципрофлоксацин 250 мг, 500 мг табл.*
4 Имипенем 500 мг, амп., порошок для инъекций *
5 Меропенем 500 мг, амп., порошок для инъекций
6 Метронидазол*
7 Ко-тримоксазол*
8 Ипратропия бромид 100 мл аэрозоль *
9 Салметерол
10 Итраконазол оральный раствор 150 мл – 10 мгмл*
11 Итраконазол 100 мг, капс.*
Индикаторы эффективности лечения:
Первоначальная оценка эффективности антибактериальной терапии через 48-72 часа после начала лечения:
— снижение температуры;
— уменьшение интоксикационного синдрома;
— отсутствие дыхательной недостаточности.
— температура < 37,5о С;
— отсутствие интоксикации;
— отсутствие дыхательной недостаточности (ЧД < 20 в минуту);
— отсутствие гнойной мокроты;
— количество лейкоцитов в крови < 10 х 109/л, нейтрофилов < 80%, юных форм < 6%;
— положительная рентгенологическая динамика.
1. Рентгенография органов грудной клетки всем пациентам с клиническими признаками ВП.
2. Бактериологическое исследование мокроты.
3. Бактериологическое исследование крови (при тяжелом течении ВП) до назначения антибиотиков.
4. Начало антибактериальной терапии у всех госпитализированных пациентов с ВП в первые 4 часа с момента поступления.
5. Соответствие стартового режима антибактериальной терапии принятым стандартам терапии.
6. Использование ступенчатой терапии у госпитализированных пациентов, нуждающихся в парентеральном введении антимикробных препаратов.
7. Рекомендации по ежегодной вакцинации против гриппа.
Госпитализация
Показания для госпитализации
Данные физического обследования:
— частота дыхания ≥ 30/мин.;
— диастолическое АД ≤ 60мм рт. ст.;
— систолическое АД < 90 мм рт. ст.;
— ЧСС ≥ 125/мин.;
— температура тела < 35оС или ≥ 40оС;
— нарушение сознания.
Лабораторные и рентгенологические данные:
— лейкоциты периферической крови — < 4,0 х 109/л или > 25,0 х 109/л;
— SaO2 < 92% (по данным пульсоксиметрии);
— PaO2 < 60 мм рт.ст. и/или PaCO2 > 50 мм рт.ст. при дыхании комнатным воздухом;
— креатинин сыворотки крови > 176,7 мкмоль/л или азот мочевины > 7,0 ммоль/л;
— пневмоническая инфильтрация, локализующаяся более чем в одной доле;
— наличие полости (полостей распада);
— плевральный выпот, быстрое прогрессирование очагово-инфильтративных изменений в легких (увеличение размеров инфильтрации > 50% в течение ближайших 2-х суток);
— гематокрит < 30% или Hb < 90 г/л;
— внелегочные очаги инфекции (менингит, септический артрит и др.);
— сепсис или полиорганная недостаточность, проявляющаяся метаболическим ацидозом (pH < 7,35), коагулопатией;
— возраст старше 60 лет;
— наличие сопутствующих заболеваний (ХОБЛ, бронхоэктазы, сахарный диабет, ХПН, застойная сердечная недостаточность, выраженный дефицит массы тела);
— неэффективность стартовой антибактериальной терапии.
Невозможность адекватного ухода и выполнения всех врачебных предписаний в домашних условиях.
Показания для госпитализации в ОРИТ:
— тахипноэ ≥ 30 в мин.;
— систолическое АД < 90 мм рт.ст.;
— двухсторонняя или многодолевая пневмоническая инфильтрация;
— быстрое прогрессирование очагово-инфильтративных изменений в легких;
— септический шок;
— необходимость введения вазопрессоров > 4 часов;
— острая почечная недостаточность.
Профилактика
Вакцинация:
— вакцинация пневмококковой вакциной при наличии высокого риска развития пневмококковой инфекции;
— вакцинация гриппозной вакциной здоровых лиц до 65 лет и лиц, относящихся к группам риска.
1. Прекращение курения.
2. Лечебный режим – от строгого постельного до общего и тренирующего при постепенном и контролируемом наращивании его интенсивности.
3. Рациональное питание – сбалансированное по питательному составу, богато витаминизированное, при необходимости облегченное.
4. Адекватная этиотропная и симптоматическая медикаментозная терапия.
5. Применение перформированных физических факторов:
— респираторная физиотерапия — ПДКВ, CPAP – терапия, нормобарическая гипокситерапия, интервальная гипоксическая тренировка, оксигенотерапия, аэроионотерапия, галотерапия, искусственная сильвинитовая спелеотерапия, ингаляции высокодисперсных аэрозолей муколитических, мукорегулирующих и
стимулирующих реснитчатый эпителий, бронхолитических препаратов, стероидов при сопутствующей бронхообструкции;
— аппаратная физиотерапия – гальванизация, импульсные токи, электромагнитные волны, светолечение, чрескожная лазеротерапия, ВЛОК АУФОК, УЗ, лекарственный фонофорез, вибротерапия и др.;
6. Применение природных (естественных) лечебных факторов курортотерапии, климатолечебные процедуры, минеральные воды, лечебные грязи).
7. Кинезотерапия (ЛФК, массаж, физические тренировки).
8. Психотерапия.
Информация
Источники и литература
-
Протоколы диагностики и лечения заболеваний МЗ РК (Приказ №764 от 28.12.2007)
- 1. Чучалин А.Г., Синопальников А.И., Яковлев С.В., Страчунский Л.С., Козлов Р.С., Рачина С.А. Внебольничная пневмония у взрослых: практические рекомендации по диагностике, лечению и профилактике. Москва, 2005. 66 с. 2. Клинические рекомендации. Пульмонология/ под ред. А.Г.Чучалина. – М.: ГЭОТАР – Медиа, 2005. – 240с. 3. Чучалин А.Г., Синопальников А.И., Страчунский Л.С. Пневмония. – М.: ООО «Медицинское информационное агентство», 2006. – 464 с.:ил. 4. Практическое руководство по антиинфекционной химиотерапии. Под ред. Л.С.Страчунского, Ю.С.Белоусова, С.Н.Козлова М.: Боргес, 2002. 5. Рациональная фармакотерапия заболеваний органов дыхания: Рук. Для практикующих врачей/ А.Г.Чучалин, С.Н.Авдеев, В.В.Архипов, С.Л.Бабак и др.; Под общ. Ред. А.Г.Чучалина. – М.: Литера, 2004. – 874 с. 6. Страчунский Л.С., Козлов С.Н. Современная антимикробная химиотерапия. Руководство для врачей. М.: Боргес, 2002. 7. British Thoracic Society Guidelines for the management of community-acquired pneumonia in adults. Thorax 2001; 56 Suppl. 4: 1-64. 8. Niederman M.S., Mandell L.A., Anzueto A. et al. Guidelines for the management of adults with community-acquired pneumonia. Diagnosis, assessment of severity, antimicrobial therapy, and prevention. Am J Respir Crit Care Med 2001; 163: 1730-1754. 9. Barlow G.D., Lamping D.L., Davey P.G., Nathwani D. Evaluation of outcomes in community-acquired pneumonia: a guide for patients, physicians and policy-makers// Lancet. Infect. Dis. 2003; 3: 476-88. 10. Fine M.J., Auble T.E., Yealy D.M. et al. A prediction rule to identify low-risk patients with community-acquired pneumonia// N.Engl.J.Med.1997; 336: 243-50. 11. Клячкин Л.М., Щегольков А.М. Медицинская реабилитация больныз с заболеваниями внутренних органов: (Руководство для врачей). М.: Медицина; 2000. 12. Клячкин Л.М. Принципы реабилитации больных бронхо-легочными заболеваниями. Клин. Мед. 1992; 2: 105-109. 13. Малявин А.Г., Щегольков А.М. Медицинская реабилитация больных пневмонией. Пульмонология, 2004; 3: 93-102.
Информация
Список разработчиков:
Бакенова Р.А. – к.м.н., доцент, врач терапевт высшей категории, докторант ЦВМ РГП «ННМЦ» МЗ РК.
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Внутрибольничная пневмония
Внутрибольничная пневмония – это легочная инфекция, развившаяся спустя двое и более суток после поступления больного в стационар, при отсутствии признаков заболевания на момент госпитализации. Проявления внутрибольничной пневмонии аналогичны таковым при других формах воспаления легких: лихорадка, кашель с мокротой, тахипноэ, лейкоцитоз, инфильтративные изменения в легких и т. п., однако могут быть слабо выраженными, стертыми. Диагноз основывается на клинических, физикальных, рентгенологических и лабораторных критериях. Лечение внутрибольничной пневмонии включает адекватную антибиотикотерапию, санацию дыхательных путей (лаваж, ингаляции, физиометоды), инфузионную терапию.
Общие сведения
Внутрибольничная (нозокомиальная, госпитальная) пневмония – приобретенная в стационаре инфекция нижних дыхательных путей, признаки которой развиваются не ранее 48 часов после поступления больного в лечебное учреждение. Нозокомиальная пневмония входит в тройку самых распространенных внутрибольничных инфекций, уступая по распространенности лишь раневым инфекциям и инфекциям мочевыводящих путей. Внутрибольничная пневмония развивается у 0,5-1% больных, проходящих лечение в стационарах, а у пациентов отделений реанимации и интенсивной терапии встречается в 5-10 раз чаще. Летальность при внутрибольничной пневмонии чрезвычайно высока – от 10-20% до 70-80% (в зависимости от вида возбудителя и тяжести фонового состояния пациента).
Внутрибольничная пневмония
Причины
Основная роль в этиологии внутрибольничной бактериальной пневмонии принадлежит грамотрицательной флоре (синегнойной палочке, клебсиелле, кишечной палочке, протею, серрациям и др.) – эти бактерии обнаруживаются в секрете дыхательных путей в 50-70% случаев. У 15-30% пациентов ведущим возбудителем выступает метициллинрезистентный золотистый стафилококк. За счет различных приспособительных механизмов названные бактерии вырабатывают устойчивость к большинству известных антибактериальных средств. Анаэробы (бактериоды, фузобактерии и др.) являются этиологическими агентами 10-30% внутрибольничных пневмоний. Примерно у 4% пациентов развивается легионеллезная пневмония – как правило, она протекает по типу массовых вспышек в стационарах, причиной которых служит контаминация легионеллами систем кондиционирования и водоснабжения.
Значительно реже, чем бактериальные пневмонии, диагностируются нозокомиальные инфекции нижних дыхательных путей, вызванные вирусами. Среди возбудителей внутрибольничных вирусных пневмоний ведущая роль принадлежит вирусам гриппа А и В, РС-вирусу, у больных с ослабленным иммунитетом – цитомегаловирусу.
Общими факторами риска инфекционных осложнений со стороны дыхательных путей служат длительная госпитализация, гипокинезия, бесконтрольная антибиотикотерапия, пожилой и старческий возраст. Существенное значение имеет тяжесть состояния больного, обусловленная сопутствующими ХНЗЛ, послеоперационным периодом, травмами, кровопотерей, шоком, иммуносупрессией, комой и пр. Способствовать колонизации нижних дыхательных путей микробной флорой могут медицинские манипуляции: эндотрахеальная интубация и реинтубация, трахеостомия, бронхоскопия, бронхография и пр. Основными путями попадания патогенной микрофлоры в дыхательные пути служат аспирация секрета ротоносоглотки или содержимого желудка, гематогенное распространение инфекции из отдаленных очагов.
Вентилятор-ассоциированная пневмония возникает у больных, находящихся на ИВЛ; при этом каждый день, проведенный на аппаратном дыхании, увеличивает риск развития внутрибольничной пневмонии на 1%. Послеоперационная, или застойная пневмония, развивается у обездвиженных больных, перенесших тяжелые оперативные вмешательства, главным образом, на грудной и брюшной полости. В этом случае фоном для развития легочной инфекции служит нарушение дренажной функции бронхов и гиповентиляция. Аспирационный механизм возникновения внутрибольничной пневмонии характерен для больных с цереброваскулярными расстройствами, у которых отмечаются нарушения кашлевого и глотательного рефлексов; в этом случае патогенное действие оказывают не только инфекционные агенты, но и агрессивный характер желудочного аспирата.
Классификация
По срокам возникновения госпитальная инфекция подразделяется на раннюю и позднюю. Ранней считается внутрибольничная пневмония, возникшая в первые 5 суток после поступления в стационар. Как правило, она вызывается возбудителями, присутствовавшими в организме пациента еще до госпитализации (St. аureus, St. pneumoniae, H. influenzae и др. представителями микрофлоры верхних дыхательных путей). Обычно эти возбудители проявляют чувствительность к традиционным антибиотикам, а сама пневмония протекает более благоприятно.
Поздняя внутрибольничная пневмония манифестирует через 5 и более дней стационарного лечения. Ее развитие обусловлено собственно госпитальными штаммами (метициллинрезистентным St. аureus, Acinetobacter spp., P. аeruginosa, Enterobacteriaceae и др.), проявляющими высоковирулентные свойства и полирезистентность к противомикробным препаратам. Течение и прогноз поздней внутрибольничной пневмонии весьма серьезны.
С учетом причинных факторов выделяют 3 формы нозокомиальной инфекции дыхательных путей:
- вентилятор-ассоциированную пневмонию
- послеоперационную, или застойную пневмонию
- аспирационную пневмонию
При этом довольно часто различные формы наслаиваются друг на друга, еще в большей степени утяжеляя течение внутрибольничной пневмонии и увеличивая риск летального исхода.
Симптомы внутрибольничной пневмонии
Особенностью течения внутрибольничной пневмонии является стертость симптомов, из-за чего распознавание легочной инфекции бывает затруднительным. В первую очередь, это объясняется общей тяжестью состояния больных, связанной с основным заболеванием, хирургическим вмешательством, пожилым возрастом, коматозным состоянием и т. п.
Тем не менее, в ряде случаев заподозрить внутрибольничную пневмонию можно на основании клинических данных: нового эпизода лихорадки, увеличения количества мокроты/трахеального аспирата или изменение их характера (вязкости, цвета, запаха и пр.). Больные могут предъявлять жалобы на появление или усиление кашля, одышки, болей в грудной клетке. У пациентов, находящихся в тяжелом или бессознательном состоянии следует обратить внимание на гипертермию, увеличение ЧСС, тахикардию, признаки гипоксемии. Критериями тяжелого инфекционного процесса в легких служат признаки выраженной дыхательной (ЧД > 30/мин.) и сердечно-сосудистой недостаточности (ЧСС > 125/мин., АД < 100/60 мм рт. ст.), нарушение сознания, двустороннее или мультилобарное поражение легких и др. При этом необходимо исключить возможные неинфекционные причины кардиопульмональных расстройств: пневмоторакс, острый респираторный дистресс-синдром, отек легких, ТЭЛА, инфаркт легкого и др. Осложнениями внутрибольничной пневмонии чаще всего становятся абсцесс легкого, эмпиема плевры, сепсис.
Диагностика
Полное диагностическое обследование при подозрении на внутрибольничную пневмонию строится на сочетании клинических, физикальных, инструментальных (рентгенография легких, КТ грудной клетки), лабораторных методов (ОАК, биохимический и газовый состав крови, бакпосев мокроты).
Для выставления соответствующего диагноза пульмонологи руководствуются рекомендуемыми критериями, включающими в себя: лихорадку выше 38,3°С, усиление бронхиальной секреции, гнойный характер мокроты или бронхиального секрета, кашель, тахипноэ, бронхиальное дыхание, влажные хрипы, инспираторную крепитацию. Факт внутрибольничной пневмонии подтверждается рентгенологическими признаками (появлением свежих инфильтратов в легочной ткани) и лабораторными данными (лейкоцитозом >12,0х109/л, палочкоядерным сдвигом >10%, артериальной гипоксемией Ра02< 60 мм рт. ст., Sa02 < 90%.).
С целью верификации вероятных возбудителей внутрибольничной пневмонии и определения антибиотикочувствительности производится микробиологическое исследование секрета трахеобронхиального дерева. Для этого используются не только образцы свободно откашливаемой мокроты, но и трахеальный аспират, промывные воды бронхов. Наряду с культуральным выделение возбудителя, широко применяется ПЦР-исследование.
Лечение внутрибольничной пневмонии
Сложность лечения внутрибольничной пневмонии заключается в полирезистентности возбудителей к противомикробным препаратам и тяжести общего состояния больных. Практически во всех случаях первоначальная антибиотикотерапия является эмпирической, т. е. начинается еще до микробиологической идентификации возбудителя. После установления этиологии внутрибольничной пневмонии может быть произведена замена препарата на более действенный в отношении выявленного микроорганизма.
Препаратами выбора при внутрибольничной пневмонии, вызванной E.Coli и K. pneumoniae, служат цефалоспорины III-IV поколения, ингибиторзащищенные пенициллины, фторхинолоны. Синегнойная палочка чувствительна к сочетанию цефалоспоринов III-IV поколения (или карбапенемов) с аминогликозидами. Если госпитальные штаммы представлены St. аureus, требуется назначение цефазолина, оксациллина, амоксициллина с клавулановой кислотой и т. д. Для терапии аспергиллеза легких используется вориконазол или каспофунгин.
В начальном периоде предпочтителен внутривенный путь введения препарата, в дальнейшем при положительной динамике возможен переход на внутримышечные инъекции либо пероральный прием. Продолжительность курса антибиотикотерапии у пациентов с нозокомиальной пневмонией составляет 14-21 день. Оценка эффективности этиотропной терапии проводится по динамике клинических, лабораторных и рентгенологических показателей.
Кроме системной антибиотикотерапии, при внутрибольничной пневмонии важное внимание уделяется санации дыхательных путей: проведению бронхоальвеолярного лаважа, ингаляционной терапии, трахеальной аспирации. Больным показан активный двигательный режим: частая смена положения и присаживание в постели, ЛФК, дыхательные упражнения и т. п. Дополнительно проводится дезинтоксикационная и симптоматическая терапия (инфузии растворов, введение и прием бронхолитиков, муколитиков, жаропонижающих препаратов). Для профилактики тромбозов глубоких вен назначается гепарин или ношение компрессионного трикотажа; с целью предупреждения стрессовых язв желудка используются Н2-блокаторы, ингибиторы протонной помпы. Пациентам с тяжелыми септическими проявлениями может быть показано введение внутривенных иммуноглобулинов.
Прогноз и профилактика
Клиническими исходами внутрибольничной пневмонии могут быть разрешение, улучшение, неэффективность терапии, рецидив и летальный исход. Внутрибольничная пневмония является главной причиной смертности в структуре внутрибольничных инфекций. Это объясняется сложностью ее своевременной диагностики, особенно у пожилых, ослабленных больных, пациентов, пребывающих в коматозном состоянии.
Профилактика внутрибольничной пневмонии базируется на комплексе медицинских и эпидемиологических мероприятий: лечении сопутствующих очагов инфекции, соблюдении санитарно-гигиенического режима и инфекционного контроля в ЛПУ, предупреждении переноса возбудителей медперсоналом при проведении эндоскопических манипуляций. Чрезвычайно важна ранняя послеоперационная активизация пациентов, стимуляция откашливания мокроты; тяжелые больные нуждаются в адекватном туалете ротоглотки, постоянной аспирации трахеального секрета.
|
Литература 1. Нозокомиальная пневмония у взрослых (Национальные рекомендации)/ под ред. Чучалина А.Г., Гельфанда Б.Р.//Клиническая микробиология и антимикробная химиотерапия. — 2009 — Т.11, №2. 2. Госпитальные пневмонии/ Новиков Ю.К.// Русский медицинский журнал. — 2002 — №12. 3. Внутрибольничные инфекции/ под ред. Венцела Р.П. — 1990. 4. Госпитальные пневмонии/ Царев В.П., Крыжановский В.Л.// Лечебное дело. — 2012 — No6 (28). |
Код МКБ-10 J18 |
Внутрибольничная пневмония — лечение в Москве
Нозокомиальная пневмония — заболевание, которое характеризуется поражением легких инфекционной природы, которое развилось через 2 суток и позже после поступления человека в больницу/ОРИТ.
- Эпидемиология
- Патогенез нозокомиальной пневмонии, связанной с ИВЛ
- Диагностика нозокомиальной пневмонии
- Возбудители нозокомиальной пневмонии
- Антибактериальная терапия
- Профилактика нозокомиальной пневмонии
Нозокомиальная пневмония (НП) известна также как госпитальная или больничная. Она может быть связана с искусственной вентиляцией легких (НПИВЛ). Развивается через 2 суток и позже от начала интубации, если на момент интубации отсутствовали признаки инфекции в легких. Но в ряде случаев у больных, которым проводили хирургическую операцию, данный вид пневмонии может проявиться ранее, чем за 48 часов.
Эпидемиология
В структуре всех госпитальных инфекционных осложнений госпитальная пневмония занимает второе место, составляет 15-18%. У хирургических больных после плановых операций заболевание развивается в 6 случаях из 100. После экстренных абдоминальных операций нозокомиальная пневмония развивается в 15% случаев. Смертельные исходы при НП бывают в 19-45 случаях из 100.
При нозокомиальной пневмонии, связанной с ИВЛ и вызванной Ps. aeruginosa, летальность достигает 70 или даже 80% в странах СНГ. Если в таких случаях возбудителем являются аэробные грамотрицательные бактерии, летальность на уровне от 20 до 50%, при грамположительных бактериях — 5-20%.
Особенности нозокомиальной пневмонии у хирургических больных:
- Многофакторное инфицирование
- Развивается в первые 3-5 суток после операции
- Сложность назначения эмпирического лечения
- Сложность в диагностике
НП развивается у пациентов с абдоминальным сепсисом по таким причинам:
- повторные операции и анестезии
- длительная ИВЛ
- выраженный синдром кишечной недостаточности
- применение «инвазивных» лечебных и диагностических процедур
- синдром острого повреждения легких, связанный с абдоминальным сепсисом
- возможность гематогенного и лимфогенного зараженияиз очагов сепсиса в брюшной полости
Раннему развитию госпитальной пневмонии способствуют такие факторы:
- абдоминальный сепсис
- тяжелое состояние
- возраст от 60 лет
- массивная аспирация
- нарушение сознания
- сопутствующие ХОБЛ
- проведение длительной ИВЛ: от 72 часов
- экстренная интубация
- развитие острого респираторного дистресс-синдрома как неспецифической реакции легких
- использование инвазивных лечебных и диагностических методик
- повторная госпитализация в период до 6 месяцев
- неадекватность предшествующего антибактериального лечения
- назотрахеальная и назогастральная интубация
- торакальные или абдоминальные операции
- положение больного лежа на спине с опущенным головным концом кровати (угол до 30°)
Патогенез нозокомиальной пневмонии, связанной с ИВЛ
В ОРИТ больной может инфицироваться эндогенным или экзогенным путем. Экзогенные источники:
- ингалируемые медицинские газы
- объекты внешней среды, которые соприкасаются с дыхательными путями больного
- оборудование для проведения ИВЛ (респираторы, эндотрахеальные и трахеостомические трубки, катетеры для санации трахеобронхиального дерева и т.д.)
- воздух
- микрофлора медперсонала
- микрофлора других пациентов
Эндогенный источник заражения легких — микрофлора таких органов:
- ЖКТ
- ротоглотки
- мочевыводящих путей
- кожи
- носоглотки
- придаточных пазух носа,
- а также возбудители из альтернативных очагов инфекции
Секрет ротоглотки попадает в трахеи и бронхи после вдыхания. Когда функционирование ЖКТ так или иначе нарушается, природная, обитающая там нормально микрофлора, уже не находится в балансе. Это касается как анаэробов, так и аэробов, обитающих в желудке, кишечнике и пр. Барьерная функция кишечника нарушена. Этот процесс также играет большую роль в патогенезе нозокомиальной пневмонии.
В выше описанных случаях кишечная микрофлора заселяет верхние отделы ЖКТ, бактерии и токсины попадают в кровоток. Когда организм ослаблен, только тогда возбудители могут проявить свое патогенное влияние и вызвать развитие инфекционного процесса.
Диагностика нозокомиальной пневмонии
Признаки, которые говорят о пневмонии при ИВЛ:
- температура тела >38 °С или <36 °С
- гнойный характер мокроты
- респираторный индекс <300
- сдвиг лейкоцитарной формулы влево
- лейкоцитоз >11х109/мл или лейкопения <4х109/мл
Если есть выше перечисленные признаки, нужно не проводить обследование, а продолжать наблюдение за больным. Если зафиксированы 2 и более из данных симптомов, проводят рентгенографическое исследование. При наличии инфильтратов на рентгенограмме рекомендуется провести микробиологическое обследование и начинать эмпирическое лечение антибиотиками.
При подозрении на НПИВЛ выделяют 3 диагностические группы больных:
- I группа — диагноз пневмонии достоверен при наличии клинических, рентгенологических и микробиологических критериев
- II группа — вероятный диагноз пневмонии, при наличии лишь клинических и лабораторных или клинических и рентгенологических, или лабораторных и рентгенологических критериев
- III группа — сомнительный диагноз пневмонии — зафиксированы лишь клинические, или только лабораторные, или только рентгенологические проявления пневмонии
Антимикробное лечение проводят в обязательном порядке только пациентам из первой и второй группы.
Диагностическая бронхоскопия и бропхоальвволярный лаваж
Сначала нужно провести преоксигенацию с FiO2=1,0 длительностью 10-15 минут. Делают тотальную внутривенную анестезию, потому что использование местных анестетиков ограничено, учитывая их вероятное бактерицидное действие. Пробу нужно брать из места максимального поражения, которое определяется не только визуально, но и согласно данным рентгенографии. При диффузном инфильтративном поражении легких пробы материала нужно брать из средней доли правого легкого, также можно — из язычкового сегмента левого легкого. Лаважную жидкость нужно поместить в стерильную пробирку и безотлагательно везти в микробиологическую лабораторию.
Техника применения «слепого» защищённого катетера
Преоксигенация с FiO2=1,0 проводится на протяжении 5 минут, далее максимально дистально вводят катетер через эндотрахеальную или трахеостомическую трубку. Далее нужно выдвинуть внутренний катетер. Используют для аспирации стерильный шприц емкостью 20 мл, его присоединяют к проксимальному концу внутреннего катетера. Его на следующем этапе нужно удалить из эндотрахеальной трубки. Отделяемое нижних дыхательных путей из внутреннего катетера помещают в стерильную пробирку и немедленно доставляют в лабораторию.
Возбудители нозокомиальной пневмонии
При пневмонии, которая вызвана проведением ИВЛ, выделяют такие возбудители:
- ацинетобактер
- синегнойная палочка
- H. Influenzae (редко)
- представители семейства Enterobactriaceae
- S. pneumoniae
- золотистый стафилококк (чаще, чем S. pneumoniae)
- грибы рода Candida (редко)
Тяжелое течение НП отличается такими критериями:
— сердечно-сосудистая недостаточность
— выраженная дыхательная недостаточность
— нарушение сознания
— температура тела выше 39 °С или ниже 36 °
— проявления дисфункции органов
— мультилобарное или билатеральное поражение
— гипоксемия (раО2 <60 мм рт ст)
— гиперлейкоцитоз (>30х109/л) или лейкопения (<4х109/л)
Антибактериальная терапия
Для лечения нозокомиальной пневмонии у хирургических пациентов нужно учитывать:
- выявленного возбудителя и его чувствительность к антибиотикам
- продолжительность проведения ИВЛ и время пребывания человека в отделении реанимации
- влияние предшествовавшей антибактериальной терапии на возбудителя НП
Нозокомиальная пневмония у больных хирургического отделения лечится почти всегда цефотаксимом/ цефтриаксоном, цефуроксимом. Также эффективны Амоксициллин/клавуланат и Фторхинолоны (например, пефлоксацин). Нозокомиальная пневмония у больных ОРИТ без ИВЛ требует терапии Цефалоспоринами III поколения с антипсевдомонадной активностью в комбинации с амикацином. Альтерантивное лечение: Цефоперазон + сульбактам. Если есть серьезное подозрение на MRSA, любую из выше названных схем можно дополнить линезолидом или ванкомицином.
Если антибактериальное лечение НП неэффективно, причины могут заключаться в следующем:
- тяжесть состояния больного (по шкале APACHE II значение >25)
- несанированный очаг хирургической инфекции
- персистенция проблемных возбудителей
- высокая антибиотикорезистентность возбудителей нозокомиальной пневмонии, связанной с проведением ИВЛ
- развитие суперинфекции (Pseudomonas spp., Enterobacter spp. и т.д.)
- микроорганизмы, на которые не влияет эмпирическая терапия (Aspergillus spp , Candida spp и пр.)
- позднее начало адекватной антибактериальной терапии
- неправильный подбор препаратов
- низкие дозы и концентрация антибиотика в плазме и тканях больного
- нарушения режима дозирования препаратов (неправильная разовая доза, неадекватный способ введения, нарушения правильного интервала между введениями лекарства пациенту)
Профилактика нозокомиальной пневмонии
Профилактика НПИВЛ эффективная только при условии проведения проводят в рамках общей системы инфекционного контроля, который касается множества внутрибольничных инфекций. Пациентов с инфекционными осложнениями следует изолировать от других. Рекомендуется придерживаться принципа «одна сестра — один больной». Следует своевременно обнаруживать и проводить правильную хирургическую санацию (обработку) альтернативных очагов инфекции. Среди профилактических мер также называют сокращение предоперационного периода.
Профилактика аспирации
- ИВЛ не проводят при остром респираторном дистресс-синдроме и септическом остром повреждении легких
- немедленно удалять инвазивные устройства по устранении клинических показаний для их использования
- при назотрахеальной интубации риск развития НПИВЛ выше, если сравнивать с оротрахеальной интубацией
- избегать повторных эндотрахеальных интубаций у пациентов, находившихся на ИВЛ, по возможности
- перед экстубацией трахеи нужно убедиться, что из надманжеточного пространства секрет удален
- нужно постоянно аспирировать секрет из надманжеточного пространства
- при высоком риске аспирационной пневмонии пациентов на ИВЛ нужно приподнимать их кровать в области головы на 30-45°
- проводить адекватный туалет ротоглотки в целях профилактики орофарингеальной колонизации
- медперсоналу важно строго придерживаться гигиены рук: мыть, проводить антисептику и осуществлять косметический уход
- если руки загрязнены, следует вымыть их мылом и водой, в ряде случаев нужно использовать для очищения спиртовой антисептик, чтобы уничтожить транзиторную микрофлору
- если руки визуально чистые, гигиеническую антисептику рук всё равно проводят
Профилактика экзогенного инфицирования
Гигиеническая асептика рук проводится в таких случаях:
- перед надеванием стерильных перчаток при постановке центрального внутрисосудистого катетера
- перед непосредственным контактом с пациентом
- перед постановкой инвазивных устройств
- после контакта с интактной кожей пациента (перекладывание больного, измерение АД и/или пульса)
- после снятия перчаток
Для антисептической очистки рук нельзя применять салфетки, пропитанные антисептиком.
Другие профилактические меры
Трахеостомия во всех случаях выполняется в стерильных условиях. Замена трахеостомической трубки — также. Трубки стерилизируют. При выполнении санации трахеобронхиального дерева персонал надевает чистые одноразовые или стерильные перчатки. Перед использованием дыхательных контуров многократного применения их всегда стерилизуют или проводят дезинфекцию высокого уровня. Любой конденсат в контуре важно вовремя удалить. При проведении ИВЛ опытные врачи рекомендуют применять бактериальные фильтры.
Закрытые аспирационные системы позволяют проводить лаваж трахеобронхиального дерева, санацию, забор отделяемого трахеобронхиального дерева в условиях, когда контакта с окружающей средой совершенно нет. Это позволяет исключить контаминацию нижних дыхательных путей через просвет интубационной трубки.
Медицинский эксперт статьи
Новые публикации
Нозокомиальная пневмония
, медицинский редактор
Последняя редакция: 19.11.2021
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
В соответствии с принятыми в настоящее время критериями, к нозокомиальной пневмонии (синонимы: госпитальная пневмония, вентилятор-ассоциированная пневмония)) относят лишь случаи инфекционного поражения легких, развившегося не ранее чем через 48 ч. после поступления больного в лечебное учреждение. Нозокомиальная пневмония (НП), связанная с ИВЛ (НПИВЛ), — воспалительное поражение лёгких, развившееся не ранее чем через 48 ч от момента интубации и начала проведения ИВЛ, при отсутствии признаков легочной инфекции на момент интубации. Однако во многих случаях у хирургических больных манифестация нозокомиальной пневмонии возможна и в более ранние сроки.

Эпидемиология нозокомиальной пневмонии
Нозокомиальная пневмония занимает II место в структуре всех госпитальных инфекционных осложнений и составляет 15-18%. Частота развития НП у хирургических больных после плановых операций — 6%, после экстренных абдоминальных операций (воспалительные и деструктивные заболевания) — 15% НП — наиболее частое инфекционное осложнение в ОРИТ. НПИВЛ составляет 36% всех случаев послеоперационной пневмонии. Частота развития НПИВЛ — 22-55% в плановой хирургии при ИВЛ более 2 сут, в экстренной абдоминальной хирургии — 34,5%, при ОРДС — 55%. Частота развития нозокомиальной пневмонии у пациентов хирургических ОРИТ, которым не проводят ИВЛ, не превышает 15%. Летальность при НП — 19-45% (зависит от тяжести основного заболевания и объема операции). Летальность при НПИВЛ в гнойносептической абдоминальной хирургии достигает 50-70% в зависимости от основного заболевания, возбудителя и адекватности лечебной тактики. Атрибутивная летальность при НПИВЛ составляет 23% и более. Распространенность НПИВЛ в конкретном ОРИТ за определенный период времени рассчитывают по формуле:
Частота развития НПИВЛ х 1000 / Общее количество ИВЛ-дней
Летальности при НПИВЛ зависит и от возбудителя, обнаруживаемого в отделении.
Летальность при нозокомиальной пневмонии, связанной с искусственной вентиляцией легких, в зависимости от возбудителя
| Возбудители | Летальность, % |
|
Ps. aeruginosa |
70-80 |
|
Грамположительные бактерии |
5-20 |
|
Аэробные грамотрицательные бактерии |
20-50 |

Этиологическая структура нозокомиальной пневмонии
Спектр возбудителей НП зависит от «микробиологического пейзажа» определенного лечебного учреждения и ОРИТ. Кроме того, на этиологическую структуру нозокомиальной пнемонии оказывают влияние сопутствующие заболевания (особенно ХОБЛ) и характер основного патологического процесса, потребовавшего применения ИВЛ (травматический шок с аспирацией, тяжелый сепсис, оперативные вмешательства у больных высокой степени риска). В целом, при НПИВЛ у хирургических больных преобладают грамотрицательные микроорганизмы синегнойная палочка, ацинетобактер, представители семейства Enterobactriaceae, значительно реже выявляют H. Influenzae. Среди грамположительных кокков в развитии нозокомиальной пнемонии особое место занимает золотистый стафилококк, по этиологической роли значительно превосходящий S. pneumoniae. В ряде случаев (4-6%) определенную роль в поддержании пневмонии играют грибы рода Candida.
Патогенез нозокомиальной пневмонии, связанной с искусственной вентиляцией лёгких
Выделяют два источника инфицирования больного ОРИТ:
- экзогенный,
- эндогенный.
К экзогенным источникам инфицирования лёгких относят объекты внешней среды, прямо или опосредованно соприкасающиеся с дыхательными путями больного воздух, ингалируемые медицинские газы, оборудование для проведения ИВЛ (эндотрахеальные и трахеостомические трубки, респираторы, дыхательные контуры, катетеры для санации трахеобронхиального дерева, бронхоскопы), а также микрофлора других пациентов и медицинского персонала.
Эндогенный источник инфицирования легких — микрофлора ротоглотки, ЖКТ, кожи, мочевыводящих путей, придаточных пазух носа, носоглотки, а также возбудители из альтернативных очагов инфекции.
Высококонтаминированный секрет ротоглотки проникает в трахеобронхиальное дерево путём микроаспирации. Опасность аспирации секрета ротоглотки увеличивается у пациентов, которым проводят ИВЛ, из-за наличия интубационной трубки, повреждающей слизистую оболочку ротглотки и трахеи, нарушающей функцию реснитчатого эпителия и препятствующей как спонтанной экспекторации мокроты, так и акту глотания. Бактериальная колонизация ротоглотки увеличивает риск развития НПИВЛ из-за возможности миграции бактерий около манжеты интубационной трубки.
Большую роль в патогенезе нозокомиальной пневмонии играет транслокация условно-патогенных бактерий из ЖКТ. В желудочно-кишечном тракте здорового человека обитает очень много микробов — как анаэробов, так и аэробов Они поддерживают адекватную моторную, секреторную и метаболическую функции ЖКТ Именно анаэробная часть кишечной микрофлоры обеспечивает колонизационную резистентность и подавляет рост потенциально патогенной аэробной бактериальной микрофлоры. Однако под влиянием травм, нарушений гемодинамики и метаболизма или при других патологических состояниях развивается ишемия кишечной стенки и нарушается моторная, секреторная и барьерная функции кишечника. Происходит ретроградное заселение кишечной микрофлорой верхних отделов ЖКТ, а также, вследствие нарушения барьерной функции энтероцитов, транслокация бактерий и их токсинов в портальный и системный кровоток. Полисистемный многофакторный бактериологический анализ у больных ОРИТ подтвердил, что динамика контаминации брюшной полости, ЖКТ, кровяного русла, а также лёгочной ткани зависит от морфофункциональной недостаточности кишечника.
Развитие инфекционного процесса в лёгких можно рассматривать как результат нарушения баланса между факторами агрессии, способствующими попаданию в дыхательные пути большого количества высоковирулентных микроорганизмов, и факторами противоинфекционной защиты. Только в условиях критического ослабления факторов защиты возбудители способны проявить свою патогенность и вызвать развитие инфекционного процесса.
Особенности нозокомиальной пневмонии в хирургии
- Раннее развитие (в первые 3-5 сут послеоперационного периода — 60-70% всех нозокомиальных пневмоний)
- Многофакторное инфицирование.
- Трудности нозологического и дифференциального диагноза.
- Сложность назначения эмпирической терапии.
- Частота развития НПИВЛ у больных с гнойно-воспалительными очагами в брюшной полости — 64%.
Причины высокой частоты развития НП у больных с абдоминальным сепсисом:
- длительная ИВЛ,
- повторные операции и анестезии,
- применение «инвазивных» лечебных и диагностических процедур,
- выраженный синдром кишечной недостаточности, предрасполагающий к транслокации патогенных микроорганизмов и их токсинов из ЖКТ,
- возможность гематогенного и лимфогенного инфицирования из септических очагов в брюшной полости,
- синдром острого повреждения легких, связанный с абдоминальным сепсисом, — «благодатная» почва для развития нозокомиальной пневмонии.
Факторы, способствующие раннему развитию нозокомиальной пневмонии:
- тяжесть состояния (высокий балл по APACHE II),
- абдоминальный сепсис,
- массивная аспирация,
- возраст старше 60 лет,
- сопутствующие ХОБЛ,
- нарушение сознания,
- экстренная интубация,
- проведение длительной (более 72 ч) ИВЛ,
- использование инвазивных лечебных и диагностических методик, что повышает риск экзогенного инфицирования,
- развитие острого респираторного дистресс-синдрома как неспецифической реакции легких,
- неадекватность предшествующей антибактериальной терапии,
- повторная госпитализация в течение 6 мес,
- торакальные или абдоминальные операции,
- назотрахеальная и назогастральная интубация,
- положение на спине с опущенным головным концом кровати (угол менее 30°).

Диагностика нозокомиальной пневмонии
Рекомендации health. A. Science policy committee of the american college of chest physians, 2000.
Подозрение на нозокомиальную пневмонию при проведении ИВЛ должно возникать при наличии двух и более из следующих признаков:
- гнойный характер мокроты,
- лихорадка >38 °С или гипотермия <36 °С,
- лейкоцитоз >11х109/мл или лейкопения <4х109/мл, сдвиг лейкоцитарной формулы влево (>20% палочкоядерных или любое количество юных форм),
- paО2/FiО2 (респираторный индекс) <300.
При отсутствии вышеуказанных симптомов нет необходимости в дальнейшем обследовании, целесообразно проводить наблюдение (доказательства II уровня).
При наличии двух и более из вышеуказанных симптомов необходимо рентгенографическое исследование. При нормальной рентгенограмме — необходимо искать альтернативные причины возникновения симптомов (доказательства III уровня).
При наличии инфильтратов на рентгенограмме возможны два тактических варианта (доказательства III уровня).
При наличии инфильтратов на рентгенограмме следует выполнить микробиологическое обследование (количественные методы эндобронхиальный аспират, БАЛ, защищенные щетки, бронхоскопические методы) и назначить эмпирическую антибиотикотерапию (АБТ) Адекватная эмпирическая АБТ у пациентов с подозрением на пневмонию повышает выживаемость (доказательства II уровня). В случае отсутствия бактериологического подтверждения при стабильном состоянии пациента АБТ может быть остановлена.
Для объективизации оценки клинических, лабораторных и рентгенологических данных у больных с подозрением на НПИВЛ целесообразно использовать шкалу CPIS (Clinical Pulmonary Infection Score)
- Температура, °C
- 36,5-38,4 — 0 баллов,
- >38,5 или <38,9 — 1 балл,
- >39 или <36 — 2 балла
- Лейкоциты, х109
- 4-11 — 0 баллов,
- <4 или >11 — 1 балл + 1 балл, при наличии юных форм
- Бронхиальная секреция
- необходимость санации ТБД <14 раз в сутки — 0 баллов,
- необходимость санации ТБД >14 = 1 балл + 1 балл, если секреции имеют гнойный характер
- pаO2/FiO2 mmHg
- >240 или ОПЛ/ОРДС — 0 баллов,
- <240 при отсутствии ОПЛ/ОРДС — 1 балл
- Рентгенография лёгких
- отсутствие инфильтратов — 0 баллов,
- диффузные инфильтраты — 1 балл,
- локализованный инфильтрат — 2 балла.
- Микробиологический анализ трахеального аспирата (полуколичественный метод 0, +, ++ или +++)
- нет роста или 0-+ — 0 баллов.
- ++-+++ — 1 балл + 1 балл, при выделении того же микроорганизма (окраска по Грамму).
Диагноз НПИВЛ считают подтвержденным при 7 и более баллах по шкале CPIS.
Учитывая, что CPIS неудобна в рутинной практике, более приемлемым стал ее модифицированный вариант — шкала ДОП (шкала диагностики и оценки тяжести пневмонии), которая представлена в таблице.
Чувствительность шкалы составляет 92%, специфичность — 88% Оценка 6-7 баллов соответствует умеренной тяжести пневмонии, 8-9 — тяжёлой, 10 и более — крайне тяжелой пневмонии. Доказана диагностическая ценность шкалы ДОП. Ее использование целесообразно для динамического наблюдения за больными, а также для оценки эффективности проводимой терапии
Шкала диагностики и оценки тяжести пневмонии
| Показатель | Значение | Баллы |
| Температура тела, С |
36,0-37,9 38,0-39,0 <36 0 или >39,0 |
0 1 2 |
| Количество лейкоцитов, х109 |
4,9-10,9 11 0-17 0 или >20 палочкоядерных форм >17,0 или присутствие любого количества юных форм |
0 1 2 |
| Респираторный индекс раО2/FiO2 |
>300 300-226 225-151 <150 |
0 1 2 3 |
| Бронхиальная секреция |
+/- |
0 |
|
+++ |
2 |
|
| Инфильтраты в легких (по результатам рентгенографии) |
Отсутствие |
0 |
|
Локальные |
1 |
|
|
Сливные, двусторонние, с абсцедированием |
2 |
Среди больных с подозрением на НПИВЛ можно выделить три диагностические группы
- I группа — диагноз пневмонии достоверен при наличии клинических, рент-генологических и микробиологических критериев Как показывает клинический опыт, полный комплекс диагностических признаков можно выявить у 31% больных.
- II группа — вероятный диагноз пневмонии, при наличии лишь клинических и лабораторных или клинических и рентгенологических, или лабораторных и рентгенологических критериев. Такой «диагностический набор» можно выявить у 47% больных.
- III группа — сомнительный диагноз пневмонии — есть только клинические, или только лабораторные, или только рентгенологические признаки пневмонии. Эта диагностическая группа составляет 22% среди всех больных с подозрением на НПИВЛ.
Антимикробная терапия обязательна больным I и II диагностических групп. При сомнительном диагнозе нозокомиальной пневмонии целесообразно дальнейшее динамическое наблюдение.

Особенности микробиологической диагностики нозокомиальной пневмонии
Забор материала для микробиологического исследования необходимо производить до начала (или смены) антибактериальной терапии.
Для забора и микробиологического исследования материала из трахеобронхиального дерева чаще всего применяют следующие методы.

Диагностическая бронхоскопия и бропхоальвволярный лаваж
Исследование предваряют преоксигенацией с FiO2=1,0 в течение 10-15 мин. Процедуру проводят в условиях тотальной внутривенной анестезии, так как применение местных анестетиков ограничено, учитывая их возможное бактерицидное действие. Забор пробы производят из зоны наибольшего поражения, определяемой по данным рентгенограммы и визуально. В случае диффузного инфильтративного поражения легких пробы материала забирают из средней доли правого легкого или из язычкового сегмента левого легкого. Отделяемое (лаважную жидкость) нижних дыхательных путей из внутреннего катетера помещают в стерильную пробирку и немедленно доставляют в микробиологическую лабораторию.

Техника использования «слепого» защищённого катетера
После пятиминутной преоксигенации с FiO2=1,0 наиболее дистально вводят катетер через эндотрахеальную или трахеостомическую трубку. После этого выдвигают внутренний катетер (при этом разрушается пленка, защищающая внутренний катетер от путевой контаминации). Аспирацию производят с использованием 20 мл стерильного шприца, присоединенного к проксимальному концу внутреннего катетера. Затем приспособление удаляют из эндотрахеальной трубки, а отделяемое нижних дыхательных путей из внутреннего катетера помещают в стерильную пробирку и немедленно доставляют в микробиологическую лабораторию.
Диагностическая значимость количественных культур эндотрахеальных аспиратов зависит от степени бактериальной контаминации и предшествующего применения антибиотиков.
Чувствительность и специфичность количественных методов диагностики нозокомиальной пневмонии, связанной с искусственной вентиляцией легких
| Методика | Дигностическое значение, КОЕ/мл | Чувствительность, % | Специфичность, % |
|
Количественная эндотрахеальная аспирация |
105-106 |
67-91 |
59-92 |
|
«Защищенная» браш-биопсия |
>103 |
64-100 |
60-95 |
|
БАЛ |
>104 |
72-100 |
69-100 |
|
«Защищенный» БАЛ |
>104 |
82-92 |
ВЗ-97 |
|
«Защищенный слепой» катетер |
>104 |
100 |
82,2 |
Бронхоскопические (инвазивные) методы требуют применения специального оборудования, привлечения дополнительного персонала и обладают низкой воспроизводимостью. «Инвазивная» диагностика НПИВЛ не приводит к достоверному улучшению отдаленных результатов лечения.
Критерии тяжелого течения нозокомиальной пневмонии
- Выраженная дыхательная недостаточность (ЧД >30 в минуту).
- Развитие сердечно-сосудистой недостаточности (САД <100 мм ртст, ДАД <60 мм. рт. ст.).
- Температура тела >39 °С или <36 °С.
- Нарушение сознания.
- Мультилобарное или билатеральное поражение.
- Клинические признаки дисфункции органов.
- Гиперлейкоцитоз (>30х109/л) или лейкопения (<4х109/л).
- Гипоксемия (раО2 <60 мм рт ст)
Антибактериальная терапия нозокомиальной пневмонии у хирургических больных
Для назначения адекватной эмпирической терапии следует принимать во внимание следующие основополагающие факторы:
- влияние на предполагаемую этиологию заболевания сроков пребывания пациента в ОРИТ и продолжительность проведения ИВЛ,
- особенности видового состава возбудителей НПИВЛ и их чувствительности к антимикробным препаратам в конкретном лечебном учреждении,
- влияние предшествовавшей антибактериальной терапии на этиологический спектр НПИВЛ и на чувствительность возбудителей к антимикробным препаратам.
Схемы эмпирической антибактериальной терапии нозокомиальной пневмонии у хирургических больных
|
Клиническая ситуация |
Режим антибактериальной терапии |
|
Нозокомиальная пневмония у больных хирургического отделения |
Цефалоспорины II поколения (цефуроксим), Цефалоспорины III поколения, не обладающие антипсевдомонадной активностью (цефтриаксон, цефотаксим), Фторхинолоны (ципрофлоксацин, пефлоксацин, левофлоксацин), |
|
Нозокомиальная пневмония у больных ОРИТ без ИВЛ |
Цефалоспорины III поколения обладающие антипсевдомонадной активностью (цефтазидим цефоперазон), Цефалоспорины IV поколения, |
|
Нозокомиальная пневмонияивл без СПОН (APACHE II меньше 15) |
Цефалоспорины III поколения, обладающие антипсевдомонадной активностью (цефтазидим, цефоперазон) + амикацин |
|
НПивл + СПОН (APACHE II больше 15) |
Имипенем + циластатин |
Примечания
- При обоснованном подозрении на MRSA любая из схем может быть дополнена ванкомицином или линезолидом.
- При высоком риске аспирации или ее верификации клинико-диагностическими методами антибактериальные препараты, не обладающие активностью в отношении анаэробных возбудителей, целесообразно комбинировать с метронидазолом или клиндамицином.
Причины неэффективности антибактериальной терапии нозокомиальной пневмонии:
- несанированный очаг хирургической инфекции,
- тяжесть состояния больного (APACHE II >25),
- высокая антибиотикорезистентность возбудителей НПИВЛ,
- персистенция проблемных возбудителей (MRSA, Р. aeruginosa, Acinetobacter spp, S. maltophilia),
- микроорганизмы «вне спектра» действия эмпирической терапии (Candida spp., Aspergillus spp , Legionella spp., P. carinnii),
- развитие суперинфекции (Enterobacter spp., Pseudomonas spp., грибы, Clostridium difficile),
- неадекватный выбор препаратов,
- позднее начало адекватной антибактериальной терапии,
- несоблюдение режима дозирования препаратов (способа введения, разовой дозы, интервала между введениями),
- низкие дозы и концентрация антибиотика в плазме и тканях.

Профилактика нозокомиальной пневмонии
Профилактика НПИВЛ может быть эффективной, только если ее проводят в рамках общей системы инфекционного контроля, охватывающей все элементы лечебно-диагностического процесса и направленной на профилактику различных типов внутрибольничных инфекций. Здесь приведены лишь некоторые мероприятия, наиболее прямо ориентированные на профилактику именно нозокомиальной пневмонии. Такие мероприятия, как, например, изоляция пациентов с инфекционными осложнениями, внедрение принципа «одна сестра — один больной», сокращение предоперационного периода, своевременное выявление и адекватная хирургическая санация альтернативных очагов инфекции, безусловно, играют важную роль в предупреждении нозокомиальной пневмонии, как и других форм внутрибольничных инфекций, но имеют более универсальный характер и в данном документе не рассмотрены.
Все требования, изложенные в этом подразделе, основаны на результатах научных исследований и практического опыта, учитывают требования законодательства Российской Федерации и данные международной практики. Здесь применена следующая система ранжирования мероприятий по степени их обоснованности.
Требования, обязательные для исполнения и убедительно обоснованные данными методически совершенных экспериментальных, клинических или эпидемиологических исследований (метаанализы, систематические обзоры рандомизированных контролируемых испытаний (РКИ), отдельные хорошо организованные РКИ). В тексте они обозначены — 1А.
Требования, обязательные для исполнения и обоснованные данными ряда заслуживающих внимания экспериментальных, клинических или эпидемиологических исследований с незначительной вероятностью систематической ошибки и высокой вероятностью наличия причинно-следственной связи (когортные исследования без рандомизации, исследования случай-контроль и т п) и имеющие убедительное теоретическое обоснование. В тексте они обозначены — 1Б.
Требования, обязательность выполнения которых диктуется действующим федеральным или местным законодательством. В тексте они обозначены — 1В.
Требования, рекомендуемые для исполнения, которые основаны на предположительных данных клинических или эпидемиологических исследований и имеют определенное теоретическое обоснование (опираются на мнение ряда авторитетных экспертов). В тексте они обозначены цифрой 2.
Требования, традиционно рекомендуемые для исполнения, однако при этом не существует убедительных доказательств ни «за», ни «против» их выполнения, а мнения экспертов расходятся. В тексте они обозначены цифрой 3.
Приведенная система ранжирования не подразумевает оценки эффективности мероприятий и отражает лишь качество и количество исследований, данные которых легли в основу разработки предлагаемых мероприятий.
Борьба с эндогенным инфицированием

Профилактика аспирации
- Следует удалять инвазивные устройства, такие как эндотрахеальные, трахеостомические и (или) энтеральные (назо-, орогастральные, -интестинальные) трубки, немедленно по устранении клинических показаний для их использования (1Б).
- При септическом остром повреждении легких (ОПЛ) или остром респираторном дистресс-синдроме (ОРДС) проведение неинвазивной ИВЛ неэффективно и опасно для жизни.
- Следует, насколько возможно, избегать повторных эндотрахеальных интубаций у пациентов, находившихся на ИВЛ (1Б).
- Риск развития НПИВЛ при назотрахеальной интубации выше, чем при оротрахеальной (1Б).
- Целесообразна постоянная аспирация секрета из надманжеточного пространства (1Б).
- Перед экстубацией трахеи (сдутием манжеты) следует убедиться, что секрет удален из надманжеточного пространства (1Б).
- У пациентов с высоким риском аспирационной пневмонии (находящихся на ИВЛ, с назогастральной, назоинтестинальной трубкой), головной конец кровати должен быть приподнят на 30-45° (1Б).
- Для профилактики орофарингеальной колонизации следует проводить адекватный туалет ротоглотки — аспирацию слизи специальным катетером, а также обработку антисептическими растворами (например, 0,12% раствором хлоргексидина биглюконата) у пациентов после кардиохирургических операций (2) и других пациентов с высоким риском развития пневмонии (3).
Борьба с экзогенным инфицированием

Гигиепа рук медицинского персонала
- Гигиена рук медицинских работников — общее понятие, обозначающее ряд мероприятий, включающих мытьё рук, антисептику рук и косметический уход за кожей рук медицинского персонала.
- При загрязнении необходимо вымыть руки водой и мылом В остальных случаях следует проводить гигиеническую антисептику рук с помощью спиртового антисептика (1А). Гигиеническая антисептика рук — антисептика рук медицинского персонала, целью которой считают удаление или уничтожение транзиторной микрофлоры.
- Следует проводить гигиеническую антисептику рук, даже если руки визуально не загрязнены (1А)
Гигиеническую антисептику рук следует проводить:
- перед непосредственным контактом с пациентом,
- перед надеванием стерильных перчаток при постановке центрального внутрисосудистого катетера,
- перед постановкой мочевых катетеров, периферических сосудистых катетеров или других инвазивных устройств, если эти манипуляции не требуют хирургического вмешательства,
- после контакта с интактной кожей пациента (например, при измерении пульса или артериального давления, перекладывании пациента и т п ),
- после снятия перчаток (1Б).
Гигиеническую антисептику рук при выполнении манипуляций по уходу за пациентом следует проводить при переходе от контаминированных участков тела пациента к чистым, а также после контакта с объектами окружающей среды (включая медицинское оборудование), находящимися в непосредственной близости от пациента (2).
Не следует применять для антисептики рук салфетки/шарики, пропитанные антисептиком (1Б).
Мероприятия по совершенствованию гигиены рук должны быть неотъемлемой частью программы инфекционного контроля в лечебно-профилактическом учреждении и иметь приоритетное финансирование (1Б).
Уход за пациентами с трахеостомой
Трахеостомию следует выполнять в стерильных условиях (1Б).
Замену трахеостомической трубки следует выполнять в стерильных условиях, трахеостомические трубки необходимо подвергать стерилизации или дезинфекции высокого уровня (1Б).

Санация дыхательных путей
При выполнении санации трахеобронхиального дерева (ТБД) следует надевать стерильные или чистые одноразовые перчатки (3).
При использовании открытых систем для аспирации секрета дыхательных путей следует применять стерильные катетеры однократного применения (2).

Уход за дыхательной аппаратурой
Не следует без особых показаний (явное загрязнение, нарушение функционирования и т п ) производить замену дыхательного контура при использовании у одного пациента исходя только из продолжительности его применения (1А).
Перед использованием дыхательных контуров многократного применения следует подвергать их стерилизации или дезинфекции высокого уровня (1Б-В).
Следует своевременно удалять любой конденсат в контуре (1А).
Рекомендуют использовать бактериальные фильтры при проведении ИВЛ (2).
Для заполнения резервуаров увлажнителей следует использовать стерильную или пастеризованную дистиллированную воду (1Б).
Рекомендуют использовать фильтры тепловлагообменники (ТВО) (2).
Закрытые аспирационные системы (ЗАС) предназначены для проведения санации, лаважа трахеобронхиального дерева и забора отделяемого трахеобронхиального дерева (ТБД) для микробиологического анализа в закрытом режиме, т. е. в условиях, полностью отделённых от окружающей среды. Целью создания таких систем было исключение контаминации нижних дыхательных путей через просвет интубационной трубки при «традиционной» сананции ТБД и уменьшение отрицательного влияния процедуры санации трахеи на параметры вентиляции при «агрессивных» режимах ИВЛ Закрытая аспирационная система встраивается в контур «больной-аппарат ИВЛ» между дыхательным фильтром и интубационной трубкой. Если при проведении ИВЛ используется активное увлажнение при помощи стационарного увлажнителя, система устанавливается между интубационной трубкой и У-образным соединителем дыхательного контура.
Таким образом, создается единое закрытое герметичное пространство «аппарат ИВЛ — дыхательный фильтр — закрытая аспирационная система — интубационная трубка — пациент». В дистальной части системы находятся кнопка управления вакуумом и коннектор, к которому подсоединяется трубка вакуум-аспиратора и, при необходимости, устройство для взятия трахео-бронхиального аспирата для выполнения лабораторных и микробиологических исследований. Поскольку закрытая аспирационная система предполагает защиту аспирационного катетера от контакта с внешней средой, он покрыт специальным защитным рукавом, наличие которого исключает контакт рук персонала с поверхностью катетера. В то же время воздух, находящийся в защитном рукаве (потенциально контаминированный флорой пациента), при введении катетера в интубационную трубку удаляется во внешнюю среду, а воздух, входящий из внешней среды в защитный рукав при выведении катетера из трахеи, может быть, в свою очередь, контаминирован чужеродной для пациента флорой. Повторяющееся беспрепятственное движение воздуха в обоих направлениях при повторных эпизодах санации трахеи становится источником взаимного инфицирования пациента и окружающей среды отделения. Очевидно, что в идеале воздух, движущийся из защитного рукава и обратно, должен проходить микробиологическую «очистку». С этой точки зрения в условиях ОРИТ предпочтительно использовать истинно закрытые аспирационные системы, которые снабжены собственным встроенным антибактериальным фильтром, исключающим возможность взаимного контаминирования среды ОРИТ и больного патогенной микрофлорой Накопленные в настоящее время данные о применении ЗАС со встроенным фильтром указывают на существенное снижения числа нозокомиального трахеобронхита и пневмонии, связанных с проведением ИВЛ, значительное увеличение средних сроков от начала ИВЛ до возникновения пневмонии, что может быть эффективным средством профилактики инфекций дыхательных путей у больных с длительной ИВЛ.

Внутрибольничная пневмония (синонимы: госпитальная пневмония, нозокомиальная пневмония) — пневмония, которая развивается через 48-72 часа после поступления больного в стационар и которая не существовала и не находилась в фазе инкубационного периода до момента поступления.
Нозокомиальная пневмония, связанная с ИВЛ, — пневмония, развившаяся не ранее чем через 48 часов от момента интубации и начала проведения ИВЛ, при отсутствии признаков легочной инфекции на момент интубации. Однако во многих случаях у хирургических больных манифестация нозокомиальной пневмонии возможна и в более ранние сроки.
Частота больничной пневмонии достигает 20 % от числа всех больничных инфекций и наблюдается чаще у больных после операций на грудной или брюшной полости, у больных, которые находятся на искусственной вентиляции лёгких и у больных с иммунодефицитом.
Факторы, предрасполагающие к развитию больничной пневмонии
- хронические заболевания лёгких
- лечение в отделении интенсивной терапии
- терапия внебольничной пневмонии
- интубация трахеи и наркоз
- бронхоскопия
- иммунодефицитные состояния
- хирургические операции на грудной и брюшной полости
- длительное пребывание в горизонтальном положении
- курение
- почечная недостаточность
- нарушения сознания
- неконтролируемая антибиотикотерапия препаратами широкого спектра действия
Причины больничных пневмоний
| Возбудитель | Частота |
|---|---|
| Pseudomonas aeruginosa | 17 % |
| Staphylococcus aureus | 13 % |
| Klebsiella pneumoniae | 11,5 % |
| Escherichia coli | 6,5 % |
| другие Грам (-) кишечные аэробные бациллы | до 14 % |
| Haemophilus influenzae | ?? |
| Pneumocystis carini | ?? |
| Mycoplasma pneumoniae | ?? |
| Legionella pneumophila | ?? |