Овитрель — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛС-002622
Торговое наименование препарата
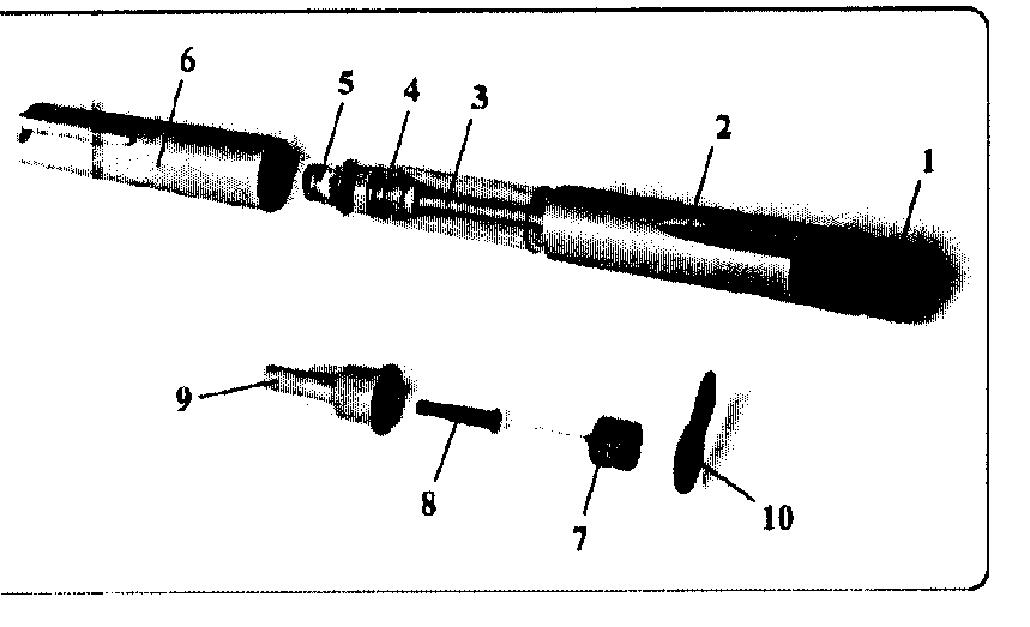
Овитрель®
Международное непатентованное наименование
Хориогонадотропин альфа
Лекарственная форма
раствор для подкожного введения
Состав
Один заполненный шприц с 0,5 мл раствора содержит: активное вещество — хориогонадотропин альфа 250 мкг (6500 ME) и вспомогательные вещества: маннитол 27,3 мг, метионин 0,1 мг, полоксамер 188 0,05 мг, фосфорная кислота 0,49 мг, натрия гидроксид q.s. для корректировки рН, вода для инъекций до 0,5 г.
Описание
Прозрачный или слегка опалесцирующий бесцветный или светло-желтый раствор.
Фармакотерапевтическая группа
Лютеинизирующее средство
Код АТХ
G03GA08
Фармакодинамика:
Овитрель® содержит хориогонадотропин альфа, который производится при помощи рекомбинантной ДНК технологии. Он имеет ту же аминокислотную последовательность, что и естественный человеческий хорионический гонадотропин. Хорионический гонадотропин связывает трансмембранные рецепторы лютеинизирующего гормона (ЛГ) на поверхности клеток теки и гранулезы яичника. Вызывает инициирование ооцитарного мейоза, разрыв фолликулов(овуляцию), формирование желтого тела, продукцию прогестерона и эстрадиола желтым телом.
Фармакокинетика:
Всасывание и распределение
После внутривенного введения хориогонадотропин альфа распределяется во внеклеточную жидкость с периодом полураспределения около 4,5 часов. Стационарный объем распределения и общий клиренс составляют 6 л и 0,2 л/час соответственно.
При подкожном введении хориогонадотропина альфа абсолютная биодоступность составляет приблизительно 40%, конечный период полувыведения — около 30 часов.
Выведение и метаболизм
Метаболизм и выведение хориогонадотропина альфа аналогичны эндогенному хорионическому гонадотропину.
Показания:
В протоколе индукции множественного созревания фолликулов для вспомогательных репродуктивных технологий (ВРТ), в том числе для экстракорпорального оплодотворения (ЭКО), с целью индукции финального созревания фолликулов и лютеинизации после стимуляции препаратами гонадотропинов.
При ановуляторном или олигоовуляторном бесплодии для индукции овуляции и лютеинизации в конце стимуляции роста фолликулов.
Противопоказания:
— Гиперчувствительность к активному компоненту и к любому из вспомогательных компонентов, входящих в состав препарата;
— Опухоли гипотоламуса и гипофиза;
— Объемные новообразования яичника или кисты, несвязанные с поликистозом яичников.
— Вагинальные кровотечения неясной этиологии.
— Рак яичника, матки или молочной железы.
— Внематочная беременность в течение 3 предыдущих месяцев.
— Тромбоэмболия.
— Первичная овариальная недостаточность.
— Врожденные пороки развития половых органов, несовместимые с беременностью.
— Фибромиома матки, несовместимая с беременностью.
— Постменопауза.
С осторожностью:
С осторожностью следует назначать Овитрель® пациенткам, страдающим тяжелыми системными заболеваниями, в тех случаях, когда беременность может привести к их обострению.
Беременность и лактация:
В период беременности и грудного вскармливания препарат Овитрель® не назначается.
Данные об экскреции хориогонадотропина альфа в грудное молоко отсутствуют.
Способ применения и дозы:
Овитрель® вводится подкожно. Каждый шприц или шприц-ручка предназначены только для однократного использования.
Лечение следует проводить только под руководством врача, имеющего опыт в лечении бесплодия.
В протоколе индукции множественного созревания фолликулов для ВРТ, в том числе для ЭКО, с целью индукции финального созревания фолликулов и лютеинизации после стимуляции препаратами гонадотропинов:
Овитрель® в дозе 250 мкг (содержимое 1 шприца или 1 шприц-ручки) вводится однократно через 24-48 часов после последнего введения препарата фолликулостимулирующего гормона или ЛГ и достижения оптимального уровня развития фолликула.
При ановуляторном или олигоовуляторном бесплодии для индукции овуляции и лютеинизаиии в конце стимуляции роста фолликулов:
Овитрель® в дозе 250 мкг (содержимое 1 шприца или 1 шприц-ручки) вводится однократно через 24-48 часов после достижения оптимального уровня развития фолликула. Рекомендуется половой контакт в день введения препарата Овитрель® и на следующий день.
Рекомендации по самостоятельному введению препарата Овитрель®.
Самостоятельное введение возможно только пациентами, прошедшими соответствующее обучение и имеющими возможность обратиться за советом к врачу- специалисту.
При самостоятельном введении пациентке следует внимательно прочитать и строго следовать нижеприведенной инструкции по введению препарата:
Перед введением:
1. Вымойте руки. Важно чтобы Ваши руки и предметы, которые Вы используете, были чистыми.
2. Подготовьте чистую поверхность и разложите на ней все, что нужно для инъекции:
1. два тампона, смоченных спиртом (к упаковке не прилагаются);
2. один шприц с препаратом или одна шприц-ручка и игла для инъекции.
Для шприца:
1. Введение инъекции:Сразу же проведите инъекцию:
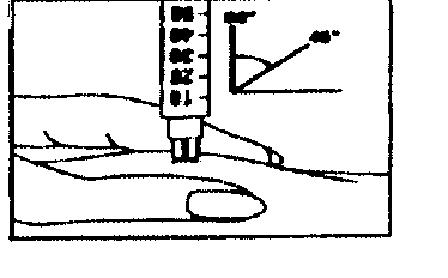
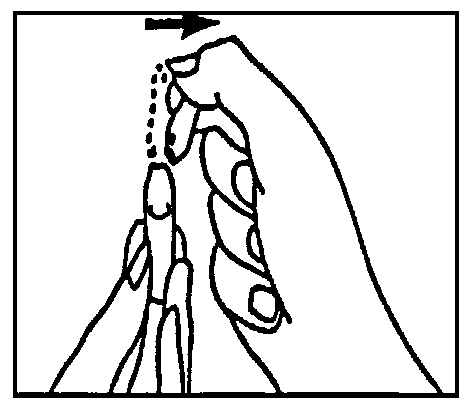
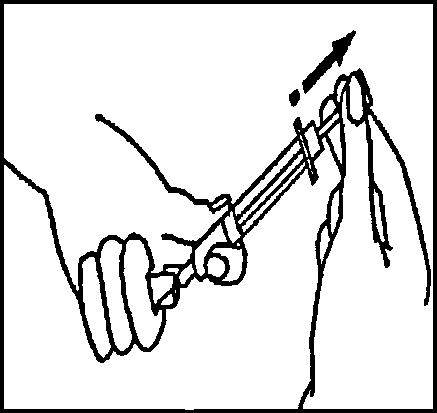
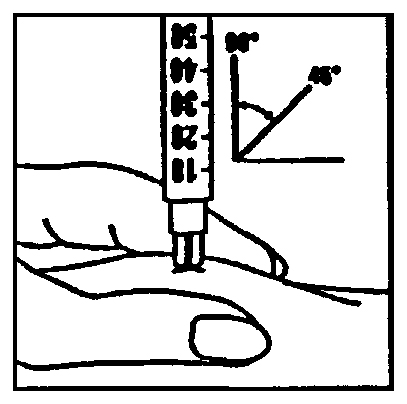
Выберите место для инъекции в соответствии с рекомендациями Вашего лечащего врача или медсестры (живот, передняя часть бедра). Протрите выбранный участок тампоном со спиртом. Сильно стяните кожу пальцами и коротким энергичным движением направьте иглу под углом 45° — 90° в кожную складку. Проводите подкожную инъекцию, как Вас учили. Избегайте попадания препарата непосредственно в вену. Вводите раствор, осторожно нажимая на поршень. Используйте столько времени, сколько Вам нужно для того, чтобы ввести весь объем раствора. Сразу же после инъекции выньте иглу и протрите круговыми движениями кожу в месте инъекции тампоном со спиртом.
2. Утилизация использованных принадлежностей: Сразу после инъекции поместите использованный шприц в контейнер для хранения острых предметов. Весь неиспользованный раствор должен быть уничтожен.
Для шприц-ручки:
Используйте шприц-ручку только для себя, не позволяйте пользоваться ей никому другому.
Вводите препарат Овитрель® так, как показывал врач или медсестра.
На иллюстрации ниже показан внешний вид шприц-ручки с указанием ее отдельных элементов:
1. кнопка для установки дозы
2. табло указателя дозы
3. поршень
4. отсек с резервуаром
5. наконечник с резьбой
6. колпачок шприц-ручки
7. съемная игла
8. внутренний колпачок иглы
9. наружний колпачок иглы
10. защитная наклейка
1. Подготовка шприц-ручки к проведению инъекции
1.1 Снимите колпачок со шприц-ручки
1.2 Наденьте иглу
— Возьмите иглу — используйте только одноразовые иглы, поставляемые вместе с предварительно заполненной шприц-ручкой Овитрель®.
— Убедитесь в том, что защитная наклейка на наружном колпачке иглы не повреждена и не ослаблена.
ВНИМАНИЕ:
Если защитная наклейка повреждена или ослаблена, не используйте эту иглу. Возьмите другую. Неиспользованную иглу выбросьте вместе с надетым на нее наружным колпачком. Инструкции по утилизации ненужных игл получите у своего врача или медсестры.
— Снимите защитную наклейку.
— Прочно удерживайте наружный колпачок иглы.
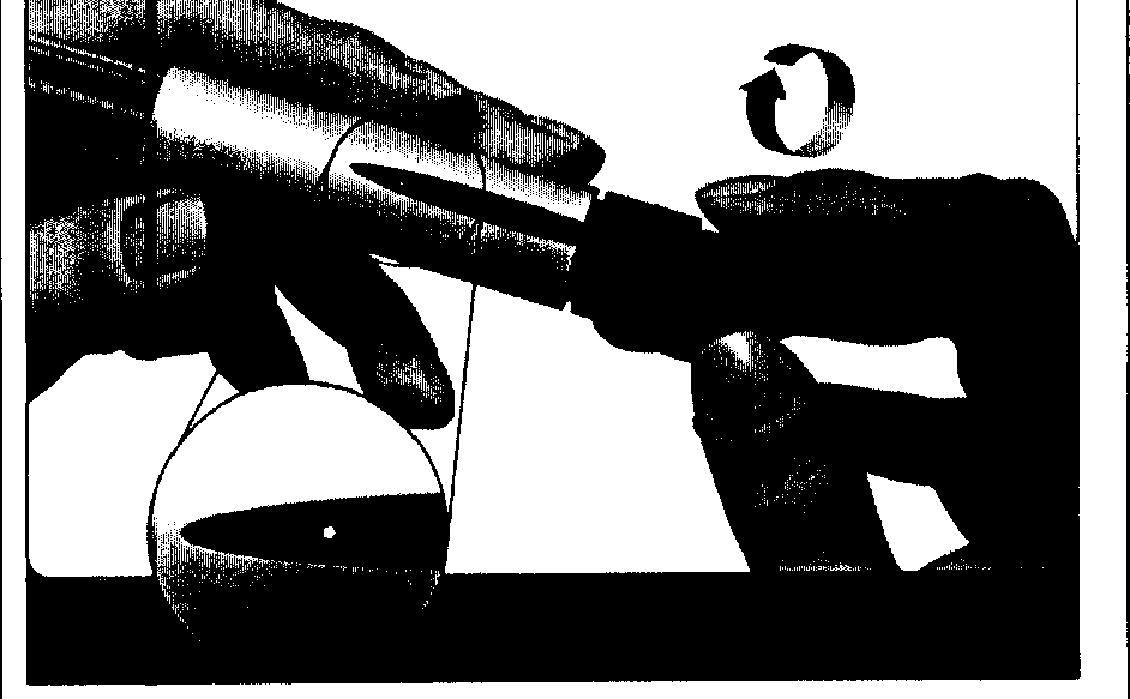
— Вставьте наконечник шприц-ручки с резьбой в наружный колпачок иглы и навинчивайте наружный колпачок до тех пор, пока он прочно не зафиксируется.
1.3 Удалите крупные воздушные пузырьки:
— Внимательно осмотрите отсек с резервуаром.
— Если Вы не обнаружили крупного воздушного пузырька, значит, шприц-ручка готова к использованию. В таком случае перейдите к пункту 2 «Установка дозы на 250».
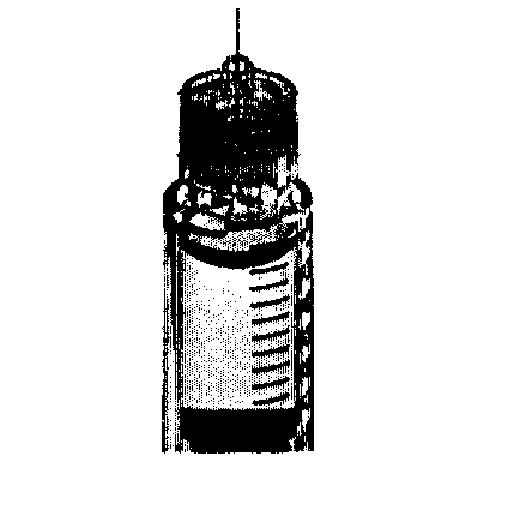
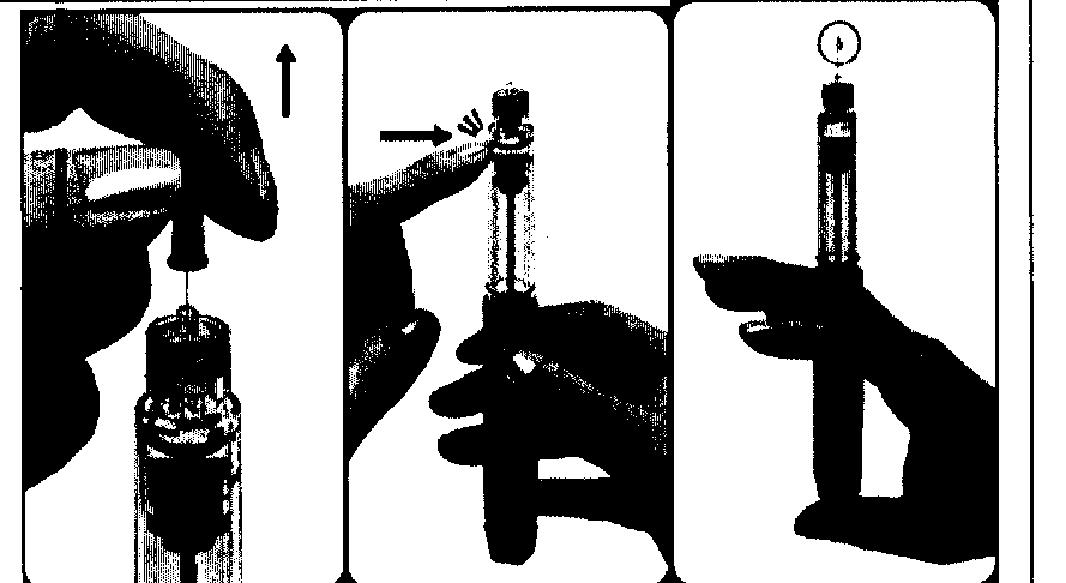
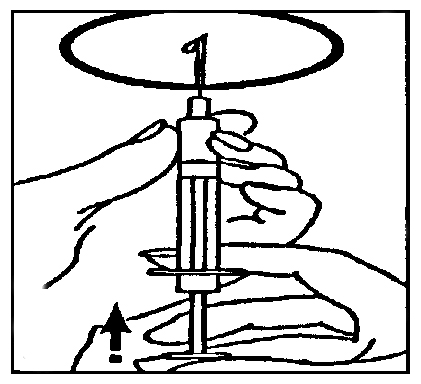
Воздушный пузырек считается крупным, если полностью заполняет наконечник отсека с картриджем при удерживании шприц-ручки иглой вверх (см. рисунок). Если Вы видите внутри отсека с резервуаром большой воздушный пузырек, его необходимо удалить. В шприц-ручке может оставаться несколько мелких воздушных пузырьков, прилипших к внутренней стенке отсека с резервуаром. Не обращайте внимания на мелкие пузырьки, их удалять не обязательно.
Чтобы удалить крупный воздушный пузырек
1. Осторожно поворачивайте кнопку для установки дозы по часовой стрелке до тех пор, пока на табло указателя дозы не появится точка (-). Если Вы проскочили это положение, просто поверните кнопку обратно на точку (-).
2. Затем снимите внутренний колпачок иглы и удерживайте шприц-ручку иглой вверх.
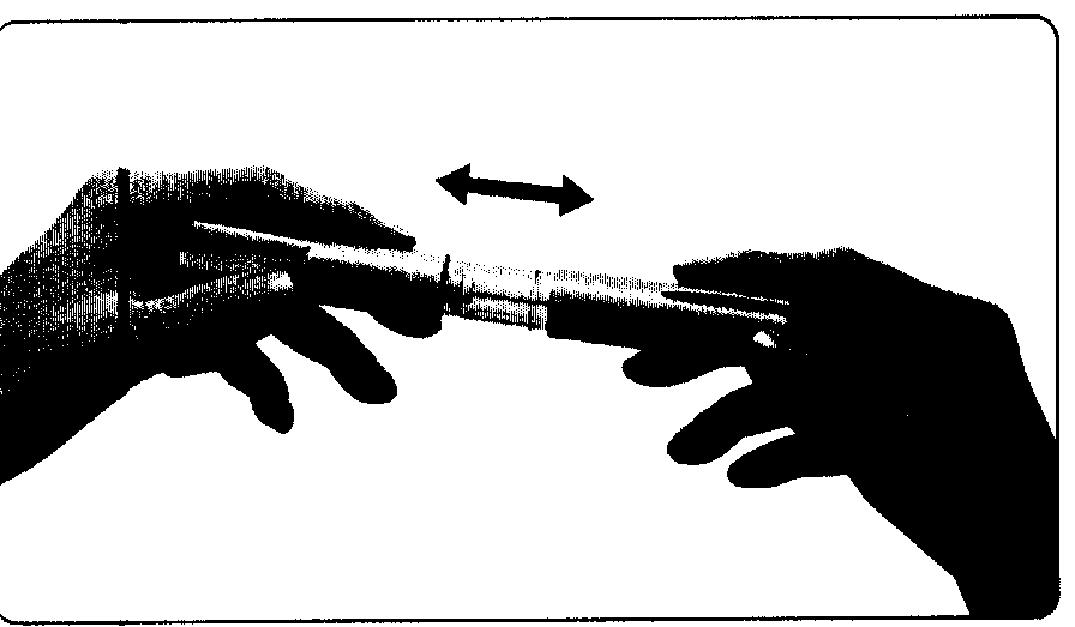
3. Слегка постучите по отсеку с резервуаром пальцем так, чтобы все воздушные пузырьки всплыли наверх к игле. Продолжая удерживать шприц-ручку иглой вверх и плавно нажимая на кнопку для установки дозы продвиньте поршень настолько, чтобы выпустить воздушный пузырек.
4. На кончике иглы должна появиться капля раствора; это означает, что Ваша шприц-ручка готова к проведению инъекции.
5. Если раствор не проступил на кончике иглы, повторите манипуляции, описанные выше, еще раз (максимальное количество попыток — 2), начиная с шага 1 (пункт «Чтобы удалить большой воздушный пузырек»).
2. Установка дозы на 250
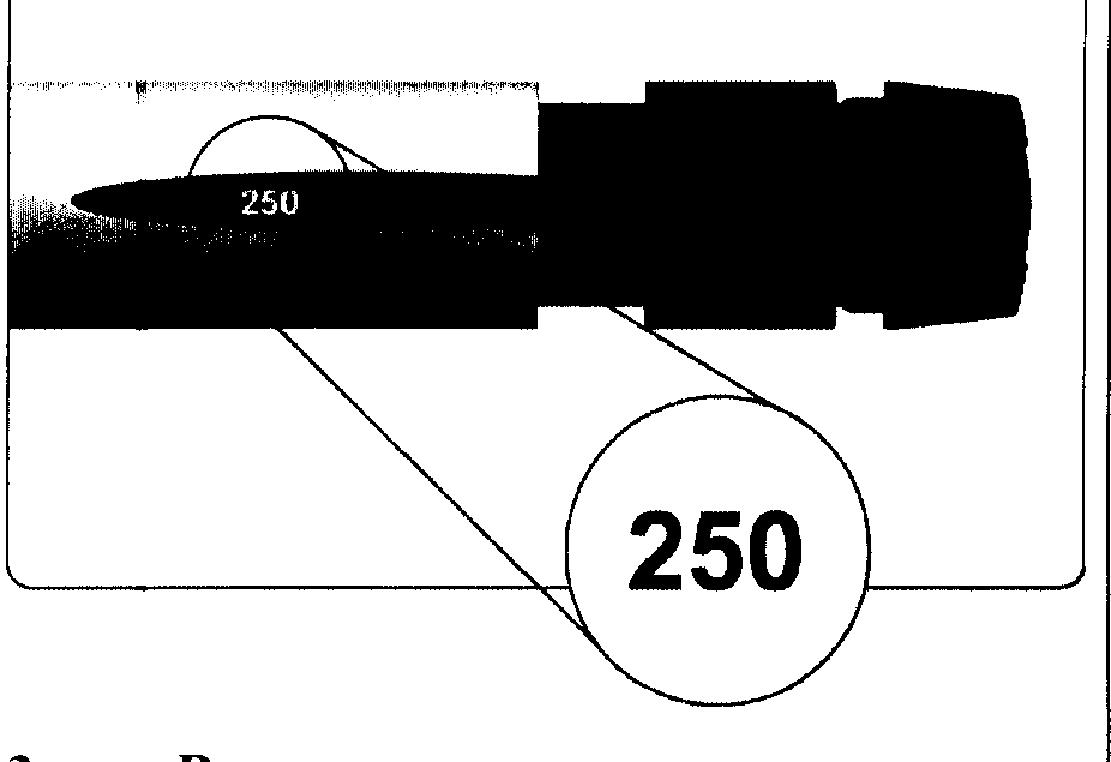
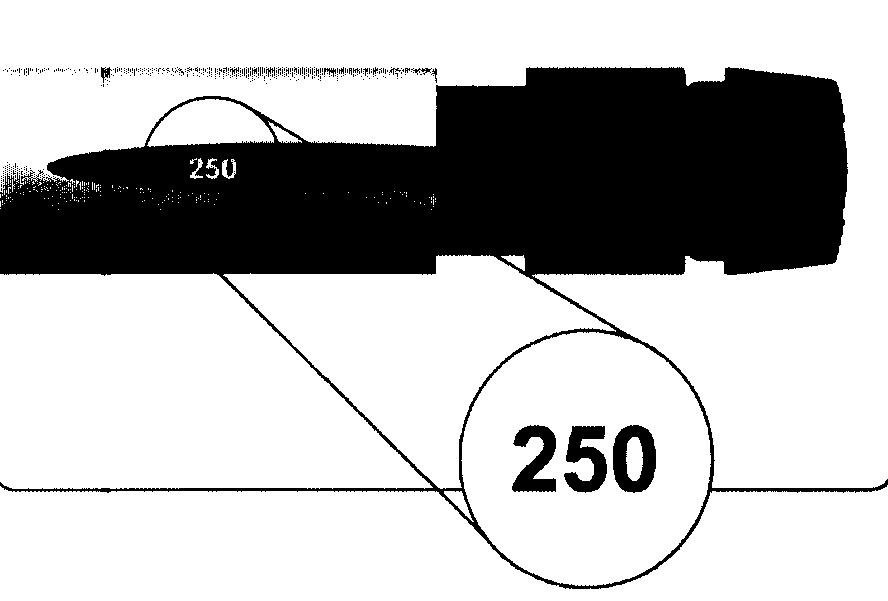
— Аккуратно поворачивайте кнопку для установки дозы по часовой стрелке до тех пор, пока на табло указателя дозы вместо прямой линии не появится число «250».
— Проворачивая кнопку для установки дозы не следует на нее давить или, наоборот, оттягивать.
— На табло указателя дозы должно появиться число «250», как показано на рисунке ниже.
3. Введение дозы
1. Выберите место для инъекции, указанное врачом или медсестрой.
2. Продезинфицируйте место инъекции, протерев его тампоном, смоченным в спирте.
3. Убедитесь еще раз, чтона табло выставлено число «250». Если на табло числа нет, необходимо установить правильную дозу (см. раздел 2 «Установка дозы на 250»).
4. Аккуратно снимите внутренний колпачок и выбросьте его (если это еще не было сделано при выполнении инструкций из пункта 1.3 «Удалите крупные воздушные пузырьки»).
Введите дозу в соответствии с указаниями Вашего врача или медсестры
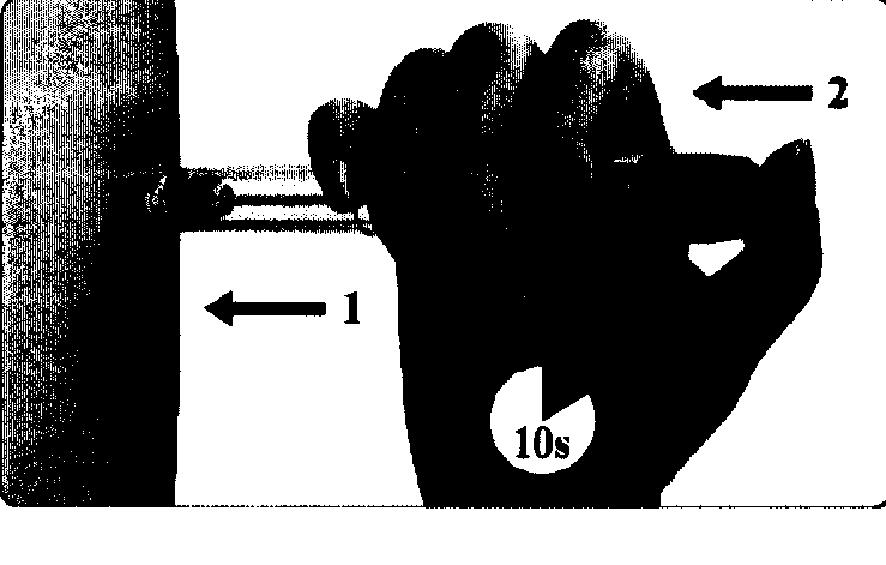
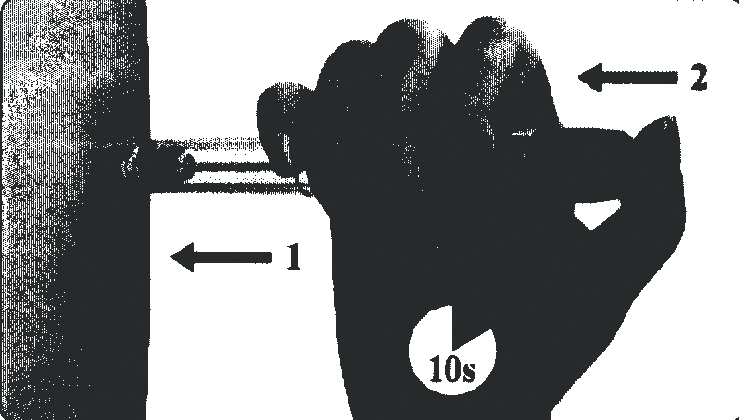
— Сначала медленно введите иглу под кожу, после чего надавите на кнопку для установки дозы до упора, как показано на рисунке ниже.
— Число с дозировкой, указанное на табло указателя дозы, вернется обратно в положение «О». Это означает, что была введена вся доза.
— Оставьте иглу под кожей при нажатой кнопке для установки дозы минимум на 10 секунд.
— По прошествии 10 секунд выньте иглу, удерживая кнопку для установки дозы в нажатом положении.
4. После инъекции
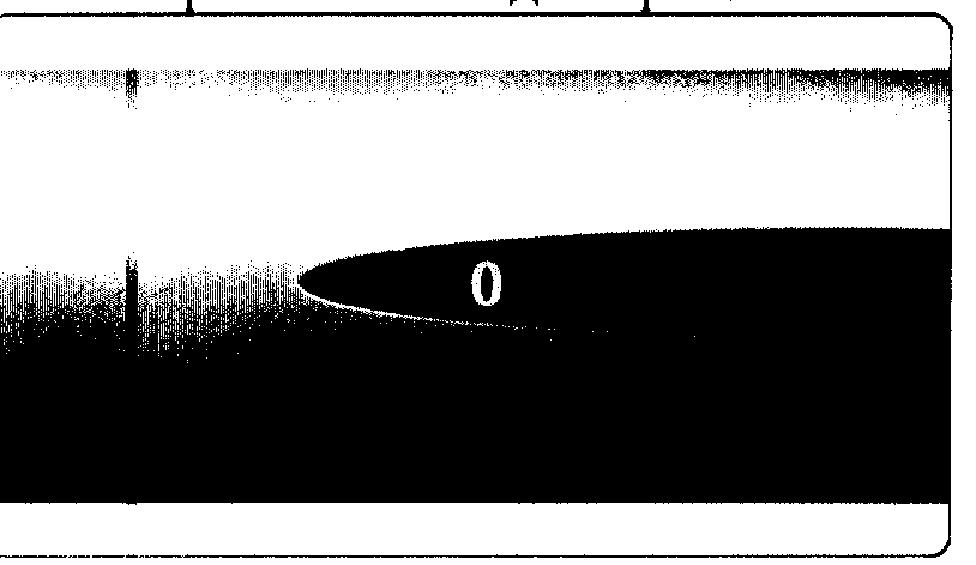
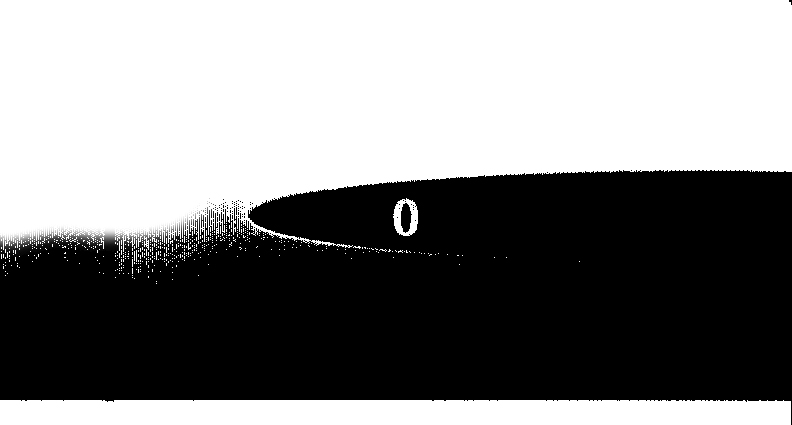
4.1 Убедитесь, что на табло указателя дозы появилось число «0»
— Это означает, что доза была введена полностью. Не предпринимайте попыток провести инъекцию второй раз.
— Если на табло число «0» не появилось, свяжитесь с Вашим врачом или медсестрой.
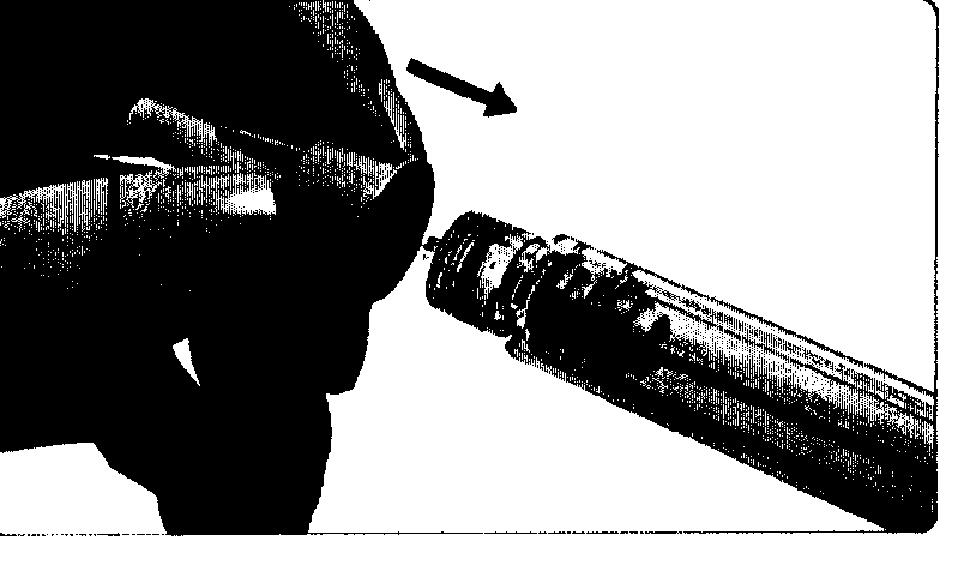
4.2 Снятие иглы
— Крепко удерживайте шприц-ручку за отсек с резервуаром.
— Осторожно наденьте наружный колпачок на иглу.
— Затем сожмите наружный колпачок и отвинтите иглу.
— Будь осторожны, не уколитесь об иглу.
— Теперь наденьте колпачок шприц-ручки обратно на ручку.
4.3 Утилизация
— Никогда не используйте иглу или шприц-ручку повторно.
— Выполнив инъекцию утилизируйте использованную иглу и шприц-ручку, соблюдая меры предосторожности.
— Лучше всего поместить ее обратно в упаковку от производителя. Лекарственные препараты не следует выбрасывать в канализацию или утилизировать вместе с бытовыми отходами. Когда шприц-ручка закончится, получите у своего врача или медсестры инструкции по ее утилизации.
Если Вы ввели слишком большую дозу препарата,могут появиться симптомы синдрома гиперстимуляции яичников (СГЯ), которые описаны в разделе «Особые указания» или «Побочные эффекты». Если эти симптомы появились, проконсультируйтесь с врачом.
Если Вы забыли ввести препарат, проконсультируйтесь с врачом как можно скорее.
Побочные эффекты:
При применении лекарственного препарата Овитрель® возможно развитие побочных эффектов.В процессе сравнительных клинических исследованиях различных доз препарата Овитрель® была показана дозозависимость появления таких побочных эффектов как СГЯ, тошнота и рвота. СГЯ наблюдался приблизительно у 4% пациентов, получавших Овитрель® Тяжелая форма СГЯ отмечалась менее, чем у 0,5% пациентов.
В зависимости от частоты появления побочные эффекты расцениваются как очень частые (≥1/10), частые (≥1/100 и <1/10), нечастые (≥1/1000 и <1/100), редкие (≥1/10000 и <1/1000), очень редкие (<1/10000, включая единичные сообщения). Частота побочных эффектов в каждой группе указана в порядке убывания.Взависимости от частоты встречаемости побочные явления могут быть разделены на группы:
Иммунная система: очень редко — от легкой до тяжелой реакции гиперчувствительности, включая анафилактические реакции и шок.
ЦНС: нечасто — депрессия, раздражительность, возбуждение.
Нервная система: часто — головная боль.
Сосудистая система: очень редко — тромбоэмболия, обычно связанная с тяжелой формой СГЯ.
Пищеварительная система: часто тошнота, рвота, боль в животе, нечасто -диарея.
Кожа и подкожная клетчатка: очень редко -легкие обратимые кожные реакции в виде сыпи.
Репродуктивная система и молочные железы: часто — СГЯ легкой или средней степени тяжести, нечасто — тяжелая форма СГЯ, болезненность молочных желез.
Общие и местные реакции: часто — утомляемость, реакции в месте инъекции.
Передозировка:
Данные о передозировке препаратом отсутствуют. Тем не менее, при передозировке процессе стимуляции яичников возможно развитие СГЯ (см. «Особые указания»).
Клинически он характеризуется образованием крупных кист яичника с риском их разрыва (перфорации), симптомами асцита и циркуляторными расстройствами.
Взаимодействие:
Данные о взаимодействии с другими лекарственными средствами отсутствуют. Тем не менее, пациентке необходимо информировать врача о всех лекарственных средствах (в том числе безрецептурных), которые она принимает в настоящее время или недавно принимала.
Особые указания:
Перед началом лечения необходимо установить причины бесплодия у пациентки и ее партнера и оценить предполагаемые факторы риска при наступлении беременности. Особенно следует учитывать симптомы гипотиреоза, адренокортикальной недостаточности, гиперпролактинемии, наличие опухолей
гипофиза или гипоталамуса, и применяемые специфические методы терапии.
Синдром гиперстимуляции яичников (СГЯ)
В процессе стимуляции яичников повышается риск возникновения СГЯ из-за одновременного созревания большого числа фолликулов.
СГЯ может стать серьезным осложнением, характеризующимся образованием крупных кист яичника с риском их разрыва, увеличением веса, одышкой, олигурией или наличием асцита в клинической картине циркуляторных нарушений. СГЯ тяжелой степени в редких случаях может сопровождаться гемоперитонеумом, острым легочным дистресс-синдромом, перекрутом яичника и тромбоэмболией.
С целью снижения риска СГЯ в протоколе стимуляции роста фолликулов рекомендуется тщательное наблюдение за ответной реакцией яичников при помощи ультразвукового исследования и определение уровня эстрадиола в крови перед началом курса лечения и во время него.
При ановуляции риск развития СГЯ повышается при концентрации эстрадиола в плазме крови > 1500 пг/мл (5400 пмоль/л) и наличие более 3 фолликулов диаметром 14 мм или более. При ВРТ риск развития СГЯ повышается при концентрации эстрадиола > 3000 пг/мл (11000 пмоль/л) или наличии 18 или более фолликулов диаметром 11 мм и более.
СГЯ, вызванный чрезмерным ответом яичника, можно избежать, если отменить введение чХГ. Поэтому, если уровень эстрадиола в сыворотке крови > 5500 пг/мл (20 ООО пмоль/л) и/или когда в наличии 30 или более фолликулов, следует воздержаться от применения чХГ. Пациенткам рекомендуют воздержаться от коитуса или использовать барьерные методы контрацепции не менее 4-х дней.
Многоплодная беременность
По сравнению с естественным оплодотворением при проведении стимуляции возрастает риск многоплодной беременности. В большинстве случаев рождаются двойни. При применении методов вспомогательной репродукции количество родившихся младенцев соответствует числу эмбрионов, перенесенных в полость матки.
Использование рекомендованных доз препарата Овитрель®, схемы лечения и тщательный мониториг в процессе терапии минимизируют риск возникновения СГЯ и многоплодной беременности.
Невынашивание беременности
Статистика выкидышей после лечения ановуляторного бесплодия, в том числе с помощью ВРТ, превышает показатели в среднем по популяции, но сравнима с другими видами бесплодия.
Внематочная беременность
У пациенток с заболеваниями маточных труб в анамнезе повышен риск внематочной беременности независимо от того, получена ли беременность обычным путем или в процессе лечения бесплодия. Вероятность внематочной беременности после применения вспомогательных репродуктивных технологий выше, чем в общей популяции.
Врожденные аномалии развития
Частота врожденных аномалий после применения программ ВРТ может быть несколько выше, чем при естественной беременности и родах. Тем не менее, неизвестно, связано ли это с особенностью родителей (например, возраст матери, качество спермы) и многоплодной беременностью или же непосредственно с процедурами ВРТ.
Тромбоэмболические осложнения
У пациенток с недавно перенесенными или текущими тромбоэмболическими заболеваниями, а также при вероятном риске их возникновения при наличии заболевания в анамнезе или у родственников, применение гонадотропинов может увеличить этот риск или осложнить течение данных заболеваний. Для пациенток данной группы польза от терапии должна быть соотнесена с возможным риском. Следует отметить, что беременность сама по себе, как и СГЯ, несет повышенный риск тромбоэмболических нарушений, таких как эмболия легких, ишемический инсульт или инфаркт миокарда.
Влияние на лабораторные показатели
Ведение препарата Овитрель® может влиять на иммунологическую картину уровня чХГ в сыворотке крови и в моче в течение 10 дней и привести к появлению ложноположительной реакции при проведении теста на беременность.
Прочая информация
Во время проведения терапии препаратом Овитрель® возможна незначительная стимуляция функции щитовидной железы.
Если проявления побочных реакций усиливаются или Вы отмечаете побочные эффекты, не упомянутые в инструкции, пожалуйста, сообщите об этом Вашему лечащему врачу.
В течение срока годности препарат (только для шприцев) может храниться вне холодильника при температуре не выше 25 °С 30 дней. Если по истечении 30 дней такого хранения препарат не был использован, он должен быть уничтожен.
Влияние на способность управлять транспортными средствами и механизмами:
Практически не влияет на управление транспортным средством или каким-либо другим механизмом.
Форма выпуска/дозировка:
Раствор для подкожного введения, 250 мкг/0,5 мл.
Упаковка:
0,5 мл раствора, содержащего 250 мкг (6500 ME) хориогонадотропина альфа в бесцветном стеклянном шприце с иглой для инъекций, закрытой защитным колпачком с резиновой прокладкой.
0,5 мл раствора, содержащего 250 мкг (6500 ME) хориогонадотропина альфа в шприц-ручке.
1 шприц упакован в пластиковый контейнер, помещенный в картонную пачку с Инструкцией по применению.
1 шприц-ручка и 1 игла для инъекции упакованы в пластиковый контейнер, помещенный в картонную пачку с инструкцией по применению.
Условия хранения:
При температуре 2 — 8 °С в оригинальной упаковке. Не замораживать. Хранить в недоступном для детей месте.
Срок годности:
2 года. Не использовать препарат после истечения срока годности.
Условия отпуска
По рецепту
Производитель
Мерк Сероно С.п.А., Via delle Magnolie 15 (loc. frazione Zona Industriale), 70026 Modugno (BA), Italy, Италия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
Мерк Сероно С.п.А.
Купить Овитрель в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Описание препарата Овитрель® (лиофилизат для приготовления раствора для подкожного введения, 250 мкг) основано на официальной инструкции, утверждено компанией-производителем в 2012 году
Дата согласования: 03.10.2012
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Характеристика
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Отзывы
Действующее вещество
ATX
Фармакологическая группа
Состав
| Лиофилизат для приготовления раствора для подкожного введения | 1 заполненный шприц |
| активное вещество: | |
| хориогонадотропин альфа | 250 мкг (6500 МЕ ) |
| вспомогательные вещества: маннитол — 27,3 мг |
Описание лекарственной формы
Лиофилизат для приготовления раствора для п/к введения — порошок или пористая масса белого или почти белого цвета.
Раствор для подкожного введения — прозрачный или слегка опалесцирующий, бесцветный или светло-желтого цвета.
Фармакологическое действие
Фармакологическое действие
—
гонадотропное, лютеинизирующее.
Характеристика
Рекомбинантный хориогонадотропин альфа имеет ту же аминокислотную последовательность, что и человеческий хорионический гонадотропин, содержащийся в моче.
Фармакодинамика
Овитрель® содержит хориогонадотропин альфа (ХГ альфа), который производится при помощи рекомбинантной ДНК технологии. Он имеет ту же аминокислотную последовательность, что и естественный человеческий ХГ. ХГ связывает трансмембранные рецепторы ЛГ на поверхности клеток теки и гранулезы яичника. Вызывает инициирование ооцитарного мейоза, разрыв фолликулов (овуляцию), формирование желтого тела, продукцию прогестерона и эстрадиола желтым телом.
Фармакокинетика
Всасывание и распределение. После в/в введения ХГ альфа распределяется во внеклеточную жидкость с периодом полураспределения около 4,5 ч.
Стационарный Vd и общий клиренс составляют 6 л и 0,2 л/ч соответственно.
При подкожном введении ХГ альфа абсолютная биодоступность составляет приблизительно 40%, конечный T1/2 — около 30 ч.
Выведение и метаболизм. Метаболизм и выведение ХГ альфа аналогичны эндогенному ХГ.
Показания
в протоколе индукции множественного созревания фолликулов для вспомогательных репродуктивных технологий (ВРТ), в т.ч. для экстракорпорального оплодотворения (ЭКО), с целью индукции финального созревания фолликулов и лютеинизации после стимуляции препаратами гонадотропинов;
при ановуляторном или олигоовуляторном бесплодии для индукции овуляции и лютеинизации в конце стимуляции роста фолликулов.
Противопоказания
повышенная чувствительность к активному компоненту и к любому из вспомогательных компонентов, входящих в состав препарата;
опухоли в области гипоталамуса и гипофиза;
объемные новообразования яичника или кисты, несвязанные с поликистозом яичника;
вагинальные кровотечения неясного генеза;
злокачественные новообразования яичника, матки или молочной железы;
внематочная беременность в течение 3 предыдущих месяцев;
тромбоэмболия;
первичная овариальная недостаточность;
врожденные пороки развития половых органов, несовместимые с беременностью;
фибромиома матки, несовместимая с беременностью;
постменопауза.
С осторожностью следует назначать Овитрель® пациенткам с серьезными системными заболеваниями в тех случаях, когда беременность может привести к их обострению.
Применение при беременности и кормлении грудью
В период беременности и грудного вскармливания препарат Овитрель® не назначается. Данные об экскреции ХГ альфа в грудное молоко отсутствуют.
Способ применения и дозы
П/к. Каждый флакон или шприц предназначены только для однократного использования.
При применении в протоколе индукции множественного созревания фолликулов для вспомогательных репродуктивных технологий (в т.ч. для ЭКО) с целью индукции финального созревания фолликулов и лютеинизации после стимуляции препаратами гонадотропинов Овитрель® в дозе 250 мкг (содержимое 1 флакона или 1 шприца) вводят однократно через 24–48 ч после последнего введения препарата ФСГ или ЛГ и достижения оптимального уровня развития фолликула.
При ановуляторном или олигоовуляторном бесплодии для индукции овуляции и лютеинизации в конце стимуляции роста фолликулов Овитрель® в дозе 250 мкг (содержимое 1 флакона или 1 шприца) вводится однократно через 24–48 ч после последнего введения препарата ФСГ или ЛГ и достижения оптимального уровня развития фолликула. Рекомендуется половой контакт в день введения препарата и на следующий день.
Порядок самостоятельного введения препарата
1. Необходимо вымыть руки.
2. Подготовить чистую поверхность и разложить на ней: 2 тампона, смоченные спиртом (к упаковке не прикладываются), 1 шприц с препаратом.
3. Далее следует сразу же провести инъекцию (в область живота или переднюю часть бедра). Для этого следует протереть выбранный участок тампоном со спиртом. Сильно стянуть кожу пальцами и, направив иглу под углом 45–90° в кожную складку, сделать п/к инъекцию. Необходимо избегать попадания препарата в вену. Препарат вводят медленно, осторожно нажимая на поршень. После извлечения иглы протереть круговыми движениями место инъекции тампоном со спиртом.
4. Сразу после инъекции следует поместить использованный шприц в контейнер для хранения острых предметов. Весь неиспользованный объем следует уничтожить.
Побочные действия
При применении лекарственного препарата Овитрель® возможно развитие побочных эффектов, которые в зависимости от частоты появления расцениваются как очень частые (≥1/10), частые (≥1/100 и <1/10), нечастые (≥1/1000 и <1/100), редкие (≥1/10000 и <1/1000), очень редкие (<1/10000, включая единичные сообщения).
Частота побочных эффектов в каждой группе указана в порядке убывания. В зависимости от частоты встречаемости побочные явления могут быть разделены на группы:
Со стороны иммунной системы: очень редко — от легкой до тяжелой реакции гиперчувствительности, включая анафилактические реакции и шок.
Со стороны ЦНС: часто — головная боль. нечасто — депрессия, раздражительность, возбуждение.
Со стороны сосудистой системы: часто — тромбоэмболия, обычно связанная с тяжелой формой синдрома гиперстимуляции яичников (СГЯ).
Со стороны пищеварительной системы: часто – тошнота, рвота, боль в животе, нечасто — диарея.
Со стороны кожи и подкожной клетчатки: очень редко — легкие обратимые кожные реакции в виде сыпи.
Со стороны репродуктивной системы и молочных желез: часто — СГЯ легкой или средней степени тяжести, нечасто — тяжелая форма СГЯ, болезненность молочных желез.
Общие и местные реакции: часто — утомляемость, реакции в месте инъекции.
Взаимодействие
Данные о взаимодействии с другими ЛС отсутствуют. Тем не менее, пациентке необходимо информировать врача о всех ЛС (в т.ч. безрецептурных), которые она принимает в настоящее время или недавно принимала.
Передозировка
Данные о передозировке препарата отсутствуют.
Симптомы: возможно развитие СГЯ, характеризующегося образованием крупных кист яичника с риском их разрыва (перфорации), развитием асцита и расстройств кровообращения.
Лечение: при высоком риске развития СГЯ рекомендуется отменить введение человеческого ХГ. Пациенткам в течение не менее 4 дней рекомендуется воздержаться от полового контакта или использовать барьерные методы контрацепции.
Особые указания
Перед началом лечения необходимо установить причины бесплодия у пациентки и ее партнера и оценить предполагаемые факторы риска при наступлении беременности. Следует учитывать наличие клинически выраженного гипотиреоза, надпочечниковой недостаточности, гиперпролактинемии, а также опухоли гипоталамо-гипофизарной области в анамнезе и применяемые специфические методы терапии.
В процессе стимуляции яичников пациентки подвергаются риску развития СГЯ из-за одновременного созревания большого числа фолликулов. СГЯ тяжелой степени может стать серьезным осложнением стимуляции. С целью снижения риска развития этого осложнения в протоколе стимуляции роста фолликулов рекомендуется тщательное наблюдение за ответной реакцией яичников при помощи УЗИ и определение уровня эстрадиола в крови перед началом курса лечения и во время него.
По сравнению с естественным оплодотворением при проведении стимуляции возрастает риск многоплодной беременности. В большинстве случаев рождаются двойни. При применении методов вспомогательной репродукции количество родившихся младенцев соответствует числу эмбрионов, перенесенных в полость матки.
Статистика выкидышей после лечения ановуляторного бесплодия (в т.ч. с помощью ВРТ) превышает показатели в среднем по популяции, но сравнима с другими видами бесплодия.
Введение препарата Овитрел® может влиять на иммунологическую картину уровня человеческого ХГ в сыворотке крови и моче в течение 10 дней и привести к появлению ложноположительной реакции при проведении теста на беременность.
Во время проведения терапии препаратом Овитрель® возможна незначительная стимуляция функции щитовидной железы.
Перед началом лечения необходимо установить причины бесплодия у пациентки и ее партнера и оценить предполагаемые факторы риска при наступлении беременности. Особенно следует учитывать симптомы гипотиреоза, адренокортикальной недостаточности, гиперпролактинемии, наличие опухолей гипофиза или гипоталамуса, и применяемые специфические методы терапии.
Синдром гиперстимуляции яичников (СГЯ)
В процессе стимуляции яичников повышается риск возникновения СГЯ из-за одновременного созревания большого числа фолликулов. СГЯ может стать серьезным осложнением, характеризующимся образованием крупных кист яичника с риском их разрыва, увеличением веса, одышкой, олигурией или наличием асцита в клинической картине циркуляторных нарушений. СГЯ тяжелой степени в редких случаях может сопровождаться гемоперитонеумом, острым легочным дистресс-синдромом, перекрутом яичника и тромбоэмболией.
С целью снижения риска СГЯ в протоколе стимуляции роста фолликулов рекомендуется тщательное наблюдение за ответной реакцией яичников при помощи УЗИ и определение уровня эстрадиола в крови перед началом курса лечения и во время него.
При ановуляции риск развития СГЯ повышается при концентрации эстрадиола в плазме крови >1500 пг/мл (5400 пмоль/л) и наличии более 3 фолликулов диаметром 14 мм или более. При ВРТ риск развития СГЯ повышается при концентрации эстрадиола >3000 пг/мл (11000 пмоль/л) или наличии 18 или более фолликулов диаметром 11 мм и более.
СГЯ, вызванный чрезмерным ответом яичника, можно избежать, если отменить введение человеческого ХГ. Поэтому если уровень эстрадиола в сыворотке крови >5500 пг/мл (20000 пмоль/л) и/или когда в наличии 30 или более фолликулов, следует воздержаться от применения человеческого ХГ. Пациенткам рекомендуют воздержаться от коитуса или использовать барьерные методы контрацепции не менее 4 дней.
Многоплодная беременность
По сравнению с естественным оплодотворением при проведении стимуляции возрастает риск многоплодной беременности. В большинстве случаев рождаются двойни. При применении методов вспомогательной репродукции количество родившихся младенцев соответствует числу эмбрионов, перенесенных в полость матки.
Использование рекомендованных доз препарата Овитрель®, схемы лечения и тщательный мониторинг в процессе терапии минимизируют риск возникновения СГЯ и многоплодной беременности.
Невынашивание беременности
Статистика выкидышей после лечения ановуляторного бесплодия, в том числе с помощью ВРТ, превышает показатели в среднем по популяции, но сравнима с другими видами бесплодия.
Внематочная беременность
У пациенток с заболеваниями маточных труб в анамнезе повышен риск внематочной беременности независимо от того, получена ли беременность обычным путем или в процессе лечения бесплодия. Вероятность внематочной беременности после применения вспомогательных репродуктивных технологий выше, чем в общей популяции.
Врожденные аномалии развития
Частота врожденных аномалий после применения программ ВРТ может быть несколько выше, чем при естественной беременности и родах. Тем не менее, неизвестно, связано ли это с особенностью родителей (например возраст матери, качество спермы) и многоплодной беременностью или же непосредственно с процедурами ВРТ.
Тромбоэмболические осложнения
У пациенток с недавно перенесенными или текущими тромбоэмболическими заболеваниями, а также при вероятном риске их возникновения при наличии заболевания в анамнезе или у родственников, применение гонадотропинов может увеличить этот риск или осложнить течение данных заболеваний. Для пациенток данной группы польза от терапии должна быть соотнесена с возможным риском.
Следует отметить, что беременность сама по себе, как и СГЯ, несет повышенный риск тромбоэмболических нарушений, таких как эмболия легких, ишемический инсульт или инфаркт миокарда.
Влияние на лабораторные показатели
Введение препарата Овитрель® может влиять на иммунологическую картину уровня чХГ в сыворотке крови и в моче в течение 10 дней и привести к появлению ложноположительной реакции при проведении теста на беременность.
Прочая информация
Во время проведения терапии препаратом Овитрель® возможна незначительная стимуляция функции щитовидной железы.
Если проявления побочных реакций усиливаются или развиваются побочные эффекты, не упомянутые в инструкции, необходимо сообщить об этом лечащему врачу.
В течение срока годности препарат может храниться вне холодильника при температуре не выше 25 °C 30 дней. Если по истечении 30 дней такого хранения препарат не был использован, он должен быть уничтожен.
Влияние на управление транспортными средствами. Практически не влияет на управление транспортным средством или каким-либо другим механизмом.
Форма выпуска
Раствор для подкожного введения, 250 мкг/0,5 мл. 0,5 мл раствора, содержащего 250 мкг (6500 МЕ) хориогонадотропина альфа. В бесцветном стеклянном шприце с иглой для инъекций, закрытой защитным колпачком с резиновой прокладкой. Шприц упакован в пластиковый контейнер, помещенный в картонную пачку.
Производитель
Мерк Сероно С.п.А.
Виа Касилина 125, 00176 Рим, Италия.
Адрес производства
Мерк Сероно С.п.А.
Виа делле Маниолие 15 (район Индустриальной зоны) 70026 Модугно (БА), Италия.
Претензии потребителей и информацию о нежелательных явлениях следует направлять по адресу:
Представительство компании Арес Трейдинг С.А.
125445, Москва, ул. Смольная 24Д, офис ООО «Мерк».
Тел: (495) 937-33-04, факс: (495) 937-33-05.
e-mail: safety@merck.ru.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Растворитель – 3 г
Не применять по истечении срока годности, указанного на упаковке.
Информация о групповых и нозологических аналогах предназначена
только для
специалистов.
Групповые и нозологические аналоги не являются полными аналогами препаратов, решение об их использовании может быть принято только специалистом при назначении терапии в отсутствие препаратов первой линии.
Групповые аналоги: 17
| Название | Форма выпуска | Владелец рег. уд. | ||
|
Альтерпур |
Лиофилизат д/пригот. р-ра д/в/м и п/к введения 75 МЕ: фл. 1 или 10 шт. в компл. с растворителем рег. №: ЛП-000134 Лиофилизат д/пригот. р-ра д/в/м и п/к введения 150 МЕ: фл. 1 или 10 шт. в компл. с растворителем рег. №: ЛП-000134 |
IBSA Institut Biochimique (Швейцария) Интересы в РФ представляет: Фарма Риаче Лимитед (Великобритания) контакты: Фарма Риаче Лтд. (Великобритания) |
||
|
Гонал-ф® |
Лиофилизат д/пригот. р-ра д/п/к введения 5.5 мкг (75 МЕ): фл. 1, 5 или 10 шт. в компл. с растворителем рег. №: ЛС-000200 |
Мерк (Россия) Произведено и расфасовано (лиофилизат): MERCK SERONO S.A., Succursale d’Aubonne (Швейцария) Произведено и расфасовано (растворитель): MERCK SERONO (Италия) Упаковка и выпускающий контроль качества: MERCK SERONO S.A., Succursale d’Aubonne (Швейцария) |
||
|
Гонал-ф® |
Р-р д/п/к введения 22 мкг (300 МЕ)/0.5 мл: шприц-ручки 1 шт. в компл. с иглами рег. №: ЛС-000957 |
Мерк (Россия) Произведено: MERCK SERONO (Италия) |
||
|
Гонал-ф® |
Р-р д/п/к введения 33 мкг (450 МЕ)/0.75 мл: шприц-ручки 1 шт. в компл. с иглами рег. №: ЛС-000957 |
Мерк (Россия) Произведено: MERCK SERONO (Италия) |
||
|
Гонал-ф® |
Р-р д/п/к введения 66 мкг (900 МЕ)/1.5 мл: шприц-ручки 1 шт. в компл. с иглами рег. №: ЛС-000957 |
Мерк (Россия) Произведено: MERCK SERONO (Италия) |
||
|
Луверис® |
Лиофилизат д/пригот. р-ра д/п/к введения 75 МЕ: фл. 1, 3 или 10 шт. в компл. с растворителем рег. №: П N015642/01 |
MERCK SERONO (Италия) Произведено: MERCK SERONO S.A., Succursale d’Aubonne (Швейцария) |
||
|
Менопур® |
Лиофилизат д/пригот. р-ра д/в/м и п/к введения 75 МЕ+75 МЕ: фл. 5 или 10 шт. в компл. с растворителем рег. №: ЛП-(000300)-(РГ-RU ) Предыдущий рег. №: П N015764/01 |
FERRING (Германия) Произведено (лиофилизат): FERRING (Германия) Произведено (растворитель): HAUPT PHARMA WULFING (Германия) ZENTIVA (Чешская Республика) Упаковано: FERRING INTERNATIONAL CENTER (Швейцария) Выпускающий контроль качества: FERRING (Германия) контакты: ФЕРРИНГ ФАРМАСЕТИКАЛЗ Б.В. (Нидерланды) |
||
|
Менопур® Мультидоза |
Лиофилизат д/пригот. р-ра д/п/к введения 600 МЕ+600 МЕ: фл. 1 шт. в компл. с растворителем рег. №: ЛП-(000296)-(РГ-RU ) Предыдущий рег. №: ЛП-002518 Лиофилизат д/пригот. р-ра д/п/к введения 1200 МЕ+1200 МЕ: фл. 1 шт. в компл. с растворителем рег. №: ЛП-(000296)-(РГ-RU ) Предыдущий рег. №: ЛП-002518 |
FERRING-LECIVA (Чешская Республика) Произведено: FERRING (Германия) Упаковано: FERRING INTERNATIONAL CENTER (Швейцария) |
||
|
Мериоферт |
Лиофилизат д/пригот. р-ра д/в/м и п/к введения 75 МЕ+75 МЕ: фл. 1 шт. в компл. с растворителем рег. №: ЛП-000120 Лиофилизат д/пригот. р-ра д/в/м и п/к введения 150 МЕ+150 МЕ: фл. 1 шт. в компл. с растворителем рег. №: ЛП-000120 |
IBSA Institut Biochimique (Швейцария) Произведено (лиофилизат): IBSA Institut Biochimique (Швейцария) Произведено (растворитель): IBSA Farmaceutici Italia S.r.l. (Италия) Выпускающий контроль качества: IBSA Institut Biochimique (Швейцария) |
||
|
Перговерис® |
Лиофилизат д/пригот. р-ра д/п/к введения 150 МЕ + 75 МЕ: фл. 1, 3 или 10 шт. в компл. с растворителем рег. №: ЛП-001160 |
Мерк (Россия) Произведено: MERCK SERONO S.A., Succursale d’Aubonne (Швейцария) |
||
|
Примапур® |
Р-р д/п/к введения 22 мкг/0.5 мл: шприц-ручки 1 шт. в компл. с иглами рег. №: ЛП-005826 Р-р д/п/к введения 33 мкг/0.75 мл: шприц-ручки 1 шт. в компл. с иглами рег. №: ЛП-005826 Р-р д/п/к введения 66 мкг/1.5 мл: шприц-ручки 1 шт. в компл. с иглами рег. №: ЛП-005826 |
АйВиФарма (Россия) Произведено: ЗАВОД МЕДСИНТЕЗ (Россия) ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (Россия) |
||
|
Пурегон® |
Р-р д/п/к введения 300 МЕ/0.36 мл : картриджи 1 шт. в компл. с иглами (6 шт.) рег. №: ЛС-001648 |
N.V. ORGANON (Нидерланды) |
||
|
Пурегон® |
Р-р д/п/к введения 600 МЕ/0.72 мл: картриджи 1 шт. в компл. с иглами (6 шт.) рег. №: ЛС-001648 |
N.V. ORGANON (Нидерланды) |
||
|
Пурегон® |
Р-р д/п/к введения 900 МЕ/1.08 мл: картриджи 1 шт. в компл. с иглами (9 шт.) рег. №: ЛСР-000292/10 |
N.V. ORGANON (Нидерланды) Произведено: VETTER PHARMA-FERTIGUNG (Германия) |
||
|
Рековелль® |
Р-р д/п/к введения 33.3 мкг/1 мл: 0.36 мл картридж со шприц-ручкой, в компл. с иглами (3 шт.) рег. №: ЛП-(000311)-(РГ-RU ) Предыдущий рег. №: ЛП-006142 Р-р д/п/к введения 33.3 мкг/1 мл: 1.08 мл картридж со шприц-ручкой, в компл. с иглами (9 шт.) рег. №: ЛП-(000311)-(РГ-RU ) Предыдущий рег. №: ЛП-006142 Р-р д/п/к введения 33.3 мкг/1 мл: 2.16 мл картридж со шприц-ручкой, в компл. с иглами (15 шт.) рег. №: ЛП-(000311)-(РГ-RU ) Предыдущий рег. №: ЛП-006142 |
FERRING PHARMACEUTICALS A/C (Дания) Произведено и расфасовано: VETTER PHARMA-FERTIGUNG (Германия) Упаковано: FERRING CONTROLLED THERAPEUTICS (Великобритания) Выпускающий контроль качества: FERRING (Германия) |
||
|
Фоллитроп® |
Лиофилизат д/пригот. р-ра д/в/м и п/к введения 75 МЕ: фл. 1 шт. в компл. с растворителем рег. №: ЛСР-008834/09 |
LG CHEM (Республика Корея) |
||
|
Элонва® |
Р-р д/п/к введения 100 мкг/0.5 мл: шприц 1 мл с иглой рег. №: ЛП-(000342)-(РГ-RU ) Предыдущий рег. №: ЛП-001212 Р-р д/п/к введения 150 мкг/0.5 мл: шприц 1 мл с иглой рег. №: ЛП-(000342)-(РГ-RU ) Предыдущий рег. №: ЛП-001212 |
N.V. ORGANON (Нидерланды) Произведено и расфасовано: VETTER PHARMA-FERTIGUNG (Германия) Выпускающий контроль качества: N.V. ORGANON (Нидерланды) |
Нозологические аналоги: 10
| Название | Форма выпуска | Владелец рег. уд. | ||
|
Гонадотропин Менопаузный |
Лиофилизат д/пригот. р-ра д/в/м введения 75 МЕ+75 МЕ: амп. 5 или 10 шт. в компл. с растворителем или без рег. №: ЛП-001820 |
ЭЛЛАРА (Россия) |
||
|
Гонадотропин хорионический |
|
Лиофилизат д/пригот. р-ра д/в/м введения 1000 МЕ: фл. 5 шт. в компл. с растворителем рег. №: ЛС-002469 |
МОСКОВСКИЙ ЭНДОКРИННЫЙ ЗАВОД (Россия) |
|
|
Гонадотропин хорионический |
|
Лиофилизат д/пригот. р-ра д/в/м введения 1500 МЕ: фл. 5 шт. в компл. с растворителем рег. №: ЛС-002469 |
МОСКОВСКИЙ ЭНДОКРИННЫЙ ЗАВОД (Россия) |
|
|
Гонадотропин хорионический |
Лиофилизат д/пригот. р-ра д/в/м введения 500 МЕ: фл. 5 шт. рег. №: ЛП-006995 Лиофилизат д/пригот. р-ра д/в/м введения 1000 МЕ: фл. 5 шт. рег. №: ЛП-006995 Лиофилизат д/пригот. р-ра д/в/м введения 1500 МЕ: фл. 5 шт. рег. №: ЛП-006995 Лиофилизат д/пригот. р-ра д/в/м введения 5000 МЕ: фл. 5 шт. рег. №: ЛП-006995 |
ЭНДОКРИННЫЕ ТЕХНОЛОГИИ (Россия) Произведено: Фирма ФЕРМЕНТ (Россия) |
||
|
Гонадотропин хорионический |
|
Лиофилизат д/пригот. р-ра д/в/м введения 500 МЕ: фл. 5 шт. в компл. с растворителем рег. №: ЛС-002469 |
МОСКОВСКИЙ ЭНДОКРИННЫЙ ЗАВОД (Россия) |
|
|
Гонадотропин хорионический |
|
Лиофилизат д/пригот. р-ра д/в/м введения 5000 МЕ: фл. 5 шт. в компл. с растворителем рег. №: ЛС-002615 |
МОСКОВСКИЙ ЭНДОКРИННЫЙ ЗАВОД (Россия) |
|
|
Клостилбегит® |
Таб. 50 мг: 10 шт. рег. №: ЛП-(000161)-(РГ-RU ) Предыдущий рег. №: П N014432/01 |
EGIS Pharmaceuticals (Венгрия) |
||
|
Хорагон® |
Порошок д/инъекц. 1500 МЕ: амп. 3 шт. в компл. с растворителем рег. №: П N012469/01-2000 Порошок д/инъекц. 5000 МЕ: амп. 3 шт. в компл. с растворителем рег. №: П N012469/01-2000 |
FERRING (Германия) |
||
|
ХуМоГ |
Лиофилизат д/пригот. р-ра д/в/м введения 150 МЕ+150 МЕ: фл. 1 шт. в компл. с растворителем рег. №: ЛС-001964 |
BHARAT SERUMS & VACCINES (Индия) |
||
|
ХуМоГ |
Лиофилизат д/пригот. р-ра д/в/м введения 75 МЕ+75 МЕ: фл. 1 шт. в компл. с растворителем рег. №: ЛС-001964 |
BHARAT SERUMS & VACCINES (Индия) |
Овитрель аналоги и цены
Всего найдено 26 аналогов Овитрель
Все аналоги Овитрель подобраны по международной системе классификации лекарственных средств АТС (анатомо-терапевтическо-химическая классификация).
Действующие вещества: Сhoriogonadotropin alfa
Укажите ваш точный адрес, чтобы купить Овитрель в ближайшей аптеке
Средняя цена
3837
2173 – 5500 руб
Аналоги по показанию и способу применения
Аналоги совпадают по коду ATC 4-го уровня. Лекарственные препараты, имеющие различный состав, но могут быть схожи по показанию и способу применения.
-
Прегнил
4 предложения по цене от 1,222.00 до 39,900.00 руб
-
Хорагон
1 предложение по цене от 930.00 до 930.00 руб
-
Хориомон
3 предложения по цене от 1,674.00 до 7,725.00 руб
-
Гонадотропин
53 предложения по цене от 428.00 до 39,900.00 руб
-
Меногон
3 предложения по цене от 10,500.00 до 24,000.00 руб
-
Менопур 75
26 предложений по цене от 1,000.00 до 44,883.00 руб
-
Мерионал
6 предложений по цене от 1,575.00 до 51,312.00 руб
-
Хумог
10 предложений по цене от 989.00 до 2,834.00 руб
-
Менопур
35 предложений по цене от 1,000.00 до 65,396.00 руб
-
Гонал-Ф
46 предложений по цене от 1,179.00 до 18,838.00 руб
-
Пурегон
30 предложений по цене от 890.00 до 57,700.00 руб
-
Луверис
8 предложений по цене от 1,560.00 до 9,250.00 руб
-
Элонва
15 предложений по цене от 13,000.00 до 118,600.00 руб
-
Перговерис
16 предложений по цене от 2,659.00 до 16,266.00 руб
Аналоги по коду ATC 3-го уровня
Аналоги совпадают по коду ATC 3-го уровня. Лекарственные препараты, имеющие различный состав, но могут быть схожи по показания и способу применения.
-
Клостилбегит
33 предложения по цене от 517.00 до 9,800.00 руб
Все аналоги Овитрель представлены исключительно в ознакомительных целях и не являются поводом для самостоятельного принятия решения о замене препарата. Перед употреблением препарата проконсультируйтесь с врачом и ознакомьтесь с инструкцией по применению.
САМОЛЕЧЕНИЕ МОЖЕТ НАНЕСТИ ВРЕД ВАШЕМУ ЗДОРОВЬЮ
Овитрель инструкция
Инструкция по применению. Противопоказания и форма выпуска.
ИНСТРУКЦИЯ
по медицинскому применению препарата
ОВИТРЕЛЬ® (OVITRELLE®) Регистрационный номер: П № 015668/01
Торговое название препарата: Овитрель®
Международное непатентованное название:
Хориогонадотропин альфаЛекарственная форма:
лиофилизат для приготовления раствора для подкожного введенияСостав:
1 флакон содержит:
Действующее вещество: хориогонадотропин альфа 250 мкг (6500 ME )
Вспомогательные вещества: сахароза, фосфорная кислота, натрия гидроксид. 1 флакон или ампула с растворителем содержит 1 мл воды для инъекций.
Описание:
лиофилизированный порошок или пористая масса (лиофилизат) белого или почти белого цвета
Фармакотерапевтическая группа:
Лютеинизирующее средство.
Код ATX: G03GA08.
Фармакологические свойства
Фармакодинамика:
Содержит хориогонадотропин альфа, который производится при помощи рекомбинантной ДНК технологии. Он имеет ту же аминокислотную последовательность, что и человеческий хорионический гонадотропин, содержащийся в моче. Связывает трансмембранные рецепторы ЛГ на поверхности клеток теки и гранулезы яичника. Вызывает инициирование ооцитарного мейоза, разрыв фолликулов (овуляцию), формирование желтого тела, продукцию прогестерона и эстрадиола желтым телом.
Фармакокинетика:
При подкожном введении хориогонадотропин альфа абсолютная биодоступность составляет приблизительно 40%, период полувыведения — около 30 часов.
Показания к применению:
- В протоколе индукции множественного созревания фолликулов (суперовуляция) для вспомогательных репродуктивных технологий (ВРТ), в том числе для экстракорпорального оплодотворения (ЭКО), с целью индукции финального созревания фолликулов и лютеинизации после стимуляции препаратами гонадотропинов.
- При ановуляторном или олигоовуляторном бесплодии для индукции овуляции и лютеинизации в конце стимуляции роста фолликулов.Противопоказания:
- Опухоли в области гипоталамуса и гипофиза;
- Гиперчувствительность к активному компоненту и к любому из вспомогательных компонентов, входящих в состав препарата;
- Объемные новообразования яичника или кисты, не связанные с поликистозом яичника.
- Вагинальные кровотечения неясного генеза.
- Рак яичника, матки или молочной железы.
- Внематочная беременность в течение 3 предыдущих месяцев.
- Тромбоэмболия
- Первичная овариальная недостаточность.
- Врожденные пороки развития половых органов, несовместимые с беременностью.
- Фибромиома матки, несовместимая с беременностью
- Постменопауза.С осторожностью
следует назначать Овитрель® пациенткам, страдающим серьезными системными заболеваниями, в тех случаях, когда беременность может привести к их обострению.Способ применения и дозы:
Вводится подкожно.
Каждый флакон предназначен только для однократного использования.
В протоколе индукции множественного созревания фолликулов (суперовуляция) для вспомогательных репродуктивных технологий (ВРТ), в том числе для экстракорпорального оплодотворения (ЭКО), с целью индукции финального созревания фолликулов и лютеинизации после стимуляции препаратами гонадотропинов:
Овитрель® в дозе 250 мкг (содержимое 1 флакона) вводится однократно через 24-48 часов после последнего введения препарата фолликулостимулирующего гормона или лютеинизирующего гормона после достижения оптимального уровня развития фолликула.
При ановуляторном или олигоовуляторном бесплодии для индукции овуляции и лютеинизации в конце стимуляции роста фолликулов:
Овитрель® в дозе 250 мкг (содержимое 1 флакона ) вводится однократно через 24-48 часов после последнего введения препарата фолликулостимулирующего гормона или лютеинизирующего гормона после достижения оптимального уровня развития фолликула. Рекомендуется половой контакт в день введения препарата и на следующий день.Если пациентка вводит Овитрель® самостоятельно, ей следует внимательно прочитать и строго следовать нижеприведенной инструкции по введению препарата:1.Вымойте руки. Важно, чтобы Ваши руки и предметы, которые Вы используете, были чистыми.
2.Подготовьте чистую поверхность и разложите на ней все, что нужно для инъекции: - один флакон препарата Овитрель®,
- одна ампула или один флакон с растворителем,
- два тампона, смоченных спиртом
- один шприц,
- одна игла большего диаметра для набора растворителя,
- тонкая игла для подкожного введения,
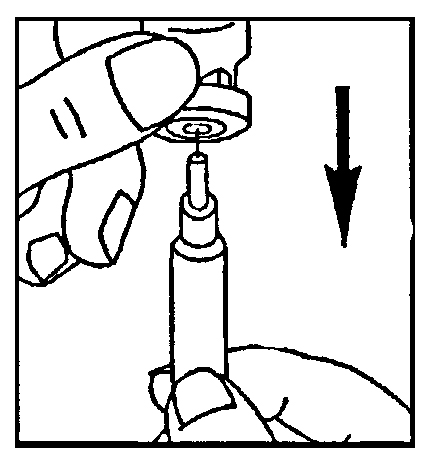
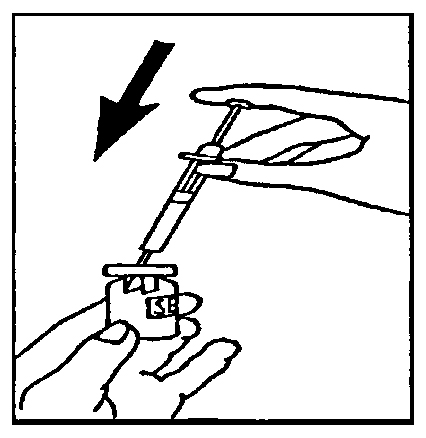
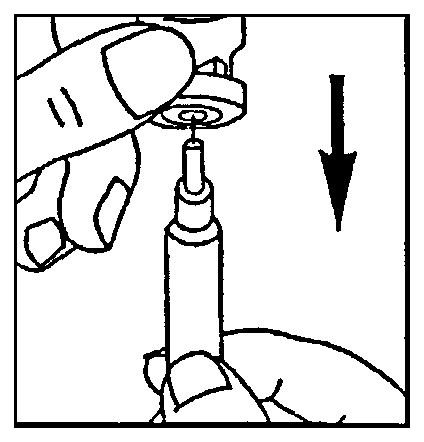
- контейнер для острых предметов для безопасной утилизации стеклянных деталей и игл. 3.Вскрытие ампулы с растворителем: На верхнем конце ампулы с растворителем Вы должны увидеть маленькую цветную точку. Чуть ниже этого места стекло ампулы обработано специальным образом, для того чтобы было легче её вскрыть. Осторожно постучите по верхнему концу ампулы, так чтобы жидкость, находящаяся в нем, переместилась в нижний отдел. Теперь сильно надавите на стебель и вскройте ампулу в противоположном от цветной точки направлении. Осторожно поставьте вскрытую ампулу в вертикальном положении на рабочую поверхность. 4.Набор в шприц растворителя из ампулы: Наденьте иглу для набора растворителя на шприц. Держа шприц в одной руке, возьмите другой рукой вскрытую ампулу, поместите иглу внутрь ампулы и вберите в шприц весь растворитель. Осторожно положите шприц на рабочую поверхность, стараясь не задеть иглу. 4′. Набор в шприц растворителя из флакона: Снимите защитную крышку с флакона для растворителя. Наденьте на шприц иглу для набора растворителя (большую по диаметру). Втяните в шприц немного воздуха, поднимая поршень примерно до деления 1 мл. Затем вставьте иглу во флакон, нажмите на поршень, удаляя воздух. Переверните флакон вверх дном и медленно наберите растворитель в шприц.
Осторожно положите шприц на рабочую поверхность, стараясь не задеть иглу. 5.Приготовление раствора для инъекции: Снимите защитную крышку с флакона, где содержится препарат Овитрель®, с помощью шприца медленно введите растворитель во флакон. Осторожно перемешайте содержимое круговыми движениями. Не встряхивайте. Препарат сразу же должен раствориться и дать прозрачный раствор. Препарат должен использоваться сразу после растворения. Не следует вводить раствор, если он непрозрачен или содержит твердые частицы. Переверните флакон вверх дном, снова наберите раствор в шприц. 6. Введение инъекции:Смените иглу с большим диаметром на тонкую. Удалите пузырьки воздуха: если Вы обнаружите в шприце пузырьки воздуха, направьте шприц иглой вверх и осторожно постучите по стенкам шприца, так чтобы воздух собрался в верхней части. Осторожно нажмите на поршень, удаляя пузырьки воздуха. Сразу же введите инъекцию: Ваш лечащий врач или медсестра должно быть уже посоветовали Вам, куда делать инъекцию (например, в живот, переднюю часть бедра). Протрите выбранный участок тампоном со спиртом. Сильно стяните кожу пальцами и направляйте иглу под углом 45° — 90° коротким энергичным движением. Проводите подкожную инъекцию, как Вас учили. Не делайте инъекцию непосредственно в вену. Вводите раствор, осторожно нажимая на поршень. Используйте столько времени, сколько Вам нужно для того, чтобы ввести весь объем раствора. Сразу же после этого выньте иглу и протрите кожу в месте инъекции тампоном со спиртом, используя при этом круговые движения.
7.Утилизация использованных принадлежностей:
Сразу после инъекции поместите использованные иглы и пустые стеклянные емкости в контейнер для хранения острых предметов. Весь неиспользованный объем раствора должен быть уничтожен.Побочное действие:
Местные реакции: боль в месте введения инъекции
Общие: головная боль, чувство усталости.
Со стороны ЦНС: редко — депрессия, раздражительность, чувство беспокойства.
Со стороны пищеварительной системы: рвота/тошнота, боль в животе, редко диарея.
Со стороны репродуктивной системы: синдром гиперстимуляции яичников, редко синдром гиперстимуляции яичника тяжелой степени, болезненность молочных желез,Передозировка:
Данные о передозировке препаратом отсутствуют. Тем не менее при передозировке в процессе стимуляции яичников возможно развитие синдрома гиперстимуляции яичников (СГЯ) (см. «Особые указания»). Клинически он характеризуется образованием крупных кист яичника с риском их разрыва (перфорации), симптомами асцита и циркуляторными расстройствами.
В случае высокого риска СГЯ рекомендуется отменить введение человеческого хориогонадотропина. Пациенткам в течение не менее 4х дней рекомендуется воздержаться от полового контакта или использовать барьерные методы контрацепции.Взаимодействие с другими лекарственными средствами:
Данные о взаимодействии с другими лекарственными средствами отсутствуют. Тем не менее пациентке необходимо информировать врача о всех лекарственных средствах (в том числе безрецептурных), которые она принимает в настоящее время или недавно принимала.Особые указания:
Перед началом лечения необходимо установить причины бесплодия у пациентки и ее партнера и оценить предполагаемые факторы риска при наступлении беременности. Особенно следует учитывать симптомы гипотиреоза, надпочечниковой недостаточности, гиперпролактенемии, наличие опухолей в гипоталамо-гипофизарной области, применяемые специфические методы терапии.
В процессе стимуляции яичников пациентки подвергаются риску развития синдрома гиперстимуляции яичников (СГЯ) из-за одновременного созревания большого числа фолликулов. СГЯ тяжелой степени может стать серьезным осложнением стимуляции. С целью снижения риска синдрома гиперстимуляции в протоколе стимуляции роста фолликулов рекомендуется тщательное наблюдение за ответной реакцией яичников при помощи ультразвукового исследования и определение уровня эстрадиола в крови перед началом курса лечения и во время него.
По сравнению с естественным оплодотворением при проведении стимуляции возрастает риск многоплодной беременности. В большинстве случаев рождаются двойни. При применении методов вспомогательной репродукции количество родившихся младенцев соответствует числу эмбрионов, перенесенных в полость матки.
Статистика выкидышей после лечения ановуляторного бесплодия, в том числе с помощью вспомогательных репродуктивных технологий, превышает показатели в среднем по популяции, но сравнима с другими видами бесплодия. Введение Овитреля® может влиять на иммунологическую картину уровня человеческого хорионического гонадотропина (чХГ) в сыворотке крови и в моче в течение 10 дней и привести к появлению ложной положительной реакции при проведении теста на беременность.
Во время проведения терапии препаратом Овитрель® возможна незначительная стимуляция функции щитовидной железы.Форма выпуска.
Лиофилизат для приготовления раствора для подкожного введения во флаконе, содержащем 250 мкг (6500 ME) хориогонадотропина альфа, в комплекте с растворителем -водой для инъекций 1 мл во флаконах или ампулах. По 1, 2 или 10 флаконов с препаратом и с таким же количеством флаконов или ампул с растворителем в пластиковом контейнере и затем в картонной коробке вместе с Инструкцией по применению.Срок годности.
Препарат: 2 года
Растворитель: 3 года.
Не использовать препарат после истечения срока годности, указанного на упаковке.Условия хранения.
В оригинальной упаковке при температуре не выше 25°С.
Хранить в недоступном для детей месте. Список Б.Условия отпуска из аптек.
По рецепту.
Регистрационный номер
ЛС-002622
Торговое наименование
Овитрель®
Международное непатентованное наименование
Хориогонадотропин альфа
Лекарственная форма
раствор для подкожного введения
Состав
Один заполненный шприц с 0,5 мл раствора содержит: активное вещество — хориогонадотропин альфа 250 мкг (6500 МЕ) и вспомогательные вещества: маннитол 27,3 мг, метионин 0,1 мг, полоксамер 188 0,05 мг, фосфорная кислота 0,49 мг, натрия гидроксид q.s. для корректировки pH, вода для инъекций до 0,5 г.
Описание
Прозрачный или слегка опалесцирующий бесцветный или светло-жёлтый раствор.
Фармакотерапевтическая группа
Лютеинизирующее средство
Код АТХ
G03GA08
Фармакологические свойства
Фармакодинамика
Овитрель® содержит хориогонадотропин альфа, который производится при помощи рекомбинантной ДНК технологии. Он имеет ту же аминокислотную последовательность, что и естественный человеческий хорионический гонадотропин. Хорионический гонадотропин связывает трансмембранные рецепторы лютеинизирующего гормона (ЛГ) на поверхности клеток теки и гранулезы яичника. Вызывает инициирование ооцитарного мейоза, разрыв фолликулов(овуляцию), формирование желтого тела, продукцию прогестерона и эстрадиола жёлтым телом.
Фармакокинетика
Всасывание и распределение
После внутривенного введения хориогонадотропин альфа распределяется во внеклеточную жидкость с периодом полураспределения около 4,5 часов. Стационарный объём распределения и общий клиренс составляют 6 л и 0,2 л/час соответственно.
При подкожном введении хориогонадотропина альфа абсолютная биодоступность составляет приблизительно 40 %, конечный период полувыведения — около 30 часов.
Выведение и метаболизм
Метаболизм и выведение хориогонадотропина альфа аналогичны эндогенному хорионическому гонадотропину.
Показания
В протоколе индукции множественного созревания фолликулов для вспомогательных репродуктивных технологий (ВРТ), в том числе для экстракорпорального оплодотворения (ЭКО), с целью индукции финального созревания фолликулов и лютеинизации после стимуляции препаратами гонадотропинов.
При ановуляторном или олигоовуляторном бесплодии для индукции овуляции и лютеинизации в конце стимуляции роста фолликулов.
Противопоказания
- Гиперчувствительность к активному компоненту и к любому из вспомогательных компонентов, входящих в состав препарата;
- Опухоли гипотоламуса и гипофиза;
- Объёмные новообразования яичника или кисты, несвязанные с поликистозом яичников.
- Вагинальные кровотечения неясной этиологии.
- Рак яичника, матки или молочной железы.
- Внематочная беременность в течение 3 предыдущих месяцев.
- Тромбоэмболия.
- Первичная овариальная недостаточность.
- Врожденные пороки развития половых органов, несовместимые с беременностью.
- Фибромиома матки, несовместимая с беременностью.
- Постменопауза.
С осторожностью
С осторожностью следует назначать Овитрель® пациенткам, страдающим тяжелыми системными заболеваниями, в тех случаях, когда беременность может привести к их обострению.
Применение при беременности и в период грудного вскармливания
В период беременности и грудного вскармливания препарат Овитрель® не назначается.
Данные об экскреции хориогонадотропина альфа в грудное молоко отсутствуют.
Способ применения и дозы
Овитрель® вводится подкожно. Каждый шприц или шприц-ручка предназначены только для однократного использования.
Лечение следует проводить только под руководством врача, имеющего опыт в лечении бесплодия.
В протоколе индукции множественного созревания фолликулов для ВРТ, в том числе для ЭКО, с целью индукции финального созревания фолликулов и лютеинизации после стимуляции препаратами гонадотропинов:
Овитрель® в дозе 250 мкг (содержимое 1 шприца или 1 шприц-ручки) вводится однократно через 24-48 часов после последнего введения препарата фолликулостимулирующего гормона или ЛГ и достижения оптимального уровня развития фолликула.
При ановуляторном или олигоовуляторном бесплодии для индукции овуляции и лютеинизаиии в конце стимуляции роста фолликулов:
Овитрель® в дозе 250 мкг (содержимое 1 шприца или 1 шприц-ручки) вводится однократно через 24-48 часов после достижения оптимального уровня развития фолликула. Рекомендуется половой контакт в день введения препарата Овитрель® и на следующий день.
Рекомендации по самостоятельному введению препарата Овитрель®.
Самостоятельное введение возможно только пациентами, прошедшими соответствующее обучение и имеющими возможность обратиться за советом к врачу- специалисту.
При самостоятельном введении пациентке следует внимательно прочитать и строго следовать нижеприведенной инструкции по введению препарата:
Перед введением:
1. Вымойте руки. Важно чтобы Ваши руки и предметы, которые Вы используете, были чистыми.
2. Подготовьте чистую поверхность и разложите на ней все, что нужно для инъекции:
1. два тампона, смоченных спиртом (к упаковке не прилагаются);
2. один шприц с препаратом или одна шприц-ручка и игла для инъекции.
Для шприца:
1. Введение инъекции: Сразу же проведите инъекцию:
Выберите место для инъекции в соответствии с рекомендациями Вашего лечащего врача или медсестры (живот, передняя часть бедра). Протрите выбранный участок тампоном со спиртом. Сильно стяните кожу пальцами и коротким энергичным движением направьте иглу под углом 45° — 90° в кожную складку. Проводите подкожную инъекцию, как Вас учили. Избегайте попадания препарата непосредственно в вену. Вводите раствор, осторожно нажимая на поршень. Используйте столько времени, сколько Вам нужно для того, чтобы ввести весь объём раствора. Сразу же после инъекции выньте иглу и протрите круговыми движениями кожу в месте инъекции тампоном со спиртом.
2. Утилизация использованных принадлежностей: Сразу после инъекции поместите использованный шприц в контейнер для хранения острых предметов. Весь неиспользованный раствор должен быть уничтожен.
Для шприц-ручки:
Используйте шприц-ручку только для себя, не позволяйте пользоваться ей никому другому.
Вводите препарат Овитрель® так, как показывал врач или медсестра.
На иллюстрации ниже показан внешний вид шприц-ручки с указанием её отдельных элементов:
1. кнопка для установки дозы
2. табло указателя дозы
3. поршень
4. отсек с резервуаром
5. наконечник с резьбой
6. колпачок шприц-ручки
7. съемная игла
8. внутренний колпачок иглы
9. наружний колпачок иглы
10. защитная наклейка
1. Подготовка шприц-ручки к проведению инъекции
1.1 Снимите колпачок со шприц-ручки
1.2 Наденьте иглу
— Возьмите иглу — используйте только одноразовые иглы, поставляемые вместе с предварительно заполненной шприц-ручкой Овитрель®.
— Убедитесь в том, что защитная наклейка на наружном колпачке иглы не повреждена и не ослаблена.
ВНИМАНИЕ:
Если защитная наклейка повреждена или ослаблена, не используйте эту иглу. Возьмите другую. Неиспользованную иглу выбросьте вместе с надетым на неё наружным колпачком. Инструкции по утилизации ненужных игл получите у своего врача или медсестры.
— Снимите защитную наклейку.
— Прочно удерживайте наружный колпачок иглы.
— Вставьте наконечник шприц-ручки с резьбой в наружный колпачок иглы и навинчивайте наружный колпачок до тех пор, пока он прочно не зафиксируется.
1.3 Удалите крупные воздушные пузырьки:
— Внимательно осмотрите отсек с резервуаром.
— Если Вы не обнаружили крупного воздушного пузырька, значит, шприц-ручка готова к использованию. В таком случае перейдите к пункту 2 «Установка дозы на 250».
Воздушный пузырек считается крупным, если полностью заполняет наконечник отсека с картриджем при удерживании шприц-ручки иглой вверх (см. рисунок). Если Вы видите внутри отсека с резервуаром большой воздушный пузырек, его необходимо удалить. В шприц-ручке может оставаться несколько мелких воздушных пузырьков, прилипших к внутренней стенке отсека с резервуаром. Не обращайте внимания на мелкие пузырьки, их удалять не обязательно.
Чтобы удалить крупный воздушный пузырек
1. Осторожно поворачивайте кнопку для установки дозы по часовой стрелке до тех пор, пока на табло указателя дозы не появится точка (-). Если Вы проскочили это положение, просто поверните кнопку обратно на точку (-).
2. Затем снимите внутренний колпачок иглы и удерживайте шприц-ручку иглой вверх.
3. Слегка постучите по отсеку с резервуаром пальцем так, чтобы все воздушные пузырьки всплыли наверх к игле. Продолжая удерживать шприц-ручку иглой вверх и плавно нажимая на кнопку для установки дозы продвиньте поршень настолько, чтобы выпустить воздушный пузырек.
4. На кончике иглы должна появиться капля раствора; это означает, что Ваша шприц-ручка готова к проведению инъекции.
5. Если раствор не проступил на кончике иглы, повторите манипуляции, описанные выше, ещё раз (максимальное количество попыток — 2), начиная с шага 1 (пункт «Чтобы удалить большой воздушный пузырек»).
2. Установка дозы на 250
— Аккуратно поворачивайте кнопку для установки дозы по часовой стрелке до тех пор, пока на табло указателя дозы вместо прямой линии не появится число «250».
— Проворачивая кнопку для установки дозы не следует на неё давить или, наоборот, оттягивать.
— На табло указателя дозы должно появиться число «250», как показано на рисунке ниже.
3. Введение дозы
1. Выберите место для инъекции, указанное врачом или медсестрой.
2. Продезинфицируйте место инъекции, протерев его тампоном, смоченным в спирте.
3. Убедитесь ещё раз, что на табло выставлено число «250». Если на табло числа нет, необходимо установить правильную дозу (см. раздел 2 «Установка дозы на 250»).
4. Аккуратно снимите внутренний колпачок и выбросьте его (если это ещё не было сделано при выполнении инструкций из пункта 1.3 «Удалите крупные воздушные пузырьки»).
Введите дозу в соответствии с указаниями Вашего врача или медсестры
— Сначала медленно введите иглу под кожу, после чего надавите на кнопку для установки дозы до упора, как показано на рисунке ниже.
— Число с дозировкой, указанное на табло указателя дозы, вернется обратно в положение «О». Это означает, что была введена вся доза.
— Оставьте иглу под кожей при нажатой кнопке для установки дозы минимум на 10 секунд.
— По прошествии 10 секунд выньте иглу, удерживая кнопку для установки дозы в нажатом положении.
4. После инъекции
4.1 Убедитесь, что на табло указателя дозы появилось число «0»
— Это означает, что доза была введена полностью. Не предпринимайте попыток провести инъекцию второй раз.
— Если на табло число «0» не появилось, свяжитесь с Вашим врачом или медсестрой.
4.2 Снятие иглы
— Крепко удерживайте шприц-ручку за отсек с резервуаром.
— Осторожно наденьте наружный колпачок на иглу.
— Затем сожмите наружный колпачок и отвинтите иглу.
— Будь осторожны, не уколитесь об иглу.
— Теперь наденьте колпачок шприц-ручки обратно на ручку.
4.3 Утилизация
— Никогда не используйте иглу или шприц-ручку повторно.
— Выполнив инъекцию утилизируйте использованную иглу и шприц-ручку, соблюдая меры предосторожности.
— Лучше всего поместить её обратно в упаковку от производителя. Лекарственные препараты не следует выбрасывать в канализацию или утилизировать вместе с бытовыми отходами. Когда шприц-ручка закончится, получите у своего врача или медсестры инструкции по её утилизации.
Если Вы ввели слишком большую дозу препарата, могут появиться симптомы синдрома гиперстимуляции яичников (СГЯ), которые описаны в разделе «Особые указания» или «Побочные эффекты». Если эти симптомы появились, проконсультируйтесь с врачом.
Если Вы забыли ввести препарат, проконсультируйтесь с врачом как можно скорее.
Побочное действие
При применении лекарственного препарата Овитрель® возможно развитие побочных эффектов. В процессе сравнительных клинических исследованиях различных доз препарата Овитрель® была показана дозозависимость появления таких побочных эффектов как СГЯ, тошнота и рвота. СГЯ наблюдался приблизительно у 4 % пациентов, получавших Овитрель® Тяжёлая форма СГЯ отмечалась менее, чем у 0,5 % пациентов.
В зависимости от частоты появления побочные эффекты расцениваются как очень частые (≥1/10), частые (≥1/100 и <1/10), нечастые (≥1/1000 и <1/100), редкие (≥1/10000 и <1/1000), очень редкие (<1/10000, включая единичные сообщения). Частота побочных эффектов в каждой группе указана в порядке убывания. В зависимости от частоты встречаемости побочные явления могут быть разделены на группы:
Иммунная система: очень редко — от лёгкой до тяжёлой реакции гиперчувствительности, включая анафилактические реакции и шок.
ЦНС: нечасто — депрессия, раздражительность, возбуждение.
Нервная система: часто — головная боль.
Сосудистая система: очень редко — тромбоэмболия, обычно связанная с тяжёлой формой СГЯ.
Пищеварительная система: часто тошнота, рвота, боль в животе, нечасто -диарея.
Кожа и подкожная клетчатка: очень редко -лёгкие обратимые кожные реакции в виде сыпи.
Репродуктивная система и молочные железы: часто — СГЯ лёгкой или средней степени тяжести, нечасто — тяжёлая форма СГЯ, болезненность молочных желёз.
Общие и местные реакции: часто — утомляемость, реакции в месте инъекции.
Передозировка
Данные о передозировке препаратом отсутствуют. Тем не менее, при передозировке процессе стимуляции яичников возможно развитие СГЯ (см. «Особые указания»).
Клинически он характеризуется образованием крупных кист яичника с риском их разрыва (перфорации), симптомами асцита и циркуляторными расстройствами.
Взаимодействие с другими лекарственными средствами
Данные о взаимодействии с другими лекарственными средствами отсутствуют. Тем не менее, пациентке необходимо информировать врача о всех лекарственных средствах (в том числе безрецептурных), которые она принимает в настоящее время или недавно принимала.
Особые указания
Перед началом лечения необходимо установить причины бесплодия у пациентки и её партнера и оценить предполагаемые факторы риска при наступлении беременности. Особенно следует учитывать симптомы гипотиреоза, адренокортикальной недостаточности, гиперпролактинемии, наличие опухолей
гипофиза или гипоталамуса, и применяемые специфические методы терапии.
Синдром гиперстимуляции яичников (СГЯ)
В процессе стимуляции яичников повышается риск возникновения СГЯ из-за одновременного созревания большого числа фолликулов.
СГЯ может стать серьёзным осложнением, характеризующимся образованием крупных кист яичника с риском их разрыва, увеличением веса, одышкой, олигурией или наличием асцита в клинической картине циркуляторных нарушений. СГЯ тяжёлой степени в редких случаях может сопровождаться гемоперитонеумом, острым легочным дистресс-синдромом, перекрутом яичника и тромбоэмболией.
С целью снижения риска СГЯ в протоколе стимуляции роста фолликулов рекомендуется тщательное наблюдение за ответной реакцией яичников при помощи ультразвукового исследования и определение уровня эстрадиола в крови перед началом курса лечения и во время него.
При ановуляции риск развития СГЯ повышается при концентрации эстрадиола в плазме крови > 1500 пг/мл (5400 пмоль/л) и наличие более 3 фолликулов диаметром 14 мм или более. При ВРТ риск развития СГЯ повышается при концентрации эстрадиола > 3000 пг/мл (11000 пмоль/л) или наличии 18 или более фолликулов диаметром 11 мм и более.
СГЯ, вызванный чрезмерным ответом яичника, можно избежать, если отменить введение чХГ. Поэтому, если уровень эстрадиола в сыворотке крови > 5500 пг/мл (20 ООО пмоль/л) и/или когда в наличии 30 или более фолликулов, следует воздержаться от применения чХГ. Пациенткам рекомендуют воздержаться от коитуса или использовать барьерные методы контрацепции не менее 4-х дней.
Многоплодная беременность
По сравнению с естественным оплодотворением при проведении стимуляции возрастает риск многоплодной беременности. В большинстве случаев рождаются двойни. При применении методов вспомогательной репродукции количество родившихся младенцев соответствует числу эмбрионов, перенесенных в полость матки.
Использование рекомендованных доз препарата Овитрель®, схемы лечения и тщательный мониториг в процессе терапии минимизируют риск возникновения СГЯ и многоплодной беременности.
Невынашивание беременности
Статистика выкидышей после лечения ановуляторного бесплодия, в том числе с помощью ВРТ, превышает показатели в среднем по популяции, но сравнима с другими видами бесплодия.
Внематочная беременность
У пациенток с заболеваниями маточных труб в анамнезе повышен риск внематочной беременности независимо от того, получена ли беременность обычным путём или в процессе лечения бесплодия. Вероятность внематочной беременности после применения вспомогательных репродуктивных технологий выше, чем в общей популяции.
Врожденные аномалии развития
Частота врожденных аномалий после применения программ ВРТ может быть несколько выше, чем при естественной беременности и родах. Тем не менее, неизвестно, связано ли это с особенностью родителей (например, возраст матери, качество спермы) и многоплодной беременностью или же непосредственно с процедурами ВРТ.
Тромбоэмболические осложнения
У пациенток с недавно перенесенными или текущими тромбоэмболическими заболеваниями, а также при вероятном риске их возникновения при наличии заболевания в анамнезе или у родственников, применение гонадотропинов может увеличить этот риск или осложнить течение данных заболеваний. Для пациенток данной группы польза от терапии должна быть соотнесена с возможным риском. Следует отметить, что беременность сама по себе, как и СГЯ, несет повышенный риск тромбоэмболических нарушений, таких как эмболия лёгких, ишемический инсульт или инфаркт миокарда.
Влияние на лабораторные показатели
Ведение препарата Овитрель® может влиять на иммунологическую картину уровня чХГ в сыворотке крови и в моче в течение 10 дней и привести к появлению ложноположительной реакции при проведении теста на беременность.
Прочая информация
Во время проведения терапии препаратом Овитрель® возможна незначительная стимуляция функции щитовидной железы.
Если проявления побочных реакций усиливаются или Вы отмечаете побочные эффекты, не упомянутые в инструкции, пожалуйста, сообщите об этом Вашему лечащему врачу.
В течение срока годности препарат (только для шприцев) может храниться вне холодильника при температуре не выше 25 °C 30 дней. Если по истечении 30 дней такого хранения препарат не был использован, он должен быть уничтожен.
Влияние на способность управлять транспортными средствами, механизмами
Практически не влияет на управление транспортным средством или каким-либо другим механизмом.
Форма выпуска
Раствор для подкожного введения, 250 мкг/0,5 мл.
0,5 мл раствора, содержащего 250 мкг (6500 МЕ) хориогонадотропина альфа в бесцветном стеклянном шприце с иглой для инъекций, закрытой защитным колпачком с резиновой прокладкой.
0,5 мл раствора, содержащего 250 мкг (6500 МЕ) хориогонадотропина альфа в шприц-ручке.
1 шприц упакован в пластиковый контейнер, помещённый в картонную пачку с Инструкцией по применению.
1 шприц-ручка и 1 игла для инъекции упакованы в пластиковый контейнер, помещённый в картонную пачку с инструкцией по применению.
Хранение
При температуре 2 — 8 °C в оригинальной упаковке. Не замораживать. Хранить в недоступном для детей месте.
Срок годности
2 года. Не использовать препарат после истечения срока годности.
Условия отпуска из аптек
Отпускают по рецепту.