МНН: олокизумаб — аналоги
Важно: аналоги содержат действующее вещество олокизумаб, но не являются эквивалентной заменой друг другу
Уточнить
Олокизумаб — гуманизированное моноклональное антитело, которое селективно связывается с человеческим ИЛ-6 и нейтрализует его эффекты. Позиционируется как средство для лечения ревматоидного артрита. Проводятся клинические испытания при болезни Крона и при COVID-19.
Артлегиа
Артлегиа (олокизумаб, р-р для п/к введения). Биотехнологический ингибитор интерлейкина-6 для лечения ревматоидного артрита. Производитель: «Р-фарм» (Россия).
Содержание
-
Русское название
-
Английское название
-
Латинское название
-
Фармакологическая группа вещества Олокизумаб
-
Нозологическая классификация
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Олокизумаб
-
Противопоказания
-
Ограничения к применению
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Олокизумаб
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Источники информации
-
Торговые названия с действующим веществом Олокизумаб
Русское название
Олокизумаб
Английское название
Olokizumab
Латинское название
Olokizumabum (род. Olokizumabi)
Фармакологическая группа вещества Олокизумаб
Нозологическая классификация
Фармакологическое действие
—
иммунодепрессивное, ингибирующее ИЛ-6.
Характеристика
Гуманизированное (с присоединенным гипервариабельным участком) моноклональное антитело, относящееся к изотипу IgG4κ.
Фармакология
Фармакодинамика
Олокизумаб селективно связывается с человеческим ИЛ-6 и эффективно нейтрализует эффекты ИЛ-6 in vivo и in vitro. Полученные данные свидетельствуют о том, что олокизумаб не связывается в значительной степени с другими молекулами семейства ИЛ-6 и не влияет на их функционирование, а также не активирует сигнальный путь ИЛ-6.
В двойных слепых рандомизированных клинических исследованиях II фазы п/к введение олокизумаба в дозе от 60 до 480 мг/мес пациентам со среднетяжелым или тяжелым ревматоидным артритом вызывало выраженное снижение уровня С-реактивного белка (СРБ) в плазме в течение 7 дней от начала лечения, сохранявшееся в течение не менее 10 нед после однократного введения и в течение всего периода терапии при многократном введении.
У пациентов со среднетяжелым или тяжелым ревматоидным артритом, недостаточно контролируемым терапией метотрексатом, п/к введение олокизумаба в дозе 64 мг каждые 2 нед (к2н) или 64 мг каждые 4 нед (к4н) вызывало резкое снижение среднего уровня СРБ в плазме ко 2-й нед лечения. Низкие уровни СРБ сохранялись в течение 24 нед на протяжении всего периода лечения.
Клниическая эффективность
Эффективность п/к введения олокизумаба в дозе 64 мг к2н и к4н была изучена у пациентов со среднетяжелым или тяжелым ревматоидным артритом, недостаточно контролируемым терапией метотрексатом, в клиническом исследовании CREDO1.
Олокизумаб в обеих дозировках был значительно эффективнее плацебо в отношении снижения активности ревматоидного артрита вне зависимости от пола, ИМТ, активности заболевания, уровня антител к ревматоидному фактору и/или циклическому пептиду, содержащему цитруллин. Длительность периода от постановки диагноза до начала лечения и продолжительность предшествующей терапии метотрексатом также не влияли на клиническую эффективность олокизумаба. Кроме того, доля пациентов, достигших низкой активности заболевания и ремиссии, была значимо выше среди получавших олокизумаб по сравнению с плацебо. У пациентов, получавших олокизумаб, также чаще отмечалось улучшение качества жизни, уменьшение боли и количества болезненных и припухших суставов. Воздействие олокизумаба было заметным уже через 4 нед лечения, выраженный эффект развивался приблизительно через 12 нед от начала введения и сохранялся в течение не менее чем 24 нед.
Фармакокинетика
Абсорбция
Биодоступность олокизумаба оценивалась на основании данных, полученных от 173 пациентов с легким или умеренным ревматоидным артритом, получавших олокизумаб в различных дозах в течение 12 нед, объединенных с данными, полученными у 40 пациентов с легким или умеренным ревматоидным артритом после однократного введения различных доз олокизумаба, и данными, полученными у 41 здорового добровольца после однократного введения различных доз олокизумаба. При п/к введении биодоступность составляет 63% (доля относительной стандартной ошибки (ОСО)=4,9%).
После однократного п/к введения олокизумаба пациентам с легким или умеренным ревматоидным артритом в дозах от 0,3 до 6 мг/кг Сmах олокузумаба в крови дозозависимо возрастала. Tmах составляло от 4 до 12 дней, при этом поддающиеся определению уровни олокизумаба сохранялись приблизительно до 16 нед.
После однократного п/к введения олокизумаба в дозе 64 мг пациентам с ревматоидным артритом средней и тяжелой степени, недостаточно контролируемым на фоне лечения метотрексатом, Сmах достигалась в среднем через 7–10 дней (табл. 1).
При многократном введении стационарная концентрация олокизумаба в крови нарастала в течение начального периода терапии и достигала равновесного состояния через 16 (64 мг к4н) и 14 (64 мг к2н) нед от начала лечения.
Таблица 1
Фармакокинетические параметры олокизумаба после п/к введения пациентам с ревматоидным артритом средней и тяжелой степени
| Фармакокинетический параметр | Исходные значения | Неделя 20 | ||
| Олокизумаб 64 мг к4н (n=18) | Олокизумаб 64 мг к2н (n=18) | Олокизумаб 64 мг к4н (n=18) | Олокизумаб 64 мг к2н (n=18) | |
| Cmax, мкг/мл (CV, %) | 6,18 (50) | 6,22 (39,2) | 17 (55,7) | 21,55 (25) |
| AUC0–t1, мкг·ч/мл (CV, %) | 2886 (45,3) | 1556 (38,9) | 8411 (29,9) | 5485 (31,8) |
| Tmax, ч | 190,2 | 234,4 | 244,5 | 127,8 |
| медиана | 166,5 | 236,7 | 167,6 | 96,7 |
| мин.–макс. | 92,8–402,3 | 95,8–359,2 | 95,4–670,7 | 0–334,7 |
1 AUC для введения к4н рассчитывалась за период 672 ч (28 дней) и для введения к2н за период 336 ч (14 дней).
Биотрансформация
В исследовании in vitro на криоконсервированных гепатоцитах человека олокизумаб оказывал ингибирующее действие на активность CYP1А1/2, CYP2В6, CYP2С9, CYP3А4/5 и CYP2С19, а также на активность транспортера NTCP.
Элиминация
Оценки клиренса олокизумаба у пациентов с легким или умеренным ревматоидным артритом составляли 0,17 л/сут (доля ОСО=4,9%) с низкой или средней индивидуальной вариабельностью.
Фармакокинетическая-фармакодинамическая зависимость
Уровень снижения СРБ у пациентов с активным ревматоидным артритом, получавших олокизумаб, не зависел от дозы. Кроме того, у пациентов с легким и умеренным ревматоидным артритом была выявлена положительная корреляция концентрации олокизумаба в плазме с уровнем нейтропении, повышением уровней ACT, АЛТ и триглицеридов в плазме, хотя величина эффекта была невелика. Также к 14-му дню после введения олокизумаба наблюдалось стойкое снижение уровня VEGF (фактор роста эндотелия сосудов, vascular endothelial growth factor) и амилоидного сывороточного белка А во всех терапевтических группах без зависимости от дозы.
Применение вещества Олокизумаб
Терапия ревматоидного артрита средней или высокой степени активности в комбинации с метотрексатом у пациентов старше 18 лет при недостаточной эффективности монотерапии метотрексатом.
Противопоказания
Гиперчувствительность к олокизумабу; активные инфекционные заболевания (в т.ч. и туберкулез); беременность; кормление грудью; детский возраст до 18 лет.
Ограничения к применению
Серьезные или оппортунистические инфекции в анамнезе; сопутствующие заболевания и состояния, являющиеся факторами риска развития инфекций (в т.ч. сахарный диабет, почечная недостаточность, прием иммуносупрессивных ЛС, пожилой возраст); пациенты, контактировавшие с больными туберкулезом (перед применением олокизумаба у таких пациентов следует оценить соотношение риска и пользы применения); пациенты с дивертикулитом или перфорациями кишечника в анамнезе и другими факторами риска перфорации кишечника; пациенты с нарушениями функции печени и печеночной недостаточностью.
Применение при беременности и кормлении грудью
Перед назначением олокизумаба женщинам детородного возраста следует выполнить тест на беременность. Лечащий врач должен подробно разъяснить риски применения олокизумаба во время беременности и проинструктировать пациентку, способную к деторождению, о необходимости использования высокоэффективных методов контрацепции и выполнения регулярных тестов на беременность во время лечения и в течение по крайней мере 6 мес после получения последней дозы. В случае, если пациентка, получающая олокизумаб, забеременеет, она должна немедленно прекратить его применение и обратиться к врачу.
Применение олокизумаба у беременных систематически не изучалось. В связи с тем, что олокизумаб показан к применению в комбинации с метотрексатом, имеющим хорошо известное тератогенное действие, применение олокизумаба при беременности не рекомендуется.
В исследованиях на животных обнаружена репродуктивная токсичность. Предполагается, что ИЛ-6 играет важную роль в раскрытии шейки матки и, возможно, в рождении плаценты. Таким образом, применение олокизумаба может нарушать родовую деятельность.
Проникновение олокизумаба в грудное молоко не изучалось. Клинические данные о риске для ребенка, находящегося на грудном вскармливании, отсутствуют. Так как олокизумаб показан к применению в комбинации с метотрексатом, который секретируется в грудное молоко, рекомендуется прекратить грудное вскармливание при назначении олокизумаба.
Фертильность
Клинические данные о влиянии олокизумаба на фертильность у человека отсутствуют. В исследованиях на животных отрицательного воздействия олокизумаба на фертильность самцов и самок яванских макак не обнаружено.
Побочные действия вещества Олокизумаб
Безопасность применения олокизумаба оценивалась в двойном слепом рандомизированном клиническом исследовании CREDO1. Всего в исследовании участвовало 428 пациентов со среднетяжелым и тяжелым ревматоидным артритом с недостаточным контролем при терапии метотрексатом. 142 пациента получали олокизумаб в дозе 64 мг один раз к2н, 143 пациента получали олокизумаб 64 мг один раз к4н, 143 пациента получали плацебо. Все пациенты находились на фоновой терапии метотрексатом. Наиболее часто встречающимися нежелательными реакциями были лейкопения, нейтропения, повышение уровня печеночных трансаминаз. Перечень нежелательных реакций приведен в соответствии с системно-органными классами MedDRA (табл. 2). В пределах каждого класса нежелательные реакции распределены по категориям частоты встречаемости: очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000) и частота неизвестна.
Таблица 2
Нежелательные лекарственные реакции на применение олокизумаба
| Системно-органный класс | Класс частоты | ||
| Очень часто | Часто | Нечасто | |
| Инфекции и паразитарные заболевания | Бронхит | Легочный туберкулез, кандидоз кожи, вульвовагинальный кандидоз, отрубевидный лишай, подкожный абсцесс, рожистое воспаление, сепсис, вызванный стафилококковой инфекцией, синдром токсического шока | |
| Со стороны крови и лимфатической системы | Лейкопения, нейтропения | Эозинофилия | |
| Со стороны обмена веществ и питания | Гиперхолестеринемия | ||
| Со стороны печени и желчевыводящих путей | Повышение уровня ACT, повышение уровня АЛТ | Повышение уровня ГГТ | |
| Со стороны кожи и подкожных тканей | Зуд, сыпь | Изменение цвета пота, дерматит, экхимозы, зудящая сыпь | |
| Общие нарушения и реакции в месте введения | Боль в месте инъекции, эритема | ||
| Данные лабораторных и инструментальных исследований | Позитивный тест на микобактерию туберкулеза |
Перфорации дивертикула
Несмотря на то что у пациентов в исследовании CREDO1 не было выявлено нежелательных явлений со стороны ЖКТ, связанных с применением олокизумаба, в продолжающихся клинических исследованиях, включающих в общей сложности более 2000 пациентов с ревматоидным артритом, были зарегистрированы случаи перфорации дивертикула, связанные с применением олокизумаба. Частота данной нежелательной реакции неизвестна. В связи с тем, что риск перфорации ЖКТ характерен для ингибиторов ИЛ-6, следует соблюдать осторожность при применении олокизумаба у пациентов с факторами риска развития перфорации ЖКТ.
Реакции гиперчувствительности
В исследовании CREDO1 наблюдалось дозозависимое увеличение реакций гиперчувствительности в группах пациентов, получавших олокизумаб. Доля пациентов, у которых в ходе лечения возникло хотя бы одно нежелательное явление, относящееся к реакциям гиперчувствительности, включая зуд, сыпь, аллергический дерматит, повышение уровня эозинофилов в крови, составила 4,2% в группе, получавшей олокизумаб к4н, 7% в группе, получавшей олокизумаб к2н, и 2,1% в группе плацебо.
В продолжающихся клинических исследованиях был зарегистрирован случай анафилактической реакции на введение олокизумаба (частота неизвестна).
Инфекции
В исследовании CREDO1 инфекции встречались с приблизительно одинаковой частотой во всех терапевтических группах: 14,1% в группе, получавшей олокизумаб 64 мг к4н, 15,4% в группе, получавшей олокизумаб 64 мг к2н, и 16,2% в группе плацебо.
В группе пациентов, получавших олокизумаб 64 мг к2н, чаще развивались связанные с инфекциями серьезные нежелательные явления (2,8%) по сравнению с группой пациентов, получавших олокизумаб 64 мг к4н (0%), и плацебо (1,4%).
В группах пациентов, получавших олокизумаб, были зарегистрированы следующие случаи серьезных инфекций, не встречавшихся в группе плацебо: подкожный абсцесс (2), легочный туберкулез (1), сепсис, вызванный стафилококковой инфекцией (1), и синдром токсического шока (1).
Повышение уровня печеночных трансаминаз
В исследовании CREDO1 частота повышения уровня АЛТ, расцененного исследователями как нежелательное явление, составляла 23,2% в группе, получавшей олокизумаб 64 мг к4н, 17,5% в группе, получавшей олокизумаб 64 мг к2н, и 17,7% в группе плацебо. Частота повышения уровня ACT, расцененного исследователями как нежелательное явление, составляла 15,5% в группе, получавшей олокизумаб к4н, 11,2% группе, получавшей олокизумаб к2н, и 7% в группе плацебо.
В целом в течение периода терапии наблюдались колебания индивидуальных уровней АЛТ. Всего подъем уровня АЛТ выше ВГН отмечался хотя бы один раз за период лечения (24 нед) приблизительно у 50% пациентов, получавших олокизумаб, и у 27% пациентов, получавших плацебо (табл. 3). Ни у кого из пациентов не отмечалось одновременного повышения АЛТ и ACT >3×ВГН с повышением уровня билирубина >2×ВГН.
Таблица 3
Повышение уровня АЛТ у пациентов в исследовании CREDO1
| Уровень АЛТ | Доля пациентов, % | |||||
| Исходный уровень | За период лечения1 | |||||
| Олокизумаб 64 мг к4н | Олокизумаб 64 мг к2н | Плацебо | Олокизумаб 64 мг к4н | Олокизумаб 64 мг к2н | Плацебо | |
| >1×ВГН, <3×ВГН | 9,9 | 8,4 | 9,9 | 52,9 | 47,5 | 27 |
| >3×ВГН, <5×ВГН | 0 | 0 | 0 | 5,7 | 6,4 | 3,5 |
| >5×ВГН | 0 | 0,7 | 0 | 5,7 | 2,8 | 1,4 |
1 Учитывалось наибольшее значение АЛТ у каждого пациента за 24-недельный период лечения.
Гиперлипидемия
В исследовании CREDO1 повышение уровня липидов крови на фоне лечения, расцененное исследователями как нежелательное явление, наблюдалось у 8,5% пациентов в группе, получавшей олокизумаб 64 мг к4н, 8,4% пациентов в группе, получавшей олокизумаб 64 мг к2н, и 2,8% пациентов в группе плацебо. В среднем уровни общего Хс, ЛПНП и ЛПВП возрастали в группах пациентов, получавших олокизумаб, в течение первых 4 нед терапии. Затем в группе, получавшей олокизумаб 64 мг к2н, средние уровни липидов снижались и к концу периода лечения возвращались к значениям в группе плацебо, тогда как у пациентов, получавших олокизумаб 64 мг к4н, высокие средние уровни липидов в крови сохранялись до конца периода лечения.
Нейтропения
В исследовании CREDO1 среднее абсолютное число нейтрофилов через 12 нед терапии снизилось в группах, получавших олокизумаб, по сравнению с плацебо и затем оставалось стабильным до конца периода лечения (табл. 4).
Таблица 4
Динамика среднего абсолютного числа нейтрофилов в течение 24 нед терапии
| Длительность лечения | Олокизумаб 64 мг к4н | Олокизумаб 64 мг к2н | Плацебо |
| До лечения | 5,9×109/л | 5,2×109/л | 5,7×109/л |
| 12 нед | 3,9×109/л | 3,4×109/л | 5,6×109/л |
| 24 нед | 3,7×109/л | 3,2×109/л | 5,3×109/л |
Соответственно доля пациентов, у которых хотя бы один раз в ходе лечения регистрировалось такое нежелательное явление, как нейтропения, составляла 11,2% в группе, получавшей олокизумаб 64 мг к4н, 7,7% в группе, получавшей олокизумаб 64 мг к2н, и 3,5% в группе плацебо.
Взаимодействие
Одновременное применение с метотрексатом не влияло на экспозицию олокизумаба. Не ожидается также влияния олокизумаба на экспозицию метотрексата при их одновременном применении, клинические данные отсутствуют. Во всех клинических исследованиях у пациентов с ревматоидным артритом олокизумаб применялся совместно с метотрексатом.
Специальные клинические исследования взаимодействия олокизумаба не проводились. По результатам клинического исследования CREDO1, не сообщалось о случаях клинически значимого взаимодействия олокизумаба с другими ЛС.
В исследовании in vitro на криоконсервированных гепатоцитах человека олокизумаб оказывал ингибирующее действие на активность CYP1A1/2, CYP2В6, CYP2С9, CYP3А4/5 и CYP2С19, а также на активность NTCP. Таким образом, следует принимать во внимание, что у пациентов с активным ревматоидным артритом может потребоваться коррекция доз ЛС, метаболизируемых данными изоформами CYP, после начала применения олокизумаба.
Концентрация следующих ЛС может снизиться при совместном применении с олокизумабом (список не является исчерпывающим): статины (симвастатин, ловастатин, аторвастатин), пероральные контрацептивы, БКК, ГКС (дексаметазон, метилпреднизолон), варфарин, хинидин, теофиллин, тизанидин, фенитоин, пимозид, циклоспорин, сиролимус, такролимус, бензодиазепины (например, диазепам, алпразолам, триазолам, мидазолам, бромазепам).
Передозировка
В клинических исследованиях случаев передозировки не наблюдалось. Однако дополнительные клинические данные показывают, что общий профиль безопасности олокизумаба у пациентов, получавших препарат в дозе 240 мг к2н (480 мг в месяц) в течение 12 нед, сопоставим с общим профилем безопасности у пациентов, получавших его в рекомендованной дозе.
Дети
Данные о передозировке олокизумаба у детей отсутствуют.
Способ применения и дозы
П/к, в область бедра или передней брюшной стенки, к2н или к4н.
Меры предосторожности
Назначать олокизумаб и наблюдать за ходом лечения разрешается врачам, имеющим опыт в диагностике и лечении ревматоидного артрита.
Анафилактические или анафилактоидные реакции
Введение ЛС, содержащих белки, может быть связано с возникновением иммунологических/аллергических или неиммунологических реакций повышенной чувствительности, которые могут быть тяжелыми. Эти реакции могут возникать в виде острой инфузионной реакции, аллергической реакции или реакции гиперчувствительности замедленного типа. Таким образом, первое введение олокизумаба следует выполнять в медицинском учреждении, где имеются ЛС и оборудование для купирования анафилактических и анафилактоидных реакций. В клинических исследованиях был отмечен случай серьезной анафилактической реакции на введение олокизумаба.
Инфекции
Для пациентов, получающих иммуносупрессивные ЛС, включая блокаторы сигнального пути ИЛ-6, характерна повышенная частота развития инфекций. Применение олокизумаба связано с повышенным риском развития или активизации инфекций. Не следует начинать терапию олокизумабом у пациентов с инфекциями в активной фазе. Следует с осторожностью применять олокизумаб у пациентов, имеющих факторы риска развития инфекций. При развитии серьезных инфекций терапию олокизумабом следует прекратить. Пациентов следует проинструктировать о возможных признаках и симптомах развития инфекции, требующих немедленного обращения к врачу.
Туберкулезная инфекция
Перед началом терапии олокизумабом необходимо провести обследование пациента на наличие латентной формы туберкулезной инфекции. Пациентам с выявленной латентной формой туберкулезной инфекции перед началом применения олокизумаба следует провести стандартный курс противотуберкулезной терапии.
Следует с осторожностью назначать олокизумаб пациентам, находящимся в тесном контакте (совместное проживание или нахождение в других замкнутых пространствах, например, на рабочем месте, общественных собраниях или в здании на протяжении длительных периодов в течение дня) с лицом, страдающим активным туберкулезом. Перед применением олокизумаба у таких пациентов следует тщательно оценить соотношение риска и пользы его применения.
Риск перфорации ЖКТ
При применении ингибиторов сигнального пути ИЛ-6 известны случаи перфорации ЖКТ, в основном на фоне дивертикулита. Следует соблюдать осторожность при применении олокизумаба у пациентов с дивертикулитом или перфорацией кишечника в анамнезе и другими факторами риска перфорации кишечника. При появлении желудочно-кишечных симптомов, таких как абдоминальная боль, на фоне лечения олокизумабом следует незамедлительно провести обследование пациента.
Почечная недостаточность
Пациентов с почечной недостаточностью не включали в клиническое исследование олокизумаба. В связи с отсутствием данных следует соблюдать осторожность при применении олокизумаба у пациентов с нарушениями функции почек.
Нарушения функции печени
Применение олокизумаба так же, как и других ингибиторов ИЛ-6, связано с повышением уровня АЛТ, ACT и ГГТ. Пациентов с уровнем АЛТ или ACT >1,5×ВГН не включали в клиническое исследование. Следует соблюдать осторожность при применении олокизумаба у пациентов с нарушениями функции печени и печеночной недостаточностью.
Мониторинг лабораторных показателей крови
В клинических исследованиях было зарегистрировано снижение абсолютного числа нейтрофилов и лейкоцитов на фоне лечения олокизумабом и другими ингибиторами ИЛ-6. По данным применения других ингибиторов ИЛ-6, нейтропения на фоне лечения не приводила к повышению частоты инфекций. Пациентов с уровнем лейкоцитов <3,5×109/л, уровнем нейтрофилов <2000×106/л (<2000/мм3) не включали в клиническое исследование.
Вакцинация
Безопасность иммунизации живыми вакцинами на фоне применения ингибиторов ИЛ-6, в т.ч. олокизумаба, не установлена. Пациентов с необходимостью вакцинации живыми вакцинами не включали в клиническое исследование.
Злокачественные новообразования
Данные о безопасности применения олокизумаба у пациентов со злокачественными новообразованиями отсутствуют, риск развития злокачественных опухолей на фоне терапии олокизумабом неизвестен.
Влияние на способность управлять транспортными средствами, механизмами. Исследования по изучению влияния олокизумаба на способность управлять транспортными средствами и механизмами не проводились. Хотя на данный момент при терапии олокизумабом нежелательные реакции, связанные с головокружением, не отмечались, головокружение часто наблюдалось при терапии другими ингибиторами ИЛ-6. Пациентам, испытывающим головокружение во время терапии олокизумабом, следует рекомендовать не управлять транспортными средствами и механизмами до тех пор, пока головокружение не прекратится.
Источники информации
Обобщенные материалы www.grls.rosminzdrav.ru, 2020.
Торговые названия с действующим веществом Олокизумаб
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Артлегиа |
47816.00 |
Фармакологическое действие
Гуманизированное (с присоединенным гипервариабельным участком) моноклональное антитело, относящееся к изотипу иммуноглобулина G4/каппа. Олокизумаб селективно связывается с человеческим ИЛ-6 и эффективно нейтрализует эффекты ИЛ-6 in vivo и in vitro. Полученные данные свидетельствуют о том. что олокизумаб не связывается в значительной степени с другими молекулами семейства ИЛ-6 и не влияет на их функционирование, а также не активирует сигнальный путь ИЛ-6.
У пациентов со среднетяжелым или тяжелым ревматоидным артритом, недостаточно контролируемым терапией метотрексатом, п/к введение олокизумаба в дозе 64 мг каждые 2 недели или 64 мг каждые 4 недели вызывало резкое снижение среднего уровня C-реактивного белка в плазме ко 2 неделе лечения. Низкие уровни СРБ сохранялись в течение 24 недель на протяжении всего периода лечения.
У пациентов, получавших олокизумаб, также чаще отмечалось улучшение качества жизни, уменьшение боли и количества болезненных и отечных суставов. Воздействие олокизумаба было заметным уже через 4 недели лечения, выраженный эффект развивался приблизительно через 12 недель от начала введения препарата и сохранялся в течение не менее чем 24 недель.
Фармакокинетика
После однократного п/к введения олокизумаба пациентам с легким или умеренным ревматоидным артритом в дозах от 0.3 до 6 мг/кг Cmax в крови дозозависимо возрастала. Время достижения Cmax составляло от 4 до 12 дней, при этом поддающиеся определению концентрации олокизумаба сохранялись до 16 нед. При многократном введении Css олокизумаба в крови нарастала в течение начального периода терапии и достигала равновесного состояния через 16 и 14 нед. от начала лечения. При п/к введении биодоступность составляет 63%. В исследовании in vitro на криоконсервированных гепатоцитах человека олокизумаб обращал ингибиторный эффект ИЛ-6 на активность CYP1A1/2, CYP2B6, CYP2C9, CYP3A4/5 и CYP2C19, а также на активность NTCP. Клиренс олокизумаба у пациентов с легким или умеренным ревматоидным артритом составлял 0.17 л/сут с низкой или средней индивидуальной вариабельностью.
Показания активного вещества
ОЛОКИЗУМАБ
Терапия пациентов старше 18 лет с ревматоидным артритом средней или высокой степени активности в комбинации с метотрексатом, при недостаточной эффективности монотерапии метотрексатом.
Режим дозирования
Вводят п/к в область бедра или передней брюшной стенки.
Доза составляет 64 мг каждые 2-4 недели.
Побочное действие
Инфекции и паразитарные заболевания: часто — бронхит; нечасто — легочный туберкулез, кандидоз кожи, вульвовагинальный кандидоз, отрубевидный лишай, подкожный абсцесс, рожистое воспаление, сепсис, вызванный стафилококковой инфекцией, синдром токсического шока.
Со стороны обмена веществ: очень часто — лейкопения, нейтропения; нечасто — гиперхолестеринемия.
Со стороны печени и желчевыводящих путей: очень часто — повышение активности АСТ, повышение активности АЛТ; часто — повышение активности ГГТ.
Со стороны кожи и подкожных тканей: часто — зуд, сыпь; нечасто — изменение цвета пота, дерматит, экхимоз, зудящая сыпь.
Общие нарушения и реакции в месте введения: нечасто — боль в месте инъекции, эритема.
Лабораторные и инструментальные данные: часто — позитивный тест на микобактерию туберкулеза.
Противопоказания к применению
Повышенная чувствительность к олокизумабу, активные инфекционные заболевания (в т.ч. туберкулез); детский возраст до 18 лет; беременность, период грудного вскармливания.
С осторожностью
У пациентов с серьезными или оппортунистическими инфекциями в анамнезе; с сопутствующими заболеваниями и состояниями, являющимися факторами риска развития инфекций (в т.ч. сахарный диабет, почечная недостаточность, прием иммуносупрессивных препаратов, пожилой возраст); у пациентов, контактировавших с больными туберкулезом; с дивертикулитом или перфорациями кишечника в анамнезе и другими факторами риска перфорации кишечника; с нарушениями функции печени и печеночной недостаточностью.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период грудного вскармливания.
Применение при нарушениях функции печени
С осторожностью применять у пациентов с нарушениями функции печени и печеночной недостаточностью.
Применение при нарушениях функции почек
С осторожностью применять при нарушениях функции почек.
Применение у детей
Противопоказано применение у детей и подростков в возрасте до 18 лет.
Применение у пожилых пациентов
С осторожностью применять у пациентов пожилого возраста.
Особые указания
Назначать лечение олокизумабом и наблюдать за ходом лечения разрешается врачам, имеющим опыт в диагностике и лечении ревматоидного артрита.
Анафилактические или анафилактоидные реакции: введение препаратов, содержащих белки, может быть связано с возникновением иммунологических/аллергических или неиммунологических реакций повышенной чувствительности к препарату, которые могут быть тяжелыми. Эти реакции могут возникать в виде острой инфузионной реакции, аллергической реакции или реакции гиперчувствительности замедленного типа.
Инфекции: для пациентов, получающих иммуносупрессивные препараты, включая блокаторы сигнального пути ИЛ-6, характерна повышенная частота развития инфекций. Применение олокизумаба связано с повышенным риском развития или активизацией инфекций. Не следует начинать терапию олокизумабом пациентам с инфекциями в активной фазе. При развитии серьезных инфекций терапию олокизумабом следует прекратить. Пациентов следует проинструктировать о возможных признаках и симптомах развития инфекции, требующих немедленного обращения к врачу.
Туберкулезная инфекция: перед началом терапии олокизумабом необходимо провести обследование пациента на наличие латентной формы туберкулезной инфекции. Пациентам с выявленной латентной формой туберкулезной инфекции перед началом терапии олокизумабом следует провести стандартный курс противотуберкулезной терапии.
Следует с осторожностью применять олокизумаб пациентам, находящимся в тесном контакте (совместное проживание или нахождение в других замкнутых пространствах, например, на рабочем месте, на общественных собраниях или в здании на протяжении длительных периодов в течение дня) с лицом, страдающим активным туберкулезом. Перед применением олокизумаба у таких пациентов следует тщательно оценить соотношение риска и пользы терапии.
Риск перфорации желудочно-кишечного тракта: при применении ингибиторов сигнального пути ИЛ-6 известны случаи перфорации желудочно-кишечного тракта, в основном на фоне дивертикулита. Следует соблюдать осторожность при применении олокизумаба у пациентов с дивертикулитом или перфорацией кишечника в анамнезе и другими факторами риска перфорации кишечника. При появлении желудочно-кишечных симптомов, таких как абдоминальная боль, на фоне лечения олокизумабом, следует незамедлительно провести обследование пациента.
Почечная недостаточность: пациентов с почечной недостаточностью не включали в клиническое исследование олокизумаба. В связи с отсутствием данных следует соблюдать осторожность при применении олокизумаба у пациентов с нарушениями функции почек.
Вакцинация: безопасность иммунизации живыми вакцинами на фоне применения ингибиторов ИЛ-6, в том числе олокизумаба, не установлена. Пациентов с необходимостью вакцинации живыми вакцинами не включали в клиническое исследование.
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по изучению влияния препарата на способность управлять транспортными средствами и механизмами не проводились. Хотя на данный момент при терапии олокизумабом нежелательные реакции, связанные с головокружением, не отмечались, головокружение часто наблюдалось при терапии другими ингибиторами ИЛ-6. Пациентам, испытывающим головокружение во время терапии препаратом Артлегиа, следует рекомендовать не управлять транспортными средствами и механизмами до тех пор, пока головокружение не прекратится.
Лекарственное взаимодействие
Одновременное применение с метотрексатом не влияло на экспозицию олокизумаба. Не ожидается также влияния олокизумаба на экспозицию метотрексата при их одновременном применении, клинические данные отсутствуют. Во всех клинических исследованиях у пациентов с ревматоидным артритом олокизумаб применялся совместно с метотрексатом.
Специальные клинические исследования лекарственных взаимодействий олокизумаба не проводились. По результатам клинического исследования СКЕ001 не сообщалось о случаях клинически значимых лекарственных взаимодействий олокизумаба с другими препаратами.
В исследовании in vitro на криоконсервированных гепатоцитах человека олокизумаб обращал ингибиторный эффект ИЛ-6 на активность CYP1A1/2, CYP2B6, CYP2C9, CYP3A4/5 и CYP2C19, а также на активность NTCP. Поэтому следует учитывать, что у пациентов с активным ревматоидным артритом может потребоваться коррекция доз препаратов, метаболизирующихся данными изоферментами, после начала применения препарата.
Концентрация следующих препаратов может снизиться при совместном применении с олокизумабом (список не является исчерпывающим): статины (симвастатин, ловастатин, аторвастатин); пероральные контрацептивы; блокаторы кальциевых каналов; ГКС (дексаметазон, метилпреднизолон); варфарин; хинидин; теофиллин; тизанидин; фенитоин; пимозид; циклоспорин; сиролимус; такролимус; бензодиазепины (например, диазепам, алпразолам, триазолам, мидазолам. бромазепам).
- Бровко М.Ю.
- Клиника им. Е.М. Тареева, Первый МГМУ им. И.М. Сеченова (Сеченовский Университет), Москва
,
- Новиков П.И.
- Клиника им. Е.М. Тареева, Первый МГМУ им. И.М. Сеченова (Сеченовский Университет), Москва
,
- Набатчикова Е.А.
- Кафедра внутренних, профессиональных болезней и ревматологии, Первый МГМУ им. И.М. Сеченова (Сеченовский Университет), Москва
,
- Буланов Н.М.
- Клиника им. Е.М. Тареева, Первый МГМУ им. И.М. Сеченова (Сеченовский Университет), Москва
,
,
- Потапов П.П.
- Клиника им. Е.М. Тареева, Первый МГМУ им. И.М. Сеченова (Сеченовский Университет), Москва. Кафедра внутренних болезней, Факультет фундаментальной медицины, МГУ им. М.В. Ломоносова, Москва
,
- Акулкина Л.А.
- Клиника им. Е.М. Тареева, Первый МГМУ им. И.М. Сеченова (Сеченовский Университет), Москва
,
- Соловьева Н.С.
- АО “Р-Фарм”, Москва
,
- Моисеев С.В.
- Клиника им. Е.М. Тареева, Первый МГМУ им. И.М. Сеченова (Сеченовский Университет), Москва
- DOI
- 10.32756/0869-5490-2022-3-9-15
- Количество просмотров
- 394
Скачать статью в PDF
Сравнить эффективность олокизумаба и тоцилизумаба в профилактике перевода на искусственную вентиляцию легких (ИВЛ) и смерти у госпитализированных пациентов с COVID-19.
В ретроспективное исследование включали всех пациентов с подтвержденным диагнозом COVID-19, которые во время госпитализации получали олокизумаб подкожно или тоцилизумаб внутривенно в любых дозах. Первичной конечной точкой исследования были перевод на ИВЛ или смерть во время госпитализации, вторичными – два компонента первичной конечной точки по отдельности и длительность госпитализации. Отношения шансов (ОШ) и 95% доверительные интервалы (ДИ) рассчитывали с помощью многофакторного линейного регрессионного анализа.
В ретроспективное исследование были включены 244 госпитализированных пациента с COVID-19, которые получили по
крайней мере одну подкожную инъекцию олокизумаба (n=157) или внутривенное введение тоцилизумаба (n=87). В обеих группах преобладали пациенты пожилого и старческого возраста, страдавшие сердечно-сосудистыми и другими сопутствующими заболеваниями. У всех пациентов определялись признаки иммунного гипервоспалительного ответа, а у 197 (80,7%) из них перед введением исследуемых препаратов была начата оксигенотерапия.
Частота комбинированной первичной конечной точки и обоих ее компонентов достоверно не отличалась между группами олокизумаба и тоцилизумаба, а сопоставимая эффективность двух препаратов в профилактике неблагоприятных исходов COVID-19 была подтверждена при многофакторном регрессионном анализе (ОШ 0,58; 95% ДИ 0,27-1,23). Медиана длительности госпитализации в двух группах была одинаковой (16 дней).
Подкожное введение олокизумаба и внутривенное введение тоцилизумаба были сопоставимыми по эффективности в профилактике интубации и смерти у пациентов с синдромом иммунного гипервоспалительного ответа, вызванного SARS-CoV-2.
На протяжении всей пандемии COVID-19 ведущей причиной госпитализации и смертности больных, инфицированных SARS-CoV-2, остается острый респираторный дистресс синдром, который чаще развивается у людей пожилого и старческого возраста и характеризуется быстрым прогрессированием дыхательной недостаточности на фоне распространенной вирусной пневмонии. В российских отделениях реанимации и интенсивной терапии (ОРИТ) летальность больных с COVID-19, нуждавшихся в респираторной поддержке, составила в среднем 65% и в значительной степени зависела от выраженности гипоксии. Летальность была относительно невысокой (10,1%) у пациентов, получавших кислород через канюли, но значительно увеличивалась у больных, которых переводили на неинвазивную (НИВЛ) и особенно искусственную (ИВЛ) вентиляцию легких (36,8% и 76,5%, соответственно) [1]. Основными факторами риска смерти больных, госпитализированных в ОРИТ, были возраст, а также мужской пол и сопутствующие заболевания, такие как ожирение, сахарный диабет 2 типа и коронарная болезнь сердца.
Одной из причин развития прогрессирующего поражения легких при COVID-19 считают иммунный гипервоспалительный ответ, вызванный SARS-CoV-2 и сопровождающийся выбросом различных цитокинов [2]. Ранее синдром выделения цитокинов, который часто называют “цитокиновым штормом”, был описан при первичном и вторичном гемофагоцитарном лимфогистиоцитозе и синдроме активации макрофагов, а также при CAR-T-клеточной терапии онкологических заболеваний [3]. Признаки гипервоспалительного ответа при COVID-19 включают в себя стойкую лихорадку и снижение степени насыщения крови кислородом (SpO 2 ) в сочетании с увеличением содержания лабораторных маркеров воспаления, в том числе С-реактивного белка (СРБ), ферритина и фибриногена [4]. Ведущую роль в патогенезе синдрома выделения цитокинов, вызванного SARS-CoV-2, отводят интерлейкину (ИЛ)6, повышение содержания которого ассоциировалось с более тяжелым течением COVID-19 и увеличением риска смерти больных [5].
Эффективным методом профилактики тяжелого течения COVID-19 является вакцинация. В когортном исследовании, проведенном в США в марте-августе 2021 г., было показано, что иммунизация мРНК-вакцинами приводит к снижению частоты госпитализаций пациентов с COVID-19, а также риска интубации и смерти у госпитализированных больных [6]. В нашем когортном исследовании у 158 госпитализированных пациентов c COVID-19, развившимся несмотря на вакцинацию Гам-КОВИД-Вак (Спутник V), риск смерти от любых причин был на 62% ниже (отношение шансов 0,38, 95% доверительный интервал 0,19-0,77), чем у 473 больных с SARS-CoV-2 инфекцией, не получавших какие-либо вакцины против COVID-19 [7]. Эффективность вакцинации в профилактике смерти была сопоставимой в подгруппах пациентов, выделенных с учетом пола, возраста и наличия сердечно-сосудистых заболеваний, и была выше у пациентов с более высокими титрами нейтрализующих антител к рецептор-связывающему домену спайкового белка вируса.
Для лечения синдрома гипервоспалительного ответа у пациентов с COVID-19 применяют глюкокортикостероиды, прежде всего дексаметазон, и различные ингибиторы ИЛ-6. Первые сообщения об успешном опыте применения тоцилизумаба, блокирующего рецептор ИЛ-6, у больных с тяжелым течением COVID-19 были опубликованы уже вскоре после начала пандемии SARS-CoV-2 инфекции в Китае [8,9], а затем и в других странах, включая Россию [10]. В большинстве контролируемых и неконтролируемых клинических исследований, проводившихся во время пандемии, изучался тоцилизумаб в форме раствора для внутривенного введения. В Российской Федерации для лечения COVID19 у госпитализированных пациентов одобрен также олокизумаб, который представляет собой моноклональное антитело, непосредственно связывающееся не с рецептором ИЛ-6, а c самим цитокином [11]. Олокизумаб выпускается в форме раствора для подкожного применения, хотя у пациентов с тяжелым течением COVID-19 допускается и внутривенное его введение [12].
Целью ретроспективного исследования было сравнение эффективности олокизумаба и тоцилизумаба в профилактике перевода на ИВЛ и смерти у госпитализированных пациентов с COVID-19.
Материал и методы
Дизайн исследования. В ретроспективное исследование, проводившееся на базе перепрофилированной клиники им. Е.М. Тареева с июня 2020 г. по февраль 2021 г., включали всех пациентов с COVID-19, которым во время госпитализации вводили олокизумаб подкожно или тоцилизумаб внутривенно в любых дозах. Диагноз COVID-19 устанавливали на основании типичных клинических проявлений и данных компьютерной томографии легких при наличии положительного результата полимеразной цепной реакции мазка из носа и/или полости рта.
Конечные точки. Всех пациентов, включенных в исследование, наблюдали до выписки из стационара или смерти. Первичной конечной точкой исследования были перевод на ИВЛ или смерть во время госпитализации, вторичными – два компонента первичной конечной точки по отдельности и длительность госпитализации.
На основании историй болезни у всех пациентов регистрировали демографические, клинические и лабораторные показатели, а также сопутствующие заболевания, которые могли оказать влияние на течение COVID-19, в том числе артериальную гипертонию, ишемическую болезнь сердца (ИБС), включая инфаркт миокарда в анамнезе, инсульт в анамнезе, фибрилляцию предсердий, ожирение, сахарный диабет, заболевания органов дыхания (хроническая обструктивная болезнь легких, бронхиальная астма, интерстициальные болезни легких), хроническую болезнь почек (ХБП), хронические заболевания печени, ревматические аутоиммунные заболевания, злокачественные опухоли и гемобластозы. Ожирение диагностировали на основании величины индекса массы тела (≥30,0 кг/м2). При анализе частоты ревматических заболеваний учитывали только аутоиммунные заболевания, такие как ревматоидный артрит, системная красная волчанка, системная склеродермия, псориатический артрит, анкилозирующий спондилит, системные васкулиты. При компьютерной томографии оценивали распространенность двусторонней вирусной пневмонии в процентах [12]. Скорость клубочковой фильтрации (СКФ) рассчитывали по формуле CKD-EPI. Стадию ХБП определяли в соответствии с рекомендациями KDIGO [13]. Тяжесть гипоксии перед введением препарата оценивали на основании SpO2 и необходимости в респираторной поддержке (не требуется, низкопоточная оксигенотерапия через канюли, высокопоточная оксигенотерапия, НИВЛ или ИВЛ).
Статистический анализ. Статистическая обработка данных выполнена с помощью программ IBM SPSS Statistics (version 21) и GraphPad Prism 8. Нормальность распределения проверяли с помощью критерия Колмогорова– Смирнова. Количественные переменные представлены в виде медианы и межквартильного интервала, качественные признаки – в виде абсолютного числа и процента. Медианы количественных переменных двух независимых групп сравнивали с помощью U-критерия Манна-Уитни, медианы качественных переменных – с помощью критерия χ2-Пирсона (количество наблюдений ≥10) и точного критерия Фишера (количество наблюдений <10). Анализ Каплана-Мейера применяли для оценки кумулятивной частоты развития комбинированного исхода, которую сравнивали между группами с помощью log-rank теста. Для выявления факторов, ассоциированных с развитием комбинированного исхода, использовали метод логистической регрессии. Исходную однофакторную модель корректировали по возрасту. Для преобразования количественных переменных в номинальные признаки (0 – нет признака, 1 – есть признак) использовались стандартные пороговые значения (альбумин, СКФ, тромбоциты) или медианы количественного ряда (лимфоциты, СРБ, D-димер). Результат представлен в виде отношения шансов (ОШ) и 95% доверительного интервала (ДИ). Достоверным считали уровень значимости р <0,05. Все результаты представлены с двусторонним уровнем значимости.
Результаты
Характеристика больных. 244 из 1396 госпитализированных пациентов с подтвержденным диагнозом COVID-19 во время госпитализации в клинику получили по крайней мере одну подкожную инъекцию олокизумаба (n=157) или внутривенное введение тоцилизумаба (n=87). Две группы были сопоставимы по возрасту и полу (табл. 1). В обеих группах преобладали пациенты пожилого и старческого возраста (более 70% из них были в возрасте 60 лет и старше, а около 20% – 80 лет и старше). У большинства пациентов имелись различные сопутствующие заболевания. Чаще всего встречались сердечно-сосудистые болезни (артериальная гипертония, ишемическая болезнь сердца и фибрилляция предсердий), ожирение, сахарный диабет и хронические заболевания легких. По частоте и спектру сопутствующих заболеваний две группы существенно не отличались, за исключением сахарного диабета, который чаще наблюдался у пациентов группы тоцилизумаба.
| Показатели | Группа олокизумаба, n=157 | Группа тоцилизумаба, n=87 | р |
|---|---|---|---|
| Примечание: приведены медианы и интерквартильный диапазон, если не указано иное. *перед введением препаратов. ХБП — хроническая болезнь почек, НПВП — нестероидные противовоспалительные препараты, ИМТ — индекс массы тела, ИБС — ишемическая болезнь сердца | |||
| Мужской пол, n (%) | 76 (48,4) | 46 (54,1) | 0,396 |
| Возраст, годы | 70 [60;78] | 66 [58;76] | 0,211 |
| Возраст, n (%) | 0,134 | ||
| <50 | 13 (8,3) | 14 (16,4) | – |
| 50-59 | 24 (15,3) | 11 (12,9) | – |
| 60-69 | 39 (24,8) | 27 (31,8) | – |
| 70-79 | 48 (30,6) | 16 (18,8) | – |
| ≥80 | 33 (21,0) | 17 (20,0) | – |
| ИМТ, кг/м2 | 29,7 [26,1;33,1] | 30,6 [27,1;34,8] | 0,146 |
| Дни до госпитализации, | 7 [4;9] | 7 [5;9] | 0,326 |
| Сопутств. болезни, n (%) | |||
| Гипертония | 114 (72,6) | 57 (67,1) | 0,365 |
| ИБС | 31 (19,7) | 22 (25,9) | 0,534 |
| Инфаркт миокарда в анамнезе | 5 (3,2) | 5 (5,9) | 0,314 |
| Фибрилляция предсердий | 20 (12,7) | 11 (12,9) | 0,940 |
| Инсульт в анамнезе | 7 (4,4) | 2 (2,3) | 0,439 |
| Сахарный диабет | 33 (21,0) | 28 (32,9) | 0,041 |
| Ожирение | 74 (47,1) | 46 (54,1) | 0,300 |
| Болезни легких | 31 (19,7) | 14 (16,5) | 0,606 |
| ХБП 3-4 стадии | 6 (3,8) | 4 (4,7) | 0,741 |
| Болезни печени | 5 (3,2) | 3 (3,5) | 0,886 |
| Опухоли и гемобластозы | 12 (7,6) | 6 (7,1) | 0,869 |
| Ревматические болезни | 9 (5,7) | 6 (7,1) | 0,683 |
| Клин. проявления, n (%) | |||
| Лихорадка | 45 (28,7) | 25 (29,4) | 0,902 |
| Кашель | 129 (82,2) | 68 (80,0) | 0,679 |
| Одышка | 20 (12,7) | 11 (12,9) | 0,979 |
| Миалгия/артралгия | 27 (17,2) | 14 (16,5) | 0,886 |
| Аносмия/агевзия | 20 (12,7) | 14 (16,5) | 0,425 |
| Тошнота/рвота | 27 (17,2) | 14 (16,5) | 0,886 |
| Диарея | 28 (17,8) | 16 (18,8) | 0,849 |
| SpO2, % | 94 [91;95] | 93 [90;95] | 0,443 |
| SpO2 ≤93%, n (%) | 73 (46,5) | 44 (51,8) | 0,489 |
| КТ легких, n (%) | 0,371 | ||
| 1 (1-24%) | 30 (19,1) | 17 (20,0) | – |
| 2 (25-49%) | 64 (40,8) | 28 (32,9) | – |
| 3 (50-74%) | 56 (35,7) | 32 (37,7) | – |
| 4 (≥75%) | 7 (4,4) | 8 (9,4) | – |
| Лабораторные показатели | |||
| Лимфоциты, ×109/л | 0,5 [0,4;0,6] | 0,5 [0,4;0,7] | 0,989 |
| Креатинин, мкмоль/л | 98,1 [90,1;113,3] | 100,5 [90,0;118,6] | 0,362 |
| СРБ, мг/л | 71,9 [53,0;122,3] | 79,2 [53,0;165,5] | 0,803 |
| D-димер, μг/мл | 0,7 [0,4;0,7] | 0,7 [0,6;1,8] | 0,009 |
| Оксигенотерапия*, n (%) | 0,048 | ||
| Не требуется | 33 (21,0) | 7 (8,2) | – |
| Через канюли | 120 (76,4) | 77 (90,6) | – |
| НИВЛ | 2 (1,3) | 0 | – |
| ИВЛ | 2 (1,3) | 1 (1,2) | – |
| Сопутств. терапия, n (%) | |||
| Антибиотики | 129 (82,2) | 77 (90,6) | 0,079 |
| НПВП | 25 (15,9) | 18 (21,2) | 0,307 |
| Фавипиравир | 13 (8,3) | 7 (8,2) | 0,990 |
| Глюкокортикостероиды | 154 (98,1) | 82 (96,5) | 0,440 |
| Гепарины | 148 (94,3) | 79 (92,9) | 0,683 |
| Длит. госпитализации, дни | 16 [13;21] | 16 [12;19] | 0,533 |
Распространенность вирусной пневмонии в группах пациентов, получавших олокизумаб или тоцилизумаб, также была сходной и примерно в 70% случаев соответствовала КТ-2 и КТ-3. Медиана SpО2 при поступлении была сопоставимой в двух группах (94% и 93%), как и доля пациентов, у которых этот показатель на воздухе составлял ≤93% (47,1% и 50,6%). Большинство пациентов непосредственно перед введением исследуемых препаратов нуждались в оксигенотерапии через канюли. В группе олокизумаба доля таких пациентов была ниже, чем в группе тоцилизумаба (76,4% и 90,6%, соответственно). В единичных случаях олокизумаб или тоцилизумаб вводили на фоне НИВЛ или ИВЛ. У всех больных имелись признаки синдрома гипервоспалительного ответа, в частности медиана содержания СРБ в группах олокизумаба и тоцилизумаба, составляла 71,9 и 79,2 мг/л, соответственно. Медиана количества лимфоцитов была одинаковой в двух группах (0,5 × 109/л). Примерно у трети больных в обеих группах сохранялась лихорадка (38,0°C) при медиане срока госпитализации 7 дней от начала заболевания.
Лечение. Олокизумаб был введен подкожно 157 пациен там в интервале от 1 до 18 дней после госпитализации (медиана 3 [1; 5]). У 150 из них препарат применяли в дозе 64 мг, а у 7 – 128 мг. Повторно препарат был введен 16 пациентам (во всех случаях по 64 мг). Тоцилизумаб вводили внутривенно 85 пациентам в интервале от 1 до 17 дней после госпитализации (медиана 2 [1; 5]). У 58 больных, получивших однократную инфузию препарата, доза составила 400 мг, у 9 – 200 мг, у 1 – 800 мг. Оставшиеся пациенты получали дозы 160 мг (1), 320 мг (2), 480 мг (1), 560 мг (3) и 600 мг (1). Повторно тоцилизумаб применяли у 9 больных, в том числе в дозе 400 мг у 6, 200 мг у 2 и 800 мг у 1.
Сопутствующая терапия была сходной в группах олокизумаба и тоцилизумаба, в частности практически все больные получали глюкокортикостероиды и низкомолекулярные гепарины, а большинство – антибактериальные препараты.
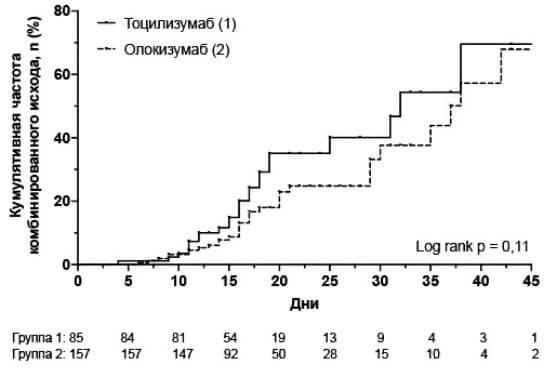
Конечные точки. Частота комбинированной первичной конечной точки, включавшей в себя перевод на ИВЛ и смерть, как и частота обоих ее компонентов в группе олокизумаба была несколько ниже, чем в группе тоцилизумаба, однако разница между группами оказалась статистически незначимой (табл. 2). Во всей выборке частота развития комбинированного исхода была достоверно выше у пациентов, получавших респираторную поддержку на момент введения препарата (27,2% против 7,5%, p=0,008). При этом частота первичной конечной точки среди пациентов, которым не требовалась или требовалась оксигенотерапия, достоверно не отличалась между группами олокизумаба и тоцилизумаба. Кумулятивная частота первичной конечной точки, которую анализировали с помощью метода Каплана-Мейера, в двух группах была сопоставимой (log rank p=0,118; рис. 1).
комбинированного исхода
(ИВЛ или смерть) в группах олокизумаба и тоцилизумаба
| Конечные точки | Группа олокизумаба | Группа тоцилизумаба | р |
|---|---|---|---|
| Примечание: *исключены пациенты, находящиеся на НИВЛ и ИВЛ на момент введения ингибитора ИЛ-6; **исключены пациенты, находившиеся на ИВЛ на момент введения исследуемого препарата | |||
| ИВЛ или смерть | |||
| Вся когорта | 33/157 (21,0) | 25/85 (29,4) | 0,144 |
| Не нуждавшиеся в O2 | 3/33 (9,1) | 0/7 (0,0) | 0,407 |
| Получавшие O2 | 30/124 (24,2) | 25/78 (32,1) | 0,222 |
| Перевод на НИВЛ* | 7/153 (4,7) | 5/84 (6,0) | 0,644 |
| Перевод на ИВЛ** | 31/155 (20,0) | 22/84 (26,2) | 0,319 |
| Смерть | 30/157 (19,1) | 25/85 (29,4) | 0,068 |
По данным логистического регрессионного анализа, факторами, ассоциировавшимися с увеличением риска интубации или смерти, были возраст, сахарный диабет и необходимость в респираторной поддержке перед введением исследуемых препаратов (табл. 3). В то же время в многофакторной модели с поправкой на различные факторы, включая возраст и оксигенотерапию, выбор между олокизумабом или тоцилизумабом не оказывал влияния на шансы достижения первичной конечной точки (ОШ 0,58; 95% ДИ 0,27-1,23). Медиана длительности госпитализации в двух группах была одинаковой (16 дней).
| Факторы | Однофакторный анализ | Многофакторный анализ | ||
|---|---|---|---|---|
| ОШ (95% ДИ) | р | ОШ (95% ДИ) | р | |
| Примечание: многофакторный анализ по всем признакам с поправкой на возраст и респираторную поддержку |
||||
| Мужской пол | 0,68 [0,38-1,23] | 0,203 | – | – |
| Возраст, годы | 1,07 [1,04-1,10] | <0,001 | 1,07 [1,03-1,11] | <0,001 |
| Ожирение | 0,93 [0,52-1,68] | 0,819 | – | – |
| Артериальная гипертония | 1,15 [0,52-2,53] | 0,732 | – | – |
| Ишемическая болезнь сердца | 0,98 [0,40-2,41] | 0,970 | – | – |
| Инфаркт миокарда в анамнезе | 1,38 [0,34-5,51] | 0,649 | – | – |
| Фибрилляция предсердий | 0,69 [0,27-1,75] | 0,438 | – | – |
| Инсульт в анамнезе | 0,18 [0,02-1,54] | 0,119 | – | – |
| Сахарный диабет | 2,27 [1,22-4,30] | 0,012 | 3,56 [1,58-8,05] | 0,002 |
| Хронические заболевания легких | 2,62 [1,31-5,22] | 0,006 | 1,34 [0,59-3,09] | 0,485 |
| ХБП 3-4 стадии | 0,79 [0,16-3,81] | 0,765 | – | – |
| Хронические заболевания печени | 0,44 [0,05-3,68] | 0,452 | – | – |
| Солидные опухоли и гемобластозы | 1,65 [0,59-4,62] | 0,408 | – | – |
| Ревматические заболевания | 1,64 [0,54-5,04] | 0,384 | – | – |
| Респираторная поддержка | 4,61 [1,37-15,58] | 0,014 | 5,67 [1,11-28,91] | 0,037 |
По данным логистического регрессионного анализа, факторами, ассоциировавшимися с увеличением риска интубации или смерти, были возраст, сахарный диабет и необходимость в респираторной поддержке перед введением исследуемых препаратов (табл. 3). В то же время в многофакторной модели с поправкой на различные факторы, включая возраст и оксигенотерапию, выбор между олокизумабом или тоцилизумабом не оказывал влияния на шансы достижения первичной конечной точки (ОШ 0,58; 95% ДИ 0,27-1,23). Медиана длительности госпитализации в двух группах была одинаковой (16 дней).
Обсуждение
Результаты нашего ретроспективного исследования свидетельствуют о том, что подкожное введение олокизумаба по эффективности в профилактике интубации и смерти не уступает внутривенному введению тоцилизумаба у госпитализированных больных с COVID-19, осложненным синдромом иммунного гипервоспалительного ответа. Частота комбинированной первичной конечной точки, включавшей интубацию и смерть от любых причин, в группе олокизумаба была недостоверно ниже, чем в группе тоцилизумаба. Вероятно, это было связано с тем, что олокизумаб несколько чаще вводили на более раннем этапе (т.е. при отсутствии потребности в оксигенотерапии), чем тоцилизумаб, в то время как частота сахарного диабета, ухудшающего прогноз при COVID-19, была выше во второй группе. В логистической регрессионной модели как необходимость в респираторной поддержке, так и сахарный диабет ассоциировались с достоверным увеличением риска перевода на ИВЛ и смерти у обследованных пациентов с COVID-19. Тем не менее, две группы пациентов не отличались по другим показателям, сопровождающимся увеличением риска тяжелого течения заболевания, а сопоставимая эффективность олокизумаба и тоцилизумаба в профилактике неблагоприятных исходов COVID-19 была подтверждена при многофакторном регрессионном анализе. Сходные данные были ранее получены и другими авторами [14].
Практически все больные, включенные в наше исследование, получали ингибиторы ИЛ-6 в сочетании с глюкокортикостероидами. В рандомизированном контролируемом исследовании RECOVERY, в которое были включены более 4000 пациентов с COVID-19 ассоциированной пневмонией, сопровождавшейся гипоксией и увеличением содержания СРБ ≥75 мг/л, достоверное снижение риска смерти на 21% было отмечено только у больных, получавших тоцилизумаб в сочетании с глюкокортикостероидами [15]. В этом исследовании доля пациентов, которым тоцилизумаб вводили без глюкокортикостероидов, была относительно небольшой (18%), а дизайн исследования не предполагал изучение эффективности тоцилизумаба в зависимости от сопутствующей терапии. Соответственно, результаты исследования RECOVERY не позволяют сделать окончательные выводы по поводу оптимальной схемы противовоспалительной терапии у пациентов с COVID-19. Тем не менее, применение глюкокортикостероидов в сочетании с ингибиторами ИЛ-6 представляется оправданным при отсутствии явных противопоказаний, таких как декомпенсированный сахарный диабет, так как они сами по себе снижают риск неблагоприятных исходов у больных со среднетяжелым и тяжелым течением COVID-19 [16].
Мы не сравнивали сроки улучшения состояния и нормализации лабораторных показателей при подкожном введении олокизумаба или внутривенном применении тоцилизумаба, учитывая ретроспективный дизайн нашего исследования. Тем не менее, медиана длительности госпитализации в группах сравнения была одинаковой (16 дней), что косвенно свидетельствовало о сопоставимой скорости действия двух препаратов.
Несмотря на адекватную терапию, включавшую ингибиторы ИЛ-6, частота интубации и смерти в нашем исследовании была достаточно высокой и составила в целом 23,8%. Однако большинство пациентов в исследованной когорте составляли лица пожилого и старческого возраста (каждый пятый – в возрасте 80 лет и старше), у которых имелись различные сопутствующие заболевания, ассоциирующиеся с тяжелым течением COVID-19 и более высоким риском смерти, прежде всего сердечно-сосудистые заболевания, ожирение и сахарный диабет 2 типа. В исследовании RECOVERY среди 2022 больных, получавших тоцилизумаб, летальность была даже выше, чем в нашей когорте (31%), хотя среди обследованных нами пациентов было больше лиц в возрасте 70 лет и старше (47% против 35%) и меньше мужчин (50% против 66%) [15]. Кроме того, большинство пациентов, включенных в наше исследование, получали олокизумаб или тоцилизумаб на фоне оксигенотерапии, а в этой выборке частота первичной конечной точки была в 3 раза выше, чем в выборке больных, которые не нуждались во введении кислорода перед применением исследуемых препаратов (27,2% и 7,5%, соответственно).
Мы не сравнивали частоту перевода на ИВЛ и смерти при назначении ингибиторов ИЛ-6 с контролем, т.е. с группой больных, не получавших ингибиторы ИЛ-6, так как эффективность препаратов этой группы в профилактике неблагоприятных исходов у пациентов с COVID-19 установлена в рандомизированных контролируемых исследованиях. Так, в исследовании RECOVERY применение тоцилизумаба у пациентов с COVID-19 ассоциированной пневмонией привело к снижению риска смерти на 15% (отношение рисков 0,85%, 95% ДИ 0,76-0,94; р=0,0028) по сравнению с таковым на фоне стандартной терапии [15]. Среди больных, не находившихся на ИВЛ на момент рандомизации, риск интубации или смерти в течение 28 дней в группе тоцилизумаба снизился на 16% по сравнению с контролем (отношение рисков 0,84, 95% ДИ 0,77-0,92; p<0,0001). В июле 2021 года применение ингибиторов рецепторов ИЛ-6 (тоцилизумаба и сарилумаба) для лечения тяжелого COVID-19 было рекомендовано экспертами ВОЗ [17]. Основанием для этой рекомендации послужили результаты мета-анализа 27 рандомизированных контролируемых исследований препаратов этой группы у 10930 пациентов с COVID-19 (медиана возраста 61 год) [18]. Полученные данные показали, что применение ингибиторов рецептора ИЛ-6 сопровождается снижением риска смерти в течение 28 дней на 14% по сравнению с обычной терапией или плацебо (отношение шансов 0,86, 95% ДИ 0,79-0,95), а также снижением риска интубации или смерти на 23% (отношение шансов 0,77, 95% ДИ 0,70-0,85)
Как и тоцилизумаб, олокизумаб первоначально разрабатывался для лечения ревматоидного артрита. Эффективность его установлена в 24-недельном многоцентровом, двойном слепом, плацебо-контролируемом исследовании CREDO 3 у 428 пациентов с активным ревматоидным артритом, не ответивших на монотерапию метотрексатом [19]. В этом исследовании олокизумаб в дозе 64 мг подкожно каждые 2 или 4 недели в сочетании с метотрексатом достоверно превосходил плацебо в комбинации с метотрексатом по частоте ответа по критериям Американской коллегии ревматологов (ACR 20; 63,6% и 70,4% против 25,9%; p<0,0001 для обоих сравнений), а также по различным вторичным показателям эффективности. В мае 2020 г. олокизумаб был зарегистрирован для лечения пациентов старше 18 лет с ревматоидным артритом средней или высокой степени активности в комбинации с метотрексатом при недостаточной эффективности монотерапии метотрексатом или ингибиторами фактора некроза опухоли, а в июне 2020 года препарат был включен во Временные рекомендации Минздрава РФ по профилактике, диагностике и лечению COVID-19. В отличие от тоцилизумаба и сарилумаба, которые блокируют рецептор ИЛ-6, олокизумаб – это гуманизированное моноклональное IgG/k антитело, взаимодействующее с самим цитокином. Теоретически уровень блокады ИЛ-6 (рецептор или сам цитокин) может отразиться на эффективности лечения, однако результаты нашего исследования свидетельствуют об обратном. Более того, полученные нами данные подтверждают эффективность подкожного применения олокизумаба в стандартной дозе 64 мг, которая была сопоставимой с эффективностью внутривенного введения тоцилизумаба в дозе 400 мг. Тем не менее, при тяжелом течении COVID-19, когда скорость действия препарата имеет критическое значение, оправданно внутривенное введение олокизумаба, в том числе в более высокой дозе [12]. При отсутствии адекватного ответа на введение первой дозы целесообразно повторное введение олокизумаба.
Наше исследование имеет ограничения. Ретроспективный дизайн его не позволял учесть все факторы, которые могли оказать влияние на исходы COVID-19 у обследованных больных, хотя группы олокизумаба и тоцилизумаба были сопоставимы по демографическим и большинству клинических показателей, а сходное влияние двух препаратов на риск неблагоприятных исходов было подтверждено при многофакторном регрессионном анализе, который проводили с поправкой на пол, возраст и другие параметры. Практически все больные группы сравнения получали тоцилизумаб в фиксированной дозе 400 мг, хотя дозу препарата рекомендуется подбирать в зависимости от массы тела. Например, в исследовании RECOVERY доза тоцилизумаба у пациентов с массой тела >90 кг составляла 800 мг, от >65 кг до 90 кг – 600 мг и от >40 кг до ≤65 кг – 400 мг [15]. Однако дефицит тоцилизумаба, наблюдавшийся через несколько месяцев после начала пандемии не только в России, но и других странах, не позволял широко применять этот препарат в более высокой дозе. При этом доза 400 мг примерно соответствует нижней границе рекомендуемой во временных рекомендациях дозы тоцилизумаба, подобранной по массе тела (4-8 мг/кг) [12]. Кроме того, результаты отдельных исследований свидетельствуют о том, что у больных с COVID19 фиксированная доза тоцилизумаба 400 мг по эффективности не уступает дозе 8 мг/кг [20]. Нельзя также исключить, что гипотетический прирост эффективности тоцилизумаба при назначении более высокой дозы у пациентов пожилого и старческого возраста, получающих глюкокортикостероиды и нуждающихся в респираторной поддержке, может нивелироваться увеличением риска развития бактериальных инфекций. Как указано выше, мы не оценивали динамику температуры тела и лабораторных показателей, в частности СРБ, в двух группах, так как ключевым показателем эффективности любой патогенетической терапии COVID-19 у госпитализированных больных является снижение риска перевода на ИВЛ и смерти. Более того, быстрое снижение содержания СРБ при введении ингибиторов ИЛ-6 не исключает возможность прогрессирования дыхательной недостаточности у пациентов с COVID-19 и, соответственно, не может служить адекватным показателем эффективности лечения.
Заключение
В нашем исследовании, проводившемся в условиях обычной клинической практики, подкожное введение олокизумаба, блокирующего ИЛ-6, по эффективности в профилактике интубации и смерти у пациентов с синдромом иммунного гипервоспалительного ответа, вызванного SARS-CoV-2, не уступало внутривенному введению тоцилизумаба.
Используемые источники
- Глыбочко П.В., Фомин В.В., Моисеев С.В. и др. Исходы у больных с тяжелым течением COVID-19, госпитализированных для респираторной поддержки в отделения реанимации и интенсивной терапии. Клин фармакол тер 2020;29(3):25-36 [Glybochko P, Fomin V, Moiseev S, et al. Clinical outcomes of patients with COVID-19 admitted for respiratory support to the intensive care units in Russia. Klinicheskaya farmakologiya i terapiya = Clin Pharmacol Ther 2020;29(3):25-36 (In Russ.)].
- Mehta P, McAuley DF, Brown M, et al. COVID-19: consider cytokine storm syndromes and immunosuppression. Lancet 2020;395:1033–4.
- Насонов Е.Л. Иммунопатология и иммунофармакотерапия коронавирусной болезни 2019 (COVID-19): фокус на интерлейкин 6. Научно-практическая ревматология. 2020;58(3):245-61 [Nasonov EL. Immunopathology and immuno pharmacotherapy of coronavirus disease 2019 (COVID-19): focus on interleukin-6. Nauchno-Prakticheskaya Revmatologiya = Rheumatology Science and Practice 2020;58(3):245-61 (In Russ.)].
- Caricchio R, Gallucci M, Dass C, et al. Preliminary predictive criteria for COVID-19 cytokine storm. Ann Rheum Dis 2021;80(1):88-95.
- Udomsinprasert W, Jittikoon J, Sangroongruangsri S, Chaikledkaew U. Circulating levels of interleukin-6 and interleukin-10, but not tumor necrosis factoralpha, as potential biomarkers of severity and mortality for COVID-19: systematic review with meta-analysis. J Clin Immunol 2021;41(1):11-22.
- Tenforde MW, Self WH, Adams K, et al.; Influenza and Other Viruses in the Acutely Ill (IVY) Network. Association between mRNA vaccination and COVID19 hospitalization and disease severity. JAMA 2021;326:2043-54.
- Надточеева В.Б., Буланов Н.М., Акулкина Л.А. и др. Эффективность вакцины Гам-КОВИД-Вак (Спутник V) в профилактике тяжелого течения
COVID-19 и смерти у госпитализированных взрослых пациентов. Клин фармакол тер 2022;31(2):20-6 [Nadtocheeva V, Bulanov N, Akulkina L, et al. Outcomes of breakthrough COVID-19 in hospitalized adult patients vaccinated with Gam-COVID-Vac (Sputnik V). Klinicheskaya farmakologiya i terapiya = Clin Pharmacol Ther 2022;31(2):20-6 (In Russ.)]. - Luo P, Liu Y, Qiu L, et al. Tocilizumab treatment in COVID-19: a single center experience. J Med Virol 2020;92(7):814-8.
- Xu X, Han M, Li T, et al. Effective treatment of severe COVID-19 patients with tocilizumab. Proc Natl Acad Sci U S A 2020;117:10970–5.
- Фомина Д.С., Потешкина Н.Г., Белоглазова И.П. и др. Сравнительный анализ применения тоцилизумаба при тяжелых COVID-19-ассоциированных пневмониях у пациентов разных возрастных групп. Пульмонология 2020;30(2):164-72 [Fomina DS, Poteshkina NG, Beloglazova IP, et al. Compa —
rative analysis of tocilizumab in severe COVID-19-associated pneumonia in patients of different age groups. Pulmonologiya 2020;30(2):164-72 (In Russ.)]. - Новиков П.И., Бровко М.Ю., Акулкина Л.А. и др. Эффективность и безопасность олокизумаба, ингибирующего интерлейкин-6, в лечении COVID19 у госпитализированных пациентов. Клин фармакол тер 2022;32(2):51-6 [Novikov P, Brovko M, Akulkina L, et al. Efficacy and safety of olokizumab, interleukin-6 inhibitor, in hospitalized patients with COVID-19. Klinicheskaya farmakologiya i terapiya = Clin Pharmacol Ther 2022; 31(2):51-6 (In Russ.)].
- Временные методические рекомендации. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 15
(22.02.2022). - Lameire NH, Levin A, Kellum JA, et al. Harmonizing acute and chronic kidney disease definition and classification: report of a Kidney Disease: Improving Global Outcomes (KDIGO) Consensus Conference. Kidney Int 2021;100(3):516-26.
- Бобкова С.С., Жуков А.А., Проценко Д.Н. и др. Сравнительная эффективность и безопасность применения препаратов моноклональных антител к ИЛ-6 упациентов с новой коронавирусной инфекцией COVID-19 тяжелого течения. Ретроспективное когортное исследование. Вестник интенсивной терапии им. А.И. Салтанова 2021;1:69–76 [Bobkova SS, Zhukov AA, Protsenko DN, et al. Comparative study of monoclonal anti-IL6 antibodies in severe new coronavirus disease COVID-19 patients. Annals of Critical Care 2021;1:69–76 (In Russ.)].
- RECOVERY Collaborative Group. Tocilizumab in patients admitted to hospital with COVID-19 (RECOVERY): a randomised, controlled, open-label, platform trial. Lancet. 2021;397:1637-45.
- RECOVERY Collaborative Group, Horby P, Lim WS, Emberson JR, et al. Dexamethasone in hospitalized patients with Covid-19. N Engl J Med 2021;384(8):693-704.
- World Health Organization. Therapeutics and COVID-19. Living Guideline, 6 July 2021.
- WHO Rapid Evidence Appraisal for COVID-19 Therapies (REACT) Working Group, Shankar-Hari M, Vale CL, Godolphin PJ, et al. Association between administration of IL-6 antagonists and mortality among patients hospitalized for COVID-19: A meta-analysis. JAMA 2021;326(6):499-518.
- Nasonov E, Fatenejad S, Feist E, et al. Olokizumab, a monoclonal antibody against interleukin 6, in combination with methotrexate in patients with rheumatoid arthritis inadequately controlled by methotrexate: efficacy and safety results of a randomised controlled phase III study. Ann Rheum Dis 2022;81:469-79.
- Stukas S, Goshua G, Kinkade A, et al. Reduced fixed dose tocilizumab 400 mg IV compared to weight-based dosing in critically ill patients with COVID-19: A before-after cohort study. Lancet Reg Health Am. 2022 Mar 23:100228.
Версия на английском языке