Дезинтегранты и супердезинтегранты — широко известный вид вспомогательных веществ, которые используются в пероральных лекарственных формах. Они способствуют дезинтеграции таблеток и содержимого капсул при помещении в водную среду. Дезинтеграция — это процесс дробления лекарственной формы на более мелкие частицы для увеличения площади поверхности. Этот этап очень важен, поскольку распад таблетки может определять доступность лекарства для растворения и последующего всасывания. Существует множества факторов, влияющих на распад лекарственной формы в зависимости от рецептуры: концентрация дезинтегранта, тип матрицы таблетки, растворимость матрицы таблетки, твердость таблетки, дозировка активного фармацевтического ингредиента (АФИ), свойства АФИ, пористость таблетки и рабочий механизм. Основными механизмами дезинтеграции являются эффект набухания, капиллярный эффект и деформация.
Механизмы действия
Усиление дезинтеграции может быть достигнуто путем добавления в рецептуру дезинтегранта или супердезинтегранта. Исследователи выдвигают теории о пяти механизмах действия (супер-) дезинтегрантов: теплота смачивания, отталкивание частиц, капиллярный эффект, эффект набухания и восстановление деформации (Carmella et al., 1988, Bele & Derle, 2012). Считается, что за действие дезинтегрирующих веществ отвечает не один механизм: дезинтеграция является результатом взаимосвязи между несколькими механизмами. Наиболее общепризнанными механизмами считаются эффект набухания, капиллярный эффект и обратимая деформация (Joshi et al., 2015).
Эффект набухания
Наиболее распространенным механизмом распада таблетки является эффект набухания. Набухание происходит в результате впитывания раствора. Это связано с многомерным расширением, при котором частицы увеличиваются во всех направлениях, создавая внутреннее давление. Это давление раздвигает соседние частицы, и матрица разрушается из-за снижения адгезии между компонентами (Desai, Liew & Heng, 2016).
При использовании дезинтегрантов, работающих по типу набухания, следует учитывать влияние пористости таблетки на ее распадаемость. Пористая матрица таблеток с большими пустотами может препятствовать процессу набухания, тем самым снижая эффективность выбранного дезинтегранта. С другой стороны, плотные материалы с низкой пористостью могут препятствовать проникновению жидкости в таблетку, таким образом тоже замедляя процесс ее распада (Desai, Liew & Heng, 2016).
Капиллярный эффект (впитывание)
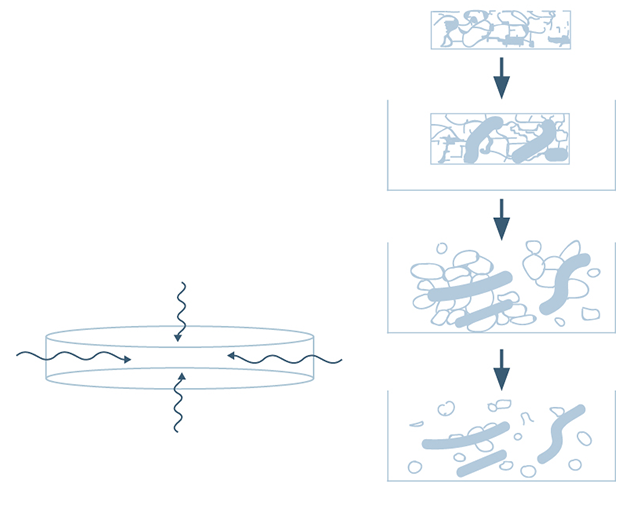
Капиллярный эффект создается при наличии в таблетке гидрофильных компонентов, способствующих впитыванию воды. Именно благодаря капиллярному эффекту вода проникает в таблетку через пористую структуру дезинтегранта. Дезинтегранты со слабыми связующими свойствами и низкой прессуемостью придают таблетке пористость, обеспечивая возможностью проникновения внутрь жидкости (Mohanachandran, Sindhumol, & Kiran, 2011). При впитывании воды физические связи между структурными компонентами лекарственной формы уменьшаются, и матрица разрушается, как показано на рисунке 1.
Обратимая деформация
Обратимая деформация возникает в результате пластической деформации дезинтегрантов, которые считаются эластичными по своей природе. Во время сжатия частицы таких дезинтегрантов деформируются с образованием межчастичных связей. Однако при попадании в водную среду такие уплотненные дезинтегранты частично восстанавливают первоначальную форму за счет механической активации (Desai, Liew & Heng, 2016). При возврате в исходное состояние внутри матрицы таблетки создается давление, приводящее к ее распаду (Shihora & Panda, 2011).
В качестве примера дезинтегранта с таким механизмом действия можно привести Solani amylum – нативный картофельный крахмал. Его можно использовать в рецептуре таблеток в концентрации от 3 до 15% по весу. Использование Solani amylum наиболее эффективно при высоком давлении прессования, так как оно способствует более высокой степени деформации его частиц, и, соответственно, более активному восстановлению деформации при контакте с водной средой (Szabó-Révész & Szepes, 2009).
Супердезинтегранты, используемые в лекарственных формах
В научных литературных источниках дезинтегранты обычно разделяют на классические и супердезинтегранты (Moreton, 2008). В группу классических дезинтегрантов входят нативный крахмал, альгиновая кислота, ионообменные смолы и микрокристаллическая целлюлоза (МКЦ).
Термин супердезинтегранты был введен вскоре после того, как стали доступны натрия крахмал гликолят, кроскармеллоза натрия и кросповидон. Эффективность супердезинтегрантов выше по сравнению с классическими дезинтегрантами, поэтому они способствуют более быстрому распаду твердой лекарственной формы при использовании их в меньшем количестве. Наиболее популярные супердезинтегранты крайне эффективны при низких уровнях концентрации (2-5% масс.).
Натрия крахмал гликолят – Primojel®
Первым супердезинтегрантом, появившемся на рынке, стал натрия крахмал гликолят (SSG). На рисунке 2 представлено СЭМ-фотография натрия крахмал гликолята под торговым названием Primojel® производства DFE Pharma (Германия). Primojel® получают в результате двухступенчатой реакции, взяв за основу структуру картофельного крахмала.
Первая стадия реакции включает введение поперечных связей через цепи амилозы и амилопектина, функция которых заключается в уменьшении водорастворимой фракции и вязкости замещенного крахмала в воде. Сшивки в натрий крахмал гликоляте обеспечивают большое расстояние между цепями, облегчая проникновение воды и набухание. Вторая стадия – карбоксиметилирование. Она включает в себя замещение гидроксильных групп группами карбоксиметилового эфира натрия. Это замещение разрывает водородные связи в структуре полимера, обеспечивая ему способность поглощать большое количество воды без образования геля.
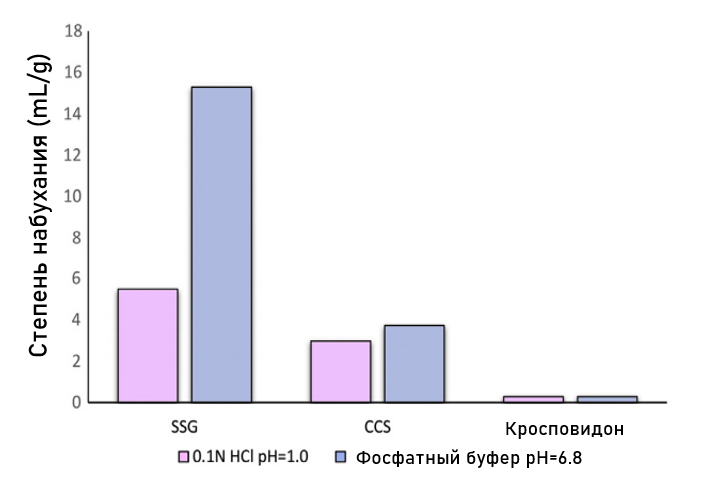
Благодаря своей уникальной структуре SSG имеет самый высокий показатель набухания по сравнению с другими типами супердезинтегрантов (см. Рисунок 3). Primojel® может впитывать количество воды в 20 раз превышающее его собственный вес и набухает в трех измерениях. Быстрое проникновение воды в таблетку и сильное набухание приводят к ее быстрому распаду.
За счет эффекта набухания Primojel® лучше всего подходит для нерастворимых матриц. При наличии растворимых или частично растворимых компонентов в матрице она растворяется, таким образом лишая дезинтегрант компонентов для воздействия, что приводит к снижению его эффективности (Moreton, 2008).
Кроскармеллоза натрия – Primellose®
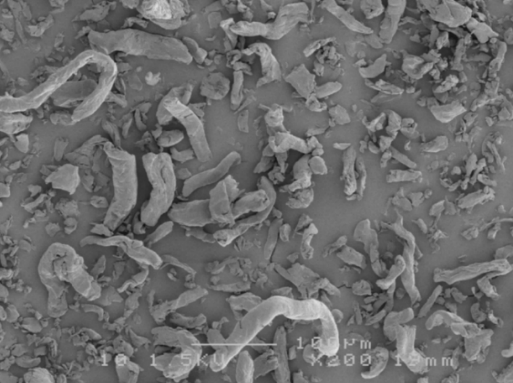
Кроскармеллоза натрия (CCS) представляет собой сетчатый полимер карбоксиметилцеллюлозы. Он производится из высококачественной древесной массы или хлопкового листа. На рисунке 4 – снимок Primellose®, произведенной из хлопка.
Производство Primellose® начинается с карбоксиметилирования цепей целлюлозы. Эта стадия уменьшает водородные связи в цепях целлюлозы, что приводит к формированию пористой структуры. Второй этап – сшивание, которое в этом случае осуществляется не внешним агентом, а через некоторые карбоксиметильные группы самой структуры. Степень сшивки влияет на два свойства дезинтегранта, а именно: содержание водорастворимого вещества и объем осаждения. Оба этих параметра снижаются при увеличении количества поперечных связей.
Кроскармеллоза натрия частично действует через эффект набухания, но набухает только в двух направлениях (Mohanachandran, Sindhumol & Kiran, 2011). Основным механизмом работы CCS является создание капиллярного эффекта, о чем свидетельствует волокнистая форма ее частиц. Длинные волокна будут функционировать на большем расстоянии в матрице таблетки, таким образом способствуя ее разрушению на большем расстоянии, чем частицы кросповидона или SSG (Moreton, 2008).
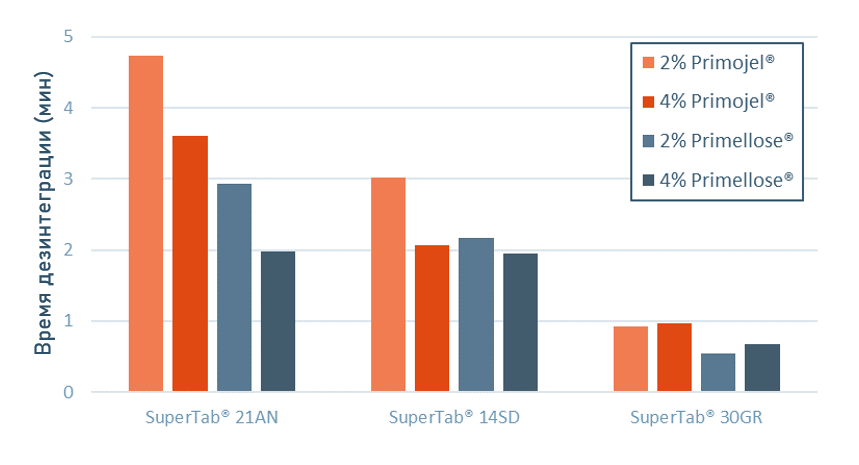
На рисунке 5 приведено сравнение времени распада таблеток с плацебо из лактозы с различными концентрациями SSG (Primojel®) и CCS (Primellose®). Для достижения наименьшего времени дезинтеграции в растворимых матрицах зачастую наиболее эффективна кроскармеллоза. На графике также показано влияние наполнителя-связующего на дезинтеграцию таблетки. Когда дезинтеграция таблетки имеет решающее значение, в качестве предпочтительного наполнителя-связующего выступает гранулированный сорт лактозы – SuperTab® 30GR производства DFE Pharma (Германия).
Кросповидон
Кросповидон представляет собой сшитый поливинилполипирролидон. Этот полимер также известен как полимер «попкорн», поскольку он обладает схожей с попкорном выпуклой структурой, как показано на рисунке 6.
Производство кросповидона осуществляется путем полимеризации с разветвлением винилпирролидона (Barabas & Adeyeye, 1996). Этот процесс происходит через свободный радикал, который может образовываться при разрыве некоторых полимерных цепей, или может быть введен с помощью инициатора свободнорадикальной полимеризации. Рост цепей может быть инициирован в нескольких точках и, следовательно, он не ограничивается одним положением, что часто приводит к высокой степени сшивки.
Ученые до сих пор не пришли к единому мнению относительно механизма действия кросповидона. Одни исследователи выдвигают предположение о механизме капиллярного эффекта с последующим вторичным набуханием (Kornblum & Stoopak, 1973), в то время как другие считают, что ключевым механизмом распада является образование высокого давления при набухании (Shu et al., 2002). Обратимая деформация также упоминается в литературе как основной механизм дезинтегрирующего действия кросповидона (Quodbach et al., 2014). Хотя точный механизм работы не до конца исследован, кросповидон обычно считается очень эффективным супердезинтегрантом. Однако существенный недостаток кросповидона заключается в том, что он может содержать следы формальдегида и пероксидов, которые могут привести к нежелательным последствиям при совмещении с другими компонентами в составе смеси (Morton, 2008).
Что следует учитывать при выборе типа дезинтегранта
Дезинтеграция таблетки — это сложный процесс, на который влияют многие факторы, такие как способ действия дезинтегранта, его концентрация, тип матрицы таблетки, ее растворимость, твердость, пористость таблетки, дозировка и свойства АФИ (Shihora & Panda, 2011). Из-за взаимодействия этих факторов невозможно предсказать, какой тип дезинтегранта обеспечит самый быстрый распад в конкретной рецептуре (Shegokar & Wiebinga, 2015).
Рекомендации по выбору разрыхлителей иногда основываются на растворимости матрицы таблетки. Набухающий супердезинтегрант, такой как Primojel®, обычно предпочтителен для нерастворимых матриц. Однако в растворимых матрицах эффект дезинтеграции при использовании данного дезинтегранта может снижаться, поскольку растворение необходимых компонентов матрицы приводит к снижению количества частиц, с помощью которых осуществляется его действие (Moreton, 2008). Для растворимых матриц часто рекомендуют разрыхлители с механизмом действия через капиллярный эффект, например, продуктом выбора может быть Primellose®, так как он обеспечивает быстрое распределение воды по матрице таблетки, ускоряя растворение ее растворимых компонентов.
Разработчики зачастую принимают окончательное решение, основываясь на своем опыте и знаниях в области химии, а не на функциональности. Основной целью специалистов должно быть создание надежной, безопасной, эффективной и высококачественной рецептуры. Надежной рецептурой считается та, которая легко адаптируется к типичным качественным вариациям АФИ, наполнителя и процесса, без ущерба для производства, стабильности или характеристик конечного продукта. Для этих целей лучше всего использовать стабильные вспомогательные вещества с высокой степенью однородности от партии к партии, чтобы сократить затраты и время разработки. Primojel® и Primellose® производства компания DFE Pharma — это супердезинтегранты с подтвержденной стабильностью значимых функциональных характеристик качества продукта.
Вывод
Дезинтеграция таблеток обеспечивает доступность лекарственного средства для растворения и последующего всасывания. Супердезинтегранты способствуют распаду твердой лекарственной формы и могут обладать различными механизмами действия, включая эффект набухания и капиллярный эффект. Разработчик должен владеть знаниями о механизмах работы различных типов дезинтегрантов. Primojel® – натрий крахмал гликолят – супердезинтегрант, обладающий наивысшим показателем степени набухания среди супердезинтегрантов и способный поглощать количество воды более чем в 20 раз превышающее его собственный вес.
Primellose® — это кроскармеллоза натрия, волокнистые частицы которой позволяют жидкости быстро проникать в структуру таблетки благодаря капиллярному эффекту.
Ключевой характеристикой для всех дезинтегрантов является их способность обеспечивать стабильно эффективную дезинтеграцию. Супердезинтегранты Primojel® и Primellose® производства компании DFE Pharma – вспомогательные фармингредиенты с доказанной однородностью от партии к партии по ключевым качественным характеристикам.
Автор статьи: Pauline H.M. Janssen and Frank Fox
DFE Pharma, Kleverstrasse 187, Goch, Germany
Перевод и редакция: ЗАО “ФПК ФармВИЛАР”

производства компании DFE Pharma,
а также по вопросам предоставления образцов
обращайтесь в ЗАО “ФПК ФармВИЛАР”
по электронной почте: RND@pharmvilar.ru
или по телефону: +7 (499) 372 13 23
www.pharmvilar.ru
Список использованных источников
- Barabas, E. S., & Adeyeye, C. M. (1996). Crospovidone. In Analytical profiles of drug substances and excipients (Vol. 24, pp. 87-163). Academic Press.
- Bele, M. H., & Derle, D. V. (2012). Mechanism of disintegrant action of polacrilin potassium: Swelling or wicking?. Acta Pharmaceutica Sinica B, 2(1), 70-76.
- Caramella, C., Colombo, P., Conte, U., Ferrari, F., Gazzaniga, A., LaManna, A., & Peppas, N. A. (1988). A physical analysis of the phenomenon of tablet disintegration. International journal of pharmaceutics, 44(1-3), 177-186.
- Desai, P. M., Liew, C. V., & Heng, P. W. S. (2016). Review of disintegrants and the disintegration phenomena. Journal of pharmaceutical sciences, 105(9), 2545-2555.
- Joshi, Y., Mastropietro, D., Muppalaneni, S., & Omidian, H. (2015). A new approach to determining the performance of superdisintegrants. Journal of Bioactive and Compatible Polymers, 30(1), 3-16.
- Kornblum SS, Stoopak SB. A new tablet disintegrating agent: cross-linked polyvinylpyrrolidone. J Pharm Sci. 1973;62(1):43-49. 52.
- Mohanachandran, P. S., Sindhumol, P. G., & Kiran, T. S. (2011). Superdisintegrants: an overview. International journal of pharmaceutical sciences review and research, 6(1), 105-109.
- Moreton, R. C. (2008). Disintegrants in tableting. In Pharmaceutical Dosage Forms-Tablets (pp. 233-266). CRC Press.
- Quodbach, J., Moussavi, A., Tammer, R., Frahm, J., & Kleinebudde, P. (2014). Tablet disintegration studied by high-resolution real-time magnetic resonance imaging. Journal of pharmaceutical sciences, 103(1), 249–255. https://doi.org/10.1002/jps.23789
- Shah, U., & Augsburger, L. (2001). Evaluation of the functional equivalence of crospovidone NF from different sources. I. Physical characterization. Pharmaceutical development and technology, 6(1), 39-51.
- Shegokar, J. & Wiebinga, C. Eye on Excipients. As appeared in Tablets & Capsules October 2015.
- Shihora, H., & Panda, S. (2011). Superdisintegrants, utility in dosage forms: a quick review. JPSBR, 1(3), 148-153.
- Shu, T., Suzuki, H., Hironaka, K., & Ito, K. (2002). Studies of rapidly disintegrating tablets in the oral cavity using co-ground mixtures of mannitol with crospovidone. Chemical and pharmaceutical bulletin, 50(2), 193-198.
- Szabó-Révész, P., & Szepes, A. (2009). Potato Starch in Pharmaceutical Technology–A Review.
- Zarmpi, P., Flanagan, T., Meehan, E., Mann, J., & Fotaki, N. (2017). Biopharmaceutical aspects and implications of excipient variability in drug product performance. European Journal of Pharmaceutics and Biopharmaceutics, 111, 1-15.
- Zhao, N., & Augsburger, L. L. (2005). Functionality comparison of 3 classes of superdisintegrants in promoting aspirin tablet disintegration and dissolution. AAPS pharmscitech, 6(4), E634-E640.
- /
- /
| CAS | 9063-38-1 |
| Брутто формула | C10H19NaO8 |
| Производитель | Silverline chemicals (Индия) |
| Упаковка | 25 кг |
| Срок годности | 5 лет c даты производства |
Производитель: Silverline chemicals (Индия)
Фармацевтика и ветеринария
Вспомогательное:
- Набухающий супердезинтегрант для нерастворимой матрицы таблеток, капсул и гранул.
БАД и Спортивное питание
Вспомогательное:
- Набухающий супердезинтегрант для нерастворимой матрицы таблеток, капсул и гранул.
| Параметр | Спецификация |
| Описание | Белый или почти белый, мелкий, сыпучий порошок, очень гигроскопичный |
| Растворимость | Практически не растворим в метиленхлориде, образует полупрозрачную суспензию в воде |
| Микроскопическое исследование | Исследование под микроскопом соответствует описанию BP, получен из картофельного крахмала с помощью сшивающего агента |
| Микроскопическое исследование | |
| A. ИК — спектроскопия | 5,5 — 7,5 |
| B | Образуется суспензия, оседающая после отстаивания |
| C | Раствор окрашивается в синий или фиолетовый цвет |
| D | Образуется плотный белый осадок |
| Внешний вид раствора | Раствор прозрачный и бесцветный |
| pH | 5,5 — 7,5 |
| Гликолят натрия | ≤ 2,0 |
| Хлорид натрия | ≤ 7,0 |
| Железо | ≤ 20 ppm |
| Потеря в массе при высушивании | ≤ 10 % |
| Анализ | 2,8 — 4,2 % |
| Микробиологическая чистота | |
| Escherichia coli Кишечная палочка |
Не обнаружена |
| Salmonella spp. Сальмонелла |
Не обнаружена |
| Остаточное количество растворителей | Растворители отсутствуют |
| Тяжелые металлы | ≤ 0,002 % |
Натрия крахмал гликолят — вспомогательное вещество, набухающий супер-дезинтегрант для производства таблеток. Идеально подходит для нерастворимой матрицы таблетки или капсулы, используется для создания гелей. Быстро набухает и абсорбирует воду, обладает более высокой текучестью по сравнению с крахмалом, увеличивает биодоступность активных веществ, помогает уменьшить размер таблетки. Используется в спортивном питании и биологически активных добавках (БАД). Натрия крахмал гликолят, поставляемый компанией Фарм Виа, произведен из картофельного крахмала и соответствует стандартам Британской фармакопеи (BP).
Эксципиент (фармакологически неактивное вещество)
Что это?
Крахмал гликолят натрия представляет собой натриевую соль карбоксиметилового эфира. Крахмальные гликолаты имеют рисовое, картофельное, пшеничное или кукурузное происхождение. Гликоат крахмала натрия представляет собой порошок от белого до почти белого цвета, без вкуса, без запаха, относительно свободно текучий.
Крахмал гликолят натрия используется в качестве наполнителя фармацевтического качества для таблеток и капсул. Крахмал гликолят натрия быстро впитывает воду, что приводит к набуханию, что приводит к быстрому распаду таблеток и гранул. Он используется в качестве дезинтегранта, суспендирующего агента и гелеобразующего агента. Без разрыхлителя таблетки могут не растворяться надлежащим образом и могут влиять на количество поглощенного активного ингредиента, тем самым снижая эффективность. 1 2
1 1 Дейв RH. Обзор фармацевтических наполнителей, используемых в таблетках и капсулах. Темы наркотиков (онлайн). Advanstar. 24.10.2008 http://drugtopics.modernmedicine.com/drugtopics/Top+News/Overview-of-pharmaceutical-excipients-used-in-tabl/ArticleStandard/Article/detail/561047. Доступ 19/19/2011
2 Формулировка. Наполнители. Крахмал натрия гликолят. 2004. http://www.pformulate.com/nastgly.htm По состоянию на 17 октября 2011 г.
Натрия крахмал гликолят
Explosol является натриевой солью карбоксиметилированного крахмала (Натрия крахмал гликолят) и получается путем частичной этерификации гидроксильных групп, содержащихся в молекулах картофельного крахмала. Данная реакция приводит к образованию эксципиента, выполняющего функцию супердезинтегранта. Продукт соответствует требованиям EP, USP/NF, BP, DAB.
Области применения:
Механизм дезинтеграции таблеток, капсул и гранул с натрием крахмал гликолятом заключается в способности данного эксципиента быстро поглощать воду и набухать. Благодаря своей универсальности, Explosol эффективен во многих рецептурах и различных процессах производства ТЛФ (влажная/сухая грануляция, прямое прессование).
В случае влажной грануляции возможно применение Explosol как до увлажнения, так и после.
Рекомендации по применению натрия крахмал гликолята:
- Хорошие результаты по распадаемости наблюдаются при концентрациях 0,5-8%. Однако концентрацию можно изменять в зависимости от особенностей рецептуры.
- Лабораторные исследования рецептур с Explosol, получаемых путем влажной грануляции, показывают оптимальные результаты при использовании равных частей эксципиента внутри и снаружи гранул.
- При влажной грануляции более быстрая дезинтеграция будет наблюдаться при использовании Explosol после увлажнения (снаружи гранул), чем при его использовании до увлажнения (внутри гранул).
- При возникновении проблем, связанных с профилем растворения, половина дозировки Explosol может быть внесена до увлажнения, а другая – сразу после образования гранулята, до добавления лубриканта.
По вопросам приобретения Натрия крахмал гликолят и получения подробной консультации по свойствам продукции, условиям поставки и заключению договора просим Вас обратиться к менеджерам.
Sodium starch glycolate, for example, is a starch often used in medication that can be sourced from a variety of ingredients and therefore can contain gluten.
From: Gluten-Related Disorders, 2022
Material Attributes and Their Impact on Wet Granulation Process Performance
Praveen Hiremath, … Vivek Agrahari, in Handbook of Pharmaceutical Wet Granulation, 2019
2.7.2 Sodium Starch Glycolate (SSG)
SSG is the sodium salt of cross-linked carboxymethyl starch. SSG is derived from starch with two chemical modifications: substitution (to increase hydrophilicity) and cross-linking (to reduce solubility and gel formation upon contact with water) (Shah & Augsburger, 2002). SSG acts as a superdisintegrant through rapid swelling because of the adsorption of large amounts of water leading to faster disintegration (Desai, Er, Liew, & Heng, 2014). Also, because of its spherical shape, SSG can have good flow properties.
Different grades of SSG are available according to particle size distribution, sodium chloride percentage, and pH. The amount of sodium in SSG is established between 2.8% and 4.2% in USP, whereas the degree of substitution (carboxymethyl groups) is not specified (Sodium Starch Glycolate. USP 39-NF 34, Rockville, MD, USA, 2016). Values for the degree of substitution between 0.23 and 0.32 have been reported (Zarmpi et al., 2017). Hydration and swelling of SSG are related to the degree of substitution. An increase in swelling and water uptake was observed as substitution increased from 0.20 to 0.29 and opposite effects were seen at higher substitution (Rudnic, Kanig, & Rhodes, 1985). A higher degree of substitution also can lead to increasing drug-excipient interactions of weakly basic drugs because the drug can be adsorbed onto the polymer (Narang et al., 2012).
The differences in the disintegration and dissolution properties of SSG were attributed to changes in the degree of cross-linking and extent of carboxymethylation (induces hydrophilicity by disrupting hydrogen bonding and allowing water access to the molecules). Disintegration efficiency has been inversely related to its level of cross-linking. Because carboxymethylation and cross-linking have opposing effects on water solubility, water access, and viscosity, a balance between the two is important for optimal performance. The phosphate group based cross-linking in SSG leads to a high spacing between SSG chains, facilitating water penetration and swelling, and reduces the gel formation (Rojas, Guisao, & Ruge, 2012). The extended swelling of SSG is attributed to phosphate cross-linking compared to the esterification in CCS, which does not allow this high spacing between the polymer chains. An increase of 25%–35% of crosslinking leads to powders with increased swelling and water uptake, but further increase in crosslinking leads to lower swelling and water uptake (Zarmpi et al., 2017).
Particle size also affects the functionality of SSG with larger particles being more efficient. A three-fold increase in particle size of SSG resulted in a proportional decrease in the disintegration time (Smallenbroek et al., 1981). As the particle size decreased, a more viscous layer is formed because of increased interaction with water, creating a barrier for drug diffusion and leading to delayed dissolution. A typical amount of SSG used in drug formulation ranges between 2% and 8% w/w (Rowe et al., 2009). SSG at higher levels (> 8% of tablet weight) causes an increase in disintegration time because of the formation of a viscous layer that hinders water penetration in the formulation (Desai et al., 2014). The purity of SSG is also important and affects its disintegration efficiency. SSG has the impurities of sodium chloride, sodium glycolate, sodium citrate, and sodium acetate as the byproducts of the synthesis of SSG. Monochloroacetate, nitriles, and nitrates are potentially reactive impurities in SSG. Weakly basic drugs can compete with the sodium counter ion in SSG, adsorbing onto the surface of the disintegrant particles (Narang et al., 2012; Wu et al., 2011).
Read full chapter
URL:
https://www.sciencedirect.com/science/article/pii/B9780128104606000129
Effects of sodium starch glycolate disintegrant on mannitol deformation, frictional and tablet physical characteristics
Muhammad Hamizan Hidzer, … Fara Wahida Ahmad Hamidi, in Reference Module in Materials Science and Materials Engineering, 2023
4 Conclusion
The addition of sodium starch glycolate (SSG) at 10%w/w until 80%w/w negatively decreased the plastic work and tablet tensile strength values. Pure mannitol (M100) only tablets have the fastest disintegration times, however comparatively slower disintegration times were recorded at the various SSG compositions evaluated in this work. Increasing the compaction pressure improved the tablet tensile strength but negatively caused increasing frictional resistance during the ejection stage. In conclusion, SSG did not improved tablet disintegration when added to mannitol hence failed to function as a disintegrant aid for mannitol tablets, as well as decreasing the tablet mechanical strength within the experimental range employed in this current work.
Read full chapter
URL:
https://www.sciencedirect.com/science/article/pii/B978032396020500011X
Critical Material Attributes in Wet Granulation
Arvind K. Bansal, … Sneha Sheokand, in Handbook of Pharmaceutical Wet Granulation, 2019
3.3.10 Type of Disintegrants
Commonly used disintegrants in wet granulation are crospovidone, CCS, and SSG, which increase the hydrostatic pressure in the formulation when it comes in contact with water. The pressure is increased either by water wicking (for crospovidone) or swelling (CCS and SSG) phenomena. These water uptake behaviors of the disintegrants also occur during the wet granulation process and result in a reduced efficacy of disintegration in dosage forms produced thereafter, as compared to the dosage forms produced using dry granulation. The efficiency loss of disintegrants on wet granulation was studied by Zhao and Augsburger (2006). The authors reported that, when these disintegrants were wet granulated, a significant increase in disintegration time (i.e., reduction of disintegrant efficiency) was observed in tablets prepared with SSG and crospovidone, while CCS was the least affected by prewetting undergone during wet granulation. The efficiency of SSG and crospovidone showed dependence on their particle size, with a decrease in particle size tending to increase their efficiency (Zhao & Augsburger, 2006).
In another study, the effects of CCS and crospovidone on process end-point determination and drug release from the tablets were determined (Narang, 2015). Crospovidone showed a rapid and sudden granule growth with a sharp end point, whereas CCS-based formulations provided slower granule growth and a smooth end point. Both CCS- and crospovidone-based formulations showed higher initial dissolution, but storage under accelerated conditions resulted in a dissolution slowdown in the case of the crospovidone-based formulation, while no such significant change was observed in the CCS-based formulation. These studies indicated that CCS as an intragranular disintegrant is likely to provide greater process robustness as well as better stability and product performance.
Another material property related to disintegrants affecting their function is the degree of substitution and cross-linking (Rudnic, Kanig, & Rhodes, 1985). These two attributes greatly affect the water uptake capacity of the disintegrants. Additionally, the ionizable functional groups in the backbone of SSG and CCS have potential for interaction with drug substances. If the interaction is significant to the extent that drug release or bioavailability is affected, these properties can become a CMA for the drug product (Narang et al., 2012).
Read full chapter
URL:
https://www.sciencedirect.com/science/article/pii/B9780128104606000099
Conventional-Release (CR) Tablets
Reynir Eyjolfsson, in Design and Manufacture of Pharmaceutical Tablets, 2015
2.5.3 Manufacturing method
Avicel PH-102, API-50 μm, Povidone, and Primojel were placed in this order in Collette-150 bowl and mixed (mixer-I, 150 rpm, and chopper-I, 1,500 rpm) for 2 min.
Avicel PH-102, API-50 μm, Povidone, and Primojel were sieved through Comil 39R (1.0 mm).
Avicel PH-102, API-50 μm, Povidone, and Primojel were remixed in Collette-150 (mixer-I, 150 rpm, and chopper-I, 1,500 rpm) for 2 min.
Avicel PH-102, API-50 μm, Povidone, and Primojel were granulated with ethanol 96% that was sprayed into the granulator bowl during 4 min (Collette-150, mixer-I, 150 rpm, and chopper-I, 1,500 rpm) followed by unaltered mixing speeds for further 1 min.
The granulate was sieved through Comil 375Q (9.5 mm).
The granulate was dried in Freund VFC-60 (220 l) fluid bed dryer until the granulate LOD was 1.0% (specification NMT 1.1%, Mettler HG-53, 100°C). Inlet air temperature was 65°C and maximum product temperature 42°C (specification NMT 45°C).
The dry granulate was sieved through Apex B-46 (1.3 mm), 2,240 rpm, knives forward.
Magnesium stearate 5712 was sieved through Comil 18R (0.5 mm) before weighing.
The sieved granulate was placed in 112 l tumbling mixer (GEI IBC), magnesium stearate 5712 placed on top of it and mixed for 5 min at 12 rpm.
Flowability of finished granulate was 4 mm (Flodex), which is excellent.
Tablet compression was performed with Manesty Betapress using 8.3 × 17 mm elliptical/oval punches with break line. Tableting speed was 30,000 tablets/h, which progressed without any technical problems.
The product had a disintegration time of about 6 min and hardness of about 140 N. Friability was 0% and coefficient of variation in determinations of content uniformity 1.2%. A bioavailability study showed that the tablets were bioequivalent to the originator’s product.
Packaged into Al/PVC blisters and cartons the tablets have a shelf life of 4 years.
Read full chapter
URL:
https://www.sciencedirect.com/science/article/pii/B9780128021828000027
Gluten and its main food sources and other components of grains that may impact on health
Justine Bold, in Gluten-Related Disorders, 2022
Other sources of gluten
Gluten can be found in starch used as a tablet binder in medicine [19]. Sodium starch glycolate, for example, is a starch often used in medication that can be sourced from a variety of ingredients and therefore can contain gluten. Also wheat starch may be used within medication [28]. Moreover, gluten has been used in dental equipment such as prosthesis and also in toothpaste [29]. Household products like food wrap can also be made of wheat starch [29]. Gluten can also be found in children’s play equipment such as finger paints and play-dough. However, there are not many studies investigating the significance of nonfood-based exposure in CeD [29]. Furthermore, cosmetics and other skin care may contain ingredients sourced from grains, hence may feasibly contain wheat proteins and gluten. Hydrolyzed wheat protein (HWP) and wheat gluten are used in skin- and hair-conditioning agents. HWP are proteins that have been broken down, when the polypeptide lengths of the hydrolysates is 30 amino acids or less the products do not elicit allergic-type 1 immediate hypersensitivity and will not induce sensitization [30]. Common ingredients in cosmetics include Triticum vulgare wheat germ oil, T. vulgare wheat germ extract, Horedeum vulgare barley extract, Avena sativa oats [31]. A small-scale study on 14 female CeD patients with dermatitis aged between 12 and 60 years of age, undertaken in Italy demonstrated skin lesions improved when gluten products were swapped to GF skin-care products [32]. It should be noted that gluten has also been found in lipstick [29].
Read full chapter
URL:
https://www.sciencedirect.com/science/article/pii/B9780128218464000073
Printing of personalized medication using binder jetting 3D printer
Ziyaur Rahman, … Mansoor A. Khan, in Precision Medicine for Investigators, Practitioners and Providers, 2020
Controlled release preparations
Powder components may contain diluent, disintegrants, sweetener, and glidant. Most commonly used diluents are lactose, mannitol, and microcrystalline cellulose. Disintegrants examples are pregelatinized starch, crospovidone, croscarmellose sodium, and sodium starch glycolate. Silicon dioxide is most commonly used as glidant [34,35]. Polyethylene oxide, polyvinyl pyrollidone (PVP K30), lactose, mannitol, maltitol, maltodextrin, Kollidon SR, Eudragit E100, Eudragit RLPO, ethylcellulose, and hydroxypropyl methylcellulose (E50), have been investigated for designing sustained release, delayed release, and rapidly dispersible tablets by BJ [36–41].
Drug(s) can be incorporated in binder solvent or powder component, depending upon the solubility, stability, and dose of the drug. If the drug is soluble in binder solvent and the dose is low, it can be solubilized in the solvent. It is recommended to incorporate drug in powder material if it is insoluble, thermolabile, and the dose is high. Similar to the drug, polymer binders could be incorporated in powder material or binder solvent, depending upon solvent characteristics, viscosity, and quantity. Polymers investigated as binders are polylactic acid, polycaprolactone, and polyvinylpyrrolidone (K17, K25, and K30 grades) ethylcellulose. Binder solvent could be aqueous, organic (ethanol, acetone, isopropanol), or hydro-organic solvents. Solvent selection is based on the solubility of drug and binder, viscosity, and surface tension. A combination of solvents can be used to optimize the printing process parameters and quality of printed dosage forms. Water, ethanol, acetone, and chloroform are investigated for BJ process [36–42].
Read full chapter
URL:
https://www.sciencedirect.com/science/article/pii/B9780128191781000460
Erlotinib
Jody Tucker Mack, in xPharm: The Comprehensive Pharmacology Reference, 2007
Basic Chemistry
| Chemical Structure | |||||
| Structure | |||||
| Chemical Formula | C22 H23 N3 O4. Cl H | ||||
| Properties | |||||
| Physical Properties | Erlotinib tablets are available in three dosage strengths containing erlotinib hydrochloride (27.3 mg, 109.3 mg, and 163.9 mg) equivalent to 25 mg, 100 mg, and 150 mg erlotinib and the following inactive ingredients: lactose monohydrate, hypromellose, hydroxypropyl cellulose, magnesium stearate, microcrystalline cellulose, sodium starch glycolate, sodium lauryl sulfate and titanium dioxide. For product identification, the tablets also contain small amounts of color additives, including FD&C Yellow #6 (25 mg only). | ||||
| Molecular Weight | 429.902 | ||||
| Solubility | Erlotinib hydrochloride (Tarceva™) is slightly soluble in water or methanol and practically insoluble in acetonitrile, acetone, ethyl acetate and hexane. Aqueous solubility of this agent is pH dependent (solubility increases at pH <5 due to protonation of the secondary amine) with a maximum solubility of 0.4 mg/mL occurs at a pH of approximately 2. | ||||
| Ionization Constant | |||||
| Value | Salt | Conditions | Reference | Comments | |
| pKa | 5.42 | 25°C | Product Information Tarceva (2004) |
Read full chapter
URL:
https://www.sciencedirect.com/science/article/pii/B9780080552323637080
OXPIRT: Ontology-based eXpert system for Production of a generic Immediate Release Tablet
Nopphadol Chalortham, … Phuriwat Leesawat, in Formulation Tools for Pharmaceutical Development, 2013
Paracetamol
As usual, information required for input gained from preformulation study and patent reviewing is fundamental to begin the system. The information on original paracetamol is shown in Figure 8.13.
Figure 8.13. Information on a paracetamol product from preformulation study and its original patent
The IF-THEN rules related to information in Figure 8.14 are listed in Table 8.7.
Figure 8.14. OXPIRT result for a paracetamol generic product
Table 8.7. Rules used for adjustment concentration of the generic paracetamol production
| Rule | Detail of rule |
|---|---|
| I | IF < hardness of the original is more than 5.0 kg > AND < type of binder is hardest > THEN < set the concentration of binders at maximum concentration > |
| II | IF disintegration time of the original is less than or equal to 180 s > AND < type of disintegrant is super-disintegrant > THEN < set the concentration of disintegrants at maximum concentration > |
| III | IF < solubility of API is sparingly soluble or slightly soluble or very slightly soluble or practically insoluble > THEN < set the concentration of lubricant at minimum concentration > |
| IV | IF < diluent exists > THEN < fill diluent until obtain the total tablet amount > |
| V | IF < flowability of API is poor or very poor or extremely poor > AND < fracture surface is rough > AND < temperature stability is stable > AND < moisture stability is stable > AND < API concentration is more than 10%> THEN < set the process type as Wet granulation > |
OXPIRT inferred a concentration of excipients and later performed a weight calculation based on the assigned concentration and tablet weight. In this case, four ingredients, microcrystalline cellulose, corn starch, sodium starch glycolate, and magnesium stearate, were considered. First, microcrystalline cellulose was involved in Rule I shown in Table 8.7. With the rule, a concentration of microcrystalline cellulose was inferred to maximum as 15% and it was computed to weight 94.50 mg. Second, sodium starch glycolate was involved in Rule II shown in Table 8.7. With the rule, a concentration of sodium starch glycolate was inferred to maximum as 5% and it was computed to weight 31.50 mg. Third, magnesium stearate is involved in Rule III shown in Table 8.7. With the rule, a concentration of magnesium stearate was inferred to minimum as 0.2% and it was computed to weight 0.13 mg. Fourth, the diluent amount is computed based on Rule IV by the total weight minus the available remaining space from the already set ingredients (i.e. 630 ‒ (500 + 94.5 + 31.5 + 0.13) = 2.7mg). Last, the process type is set to wet granulation following Rule V. With all weight computed, OXPIRT returns a result as given in Figure 8.14.
A result of OXPIRT is required to be produced in the laboratory to examine tablet properties for standard quality control. Figures 8.15 and 8.16 show, respectively, dissolution profile and graph comparing the original and the generic version gained from Figure 8.14 and the result shows pharmaceutical equivalence as difference (f1) and similarity (f2) factors are within acceptable ranges.
Figure 8.15. Pharmaceutical equivalence result between the original and the generic paracetamol
Figure 8.16. Dissolution profile of original Tylenol® tablet and generic paracetamol tablet
Read full chapter
URL:
https://www.sciencedirect.com/science/article/pii/B9781907568992500086
Clenbuterol Hydrochloride
Abdulrahman A. Al-Majed, … Hatem A. Abdel-Aziz, in Profiles of Drug Substances, Excipients and Related Methodology, 2017
5 Stability
Signoretti et al. [57] used DSC to study the physicochemical compatibility between this drug and various excipients commonly used in manufacturing of tablets in order to improve the formulation of clenbuterol. Using this method, clenbuterol was found to be compatible with talc, stearic acid, magnesium stearate, and titanium dioxide. An incompatibility was demonstrated with maize starch, pregelatinized starch, sodium starch glycolate, polyvinylpyrrolidone, Avicel PH101, and lactose.
Martin et al. [58] studied the heat stability of clenbuterol. The drug was shown to be stable in boiling water at 100°C. However, in cooking oil at 260°C, losses were observed, indicating a half-life of about 5 min. The effect of a range of cooking processes (boiling, roasting, frying, and microwaving) on clenbuterol residues in fortified and incurred tissue was studied. No net change in the amount of clenbuterol was observed in any of the cooking processes investigated, except for deep frying using extreme conditions.
There was little observed migration from the tissue into the surrounding liquid or meat juices. Clenbuterol residues were found not to be evenly distributed in the incurred raw tissue used for the investigation. The findings of this investigation show that the data obtained from the measurements of raw tissue are applicable for use in consumer exposure estimates and dietary intake calculations.
Read full chapter
URL:
https://www.sciencedirect.com/science/article/pii/S187151251730002X
Oral pellets loaded with nanoemulsions
Thi Trinh Lan Nguyen, … Thierry F. Vandamme, in Nanostructures for Oral Medicine, 2017
1.4.3 Use of other excipients in the extrusion-spheronization process
Other excipients, such as water soluble/swellable polymers (e.g., polyvinylpyrrolidone, hydroxypropyl methylcellulose, polyethylene oxide), ionic polymers (e.g., carboxypolymethylene, chitosan, Eudragit), hydrophobic/water insoluble polymer (e.g., ethylcellulose), waxes (e.g., glyceryl monostearate, carnuba wax), disintegrants (e.g., croscarmellose sodium, sodium starch glycolate, crospovidone), and polysaccharides (e.g., starch, dextrin), are also added to the formulations containing MCC in order to attain the desired drug release characteristics from the pellets (Trivedi et al., 2007).
Some of the excipients used in combination with MCC to improve pellet disintegration and/or drug release from MCC-based pellets include surface active agents. Surfactants are added to the liquid to improve wettability by lowering the interfacial tension between the liquid and drug particles. Examples are sodium lauryl sulphate, polyethylene glycol, polysorbate 80, glyceryl and sorbitan mono-oleate, sorbitan mono-palmitate, glycerol monostearate, and self-emulsifying drug delivery systems (SEDDS) (Dukić et al., 2009).
The types and concentrations of specific excipients incorporated in the formulations depend on the specific need and the desired drug-release rates from the pellets. For example, in spite of the large surface area of pellets that provides faster absorption from this dosage form, poorly soluble drugs might require super disintegrants to compensate for the delay in drug dissolution due to the high density of pellets (Souto et al., 2005) (Table 8.1).
Table 8.1. Examples of Commonly Used Excipients
| Filler | MCC, starch and derivatives, sucrose, lactose, mannitol, dicalcium diphosphate, β-cyclodextrine, glucose |
| Binder | Gelatin, HPC, HPMC, MC, PVP, sucrose, starch, water |
| Lubricant | Calcium stearate, glycerin, PEG, magnesium stearate |
| Separating agent | Kaolin, talc, silicon dioxide |
| Disintegrant | Alginates, croscarmellose sodium, sodium starch glycolate |
| pH adjuster | Citrate, phosphate |
| Surfactant | Polysorbate 80, Solidum lauryl sulphate, polyethylene glycol, glyceryl and sorbitan monooleate, sorbitan monopalmitate, glycerol monostearate, self-emulsifying systems |
| Spheronization enhancer | MCC, sodium carboxymethyl cellulose |
| Glidant | Talc, starch, magnesium stearate |
| Release modifier | Ethyl cellulose, carnauba wax, shellac |
Read full chapter
URL:
https://www.sciencedirect.com/science/article/pii/B9780323477208000092