Наропин — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
П N014458/01
Торговое название:
Наропин® (Naropin®)
Международное непатентованное название:
ропивакаин
Химическое название:
(2S)-N-(2,6-Диметилфенил)-1-пропил-пиперидин-2-карбоксамида гидрохлорид моногидрат
Лекарственная форма:
раствор для инъекций
Состав на 1 мл
Активное вещество: ропивакаина гидрохлорид моногидрат, соответствующий 2,0 мг, 7,5 мг и 10,0 мг ропивакаина гидрохлорида.
Вспомогательные вещества: натрия хлорид 8,6 мг, 7,5 мг и 7,1 мг, соответственно, 2 М раствор натрия гидроксида и/или 2 М раствор хлористоводородной кислоты для доведения рН до 4,0 — 6,0, вода для инъекций до 1,0 мл.
Описание
Прозрачный бесцветный раствор.
Характеристика
Раствор препарата Наропин® представляет собой стерильный изотонический водный раствор, не содержит консервантов и предназначен только для однократного применения. рКа ропивакаина 8,1; коэффициент распределения – 141 (n-октанол/фосфатный буфер рН 7,4 при 25°С).
Фармакотерапевтическая группа:
местноанестезирующее средство
Код АТХ: N01BB09
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Фармакодинамика
Ропивакаин – первый местный анестетик амидного типа длительного действия, являющийся чистым энантиомером. Oбладает как анестезирующим, так и обезболивающим действием. Высокие дозы ропивакаина применяются для местной анестезии при хирургических вмешательствах, низкие дозы препарата обеспечивают анальгезию (сенсорный блок) с минимальным и не прогрессирующим моторным блоком. На длительность и интенсивность блокады, вызванной ропивакаином, добавление эпинефрина не влияет. Обратимо блокируя потенциалзависимые натриевые каналы, препятствует генерации импульсов в окончаниях чувствительных нервов и проведению импульсов по нервным волокнам.
Как и другие местные анестетики может оказывать влияние на другие возбудимые клеточные мембраны (например, в головном мозге и миокарде). Если избыточное количество местного анестетика достигает системного кровотока за короткий промежуток времени, возможно проявление признаков системной токсичности. Признаки токсичности со стороны центральной нервной системы предшествуют признакам токсичности со стороны сердечно-сосудистой системы, так как наблюдаются при более низких концентрациях ропивакаина в плазме (см. раздел «Передозировка»).
Прямое действие местных анестетиков на сердце включает замедление проводимости, отрицательный инотропный эффект и, при выраженной передозировке, аритмии и остановку сердца. Внутривенное введение высоких доз ропивакаина приводит к таким же эффектам на сердце.
Внутривенные инфузии ропивакаина здоровым добровольцам показали его хорошую переносимость.
Непрямые сердечно-сосудистые эффекты (снижение АД, брадикардия), которые могут возникать после эпидурального введения ропивакаина, обусловлены возникающей симпатической блокадой.
Фармакокинетика
Концентрация ропивакаина в плазме крови зависит от дозы, пути введения и степени вас-куляризации области инъекции. Фармакокинетика ропивакаина линейная, максимальная концентрация (Cmax) пропорциональна введенной дозе.
После эпидурального введения ропивакаин полностью абсорбируется. Абсорбция носит двухфазный характер, период полувыведения (T1/2) для двух фаз составляет соответственно 14 мин и 4 ч. Замедление элиминации ропивакаина определяется медленной абсорбцией, что объясняет более длительный T1/2 после эпидурального введения по сравнению с внутривенным введением.
Общий плазменный клиренс ропивакаина — 440 мл/мин, плазменный клиренс несвязанного вещества 8 л/мин, почечный клиренс 1 мл/мин, объем распределения в равновесном состоянии 47 л, показатель печеночной экстракции около 0,4, T1/2 — 1,8 ч. Ропивакаин интенсивно связывается с белками плазмы крови (главным образом с α1-кислыми гликопротеинами), несвязанная фракция ропивакаина составляет около 6%. Длительная эпидуральная инфузия ропивакаина приводит к повышению общего содержания препарата в плазме крови, что обусловлено увеличением содержания кислых гли-копротеинов в крови после хирургических операций, при этом концентрация несвязанной, фармакологически активной формы ропивакаина в плазме крови меняется в гораздо меньшей степени, чем общая концентрация ропивакаина.
Ропивакаин проникает через плацентарный барьер с быстрым достижением равновесия по несвязанной фракции. Степень связывания с белками плазмы крови у плода меньше, чем у матери, что приводит к более низким концентрациям ропивакаина в плазме плода по сравнению с общей концентрацией ропивакаина в плазме крови матери.
Ропивакаин активно метаболизируется в организме, главным образом путем ароматического гидроксилирования. 3-гидроксиропивакаин (конъюгированный + неконъюгированный) обнаруживается в плазме крови. 3-гидрокси и 4-гидроксиропивакаин обладают более слабым местноанестезирующим действием по сравнению с ропивакаином.
После внутривенного введения 86% ропивакаина выводится с мочой и только около
1% от выделяемого с мочой препарата выводится в неизмененном виде. Около 37% 3-
гидроксиропивакаина, основного метаболита ропивакаина, выводится с мочой
преимущественно в конъюгированной форме.
1-3% ропивакаина выводится с мочой в виде следующих метаболитов: 4-гидроксиропивакаина, N-дезалкилированных метаболитов и 4-гидрокси- дезалкилированного ропивакаина.
Нет данных о рацемизации ропивакаина in vivo.
ПОКАЗАНИЯ
Анестезия при хирургических вмешательствах:
– эпидуральная блокада при хирургических вмешательствах, включая кесарево сечение;
– блокада крупных нервов и нервных сплетений;
– блокада отдельных нервов и инфильтрационная анестезия.
Купирование острого болевого синдрома:
– продленная эпидуральная инфузия или периодическое болюсное введение, например,
для устранения послеоперационной боли или обезболивания родов;
– блокада отдельных нервов и инфильтрационная анестезия;
– продленная блокада периферических нервов;
– внутрисуставная инъекция.
Купирование острого болевого синдрома в педиатрии:
– каудальная эпидуральная блокада у новорожденных и детей до 12 летнего возраста
включительно;
– продленная эпидуральная инфузия у новорожденных и детей до 12 летнего возраста
включительно.
ПРОТИВОПОКАЗАНИЯ
Гиперчувствительность к компонентам препарата.
Известная повышенная чувствительность к местным анестетикам амидного типа.
С осторожностью:
ослабленные пожилые пациенты или пациенты с тяжелыми
сопутствующими заболеваниями, такими как блокады внутрисердечной проводимости II и
III степеней (синоатриальная, атриовентрикулярная, внутрижелудочковая), прогресси
рующие заболевания печени, тяжелая печеночная недостаточность, тяжелая
хроническая почечная недостаточность, при терапии гиповолемического шока. Для
данных групп пациентов регионарная анестезия часто является предпочтительной. При
проведении “больших” блокад с целью снижения риска развития тяжелых
неблагоприятных явлений рекомендуется предварительно оптимизировать состояние
пациента, а также скорректировать дозу анестетика.
Следует соблюдать осторожность при инъекции местных анестетиков в области головы и
шеи, в связи с возможной повышенной частотой развития серьезных побочных эффектов.
При внутрисуставном введении препарата следует соблюдать осторожность при подозрении на наличие недавней обширной травмы сустава или хирургической операции со вскрытием обширных поверхностей сустава, в связи с возможностью усиления абсорбции препарата и более высокой концентрации препарата в плазме.
Особое внимание следует уделять при применении препарата у детей до 6 месяцев в связи с незрелостью органов и функций.
Пациентам, находящимся на диете с ограничением натрия, необходимо принимать во внимание содержание натрия в препарате.
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕННОСТИ И В ПЕРИОД ГРУДНОГО ВСКАРМЛИВАНИЯ
Беременность
Не выявлено влияния ропивакаина на фертильность и репродуктивную функцию, а также тератогенного действия. Не проводились исследования по оценке возможного действия ропивакаина на развитие плода у женщин.
Наропин® можно применять при беременности только, если ожидаемая польза для матери превышает потенциальный риск для плода (в акушерстве использование препарата для анестезии или анальгезии хорошо обосновано).
Исследования влияния препарата на репродуктивную функцию проводились на животных. В исследованиях на крысах ропивакаин не оказывал влияния на фертильность и репродукцию в двух поколениях. При введении максимальных доз ропивакаина беременным крысам наблюдалось увеличение смертности потомства в первые три дня после родов, что, возможно, объясняется токсическим эффектом ропивакаина на мать, приводящим к нарушению материнского инстинкта.
Исследования тератогенности на кроликах и крысах не выявили побочных эффектов ропивакаина на органогенез или развитие плода на ранних стадиях. Также в ходе перинатальных и постнатальных исследований на крысах, получавших максимально переносимую дозу препарата, не отмечалось побочных эффектов на поздние стадии развития плода, родовую деятельность, лактацию, жизнеспособность или на рост потомства.
Лактация
Не изучалось выделение ропивакаина или его метаболитов с грудным молоком. Исходя из экспериментальных данных, доза препарата, получаемого новорожденным, предположительно составляет 4% от дозы, введенной матери (концентрация препарата вмолоке/ концентрация препарата в плазме). Общая доза ропивакаина, воздействующая на ребенка при грудном кормлении, значительно меньше дозы, которая может попасть в
плод при введении анестетика матери при родах. При необходимости применения препарата в период грудного кормления следует рассмотреть соотношение потенциальной пользы для матери и возможного риска для младенца.
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ
Наропин® должен использоваться только специалистами, имеющими достаточный опыт проведения местной анестезии, или под их наблюдением.
Взрослые и дети старше 12 лет:
В целом для анестезии при хирургических вмешательствах требуются более высокие
дозы и более концентрированные растворы препарата, чем при использовании анестетика с целью обезболивания. При использовании анестетика с целью обезболивания обычно рекомендована доза 2 мг/мл. Для внутрисуставного введения рекомендована доза 7,5 мг/мл.
Дозы, указанные в таблице 1, считаются достаточными для достижения надежной блокады и являются ориентировочными при использовании препарата у взрослых, так как существует индивидуальная вариабельность скорости развития блокады и его длительности.
Данные таблицы 1 является ориентировочным руководством по дозированию препарата для проведения наиболее часто используемых блокад. При подборе дозы препарата следует основываться на клиническом опыте с учетом физического состояния пациента.
Таблица 1. Рекомендации по дозированию препарата Наропин® для взрослых:
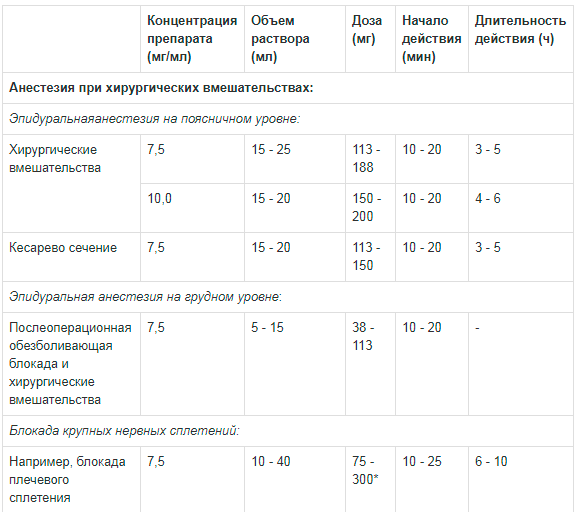
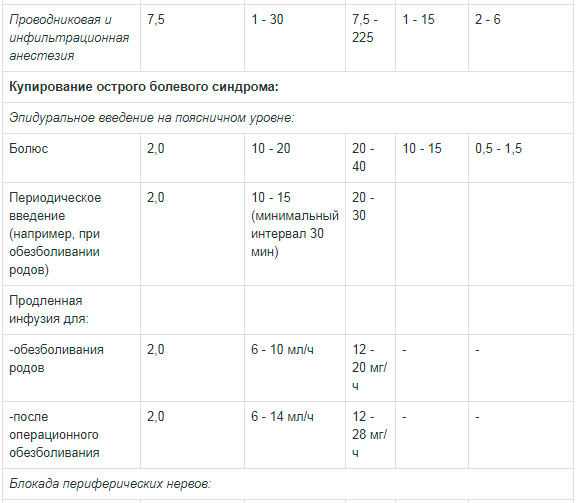
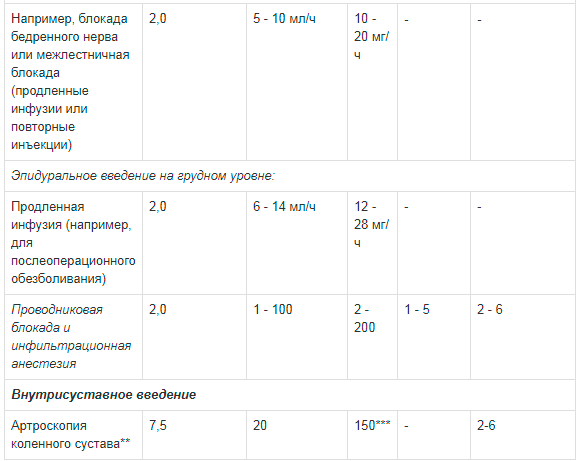
** Сообщалось о случаях хондролиза при послеоперационной продленной внутрисуставной инфузии местных анестетиков. Наропин® не следует применять для продленной внутрисуставной инфузии.Доза для блокады крупных нервных сплетений должна подбираться в соответствии с местом введения и состоянием пациента. Блокада плечевого сплетения межлестничным и надключичным доступом может быть сопряжена с высокой частотой серьезных побочных реакций вне зависимости от используемого местного анестетика.
*** Если Наропин® дополнительно использовался для других видов анестезии, максимальная доза не должна превышать 225 мг.
Для ознакомления с факторами, влияющими на метод выполнения отдельных блокад, и с требованиями, предъявляемыми к конкретным группам пациентов, следует использовать стандартные руководства.
Для предотвращения попадания анестетика в сосуд следует обязательно проводить аспирационную пробу до введения и в процессе введения препарата. Если предполагается использовать препарат в высокой дозе, рекомендуется ввести пробную дозу – 3-5 мл лидокаина с эпинефрином. Случайное внутрисосудистое введение распознается по временному увеличению частоты сердечных сокращений, а случайное интратекальное введение – по признакам спинального блока. При появлении токсических симптомов следует немедленно прекратить введение препарата.
До введения и во время введения препарата Наропин® (которое следует проводить медленно или путем увеличения вводимых последовательно доз препарата со скоростью 25-50 мг/мин) необходимо тщательно контролировать жизненно важные функции пациента и поддерживать с ним вербальный контакт.
Однократное введение ропивакаина в дозе до 250 мг при эпидуральной блокаде для проведения хирургического вмешательства обычно хорошо переносится пациентами. При блокаде плечевого сплетения с помощью 40 мл препарата Наропин® 7,5 мг/мл максимальные плазменные концентрации ропивакаина у некоторых пациентов могут достигать значения, характеризующегося легкими симптомами токсичности со стороны центральной нервной системы. Поэтому применение дозы выше 40 мл препарата Наропин® 7,5 мг/мл (300 мг ропивакаина) не рекомендовано.
При длительном проведении блокады путем продленной инфузии или повторного болюсного введения следует учитывать возможность создания токсических концентраций анестетика в крови и местного повреждения нерва. Введение ропивакаина в течение 24 ч в дозе до 800 мг суммарно при хирургических вмешательствах и для послеоперационного обезболивания, а также продленная эпидуральная инфузия после операции со скоростью до 28 мг/ч в течение 72 ч хорошо переносится взрослыми пациентами.
Для купирования послеоперационной боли рекомендуется следующая схема применения препарата: если эпидуральный катетер не был установлен при оперативном вмешательстве, после его установки выполняется эпидуральная блокада болюсной инъекцией препарата Наропин® (7,5 мг/мл). Анальгезия поддерживается инфузией препарата Наропин® (2 мг/мл). В большинстве случаев для купирования послеоперационной боли от умеренной до выраженной, инфузия со скоростью 6-14 мл/ч (12-28 мг/ч) обеспечивает адекватную анальгезию с минимальной не прогрессирующей двигательной блокадой (при использовании данной методики наблюдалось значительное снижение потребности в опиоидных анальгетиках).
Для послеоперационного обезболивания Наропин® (2 мг/мл) можно вводить непрерывно в виде эпидуральной инфузии в течение 72 ч без фентанила или в комбинации с ним (1-4 мкг/мл). При применении препарата Наропин® 2 мг/мл (6-14 мл/час) обеспечивалось адекватное обезболивание у большинства пациентов. Комбинация препарата Наропин® и фентанила приводила к улучшению обезболивания, вызывая при этом побочные эффекты, присущие наркотическим анальгетикам.
Использование препарата Наропин® в концентрации выше 7,5 мг/мл при кесаревом сечении не изучено.
Таблица 2. Рекомендации по дозированию препарата Наропин® для детей до 12 лет:
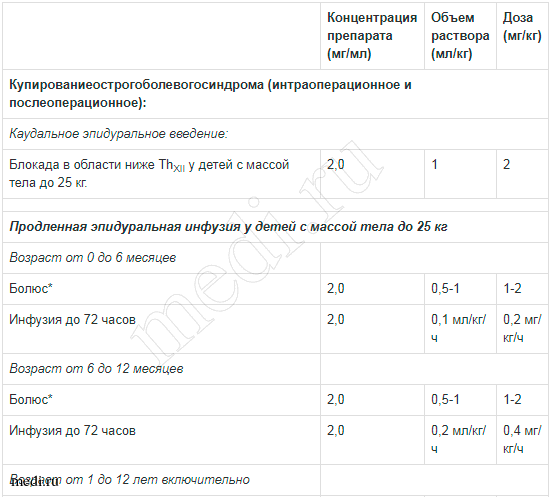

* Меньшие дозы из предлагаемого интервала рекомендуются для эпидурального введения на грудном уровне, в то время как большие дозы рекомендованы для эпидурального введения на поясничном или каудальном уровнях.
** Рекомендуется для эпидурального введения на поясничном уровне. Обоснованным является снижение дозы болюса для эпидуральной анальгезии на грудном уровне.
Дозы, указанные в таблице 2, являются руководством к использованию препарата в педиатрической практике. В тоже время существует индивидуальная вариабельность скорости развития блока и его длительности.
У детей с избыточной массой тела часто требуется постепенное снижение дозы препарата; при этом необходимо руководствоваться «идеальной» массой тела пациента. За справочной информацией о факторах, которые влияют на методы выполнения отдельных блокад и о требованиях, предъявляемых к конкретным группам пациентов, следует обращаться к специализированным руководствам. Объем раствора для каудального эпидурального введения и объем болюса для эпидурального введения не должны превышать 25 мл для любого пациента.
Для предотвращения непреднамеренного внутрисосудистого введения анестетика следует тщательно проводить аспирационную пробу до введения и в процессе введения препарата. Во время введения препарата необходимо тщательно контролировать жизненно важные функции пациента. При появлении токсических симптомов следует немедленно прекратить введение препарата.
Однократное введение ропивакаина в дозе 2 мг/мл (из расчета 2 мг/кг, объём раствора 1 мл/кг) для послеоперационной каудальной анальгезии обеспечивает адекватное обезболивание ниже уровня ThXII у большинства пациентов. Дети старше 4 лет хорошо переносят дозы до 3 мг/кг. Объем вводимого раствора для эпидурального введения на каудальном уровне может быть изменен с целью достижения различной распространенности сенсорного блока, что описано в специализированных руководствах. Независимо от типа анестезии, рекомендуется болюсное введение рассчитанной дозы препарата.
Применение препарата в концентрации выше 5 мг/мл, а также интратекальное применение препарата Наропин® у детей не исследовалось. Применение препарата Наропин® у недоношенных детей не изучалось.
Инструкции по применению раствора
Раствор не содержит консервантов и предназначен только для однократного применения. Любое количество раствора, оставшегося в контейнере после использования, должно быть уничтожено.
Невскрытый контейнер с раствором не должен быть автоклавирован. Невскрытая блистерная упаковка обеспечивает стерильность внешней поверхности контейнера и предпочтительна для использования в условиях, требующих стерильности.
ПОБОЧНОЕ ДЕЙСТВИЕ
Нежелательные реакции на Наропин® аналогичны реакциям на другие местные анестетики амидного типа. Их следует отличать от физиологических эффектов, возникающих из-за блокады симпатических нервов на фоне эпидуральной анестезии, таких как, снижение артериального давления, брадикардия, или эффектов, связанных с техникой введения препарата, таких как, местное повреждение нерва, менингит, постпункционная головная боль, эпидуральный абсцесс.
Побочные эффекты, присущие местным анестетикам
Со стороны центральнойи периферической нервной системы
Возможны нейропатия и нарушение функции спинного мозга (синдром передней спинномозговой артерии, арахноидит, синдром конского хвоста), обычно связаны с техникой проведения регионарной анестезии, а не с действием препарата.
В результате случайного интратекального введения эпидуральной дозы может произойти полный спинальный блок.
Возможны серьезные осложнения при системной передозировке и непреднамеренном внутрисосудистом введении препарата (см. раздел «Передозировка»).
Острая системная токсичность
Наропин® может вызывать острые системные токсические реакции при использовании
высоких доз или при быстром повышении его концентрации в крови при случайном
внутрисосудистом введении препарата либо его передозировке (см. раздел
«Фармакологические свойства» и «Передозировка»).
Наиболее часто встречающиеся побочные эффекты
Сообщалось о различных побочных эффектах препарата, подавляющее большинство которых было связано не с воздействием используемого анестетика, а с техникой проведения регионарной анестезии.
Наиболее часто (> 1%) отмечались следующие побочные эффекты, которые были расценены, как имеющие клиническое значение вне зависимости от того была ли установлена причинно-следственная связь с использованием анестетика: снижение артериального давления (АД)*, тошнота, брадикардия, рвота, парестезия, повышение температуры тела, головная боль, задержка мочеиспускания, головокружение, озноб, повышение артериального давления, тахикардия, гипестезия, беспокойство. Частота возникновения нежелательных эффектов представлена следующим образом: Очень часто (> 1/10); Часто (> 1/100, < 1/10); Нечасто (> 1/1000, < 1/100); Редко (> 1/10 000, < 1/1 000); Очень редко (< 1/10 000), включая отдельные сообщения.

* Снижение АД встречается у детей часто.
**Рвота встречается у детей очень часто.
ПЕРЕДОЗИРОВКА
Острая системная токсичность
При случайном внутрисосудистом введении при проведении блокад нервных сплетений или других периферических блокад наблюдались случаи возникновения судорог.
В случае неправильного введения эпидуральной дозы анестетика интратекально возможно возникновение полного спинального блока.
Случайное внутрисосудистое введение анестетика может вызвать немедленную токсическую реакцию.
При передозировке во время проведения регионарной анестезии симптомы системной токсической реакции появляются в отсроченном порядке через 15-60 мин после инъекции из-за медленного повышения концентрации местного анестетика в плазме крови.
Системная токсичность, в первую очередь, проявляется симптомами со стороны центральной нервной системы (ЦНС) и сердечно-сосудистой системы (ССС). Данные реакции вызываются высокими концентрациями местного анестетика в крови, которые могут возникнуть вследствие (случайного) внутрисосудистого введения, передозировки или исключительно высокой адсорбции из сильно васкуляризированных областей.
Реакции со стороны ЦНС схожи для всех местных анестетиков амидного типа, в то время как реакции со стороны сердечно-сосудистой системы в большей степени зависят от введенного препарата и его дозы.
Центральная нервная система
Проявления системной токсичности со стороны центральной нервной системы развиваются постепенно: сначала появляются расстройства зрения, онемение вокруг рта, онемение языка, гиперакузия, звон в ушах, головокружение. Дизартрия, тремор и мышечные подергивания являются более серьёзными проявлениями системной токсичности и могут предшествовать появлению генерализованных судорог (эти признаки не должны приниматься за невротическое поведение пациента). При прогрессировании интоксикации может наблюдаться потеря сознания, приступы судорог продолжительностью от нескольких секунд до нескольких минут, сопровождающиеся нарушением дыхания, быстрым развитием гипоксии и гиперкапнии из-за повышенной мышечной активности и неадекватной вентиляции. В тяжелых случаях может даже наступить остановка дыхания. Возникающие ацидоз, гиперкалиемия, гипокальциемия усиливают токсические эффекты анестетика.
Впоследствии, из-за перераспределения анестетика из ЦНС и его последующего метаболизма и экскреции, происходит достаточно быстрое восстановление функций, если только не была введена большая доза препарата.
Сердечно—сосудистая система
Расстройства со стороны сердечно-сосудистой системы являются признаками более серьезных осложнений. Снижение АД, брадикардия, аритмия и, в ряде случаев, даже остановка сердца могут возникать вследствие высокой системной концентрации местных анестетиков. В редких случаях остановка сердца не сопровождается предшествующей симптоматикой со стороны ЦНС. В исследованиях на добровольцах внутривенная инфузия ропивакаина приводила к угнетению проводимости и сократительной способности сердечной мышцы. Симптомам со стороны сердечно-сосудистой системы обычно предшествуют проявления токсичности со стороны ЦНС, которые можно не заметить, если больной находится под действием седативных средств (бензодиазепины или барбитураты) или под общей анестезией.
У детей ранние признаки системной токсичности местных анестетиков иногда сложнее выявить вследствие затруднений, испытываемых детьми при описании симптомов, или в случае применения регионарной анестезии в сочетании с общей анестезией.
Лечение острой токсичности
При появлении первых признаков острой системной токсичности следует немедленно прекратить введение препарата.
При появлении судорог и симптомов угнетения ЦНС больному требуется адекватное лечение, целью которого является поддержание оксигенации, купирование судорог,
поддержание деятельности сердечно-сосудистой системы. Следует обеспечить оксигенацию кислородом, а при необходимости – переход на искусственную вентиляцию легких. Если спустя 15-20 секунд судороги не прекращаются, следует использовать про-тивосудорожные средства: тиопентал натрия 1-3 мг/кг в/в (обеспечивает быстрое купирование судорог) или диазепам 0,1 мг/кг в/в (действие развивается медленнее по сравнению с действием тиопентала натрия). Суксаметоний 1 мг/кг быстро купирует судороги, но при его использовании требуется интубация и искусственная вентиляция легких.
При угнетении деятельности сердечно-сосудистой системы (снижение АД, брадикардия)
необходимо внутривенное введение 5-10 мг эфедрина, при необходимости через 2-
3 мин введение повторить. При развитии циркуляторной недостаточности или остановке
сердца следует немедленно начать стандартные реанимационные мероприятия.
Жизненно важно поддерживать оптимальную оксигенацию, вентиляцию и циркуляцию крови, а также корректировать ацидоз. При остановке сердца могут потребоваться более длительные реанимационные мероприятия.
При терапии системной токсичности у детей необходимо корректировать дозы соответственно возрасту и массе тела пациента.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ ПРЕПАРАТАМИ И ДРУГИЕ ФОРМЫ ЛЕКАРСТВЕННОГО ВЗАИМОДЕЙСТВИЯ
Возможно суммирование токсических эффектов при одновременном назначении с другими местными анестетиками или препаратами структурно сходными с местными анестетиками амидного типа.
Клиренс ропивакаина уменьшается до 77% при одновременном применении с флувоксамином, являющимся мощным конкурентным ингибитором изофермента CYP1A2, из-за возможности сходного взаимодействия следует избегать длительного применения Наропина® на фоне действия флувоксамина.
Повышение рН раствора выше 6,0 может привести к образованию преципитата из-за плохой растворимости ропивакаина при данных условиях.
Раствор Наропина® в пластиковых инфузионных мешках по своим химическим и физическим свойствам совместим со следующими лекарственными препаратами:
|
Концентрация Наропина: 1-2 мг/мл |
|
|
Добавляемый раствор |
Концентрация |
|
Фентанил |
1,0 — 10,0 мкг/мл |
|
Морфин |
20,0 — 100,0 мкг/мл |
Несмотря на тот факт, что полученные смеси сохраняют химическую и физическую стабильность в течение 30 дней при температуре не выше 30°С, исходя из данных по микробиологической чистоте, следует использовать полученные смеси растворов немедленно после приготовления.
ОСОБЫЕ УКАЗАНИЯ
Анестезия должна проводиться опытными специалистами. Обязательно наличие оборудования и лекарственных препаратов для проведения реанимационных мероприятий. До начала выполнения больших блокад должен быть установлен внутривенно катетер.
Персонал, обеспечивающий выполнение анестезии, должен быть соответствующим
образом подготовлен и знаком с диагностикой и лечением возможных побочных эффектов, системных токсических реакций и других возможных осложнений (см. раздел “Передозировка”).
Осложнением непреднамеренного субарахноидального введения может являться спинальный блок с остановкой дыхания и снижением АД. Судороги развиваются чаще при блокаде плечевого сплетения и эпидуральной блокаде, вероятно, вследствие случайного внутрисосудистого введения или быстрой абсорбции в месте инъекции. Выполнение блокад периферийных нервов может требовать введение большого объема местного анестетика в зоны с большим количеством сосудов, часто вблизи крупных сосудов, что повышает риск внутрисосудистого введения и/или быстрого системного всасывания, что может привести к высокой концентрации препарата в плазме.
Некоторые процедуры, связанные с применением местных анестетиков, такие как инъекции в области головы и шеи, могут сопровождаться повышенной частотой развития серьезных побочных эффектов, вне зависимости от типа применяемого местного анестетика. Необходимо соблюдать осторожность для предотвращения инъекции в область воспаления.
Следует соблюдать осторожность при введении препарата пациентам с блокадой внутрисердечной проводимости II и III степеней, пациентам с тяжелой почечной недостаточностью, пожилым и ослабленным пациентам.
Имеются сообщения о редких случаях остановки сердца при применении препарата Наропин® для эпидуральной анестезии или блокад периферических нервов, особенно после случайного внутрисосудистого введения препарата, у пожилых пациентов и у пациентов с сопутствующими сердечно-сосудистыми заболеваниями.
В ряде случаев реанимационные мероприятия были затруднительны. Остановка сердца, как правило, требует более длительных реанимационных мероприятий.
Поскольку Наропин® метаболизируется в печени, следует проявлять осторожность при применении препарата у больных с тяжелыми заболеваниями печени; в некоторых случаях из-за замедленной элиминации может возникнуть необходимость уменьшения повторно вводимых доз анестетика.
Обычно у больных с почечной недостаточностью при введении препарата однократно или при использовании препарата в течение непродолжительного периода времени не требуется корректировать дозу. Однако ацидоз и снижение концентрации белков в плазме крови, часто развивающиеся у больных с хронической почечной недостаточностью, могут повышать риск системного токсического действия препарата (см. раздел «Способ применения и дозы»). Риск системной токсичности также повышен при применении препарата у пациентов с пониженной массой тела и пациентов с гиповолемическим шоком.
Эпидуральная анестезия может приводить к снижению АД и брадикардии. Введение сосудосуживающих препаратов или увеличение объёма циркулирующей крови может уменьшить риск развития подобных побочных эффектов. Следует своевременно корректировать снижение АД путем внутривенного введения 5-10 мг эфедрина, при необходимости введение повторить.
При внутрисуставном введении препарата следует соблюдать осторожность при подозрении на наличие недавней обширной травмы сустава или хирургической операции со вскрытием обширных поверхностей сустава, в связи с возможностью усиления абсорбции препарата и более высокой концентрации препарата в плазме.
Пациенты, получающие терапию антиаритмическими препаратами III класса (например, амиадороном) должны находиться под тщательным наблюдением, рекомендуется ЭКГ-мониторинг в связи с риском усиления сердечно-сосудистых эффектов.
Следует избегать длительного применения препарата Наропин® у пациентов, принимающих мощные ингибиторы изофермента CYP1A2 (такие как, флувоксамин и эноксацин).
Следует учитывать возможность перекрестной гиперчувствительности при одновременном применении препарата Наропин® с другими местными анестетиками амидного типа.
Пациентам, находящимся на диете с ограничением натрия, необходимо принимать во внимание содержание натрия в препарате.
Применение препарата у новорожденных требует учета возможной незрелости органов и физиологических функций новорожденных. Клиренс несвязанной фракции ропивакаина и пипелоксилидина (ППК) зависит от массы тела и возраста ребенка в первые годы жизни. Влияние возраста выражается в развитии и зрелости функции печени, клиренс достигает максимального значения в возрасте около 1-3 лет. Период полувыведения ропивакаина составляет 5-6 часов у новорожденных и детей в возрасте 1 месяца по сравнению с 3 часами у детей более старшего возраста. В связи с недостаточным развитием функций печени системная экспозиция ропивакаина выше у новорожденных, умеренно выше – у детей от 1 до 6 месяцев по сравнению с детьми более старшего возраста. Значительные отличия в концентрациях ропивакаина в плазме крови новорожденных, выявленные в клинических исследованиях, позволяют предполагать повышенный риск возникновения системной токсичности в этой группе пациентов, особенно при продленной эпидуральной инфузии. Рекомендованные дозы для новорожденных основаны на ограниченных клинических данных.
При использовании ропивакаина у новорожденных необходимо мониторирование системной токсичности (контроль признаков токсичности со стороны центральной нервной системы, ЭКГ, контроль оксигенации крови) и местной нейротоксичности, которые следует продолжать после завершения инфузии из-за медленного выведения препарата у новорожденных.
Применение препарата в концентрации выше 5 мг/мл, а также интратекальное применение препарата Наропин® у детей не исследовалось.
Наропин® потенциально способен вызывать порфирию и может применяться у пациентов с диагнозом острая порфирия только в случаях, если нет более безопасной альтернативы. В случае повышенной чувствительности пациентов должны быть приняты необходимые меры предосторожности.
Сообщалось о случаях хондролиза при послеоперационной продленной внутрисуставной инфузии местных анестетиков. В большинстве описанных случаев, проводилась инфузия в плечевой сустав. Причинно-следственная связь с приемом анестетиков не установлена. Наропин® не следует применять для продленной внутрисуставной инфузии.
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ ТРАНСПОРТНЫМИ СРЕДСВАМИ И ДРУГИМИ МЕХАНИЗМАМИ
Помимо анальгезирующего эффекта, Наропин® может оказывать слабое транзиторное
влияние на двигательную функцию и координацию. Учитывая профиль побочных эффектов препарата, необходимо соблюдать осторожность при управлении транспортными средствами и выполнении других потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
ФОРМА ВЫПУСКА
Раствор для инъекций 2 мг/мл, 7,5 мг/мл и 10 мг/мл.
Раствор для инъекций 2 мг/мл:
По 20 мл в запаянные ампулы из полипропилена. Каждую ампулу помещают в контурную ячейковую упаковку. 5 контурных ячейковых упаковок с инструкцией по применению в картонной пачке с контролем первого вскрытия.
По 100 мл или 200 мл в полипропиленовые контейнеры (мешки), укупоренные бутилкаучуковой пробкой и листовидной алюминиевой пластинкой. Полипропиленовые контейнеры (мешки) индивидуально упакованы в контурную ячейковую упаковку из полипропилена/бумаги. По 5 контурных ячейковых упаковок в картонной пачке с инструкцией по применению.
Раствор для инъекций 7,5 мг/мл и 10 мг/мл:
По 10 мл в запаянные ампулы из полипропилена. Каждую ампулу помещают в контурную ячейковую упаковку. 5 контурных ячейковых упаковок с инструкцией по применению в картонной пачке с контролем первого вскрытия.
УСЛОВИЯ ХРАНЕНИЯ
Хранить при температуре не выше 30°С. Не замораживать. Хранить в местах, недоступных для детей.
СРОК ГОДНОСТИ
3 года. Не применять по истечении срока годности, указанного на упаковке.
УСЛОВИЯ ОТПУСКА
По рецепту.
ФИРМА-ПРОИЗВОДИТЕЛЬ
Раствор для инъекций 2 мг/мл, 7,5 мг/мл, 10 мг/мл (ампулы):
АстраЗенека АБ, SE-151 85 Содерталье, Швеция;
Раствор для инъекций 2 мг/мл (мешки):
АстраЗенека Пти Лтд, Австралия, 10-14 Картоум Роуд, Норт Райд, Новый Южный Уэльс 2113
Дальнейшая информация предоставляется по требованию:
Представительство компании АстраЗенека ЮК Лимитед, Великобритания в г. Москве и ООО АстраЗенека Фармасьютикалз
125284 г. Москва, ул. Беговая д. 3, стр. 1
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Описание препарата Наропин® (раствор для инъекций, 10 мг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2020 году
Дата согласования: 29.06.2020
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Характеристика
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Комментарий
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Отзывы
Действующее вещество
ATX
Фармакологическая группа
Состав
| Раствор для инъекций | 1 мл |
| активное вещество: | |
| ропивакаина гидрохлорид моногидрат, соответствующий ропивакаина гидрохлориду | 2,0 мг |
| 5,0 мг | |
| 7,5 мг | |
| 10 мг | |
| вспомогательные вещества: натрия хлорид 8,6 /8,0/7,5 /7,1 мг; 2 М раствор натрия гидроксида и/или 2 М раствор хлористоводородной кислоты для доведения рН до 4,0 –6,0; вода для инъекций — до 1,0 мл |
Описание лекарственной формы
Прозрачный бесцветный раствор.
Характеристика
Раствор Наропина® представляет собой стерильный изотонический водный раствор, не содержит консервантов и предназначен только для однократного применения. рКа ропивакаина — 8,1; коэффициент распределения — 141 (n-октанол/фосфатный буфер, рН 7,4 при 25 °C).
Фармакодинамика
Раствор для инъекций, 2; 7,5; 10 мг/мл
Ропивакаин — первый местный анестетик амидного типа длительного действия, являющийся чистым энантиомером. Oбладает как анестезирующим, так и обезболивающим действием. Высокие дозы ропивакаина применяются для местной анестезии при хирургических вмешательствах, низкие дозы препарата обеспечивают анальгезию (сенсорный блок) с минимальным и непрогрессирующим моторным блоком. На длительность и интенсивность блокады, вызванной ропивакаином, добавление эпинефрина не влияет. Обратимо блокируя потенциалзависимые натриевые каналы, препятствует генерации импульсов в окончаниях чувствительных нервов и проведению импульсов по нервным волокнам.
Как и другие местные анестетики, может оказывать влияние на другие возбудимые клеточные мембраны (например, в головном мозге и миокарде). Если избыточное количество местного анестетика достигает системного кровотока за короткий промежуток времени, возможно проявление признаков системной токсичности. Признаки токсичности со стороны центральной нервной системы предшествуют признакам токсичности со стороны сердечно-сосудистой системы, т.к. наблюдаются при более низких концентрациях ропивакаина в плазме (см. «Передозировка»).
Прямое действие местных анестетиков на сердце включает замедление проводимости, отрицательный инотропный эффект и, при выраженной передозировке, аритмии и остановку сердца. Внутривенное введение высоких доз ропивакаина приводит к таким же эффектам на сердце.
Внутривенные инфузии ропивакаина здоровым добровольцам показали его хорошую переносимость.
Непрямые сердечно-сосудистые эффекты (снижение АД, брадикардия), которые могут возникать после эпидурального введения ропивакаина, обусловлены возникающей симпатической блокадой.
Раствор для инъекций, 5 мг/мл
Ропивакаин — длительно действующий местный анестетик амидного типа, являющийся чистым левовращающим энантиомером. Обладает как анестезирующим, так и обезболивающим действием. Высокие концентрации ропивакаина применяются для местной анестезии при хирургических вмешательствах. В низких концентрациях вызывает сенсорный блок (анальгезию) с минимальным и непрогрессирующим моторным блоком. Обратимо блокируя потенциалзависимые натриевые каналы, препятствует генерации импульсов в окончаниях чувствительных нервов и проведению импульсов по нервным волокнам. Как и другие местные анестетики, может оказывать влияние на другие возбудимые клеточные мембраны (например, в головном мозге и миокарде), при этом возможно проявление признаков системной токсичности. Попадая в избыточных количествах в системный кровоток, может оказать угнетающее действие на центральную нервную систему и миокард (снижает возбудимость, автоматизм и проводимость). Признаки токсичности со стороны центральной нервной системы (см. «Передозировка») предшествуют признакам токсичности со стороны сердечно-сосудистой системы, т.к. наблюдаются при более низких концентрациях ропивакаина в плазме. Наропин® имеет широкий терапевтический диапазон (диапазон между дозами, оказывающими терапевтическое и токсическое действие). В исследованиях in vivo на животных показано, что ропивакаин оказывает меньшее токсическое действие на миокард по сравнению с бупивакаином. Непрямые сердечно-сосудистые эффекты (снижение АД, брадикардия), которые могут возникать после эпидурального введения ропивакаина, обусловлены возникающей симпатической блокадой.
Начало и длительность анестезии препаратом Наропин® зависят от концентрации и места введения препарата. На длительность и интенсивность блокады, вызванной ропивакаином, добавление эпинефрина практически не влияет.
Фармакокинетика
Раствор для инъекций, 2; 5; 7,5; 10 мг/мл
Концентрация ропивакаина в плазме крови зависит от дозы, пути введения и степени васкуляризации области инъекции.
Фармакокинетика ропивакаина линейная, максимальная концентрация (Cmax) пропорциональна введенной дозе.
После эпидурального введения ропивакаин полностью абсорбируется. Абсорбция носит двухфазный характер, период полувыведения (T1/2) для двух фаз составляет соответственно 14 мин и 4 ч. Замедление элиминации ропивакаина определяется медленной абсорбцией, что объясняет более длительный T1/2 после эпидурального введения по сравнению с внутривенным введением.
Общий плазменный клиренс ропивакаина – 440 мл/мин, плазменный клиренс несвязанного вещества — 8 л/мин, почечный клиренс 1 мл/мин, объем распределения в равновесном состоянии 47 л, показатель печеночной экстракции около 0,4, T1/2 — 1,8 ч.
Ропивакаин интенсивно связывается с белками плазмы крови (главным образом с α1-кислыми гликопротеинами), несвязанная фракция ропивакаина составляет около 6%.
Длительная эпидуральная инфузия ропивакаина приводит к повышению общего содержания препарата в плазме крови, что обусловлено увеличением содержания кислых гликопротеинов в крови после хирургических операций, при этом концентрация несвязанной, фармакологически активной формы ропивакаина в плазме крови меняется в гораздо меньшей степени, чем общая концентрация ропивакаина.
Ропивакаин проникает через плацентарный барьер с быстрым достижением равновесия по несвязанной фракции. Степень связывания с белками плазмы крови у плода меньше, чем у матери, что приводит к более низким концентрациям ропивакаина в плазме плода по сравнению с общей концентрацией ропивакаина в плазме крови матери.
Ропивакаин активно метаболизируется в организме, главным образом путем ароматического гидроксилирования. 3-гидроксиропивакаин (конъюгированный + неконъюгированный) обнаруживается в плазме крови. 3-гидрокси- и 4-гидроксиропивакаин обладают более слабым местноанестезирующим действием по сравнению с ропивакаином.
После внутривенного введения 86% ропивакаина выводится с мочой, и только около 1% от выделяемого с мочой препарата выводится в неизмененном виде. Около 37% 3-гидроксиропивакаина, основного метаболита ропивакаина, выводится с мочой преимущественно в конъюгированной форме.
1–3% ропивакаина выводится с мочой в виде следующих метаболитов 4-гидроксиропивакаина, N-дезалкилированных метаболитов и 4-гидрокси-дезалкилированного ропивакаина.
Нет данных о рацемизации ропивакаина in vivo.
Показания
Раствор для инъекций, 2; 7,5; 10 мг/мл
Анестезия при хирургических вмешательствах:
эпидуральная блокада при хирургических вмешательствах, включая кесарево сечение;
блокада крупных нервов и нервных сплетений;
блокада отдельных нервов и инфильтрационная анестезия.
Купирование острого болевого синдрома:
продленная эпидуральная инфузия или периодическое болюсное введение, например, для устранения послеоперационной боли или обезболивания родов;
блокада отдельных нервов и инфильтрационная анестезия;
продленная блокада периферических нервов;
внутрисуставная инъекция.
Купирование острого болевого синдрома в педиатрии:
каудальная эпидуральная блокада у новорожденных и детей до 12-летнего возраста включительно;
продленная эпидуральная инфузия у новорожденных и детей до 12-летнего возраста включительно.
Раствор для инъекций, 5 мг/мл
анестезия при хирургических вмешательствах (интратекальная блокада);
купирование острого болевого синдрома в педиатрии (блокада периферических нервов у детей с 1- до 12- летнего возраста включительно).
Противопоказания
Раствор для инъекций, 2; 7,5; 10 мг/мл
гиперчувствительность к компонентам препарата;
известная повышенная чувствительность к местным анестетикам амидного типа.
С осторожностью: ослабленные пожилые пациенты или пациенты с тяжелыми сопутствующими заболеваниями, такими как блокады внутрисердечной проводимости II и III степеней (синоатриальная, атриовентрикулярная, внутрижелудочковая), прогрессирующие заболевания печени, тяжелая печеночная недостаточность, тяжелая хроническая почечная недостаточность, при терапии гиповолемического шока. Для данных групп пациентов регионарная анестезия часто является предпочтительной. При проведении «больших» блокад с целью снижения риска развития тяжелых неблагоприятных явлений рекомендуется предварительно оптимизировать состояние пациента, а также скорректировать дозу анестетика.
Следует соблюдать осторожность при инъекции местных анестетиков в области головы и шеи в связи с возможной повышенной частотой развития серьезных побочных эффектов.
При внутрисуставном введении препарата следует соблюдать осторожность при подозрении на наличие недавней обширной травмы сустава или хирургической операции со вскрытием обширных поверхностей сустава в связи возможностью усиления абсорбции препарата и более высокой концентрации препарата в плазме.
Особое внимание следует уделять при применении препарата у детей до 6 мес в связи с незрелостью органов и функций.
Пациентам, находящимся на диете с ограничением натрия, необходимо принимать во внимание содержание натрия в препарате.
Раствор для инъекций, 5 мг/мл
Известная повышенная чувствительность к местным анестетикам амидного типа.
Ввиду отсутствия достаточного количества клинических наблюдений не рекомендуется применение препарата Наропин® у детей младше 1-го года, а также интратекальное введение препарата.
С осторожностью: ослабленные пожилые пациенты или пациенты с тяжелыми сопутствующими заболеваниями, такими как блокады внутрисердечной проводимости II и III степеней (синоатриальная, атриовентрикулярная, внутрижелудочковая), прогрессирующие заболевания печени, тяжелая печеночная недостаточность, тяжелая хроническая почечная недостаточность, при терапии гиповолемического шока, беременность, период лактации. Для данных групп пациентов регионарная анестезия является предпочтительной, при проведении больших блокад с целью снижения риска развития тяжелых неблагоприятных явлений рекомендуется предварительно оптимизировать состояние пациента, а также скорректировать дозу анестетика.
Пациентам, находящимся на диете с ограничением натрия, необходимо принимать во внимание содержание натрия в препарате.
Применение при беременности и кормлении грудью
Раствор для инъекций, 2; 7,5; 10 мг/мл
Беременность. Не выявлено влияния ропивакаина на фертильность и репродуктивную функцию, а также тератогенного действия. Не проводились исследования по оценке возможного действия ропивакаина на развитие плода у женщин.
Наропин® можно применять при беременности, только если это оправдано клинической ситуацией (в акушерстве использование препарата для анестезии или аналгезии хорошо обосновано).
Исследования влияния препарата на репродуктивную функцию проводились на животных. В исследованиях на крысах ропивакаин не оказывал влияния на фертильность и репродукцию в двух поколениях. При введении максимальных доз препарата беременным крысам наблюдалось увеличение смертности потомства в первые три дня после родов, что, возможно, объясняется токсическим эффектом ропивакаина на мать, приводящим к нарушению материнского инстинкта.
Исследования тератогенности на кроликах и крысах не выявили побочных эффектов ропивакаина на органогенез или развитие плода на ранних стадиях. Также в ходе перинатальных и постнатальных исследований на крысах, получавших максимально переносимую дозу препарата, не отмечалось побочных эффектов на поздние стадии развития плода, родовую деятельность, лактацию, жизнеспособность или на рост потомства. В ходе перинатальных и постнатальных сравнительных исследований ропивакаина с бупивакаином показано, что в отличие от ропивакаина токсическое влияние бупивакаина наблюдалось при значительно меньших дозах препарата и при более низких концентрациях несвязанного бупивакаина в крови.
Лактация. Не изучалось выделение ропивакаина или его метаболитов с грудным молоком. Исходя из экспериментальных данных, доза препарата, получаемого новорожденным, предположительно составляет 4% от дозы, введенной матери (концентрация препарата в молоке/плазме). Общая доза ропивакаина, воздействующая на ребенка при грудном вскармливании, значительно меньше дозы, которая может попасть в плод при введении анестетика матери при родах.
При необходимости применения препарата в период грудного кормления следует рассмотреть соотношение потенциальной пользы для матери и возможного риска для младенца.
Раствор для инъекций, 5 мг/мл
Беременность. Не выявлено влияния ропивакаина на фертильность и репродуктивную функцию, а также его тератогенного действия. Не проводились исследования по оценке возможного действия ропивакаина на развитие плода у женщин.
Наропин® можно применять при беременности только в том случае, если ожидаемая польза для матери превосходит потенциальный риск для плода.
Лактация. Не изучалось выделение ропивакаина или его метаболитов с грудным молоком. Исходя из экспериментальных данных, доза препарата, получаемая новорожденным, предположительно составляет 4% от дозы, введенной матери (т.е. общая доза ропивакаина, воздействующая на ребенка при грудном вскармливании, значительно меньше дозы, которая может быть получена новорожденным при введении анестетика матери при родах). При необходимости применения препарата в период грудного вскармливания следует рассмотреть соотношение потенциальной пользы для матери и возможного риска для младенца.
Способ применения и дозы
Раствор для инъекций, 2; 7,5; 10 мг/мл
Наропин® должен использоваться только специалистами, имеющими достаточный опыт проведения местной анестезии, или под их наблюдением.
Взрослые и дети старше 12 лет
В целом для анестезии при хирургических вмешательствах требуются более высокие дозы и более концентрированные растворы препарата,чем при использовании анестетика с целью обезболивания. При использовании анестетика с целью обезболивания обычно рекомендована доза 2 мг/мл. Для внутрисуставного введения рекомендована доза 7,5 мг/мл.
Дозы, указанные в таблице 1, считаются достаточными для достижения надежной блокады и являются ориентировочными при использовании препарата у взрослых, т.к. существует индивидуальная вариабельность скорости развития блокады и его длительности.
Данные таблицы 1 являются ориентировочным руководством по дозированию препарата для проведения наиболее часто используемых блокад. При подборе дозы препарата следует основываться на клиническом опыте с учетом физического состояния пациента.
Таблица 1
Рекомендации по дозированию препарата Наропин® для взрослых
| Концентрация препарата, мг/мл | Объем раствора , мл | Доза, мг | Начало действия, мин | Длительность действия, ч | |
| Анестезия при хирургических вмешательствах | |||||
| Эпидуральная анестезия на поясничном уровне | |||||
| Хирургические вмешательства | 7,5 | 15–25 | 113– 188 | 10–20 | 3–5 |
| 10,0 | 15–20 | 150– 200 | 10–20 | 4–6 | |
| Кесарево сечение | 7,5 | 15–20 | 113–150 | 10–20 | 3–5 |
| Эпидуральная анестезия на грудном уровне | |||||
| Послеоперационная обезболивающая блокада и хирургические вмешательства | 7,5 | 5–15 | 38–113 | 10–20 | — |
| Блокада крупных нервных сплетений | |||||
| Например блокада плечевого сплетения | 7.5 | 10–40 | 75–300* | 10–25 | 6–10 |
| Проводниковая и инфильтрационная анестезия | 7,5 | 1–30 | 7,5–225 | 1–15 | 2–6 |
| Купирование острого болевого синдрома | |||||
| Эпидуральное введение на поясничном уровне | |||||
| Болюс | 2,0 | 10–20 | 20–40 | 10–15 | 0,5–1,5 |
| Периодическое введение (например, при обезболивании родов) | 2,0 | 10–15 (минимальный интервал — 30 мин) | 20–30 | — | — |
| Продленная анестезия для: | |||||
| — обезболивания родов | 2,0 | 6–10 мл/ч | 12–20 мг/ч | — | — |
| — послеоперационного обезболивания | 2,0 | 6–14 мл/ч | 12–28 мг/ч | — | — |
| Блокада периферических нервов | |||||
| Например, блокада бедренного нерва или межлестничная блокада (продленные инфузии или повторные инъекции) | 2,0 | 5–10 мл/ч | 10–20 мг/ч | — | — |
| Эпидуральное введение на грудном уровне | |||||
| Продленная инфузия (например, для послеоперационного обезболивания) | 2,0 | 6–14 мл/ч | 12–28 мг/ч | — | — |
| Проводниковая блокада и инфильтрационная анестезия | 2,0 | 1–100 | 2–200 | 1–5 | 2–6 |
| Внутрисуставное введение | |||||
| Артроскопия коленного сустава** | 7,5 | 20 | 150*** | — | 2–6 |
* Доза для блокады крупных нервных сплетений должна подбираться в соответствии с местом введения и состоянием пациента. Блокада плечевого сплетения межлестничным и надключичным доступом может быть сопряжена с высокой частотой серьезных побочных реакций вне зависимости от используемого местного анестетика.
** Сообщалось о случаях хондролиза при послеоперационной продленной внутрисуставной инфузии местных анестетиков. Наропин® не следует применять для продленной внутрисуставной инфузии.
*** Если Наропин® дополнительно использовался для других видов анестезии, максимальная доза не должна превышать 225 мг.
Для ознакомления с факторами, влияющими на метод выполнения отдельных блокад, и с требованиями, предъявляемыми к конкретным группам пациентов, следует использовать стандартные руководства.
Для предотвращения попадания анестетика в сосуд следует обязательно проводить аспирационную пробу до введения и в процессе введения препарата. Если предполагается использовать препарат в высокой дозе, рекомендуется ввести пробную дозу — 3–5 мл лидокаина с эпинефрином. Случайное внутрисосудистое введение распознается по временному увеличению частоты сердечных сокращений, а случайное интратекальное введение — по признакам спинального блока. При появлении токсических симптомов следует немедленно прекратить введение препарата.
До введения и во время введения препарата Наропин® (которое следует проводить медленно или путем увеличения вводимых последовательно доз препарата со скоростью 25–50 мг/мин) необходимо тщательно контролировать жизненно важные функции пациента и поддерживать с ним вербальный контакт.
Однократное введение ропивакаина в дозе до 250 мг при эпидуральной блокаде для проведения хирургического вмешательства обычно хорошо переносится пациентами.
При блокаде плечевого сплетения с помощью 40 мл препарата Наропин® 7,5 мг/мл максимальные плазменные концентрации ропивакаина у некоторых пациентов могут достигать значения, характеризующегося легкими симптомами токсичности со стороны центральной нервной системы. Поэтому применение дозы выше 40 мл препарата Наропин® 7,5 мг/мл (300 мг ропивакаина) не рекомендовано.
При длительном проведении блокады путем продленной инфузии или повторного болюсного введения следует учитывать возможность создания токсических концентраций анестетика в крови и местного повреждения нерва. Введение ропивакаина в течение 24 ч в дозе до 800 мг суммарно при хирургических вмешательствах и для послеоперационного обезболивания, а также продленная эпидуральная инфузия после операции со скоростью до 28 мг/ч в течение 72 ч хорошо переносится взрослыми пациентами.
Для купирования послеоперационной боли рекомендуется следующая схема применения препарата: если эпидуральный катетер не был установлен при оперативном вмешательстве, после его установки выполняется эпидуральная блокада болюсной инъекцией препарата Наропин® (7,5 мг/мл). Анальгезия поддерживается инфузией препарата Наропин® (2 мг/мл). В большинстве случаев, для купирования послеоперационной боли от умеренной до выраженной, инфузия со скоростью 6–14 мл/ч (12–28 мг/ч) обеспечивает адекватную анальгезию с минимальной не прогрессирующей двигательной блокадой (при использовании данной методики наблюдалось значительное снижение потребности в опиоидных анальгетиках).
Для послеоперационного обезболивания Наропин® (2 мг/мл) можно вводить непрерывно в виде эпидуральной инфузии в течение 72 ч без фентанила или в комбинации с ним (1–4 мкг/мл). При применении препарата Наропин® 2 мг/мл (6–14 мл/час) обеспечивалось адекватное обезболивание у большинства пациентов. Комбинация препарата Наропин® и фентанила приводила к улучшению обезболивания, вызывая при этом побочные эффекты, присущие наркотическим анальгетикам.
Использование препарата Наропин® в концентрации выше 7,5 мг/мл при кесаревом сечении не изучено.
Таблица 2
Рекомендации по дозированию препарата Наропин® для детей до 12 лет
| Концентрация препарата, мг/мл | Объем раствора, мл/кг | Доза, мг/кг | |
| Купирование острого болевого синдрома (интраоперационное и послеоперационное) | |||
| Каудальное эпидуральное введение: | |||
| Блокада в области ниже ThXII у детей с массой тела до 25 кг | 2,0 | 1 | 2 |
| Продленная эпидуральная инфузия у детей с массой тела до 25 кг | |||
| Возраст от 0 до 6 месяцев | |||
| Болюс* | 2,0 | 0,5–1 | 1–2 |
| Инфузия до 72 часов | 2,0 | 0,1 мл/кг/ч | 0,2 мг/кг/ч |
| Возраст от 6 до 12 месяцев | |||
| Болюс* | 2,0 | 0,5–1 | 1–2 |
| Инфузия до 72 часов | 2,0 | 0,2 мл/кг/ч | 0,4 мг/кг/ч |
| Возраст от 1 до 12 лет включительно | |||
| Болюс** | 2,0 | 1 | |
| Инфузия до 72 часов | 2,0 | 0,2 мл/кг/ч | 0,4 мг/кг/ч |
* Меньшие дозы из предлагаемого интервала рекомендуются для эпидурального введения на грудном уровне, в то время как большие дозы рекомендованы для эпидурального введения на поясничном или каудальном уровнях.
** Рекомендуется для эпидурального введения на поясничном уровне. Обоснованным является снижение дозы болюса для эпидуральной анальгезии на грудном уровне.
Дозы, указанные в таблице 2, являются руководством к использованию препарата в педиатрической практике. В тоже время существует индивидуальная вариабельность скорости развития блока и его длительности.
У детей с избыточной массой тела часто требуется постепенное снижение дозы препарата; при этом необходимо руководствоваться «идеальной» массой тела пациента. За справочной информацией о факторах, которые влияют на методы выполнения отдельных блокад и о требованиях, предъявляемых к конкретным группам пациентов, следует обращаться к специализированным руководствам. Объем раствора для каудального эпидурального введения и объем болюса для эпидурального введения не должны превышать 25 мл для любого пациента.
Для предотвращения непреднамеренного внутрисосудистого введения анестетика следует тщательно проводить аспирационную пробу до введения и в процессе введения препарата. Во время введения препарата необходимо тщательно контролировать жизненно важные функции пациента. При появлении токсических симптомов следует немедленно прекратить введение препарата.
Однократное введение ропивакаина в дозе 2 мг/мл (из расчета 2 мг/кг, объем раствора 1 мл/кг) для послеоперационной каудальной анальгезии обеспечивает адекватное обезболивание ниже уровня ThXII у большинства пациентов. Дети старше 4 лет хорошо переносят дозы до 3 мг/кг. Объем вводимого раствора для эпидурального введения на каудальном уровне может быть изменен с целью достижения различной распространенности сенсорного блока, что описано в специализированных руководствах.
Независимо от типа анестезии, рекомендуется болюсное введение рассчитанной дозы препарата.
Применение препарата в концентрации выше 5 мг/мл, а также интратекальное применение препарата Наропин® у детей не исследовалось. Применение препарата Наропин® у недоношенных детей не изучалось.
Инструкции по применению раствора
Раствор не содержит консервантов и предназначен только для однократного применения. Любое количество раствора, оставшегося в контейнере после использования, должно быть уничтожено.
Невскрытый контейнер с раствором не должен быть автоклавирован.
Невскрытая блистерная упаковка обеспечивает стерильность внешней поверхности контейнера и предпочтительна для использования в условиях, требующих стерильности.
Раствор для инъекций, 5 мг/мл
Препарат применяется для эпидуральной, спинальной, инфильтрационной и проводниковой анестезии.
Наропин® должен использоваться только специалистами, имеющими достаточный опыт проведения регионарной анестезии, или под их наблюдением, при наличии оборудования и лекарственных препаратов для проведения реанимационных мероприятий. До начала выполнения больших блокад должны быть установлены внутривенные катетеры.
Наропин® вводят медленно или путем увеличения вводимых последовательно доз препарата со скоростью 25–50 мг/мин.
Для предотвращения попадания анестетика в сосуд следует обязательно проводить аспирационную пробу. Случайное внутрисосудистое введение распознается по временному увеличению частоты сердечных сокращений. Приведенная таблица является ориентировочным руководством по дозированию препарата для проведения интратекальной блокады. При подборе дозы препарата следует основываться на клиническом опыте с учетом физического состояния пациента.
Таблица 3
Рекомендации по дозированию препарата Наропин® для взрослых
| Концентрация препарата, мг/мл | Объем раствора, мл | Доза, мг | Начало действия, мин | Длительность действия, ч | |
| Анестезия при хирургических вмешательствах | |||||
| Интратекальная блокада | |||||
| Хирургические вмешательства | 5,0 | 3–4 | 15–20 | 1–5 | 2–6 |
Таблица 4
Рекомендации по дозированию препарата Наропин® для детей от 1-го года:
| Концентрация препарата, мг/мл | Объем раствора, мл/кг | Доза, мг/кг | |
| Купирование острого болевого синдрома (интраоперационное и послеоперационное): | |||
| Блокада периферических нервов у детей от 1 до 12 летнего возраста включительно | |||
| (например, для блокады подвздошно-пахового нерва) | 5,0 | 0,6 | 3 |
Дозы, указанные в таблице, считаются достаточными для достижения надежной блокады и являются ориентировочными при использовании препарата у взрослых, т.к. существует индивидуальная вариабельность скорости развития блока и его длительности.
Для анестезии при кесаревом сечении интратекальный способ введения ропивакаина не изучался.
Для ознакомления с факторами, влияющими на метод выполнения отдельных блокад, и с требованиями, предъявляемыми к конкретным группам пациентов, следует использовать стандартные руководства.
Не изучено применение концентрации выше 5 мг/мл у детей, а также интратекальное введение любых концентраций препарата.
Инструкции по применению раствора
Раствор не содержит консервантов и предназначен только для однократного применения. Любое количество раствора, оставшегося в контейнере после использования, должно быть уничтожено.
Невскрытый контейнер с раствором не должен быть автоклавирован.
Невскрытая блистерная упаковка обеспечивает стерильность внешней поверхности инфузионного контейнера и предпочтительна для использования в условиях, требующих стерильности.
Ввиду отсутствия достаточного количества клинических наблюдений не рекомендуется применять Наропин® у детей в возрасте до 1-го года.
Побочные действия
Раствор для инъекций, 2; 5; 7,5; 10 мг/мл
Нежелательные реакции на Наропин® аналогичны реакциям на другие местные анестетики амидного типа. Их следует отличать от физиологических эффектов, возникающих из-за блокады симпатических нервов на фоне эпидуральной анестезии, таких как снижение АД, брадикардия или эффектов, связанных с техникой введения препарата, таких как местное повреждение нерва, менингит, постпункционная головная боль, эпидуральный абсцесс.
Побочные эффекты, присущие местным анестетикам
Со стороны центральной и периферической нервной системы: возможны нейропатия и нарушение функции спинного мозга (синдром передней спинальной артерии, арахноидит, синдром конского хвоста), обычно связанные с техникой проведения регионарной анестезии, а не с действием препарата.
В результате случайного интратекального введения эпидуральной дозы может произойти полный спинальный блок.
Возможны серьезные осложнения при системной передозировке и непреднамеренном внутрисосудистом введении препарата (см. «Передозировка»).
Острая системная токсичность: Наропин® может вызывать острые системные токсические реакции при использовании высоких доз или при быстром повышении его концентрации в крови при случайном внутрисосудистом введении препарата либо его передозировке (см. «Передозировка»).
Наиболее часто встречающиеся побочные эффекты
Сообщалось о различных побочных эффектах препарата, подавляющее большинство которых было связано не с воздействием используемого анестетика, а с техникой проведения регионарной анестезии.
Наиболее часто (>1%) отмечались следующие побочные эффекты, которые были расценены как имеющие клиническое значение, вне зависимости от того была ли установлена причинно-следственная связь с использованием анестетика: снижение АД*, тошнота, брадикардия, рвота, парестезия, повышение температуры тела, головная боль, задержка мочеиспускания, головокружение, озноб, повышение АД, тахикардия, гипестезия, беспокойство.
Частота возникновения нежелательных эффектов представлена следующим образом:
Часто (>1/100, <1/10); нечасто (>1/1000, <1/100); редко (>1/10000, <1/1000); очень редко (<1/10000), включая отдельные сообщения.
Очень часто
Со стороны ССС: снижение АД*.
Со стороны ЖКТ тошнота.
Часто
Со стороны нервной системы: парестезия, головокружение, головная боль.
Со стороны ССС: брадикардия, тахикардия, гипертензия.
Со стороны ЖКТ: рвота**.
Со стороны мочеполовой системы: задержка мочеиспускания.
Общие: боль в спине, озноб, повышение температуры тела.
Нечасто
Со стороны нервной системы: беспокойство, симптомы токсичности со стороны ЦНС (судороги, большие судорожные припадки, парестезии в околоротовой зоне, дизартрия, онемение языка, нарушения зрения, звон в ушах, тремор, мышечные судороги), гипестезия.
Со стороны сосудистой системы: обморок.
Со стороны дыхательной системы: одышка, затрудненное дыхание.
Общие: гипотермия.
Редко
Со стороны ССС: аритмия, остановка сердца.
Общие: аллергические реакции (анафилактические реакции, ангионевротический отек, крапивница).
* Снижение АД встречается у детей часто.
** Рвота встречается у детей очень часто.
Взаимодействие
Раствор для инъекций, 2; 7,5; 10 мг/мл
Возможно суммирование токсических эффектов при одновременном назначении с другими местными анестетиками или препаратами, структурно сходными с местными анестетиками амидного типа.
Клиренс ропивакаина уменьшается до 77% при одновременном применении с флувоксамином, являющимся мощным конкурентным ингибитором изофермента CYP1A2; из-за возможности такого взаимодействия следует избегать длительного применения Наропина® на фоне действия флувоксамина.
Раствор Наропина® (концентрация — 1–2 мг/мл) в пластиковых инфузионных мешках по своим химическим и физическим свойствам совместим со следующими лекарственными препаратами: фентанил в концентрации 1,0–10,0 мкг/мл; морфин в концентрации 20,0–100,0 мкг/мл.
Несмотря на тот факт, что полученные смеси сохраняют химическую и физическую стабильность в течение 30 дней при температуре не выше 30 °С, исходя из данных по микробиологической чистоте, следует использовать полученные смеси растворов немедленно после приготовления.
Раствор для инъекций, 5 мг/мл
Возможно суммирование токсических эффектов при одновременном применении с другими местными анестетиками или препаратами, структурно сходными с местными анестетиками амидного типа.
Клиренс ропивакаина уменьшается до 77% при одновременном применении с флувоксамином (мощный конкурентный ингибитор изофермента CYP1A2); из-за возможности сходного взаимодействия следует избегать длительного применения препарата Наропин® на фоне действия флувоксамина.
Передозировка
Раствор для инъекций, 2; 5; 7,5; 10 мг/мл
Острая системная токсичность. При случайном внутрисосудистом введении при проведении блокад нервных сплетений или других периферических блокад наблюдались случаи возникновения судорог.
В случае неправильного введения эпидуральной дозы анестетика интратекально возможно возникновение полного спинального блока.
Случайное внутрисосудистое введение анестетика может вызвать немедленную токсическую реакцию.
При передозировке во время проведения регионарной анестезии симптомы системной токсической реакции появляются в отсроченном порядке через 15–60 мин после инъекции из-за медленного повышения концентрации местного анестетика в плазме крови. Системная токсичность в первую очередь проявляется симптомами со стороны центральной нервной системы (ЦНС) и сердечно-сосудистой системы. Данные реакции вызываются высокими концентрациями местного анестетика в крови, которые могут возникнуть вследствие (случайного) внутрисосудистого введения, передозировки или исключительно высокой адсорбции из сильно васкуляризированных областей. Реакции со стороны ЦНС схожи для всех местных анестетиков амидного типа, в то время как реакции со стороны сердечно-сосудистой системы в большей степени зависят от введенного препарата и его дозы.
Центральная нервная система
Проявления системной токсичности со стороны центральной нервной системы развиваются постепенно: сначала появляются расстройства зрения, онемение вокруг рта, онемение языка, гиперакузия, звон в ушах, головокружение. Дизартрия, тремор и мышечные подергивания являются более серьезными проявлениями системной токсичности и могут предшествовать появлению генерализованных судорог (эти признаки не должны приниматься за невротическое поведение пациента). При прогрессировании интоксикации может наблюдаться потеря сознания, приступы судорог продолжительностью от нескольких секунд до нескольких минут, сопровождающиеся нарушением дыхания, быстрым развитием гипоксии и гиперкапнии из-за повышенной мышечной активности и неадекватной вентиляции. В тяжелых случаях может даже наступить остановка дыхания. Возникающие ацидоз, гиперкалиемия, гипокальциемия усиливают токсические эффекты анестетика.
Впоследствии, из-за перераспределения анестетика из ЦНС и его последующего метаболизма и экскреции, происходит достаточно быстрое восстановление функций, если только не была введена большая доза препарата.
Сердечно-сосудистая система
Расстройства со стороны сердечно-сосудистой системы являются признаками более серьезных осложнений. Снижение АД, брадикардия, аритмия и в ряде случаев даже остановка сердца могут возникать вследствие высокой системной концентрации местных анестетиков. В редких случаях остановка сердца не сопровождается предшествующей симптоматикой со стороны ЦНС. В исследованиях у добровольцев внутривенная инфузия ропивакаина приводила к угнетению проводимости и сократительной способности сердечной мышцы. Симптомам со стороны сердечно-сосудистой системы обычно предшествуют проявления токсичности со стороны ЦНС, которые можно не заметить, если больной находится под действием седативных средств (бензодиазепины или барбитураты) или под общей анестезией.
У детей ранние признаки системной токсичности местных анестетиков иногда сложнее выявить вследствие затруднений, испытываемых детьми при описании симптомов, или в случае применения регионарной анестезии в сочетании с общей анестезией.
Лечение острой токсичности
При появлении первых признаков острой системной токсичности следует немедленно прекратить введение препарата.
При появлении судорог и симптомов угнетения ЦНС больному требуется адекватное лечение, целью которого является поддержание оксигенации, купирование судорог, поддержание деятельности сердечно-сосудистой системы. Следует обеспечить оксигенацию кислородом, а при необходимости — переход на искусственную вентиляцию легких. Если спустя 15–20 секунд судороги не прекращаются, следует использовать противосудорожные средства: тиопентал натрия 1–3 мг/кг в/в (обеспечивает быстрое купирование судорог) или диазепам 0,1 мг/кг в/в (действие развивается медленнее по сравнению с действием тиопентала натрия). Суксаметоний 1 мг/кг быстро купирует судороги, но при его использовании требуется интубация и искусственная вентиляция легких.
При угнетении деятельности сердечно-сосудистой системы (снижение АД, брадикардия) необходимо внутривенное введение 5–10 мг эфедрина, при необходимости через 2–3 мин введение повторить. При развитии циркуляторной недостаточности или остановке сердца следует немедленно начать стандартные реанимационные мероприятия. Жизненно важно поддерживать оптимальную оксигенацию, вентиляцию и циркуляцию крови, а также корректировать ацидоз. При остановке сердца могут потребоваться более длительные реанимационные мероприятия.
При терапии системной токсичности у детей необходимо корректировать дозы соответственно возрасту и массе тела пациента.
Особые указания
Раствор для инъекций, 2; 5; 7,5; 10 мг/мл
Анестезия должна проводиться опытными специалистами. Обязательно наличие оборудования и лекарственных препаратов для проведения реанимационных мероприятий. До начала выполнения больших блокад должен быть установлен внутривенно катетер.
Персонал, обеспечивающий выполнение анестезии, должен быть соответствующим образом подготовлен и знаком с диагностикой и лечением возможных побочных эффектов, системных токсических реакций и других возможных осложнений (см. раздел «Передозировка»).
Осложнением непреднамеренного субарахноидального введения может являться спинальный блок с остановкой дыхания и снижением АД. Конвульсии развиваются чаще при блокаде плечевого сплетения и эпидуральной блокаде, вероятно, вследствие случайного внутрисосудистого введения или быстрой абсорбции в месте инъекции.
Выполнение блокад периферийных нервов может требовать введение большого объема местного анестетика в зоны с большим количеством сосудов, часто — вблизи крупных сосудов, что повышает риск внутрисосудистого введения и/или быстрого системного всасывания, что может привести к высокой концентрации препарата в плазме.
Некоторые процедуры, связанные с применением местных анестетиков, такие как инъекции в области головы и шеи, могут сопровождаться повышенной частотой развития серьезных побочных эффектов, вне зависимости от типа применяемого местного анестетика. Необходимо соблюдать осторожность для предотвращения инъекции в область воспаления.
Следует соблюдать осторожность при введении препарата пациентам с блокадой внутрисердечной проводимости II и III степеней, пациентам с тяжелой почечной недостаточностью, пожилым и ослабленным пациентам.
Имеются сообщения о редких случаях остановки сердца при применении препарата Наропин® для эпидуральной анестезии или блокады периферических нервов, особенно после случайного внутрисосудистого введения препарата, у пожилых пациентов и у пациентов с сопутствующими сердечно-сосудистыми заболеваниями.
В ряде случаев реанимационные мероприятия были затруднительны. Остановка сердца, как правило, требует более длительных реанимационных мероприятий.
Поскольку Наропин® метаболизируется в печени, следует проявлять осторожность при применении препарата у больных с тяжелыми заболеваниями печени; в некоторых случаях из-за замедленной элиминации может возникнуть необходимость уменьшения повторно вводимых доз анестетика.
Обычно у больных с почечной недостаточностью при введении препарата однократно или при использовании препарата в течение непродолжительного периода времени не требуется корректировать дозу. Однако ацидоз и снижение концентрации белков в плазме крови, часто развивающиеся у больных с хронической почечной недостаточностью, могут повышать риск системного токсического действия препарата (см. «Способ применения и дозы»). Риск системной токсичности также повышен при применении препарата у пациентов с пониженной массой тела и пациентов с гиповолемическим шоком.
Эпидуральная анестезия может приводить к снижению АД и брадикардии. Введение сосудосуживающих препаратов или увеличение ОЦК может уменьшить риск развития подобных побочных эффектов. Следует своевременно корректировать снижение АД путем внутривенного введения 5–10 мг эфедрина, при необходимости повторного.
При внутрисуставном введении препарата следует соблюдать осторожность при подозрении на наличие недавней обширной травмы сустава или хирургической операции со вскрытием обширных поверхностей сустава в связи возможностью усиления абсорбции препарата и более высокой концентрации препарата в плазме.
Пациенты, получающие терапию антиаритмическими препаратами III класса (например, амиодароном), должны находиться под тщательным наблюдением, рекомендуется ЭКГ-мониторинг в связи с риском усиления сердечно-сосудистых эффектов.
Следует избегать длительного применения препарата Наропин® у пациентов, принимающих сильные ингибиторы Р4501А2 (такие как флувоксамин и эноксацин).
Следует учитывать возможность перекрестной гиперчувствительности при одновременном применении препарата Наропин® с другими местными анестетиками амидного типа.
Повышение рН раствора выше 6,0 может привести к образованию преципитата из-за плохой растворимости ропивакаина при данных условиях.
Пациентам, находящимся на диете с ограничением натрия, необходимо принимать во внимание содержание натрия в препарате.
Применение препарата у новорожденных требует учета возможной незрелости органов и физиологических функций новорожденных. Клиренс несвязанной фракции ропивакаина и пипелоксилидина (ППК) зависит от массы тела и возраста ребенка в первые годы жизни. Влияние возраста выражается в развитии и зрелости функции печени, клиренс достигает максимального значения в возрасте около 1–3 лет. T1/2 ропивакаина составляет 5–6 ч у новорожденных и детей в возрасте 1 мес по сравнению с 3 ч у детей более старшего возраста. В связи с недостаточным развитием функций печени системная экспозиция ропивакаина выше у новорожденных, умеренно выше — у детей от 1 до 6 мес по сравнению с детьми более старшего возраста. Значительные отличия в концентрациях ропивакаина в плазме крови новорожденных, выявленные в клинических исследованиях, позволяют предполагать повышенный риск возникновения системной токсичности в этой группе пациентов, особенно при продленной эпидуральной инфузии.
Рекомендованные дозы для новорожденных основаны на ограниченных клинических данных.
При использовании ропивакаина у новорожденных необходимо мониторирование системной токсичности (контроль признаков токсичности со стороны ЦНС, ЭКГ, контроль оксигенации крови) и местной нейротоксичности, которые следует продолжать после завершения инфузии из-за медленного выведения препарата у новорожденных.
Применение препарата в концентрации выше 5 мг/мл, а также интратекальное применение препарата Наропин® у детей не исследовалось.
Наропин® потенциально способен вызывать порфирию и может применяться у пациентов с диагнозом острая порфирия только в случаях, если нет более безопасной альтернативы. В случае повышенной чувствительности пациентов должны быть приняты необходимые меры предосторожности.
Сообщалось о случаях хондролизиса при постоперационной продленной внутрисуставной инфузии местных анестетиков. В большинстве описанных случаев проводилась инфузия в плечевой сустав. Причинно-следственная связь с приемом анестетиков не установлена. Наропин® не следует применять для продленной внутрисуставной инфузии.
Влияние на способность управлять транспортными средствами и другими механизмами. Помимо анальгезирующего эффекта, Наропин® может оказывать слабое транзиторное влияние на двигательную функцию и координацию. Учитывая профиль побочных эффектов препарата, необходимо соблюдать осторожность при управлении транспортными средствами и выполнении других потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
Форма выпуска
Раствор для инъекций 2 мг/мл: По 20 мл в запаянных ампулах из полипропилена. Каждую ампулу помещают в контурную ячейковую упаковку. 5 контурных ячейковых упаковок с инструкцией по применению в картонной пачке с контролем первого вскрытия.
По 100 мл или 200 мл в полипропиленовых контейнерах (мешках), укупоренных бутилкаучуковой пробкой и листовидной алюминиевой пластинкой. Полипропиленовые контейнеры (мешки) индивидуально упакованы в контурную ячейковую упаковку из полипропилена/бумаги. По 5 контурных ячейковых упаковок в картонной пачке с инструкцией по применению.
Раствор для инъекций 7,5 мг/мл и 10 мг/мл: По 10 мл в запаянных ампулах из полипропилена. Каждую ампулу помещают в контурную ячейковую упаковку. 5 контурных ячейковых упаковок с инструкцией по применению в картонной пачке с контролем первого вскрытия.
Раствор для инъекций 5 мг/мл. По 10 мл в запаянных ампулах из полипропилена. Каждую ампулу помещают в контурную ячейковую упаковку. 5 контурных ячейковых упаковок с инструкцией по применению в картонной пачке с контролем первого вскрытия.
Производитель
Раствор для инъекций 2 мг/мл; 5 мг/мл; 7,5 мг/мл; 10 мг/мл (ампулы). АстраЗенека АБ, SE-151 85 Содерталье, Швеция;
Раствор для инъекций 2 мг/мл (мешки). АстраЗенека Пти Лтд, Австралия, 10-14 Картоум Роуд, Норт Райд, Новый Южный Уэльс 2113.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение. Аспен Фарма Трейдинг Лимитед, 3016 Лейк Драйв, Ситивест Бизнес Кампус, Дублин 24, Ирландия.
Наименование, адрес организации, уполномоченной владельцем регистрационного удостоверения лекарственного препарата для медицинского применения на принятие претензий от потребителя. ООО «Аспен Хэлс», 123317, Москва, Пресненская наб., 6/2, эт. 31-й.
Тел.: (495) 969-20-51; факс: (495) 969-20-53.
Комментарий
Перед использованием препарата необходимо прочитать инструкцию по применению.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре не выше 30 °C (не замораживать).
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Рапинов
Р-р д/инъекц. 10 мг/мл: 10 мл амп. 5, 10 или 25 шт.
рег. №: ЛП-005515
от 14.05.19
Дата перерегистрации: 20.06.19
Рапинов
Р-р д/инъекц. 2 мг/мл: 10 мл амп. 5, 10 или 25 шт.
рег. №: ЛП-005515
от 14.05.19
Дата перерегистрации: 20.06.19
Р-р д/инъекц. 5 мг/мл: 10 мл амп. 5, 10 или 25 шт.
рег. №: ЛП-005515
от 14.05.19
Дата перерегистрации: 20.06.19
Р-р д/инъекц. 7.5 мг/мл: 10 мл амп. 5, 10 или 25 шт.
рег. №: ЛП-005515
от 14.05.19
Дата перерегистрации: 20.06.19
Ропивабин®
Р-р д/инъекц. 10 мг/мл: амп. 10 мл 5 или 10 шт.
рег. №: ЛП-005773
от 04.09.19
Ропивабин®
Р-р д/инъекц. 2 мг/мл: фл. 100 мл и 200 мл.
рег. №: ЛП-005773
от 04.09.19
Ропивабин®
Р-р д/инъекц. 5 мг/мл: амп. 10 мл 5 или 10 шт.
рег. №: ЛП-005773
от 04.09.19
Ропивабин®
Р-р д/инъекц. 7.5 мг/мл: амп. 10 мл 5 или 10 шт.
рег. №: ЛП-005773
от 04.09.19
Ропивакаин
Р-р д/инъекц. 10 мг/мл: 10 или 20 мл фл. 5 шт.
рег. №: ЛП-004182
от 15.03.17
Ропивакаин
Р-р д/инъекц. 2 мг/мл: 10 или 20 мл фл. 5 шт.
рег. №: ЛП-004182
от 15.03.17
Ропивакаин
Р-р д/инъекц. 2 мг/мл: 100 мл или 200 мл фл.
рег. №: ЛП-006427
от 25.08.20
Ропивакаин
Р-р д/инъекц. 2 мг/мл: амп. 10 мл 5 шт.
рег. №: ЛП-005582
от 13.06.19
Р-р д/инъекц. 5 мг/мл: амп. 10 мл 5 шт.
рег. №: ЛП-005582
от 13.06.19
Р-р д/инъекц. 7.5 мг/мл: амп. 10 мл 5 шт.
рег. №: ЛП-005582
от 13.06.19
Р-р д/инъекц. 10 мг/мл: амп. 10 мл 5 шт.
рег. №: ЛП-005582
от 13.06.19
Ропивакаин
Р-р д/инъекц. 2 мг/мл: амп. 10 мл или 20 мл 5 или 10 шт.
рег. №: ЛП-006080
от 06.02.20
Р-р д/инъекц. 5 мг/мл: амп. 10 мл или 20 мл 5 или 10 шт.
рег. №: ЛП-006080
от 06.02.20
Р-р д/инъекц. 7.5 мг/мл: амп. 10 мл или 20 мл 5 или 10 шт.
рег. №: ЛП-006080
от 06.02.20
Р-р д/инъекц. 10 мг/мл: амп. 10 мл или 20 мл 5 или 10 шт.
рег. №: ЛП-006080
от 06.02.20
Ропивакаин
Р-р д/инъекц. 2 мг/мл: фл. 10 мл 5. 10 или 20 шт.
рег. №: ЛП-005873
от 22.10.19
Р-р д/инъекц. 5 мг/мл: фл. 10 мл 5. 10 или 20 шт.
рег. №: ЛП-005873
от 22.10.19
Р-р д/инъекц. 7.5 мг/мл: фл. 10 мл 5. 10 или 20 шт.
рег. №: ЛП-005873
от 22.10.19
Р-р д/инъекц. 10 мг/мл: фл. 10 мл 5. 10 или 20 шт.
рег. №: ЛП-005873
от 22.10.19
Ропивакаин
Р-р д/инъекц. 5 мг/мл: 10 или 20 мл фл. 5 шт.
рег. №: ЛП-004182
от 15.03.17
Ропивакаин
Р-р д/инъекц. 7.5 мг/мл: 10 или 20 мл фл 5 шт.
рег. №: ЛП-004182
от 15.03.17
Ропивакаин
Р-р д/инъекций 2 мг/мл: амп. 10 мл 5, 10 или 25 шт.
рег. №: ЛП-004738
от 13.03.18
Р-р д/инъекций 5 мг/мл: амп. 10 мл 5, 10 или 25 шт.
рег. №: ЛП-004738
от 13.03.18
Р-р д/инъекций 7.5 мг/мл: амп. 10 мл 5, 10 или 25 шт.
рег. №: ЛП-004738
от 13.03.18
Р-р д/инъекций 10 мг/мл: амп. 10 мл 5, 10 или 25 шт.
рег. №: ЛП-004738
от 13.03.18
Ропивакаин
Раствор д/инъекций 2 мг/мл
рег. №: ЛП-008154
от 12.05.22
Раствор д/инъекций 5 мг/мл
рег. №: ЛП-008154
от 12.05.22
Раствор д/инъекций 7.5 мг/мл
рег. №: ЛП-008154
от 12.05.22
Раствор д/инъекций 10 мг/мл
рег. №: ЛП-008154
от 12.05.22
Ропивакаин Бинергия
Р-р д/инъекц. 10 мг/мл: 10 мл или 20 мл амп. 5 шт.
рег. №: ЛП-004935
от 18.07.18
Ропивакаин Бинергия
Р-р д/инъекц. 2 мг/мл: 5 мл, 10 мл или 20 мл амп. 5 или 10 шт., 100 или 200 мл: фл. 1 или 5 шт.
рег. №: ЛП-004935
от 18.07.18
Ропивакаин Бинергия
Р-р д/инъекц. 5 мг/мл: 10 мл или 20 мл амп. 5 шт.
рег. №: ЛП-004935
от 18.07.18
Ропивакаин Бинергия
Р-р д/инъекц. 7.5 мг/мл: 10 мл или 20 мл амп. 5 шт.
рег. №: ЛП-004935
от 18.07.18
Ропивакаин Велфарм
Р-р д/инъекц. 10 мг/мл: 5 мл, 10 мл или 20 мл амп. 5 или 10 шт.
рег. №: ЛП-004802
от 13.04.18
Ропивакаин Велфарм
Р-р д/инъекц. 2 мг/мл: 5 мл, 10 мл или 20 мл амп. 5 или 10 шт.
рег. №: ЛП-004802
от 13.04.18
Р-р д/инъекц. 5 мг/мл: 5 мл, 10 мл или 20 мл амп. 5 или 10 шт.
рег. №: ЛП-004802
от 13.04.18
Р-р д/инъекц. 7.5 мг/мл: 5 мл, 10 мл или 20 мл амп. 5 или 10 шт.
рег. №: ЛП-004802
от 13.04.18
Ропивакаин Каби
Р-р д/инъекц. 2 мг/1 мл: амп. 10 мл или 20 мл 1 или 5 шт., контейнеры 100 мл или 200 мл 5 шт.
рег. №: ЛП-002897
от 04.03.15
Р-р д/инъекц. 7.5 мг/1 мл: амп. 10 мл или 20 мл 1 или 5 шт.
рег. №: ЛП-002897
от 04.03.15
Р-р д/инъекц. 10 мг/1 мл: амп. 10 мл или 20 мл 1 или 5 шт.
рег. №: ЛП-002897
от 04.03.15
Ропивакаин Каби
Р-р д/инъекц. 5 мг/1 мл: амп. 10 мл 1 или 5 шт.
рег. №: ЛП-002897
от 04.03.15
Ропивакаин НоваМедика
Р-р д/инъекц. 2 мг/мл: фл. 20 мл 5 шт, 100 мл 1 шт.
рег. №: ЛП-006667
от 23.12.20
Р-р д/инъекц. 5 мг/мл: фл. 10 мл 5 шт.
рег. №: ЛП-006667
от 23.12.20
Р-р д/инъекц. 7.5 мг/мл: фл. 10 мл 5 шт.
рег. №: ЛП-006667
от 23.12.20
Р-р д/инъекц. 10 мг/мл: фл. 10 мл 5 шт.
рег. №: ЛП-006667
от 23.12.20
Групповые аналоги: 56
| Название | Форма выпуска | Владелец рег. уд. | ||
|
Артикаин-Бинергия с адреналином |
|
Р-р д/инъекц. 20 мг+0.005 мг/1 мл: амп. 2 мл 10 шт. или 5 мл 5 шт.; картриджи 1.7 мл 10 шт. рег. №: ЛП-004013 |
БИНЕРГИЯ (Россия) Произведено: АРМАВИРСКАЯ БИОФАБРИКА (Россия) контакты: БИНЕРГИЯ АО (Россия) |
|
|
Артикаин+Эпинефрин |
Р-р д/инъекц. (10 мг+0.005 мг)/мл: амп. 1 мл, 2 мл, 5 мл, 10 мл или 20 мл; 5, 10, 100 или 250 шт. рег. №: ЛП-008640 Р-р д/инъекц. (20 мг+0.005 мг)/мл: амп. 1 мл, 2 мл, 5 мл, 10 мл или 20 мл; 5, 10, 100 или 250 шт. рег. №: ЛП-008640 Р-р д/инъекц. (40 мг+0.005 мг)/мл: амп. 1 мл или 2 мл; 5, 10, 100 или 250 шт. рег. №: ЛП-008640 Р-р д/инъекц. (40 мг+0.01 мг)/мл: амп. 1 мл или 2 мл; 5, 10, 100 или 250 шт. рег. №: ЛП-008640 |
ВЕЛФАРМ (Россия) |
||
|
БлоккоС® |
Р-р д/инъекц. 20 мг/4 мл: амп. 5 или 10 шт. рег. №: ЛСР-010453/09 |
ФармФирма Сотекс (Россия) контакты: ФармФирма Сотекс ЗАО (Россия) |
||
|
БлоккоС® Хэви |
Р-р д/инъекц. 5 мг/мл: 4 мл амп. 5 или 10 шт. рег. №: ЛП-(000201)-(РГ-RU ) Предыдущий рег. №: ЛП-005071 |
ФармФирма Сотекс (Россия) |
||
|
Бупивакаин |
Р-р д/инъекц. 5 мг/1 мл: 4 мл амп. 5 или 10 шт. рег. №: ЛП-003590 |
ОЗОН (Россия) |
||
|
Бупивакаин |
Р-р д/инъекц. 5 мг/1 мл: 4 мл, 10 мл или 20 мл амп. 5 или 10 шт., 20 мл фл. 5 шт. рег. №: ЛП-002824 |
ВЕЛФАРМ (Россия) Произведено: СИНТЕЗ (Россия) |
||
|
Бупивакаин |
Р-р д/инъекц. 5 мг/1 мл: амп. 2 мл или 4 мл 3, 5, 10 или 20 шт. рег. №: ЛП-007887 |
Химико-фармацевтический концерн МИР (Россия) Произведено: ЭСКОМ НПК (Россия) Упаковка и выпускающий контроль качества: ЭСКОМ НПК (Россия) |
||
|
Бупивакаин |
Р-р д/инъекц. 5 мг/мл: 4 мл или 10 мл амп. 5 или 10 шт. рег. №: ЛП-005956 |
Б-ФАРМ (Россия) Произведено: ФНЦИРИП им. М.П. Чумакова РАН (Россия) |
||
|
Бупивакаин |
Р-р д/инъекц. 5 мг/мл: 4 мл или 10 мл амп. 5 или 10 шт. рег. №: ЛП-003827 |
ГРОТЕКС (Россия) |
||
|
Бупивакаин |
Р-р д/инъекц. 5 мг/мл: 4 мл или 10 мл амп. 5 или 10 шт. рег. №: ЛП-005822 |
ЭКОФАРМПЛЮС (Россия) |
||
|
Бупивакаин Гриндекс |
Р-р д/инъекц. 5 мг/1 мл: амп. 10 мл 5 шт. рег. №: ЛСР-006093/10 |
ГРИНДЕКС (Латвия) Произведено: SANTONIKA (Литва) HBM PHARMA (Словакия) контакты: ГРИНДЕКС АО (Латвия) |
||
|
Бупивакаин Гриндекс Спинал |
Р-р д/интратекального введения 5 мг/1 мл: амп. 4 мл 5 шт. рег. №: ЛСР-006092/10 |
ГРИНДЕКС (Латвия) Произведено: SANTONIKA (Литва) HBM PHARMA (Словакия) контакты: ГРИНДЕКС АО (Латвия) |
||
|
Бупивакаин Спинал Хэви |
Р-р д/инъекц. 5 мг/мл: 4 мл амп. 5 или 10 шт. рег. №: ЛП-005181 |
ФК ЭГЕН (Россия) Произведено: КУРСКАЯ БИОФАБРИКА — ФИРМА «БИОК» (Россия) |
||
|
Бупивакаин-Бинергия |
Р-р д/инъекц. 5 мг/мл: 10 мл или 20 мл фл. 5 шт. рег. №: ЛП-002462 |
БИНЕРГИЯ (Россия) Произведено: АРМАВИРСКАЯ БИОФАБРИКА (Россия) |
||
|
Бупивакаин-Лекфарм Спинал хэви |
Р-р д/интратекального введения 5 мг/мл: 4 мл амп. 5 или 10 шт. рег. №: ЛП-005043 |
ЛЕКФАРМ (Республика Беларусь) |
||
|
Валекаин |
Р-р д/инъекц. 5 мг/1 мл: фл. 4 мл 1 или 5 шт., 10 мл 5, 10 или 20 шт. рег. №: ЛП-005829 |
КРАСФАРМА (Россия) |
||
|
Леколт |
Р-р д/инъекц. 20 мг/мл: 2 мл, 5 мл или 10 мл амп. 5 или 10 шт. рег. №: ЛП-006954 |
ВЕЛТРЭЙД (Россия) Произведено: ВЕЛФАРМ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 1% (100 мг/10 мл): амп. 10 шт. рег. №: Р N003576/01 |
ОРГАНИКА (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 1% (50 мг/5 мл): амп. 10 шт. рег. №: Р N003576/01 |
ОРГАНИКА (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 1%: 2 мл амп. 10 шт. рег. №: ЛП-006463 |
ФАРМСТАНДАРТ-УфаВИТА (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 10 мг/1 мл: амп. 10 мл 5 или 10 шт. рег. №: Р N001276/01 |
БИОСИНТЕЗ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 10 мг/1 мл: амп. 3.5 мл, 5 мл или 10 мл 10 шт. рег. №: Р N001261/01 |
ДАЛЬХИМФАРМ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 10 мг/1 мл: амп. 5 мл 5 или 10 шт. рег. №: Р N001276/01 |
БИОСИНТЕЗ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 10 мг/мл: 3.5 мл или 5 мл амп. 5 или 10 шт. рег. №: ЛП-006179 |
ПРОМОМЕД РУС (Россия) Произведено: БИОХИМИК (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 2% (100 мг/5 мл): амп. 10 шт. рег. №: Р N003576/01 |
ОРГАНИКА (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 2% (200 мг/10 мл): амп. 10 шт. рег. №: Р N003576/01 |
ОРГАНИКА (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 2% (40 мг/2 мл): амп. 10 шт. рег. №: П N015364/01 |
БОРИСОВСКИЙ ЗАВОД МЕДИЦИНСКИХ ПРЕПАРАТОВ (Республика Беларусь) |
||
|
Лидокаин |
Р-р д/инъекц. 2% (40 мг/2 мл): амп. 10 шт. рег. №: ЛС-001516 |
ПРОМОМЕД РУС (Россия) Произведено: БИОХИМИК (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/1 мл: 2 мл или 10 мл амп. 10 шт. рег. №: ЛП-003014 |
ГРОТЕКС (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/1 мл: 2 мл, 5 мл или 10 мл амп. 10 шт. рег. №: ЛП-003201 |
ФАРМСИНТЕЗ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/1 мл: амп. 10 мл 5 или 10 шт. рег. №: Р N001276/01 |
БИОСИНТЕЗ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/1 мл: амп. 2 мл 5 или 10 шт. рег. №: Р N001276/01 |
БИОСИНТЕЗ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/1 мл: амп. 2 мл 5 или 10 шт., фл. 10 мл 1 шт. рег. №: П N015203/01 |
БЕЛМЕДПРЕПАРАТЫ (Республика Беларусь) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/1 мл: амп. 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N001261/01 |
ДАЛЬХИМФАРМ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/1 мл: амп. 5 мл 5 или 10 шт. рег. №: Р N001276/01 |
БИОСИНТЕЗ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/мл: 2 мл амп. 10 шт. рег. №: Р N000109/01 |
НОВОСИБХИМФАРМ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/мл: 2 мл амп. 10 шт. рег. №: ЛП-004497 |
НПЦ ФАРМЗАЩИТА (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/мл: 2 мл, 5 мл или 10 мл амп. 5 или 10 шт. рег. №: ЛП-006863 |
БРАЙТ ВЭЙ (Россия) Произведено: ВЕЛФАРМ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/мл: амп. 100 шт. рег. №: ЛП-002574 |
СЛАВЯНСКАЯ АПТЕКА (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/мл: амп. 2 мл 10 шт. рег. №: Р N001276/01 |
БИОСИНТЕЗ (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 20 мг/мл: амп. 5 или 10 шт. рег. №: ЛП-001065 |
ЭЛЛАРА (Россия) Произведено: МЦ ЭЛЛАРА (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 200 мг/10 мл: амп. 10 шт. рег. №: Р N000318/01 |
МОСХИМФАРМПРЕПАРАТЫ им. Н.А.Семашко (Россия) |
||
|
Лидокаин |
|
Р-р д/инъекц. 40 мг/2 мл: амп. 10 шт. рег. №: Р N003576/01 |
ОРГАНИКА (Россия) |
|
|
Лидокаин |
Р-р д/инъекц. 40 мг/2 мл: амп. 10 шт. рег. №: Р N000979/01 |
АТОЛЛ (Россия) Произведено: ОЗОН (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 40 мг/2 мл: амп. 10 шт. рег. №: Р N000318/01 |
МОСХИМФАРМПРЕПАРАТЫ им. Н.А.Семашко (Россия) |
||
|
Лидокаин |
Р-р д/инъекц. 40 мг/2 мл: амп. 10 шт. рег. №: ЛСР-007747/09 |
АРМАВИРСКАЯ БИОФАБРИКА (Россия) |
||
|
Лидокаин Буфус |
Р-р д/инъекц. 40 мг/2 мл: амп. 10 шт. рег. №: ЛСР-001475/09 |
ОБНОВЛЕНИЕ ПФК (Россия) |
||
|
Лидокаин Велфарм |
Р-р д/инъекц. 10 мг/мл: 5 мл или 10 мл амп. 5 или 10 шт. рег. №: ЛП-004707 Р-р д/инъекц. 20 мг/мл: 2 мл, 5 мл или 10 мл амп. 5 или 10 шт. рег. №: ЛП-004707 |
ВЕЛФАРМ (Россия) |
||
|
Лидокаин ДС |
Р-р д/инъекц. 20 мг/мл: 2 мл амп. 5 или 10 шт. рег. №: ЛП-006162 |
DANHSON-BG (Болгария) Произведено: VETPROM (Болгария) |
||
|
Лидокаин-Эском |
Р-р д/инъекц. 20 мг/мл: 2 мл, 5 мл или 10 мл амп. рег. №: ЛП-006444 |
ЭСКОМ НПК (Россия) |
||
|
Лидокаина гидрохлорид |
Р-р д/инъекц. 2% (40 мг/2 мл): амп. 10 шт. рег. №: Р N001097/01 |
ФАРМСТАНДАРТ-УФИМСКИЙ ВИТАМИННЫЙ ЗАВОД (Россия) |
||
|
Максикаин® |
Р-р д/инъекц. 5 мг/1 мл: амп. 4 или 10 мл 10 или 20 шт. рег. №: ЛП-003624 |
НОВОСИБХИМФАРМ (Россия) |
||
|
Маркаин Спинал |
Р-р д/инъекц. 20 мг/4 мл: амп. 5 шт. рег. №: П N014031/01 |
ASTRAZENECA (Швеция) Произведено: CENEXI (Франция) |
||
|
Маркаин® Спинал |
Р-р д/инъекц. 20 мг/4 мл: амп. 5 шт. рег. №: П N014031/01 |
ASPEN PHARMA TRADING (Ирландия) Произведено: CENEXI (Франция) |
||
|
Маркаин® Спинал Хэви |
Р-р д/инъекц. 20 мг/4 мл: амп. 5 шт. рег. №: П N014032/01 |
ASPEN PHARMA TRADING (Ирландия) Произведено: CENEXI (Франция) |
||
|
Хирокаин |
Р-р д/инъекций 5 мг/1 мл: амп. 10 мл 10 шт. рег. №: ЛП-003106 Р-р д/инъекций 7.5 мг/1 мл: амп. 10 мл 10 шт. рег. №: ЛП-003106 |
ЭббВи (Россия) Произведено: CURIDA AS (Норвегия) Выпускающий контроль качества: AbbVie (Италия) |
Нозологические аналоги: 104
| Название | Форма выпуска | Владелец рег. уд. | ||
|
Альфакаин СП |
Р-р д/инъекций 72 мг+0.0216 мг/1.8 мл: картриджи 100 шт. рег. №: П N009007 |
DENTSPLY FRANCE (Франция) Произведено: WEIMER PHARMA (Германия) Выпускающий контроль качества: WEIMER PHARMA (Германия) DENTSPLY FRANCE (Франция) |
||
|
Артикаин |
Р-р д/инъекц. 10 мг/мл: амп. 1 мл, 2 мл, 5 мл, 10 мл или 20 мл амп. 5 или 10 шт. рег. №: ЛП-006851 Р-р д/инъекц. 20 мг/мл: амп. 1 мл, 2 мл, 5 мл, 10 мл или 20 мл амп. 5 или 10 шт. рег. №: ЛП-006851 Р-р д/инъекц. 40 мг/мл: амп. 1 мл, 2 мл, 5 мл, 10 мл или 20 мл амп. 5 или 10 шт. рег. №: ЛП-006851 |
ВЕЛФАРМ (Россия) |
||
|
Артикаин |
|
Р-р д/инъекц. 40 мг/1 мл: амп. 2 мл 10 шт.; картриджи 1.7 мл 50 шт. рег. №: ЛСР-008522/10 |
БИНЕРГИЯ (Россия) Произведено: АРМАВИРСКАЯ БИОФАБРИКА (Россия) контакты: БИНЕРГИЯ АО (Россия) |
|
|
Артикаин |
Р-р д/инъекц. 40 мг/1 мл: амп. 2 мл 5 или 10 шт. рег. №: ЛП-001151 |
БИОХИМИК (Россия) |
||
|
Артикаин ДФ |
Р-р д/инъекц. 40 мг+0.01 мг/1 мл: картридж 1.8 мл 50 шт. рег. №: ЛП-001074 |
ХИРАТРЕЙД СП (Россия) Произведено: INDUSTRIA E COMERCIO DFL S.A. (Бразилия) |
||
|
Артикаин Инибса |
Р-р д/инъекц. 40 мг+10 мкг/1 мл: картридж 1.8 мл 10 шт. рег. №: П N014371/01 |
LABORATORIOS INIBSA (Испания) |
||
|
Артикаин Инибса |
Р-р д/инъекц. 40 мг+5 мкг/1 мл: картридж 1.8 мл 10 шт. рег. №: П N014371/01 |
LABORATORIOS INIBSA (Испания) |
||
|
Артикаин с адреналином |
|
Р-р д/инъекц. 40 мг+0.005 мг/1 мл: амп. 2 мл 10 шт.; картриджи 1.7 мл или 1.8 мл 50 шт., рег. №: ЛП-001943 |
БИНЕРГИЯ (Россия) Произведено: АРМАВИРСКАЯ БИОФАБРИКА (Россия) контакты: БИНЕРГИЯ АО (Россия) |
|
|
Артикаин с адреналином форте |
|
Р-р д/инъекц. 40 мг+0.01 мг/1 мл: амп. 2 мл 10 шт.; картриджи 1.7 мл или 1.8 мл 50 шт. рег. №: ЛСР-008523/10 |
БИНЕРГИЯ (Россия) Произведено: АРМАВИРСКАЯ БИОФАБРИКА (Россия) контакты: БИНЕРГИЯ АО (Россия) |
|
|
Артикаин-Бинергия |
|
Р-р д/инъекц. 20 мг/1 мл: амп. 2 мл 10 шт. или 5 мл 5 шт.; картриджи 1.7 мл 10 шт. рег. №: ЛП-003910 |
БИНЕРГИЯ (Россия) Произведено: АРМАВИРСКАЯ БИОФАБРИКА (Россия) контакты: БИНЕРГИЯ АО (Россия) |
|
|
Артикаин-Эген с адреналином |
Р-р д/инъекц. 40 мг+0.005 мг/мл: 1.7 мл или 1.8 мл картриджи 10, 50 или 100 шт; 2 мл амп. 10 шт. рег. №: ЛП-003638 |
ФК ЭГЕН (Россия) Произведено: ЭКОФАРМПЛЮС (Россия) |
||
|
Артифрин |
Р-р д/инъекц. 40 мг+6 мкг/1 мл: амп. 1.7 мл, картриджи 1.7 или 1.8 мл 10 или 50 шт. рег. №: ЛСР-000031 |
ФАРМАЦЕВТИЧЕСКАЯ КОМПАНИЯ ЗДОРОВЬЕ (Украина) |
||
|
Артифрин Форте |
Р-р д/инъекц. 40 мг+10 мкг/1 мл: картриджи 1.7 или 1.8 мл 10 или 50 шт. рег. №: ЛСР-000626/10 |
ФАРМАЦЕВТИЧЕСКАЯ КОМПАНИЯ ЗДОРОВЬЕ (Украина) |
||
|
Брилокаин-адреналин |
Р-р д/инъекц. 40 мг+5 мкг/1 мл: картриджи 1.7 мл или 1.8 мл рег. №: Р N000688/01-2001 |
БРЫНЦАЛОВ-А (Россия) |
||
|
Брилокаин-Адреналин Форте |
Р-р д/инъекц. 40 мг+10 мкг/1 мл: картриджи 1.7 мл или 1.8 мл рег. №: Р N000689/01-2001 |
БРЫНЦАЛОВ-А (Россия) |
||
|
Буванестин® |
|
Р-р д/инъекц. 5 мг/1 мл: амп. 4 мл или 10 мл 5 или 10 шт. рег. №: ЛП-002121 |
БИОСИНТЕЗ (Россия) |
|
|
Бупивакаин Спинал Хэви |
Р-р д/интратекального введения 5 мг/мл: амп. 5 или 10 шт. рег. №: ЛП-006112 |
ВЕЛФАРМ (Россия) |
||
|
Бьютикаин |
Крем д/местн. и наружн. прим. 2.5%+2.5%: 5 г, 30 г или 100 г тубы рег. №: ЛП-006345 |
ИНТЕЛБИО (Россия) Произведено: ФЛОРА КАВКАЗА (Россия) |
||
|
Геликаин |
Гель д/местн. прим. 20 мг/1 г: тубы одноразовые 30 г или 100 г рег. №: ЛСР-010498/08 |
DeltaSelect (Германия) Произведено: LOMAPHARM RUDOLF LOHMANN (Германия) |
||
|
Левобупивакаин |
Раствор д/инъекций 5 мг/мл рег. №: ЛП-008087 Раствор д/инъекций 7.5 мг/мл рег. №: ЛП-008087 |
АСПЕКТУС ФАРМА (Россия) |
||
|
Лидокаин Асепт |
Спрей д/местн. прим. 100 мг+500 мкг/1 мл: фл. 25 мл рег. №: ЛС-001975 |
БИОГЕН НПЦ (Россия) |
||
|
Лиоксазин® 01 |
Гель д/местн. прим. 5%: туба 15 г рег. №: ЛСР-004166/07 |
ПРОФИТ ФАРМ (Россия) Произведено: МОСКОВСКАЯ ФАРМАЦЕВТИЧЕСКАЯ ФАБРИКА (Россия) |
||
|
Мепивакаин-Бинергия |
Р-р д/инъекц. 30 мг/мл: 1.7 мл или 1.8 мл картриджи 10, 50 или 100 шт, 2 мл амп. 5 или 10 шт. рег. №: ЛП-005178 |
БИНЕРГИЯ (Россия) Произведено: АРМАВИРСКАЯ БИОФАБРИКА (Россия) |
||
|
Мепивастезин |
Р-р д/инъекц. 30 мг/1 мл: картриджи 1.7 мл 50 шт. рег. №: П N011570/01 |
JERUSALEM PHARMACEUTICAL COMPANY (JEPHARM) (Палестина) |
||
|
Новокаин |
Р-р д/инф. 0.25%: 200 мл бут. 1 или 28 шт рег. №: Р N001052/02 |
ДАЛЬХИМФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инф. 0.25%: бут. 100 мл 1 или 35 шт., 400 мл 1 или 15 шт. рег. №: Р N001052/02 |
ДАЛЬХИМФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инф. 0.5% (1 г/200 мл): бут. 1 или 28 шт. рег. №: Р N001052/02 |
ДАЛЬХИМФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инф. 0.5%: 100 мл бут. 1 или 35 шт., 400 мл бут. 1 или 15 шт. рег. №: Р N001052/02 |
ДАЛЬХИМФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.25% (500 мг/200 мл): фл. 1, 25 или 28 шт. рег. №: Р N001206/01 |
ПРОМОМЕД РУС (Россия) Произведено: БИОХИМИК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.25%: 100 мл, 200 мл или 400 мл бут. рег. №: Р N002917/01 |
ЭСКОМ НПК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.25%: 200 мл бут. 1, 24 или 28 шт., 400 мл бут. 1, 12 или 15 шт. рег. №: Р N000353/02-2001 |
БИОСИНТЕЗ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.25%: амп. 1 мл, 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N000353/03-2002 |
БИОСИНТЕЗ (Россия) Группа: БИОТЭК МФПДК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.25%: амп. 1 мл, 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N001052/01 |
ДАЛЬХИМФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.25%: амп. 2 мл или 5 мл 10 шт. рег. №: ЛС-001406 |
БИОХИМИК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.25%: бутылки 100 мл, 200 мл или 400 мл рег. №: ЛП-003521 Р-р д/инъекц. 0.5%: бутылки 100 мл, 200 мл или 400 мл рег. №: ЛП-003521 |
МОСФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.25%: фл. 100 мл, 200 мл, 250 мл, 400 мл или 500 мл 1 шт. рег. №: ЛП-003091 |
ГРОТЕКС (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.25%: фл. 200 мл или 400 мл рег. №: П N015659/01 |
НЕСВИЖСКИЙ ЗАВОД МЕДИЦИНСКИХ ПРЕПАРАТОВ (Республика Беларусь) |
||
|
Новокаин |
|
Р-р д/инъекц. 0.5 %: амп. 5 мл или 10 мл 10 шт. рег. №: Р N000347/01 |
ОРГАНИКА (Россия) |
|
|
Новокаин |
|
Р-р д/инъекц. 0.5% (1 г/200 мл): фл. 1, 25 или 28 шт. рег. №: Р N001206/01 |
БИОХИМИК (Россия) |
|
|
Новокаин |
Р-р д/инъекц. 0.5% (2 г/400 мл): фл. 1, 15 или 25 шт. рег. №: Р N001206/01 |
БИОХИМИК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5% (25 мг/5 мл): амп. 10 шт. рег. №: Р N000194/01 |
НОВОСИБХИМФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5% (50 мг/10 мл): амп. 10 шт. рег. №: Р N000194/01 |
НОВОСИБХИМФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5%: 100 мл, 200 мл или 400 мл бут. рег. №: Р N002917/01 |
ЭСКОМ НПК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5%: 200 мл бут. 1, 24 или 28 шт., 400 мл бут. 1, 12 или 15 шт. рег. №: Р N000353/02-2001 |
БИОСИНТЕЗ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5%: амп. 1 мл, 2 мл или 5 мл 10 шт. рег. №: Р N001126/01 |
ФАРМСТАНДАРТ-УФИМСКИЙ ВИТАМИННЫЙ ЗАВОД (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5%: амп. 1 мл, 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N000353/03-2002 |
БИОСИНТЕЗ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5%: амп. 1 мл, 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N001052/01 |
ДАЛЬХИМФАРМ (Россия) |
||
|
Новокаин |
|
Р-р д/инъекц. 0.5%: амп. 2 мл 10 шт. рег. №: П N015216/01 |
ФАРМАЦЕВТИЧЕСКАЯ КОМПАНИЯ ЗДОРОВЬЕ (Украина) |
|
|
Новокаин |
Р-р д/инъекц. 0.5%: амп. 2 мл или 5 мл 10 шт. рег. №: ЛС-001406 |
БИОХИМИК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5%: амп. 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N000423/01 |
АРМАВИРСКАЯ БИОФАБРИКА (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5%: амп. 2 мл, 5 мл или 10 мл 5 или 10 шт. рег. №: Р N000758/01 |
СИНТЕЗ (Россия) контакты: СИНТЕЗ ОАО акционерное курганское общество медицинских препаратов и изделий (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5%: амп. 5 мл 10 шт. рег. №: Р N000614/01 |
АТОЛЛ (Россия) Произведено: ВЕРОФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5%: амп. 5 мл или 10 мл 5 или 10 шт. или фл. 100 мл, 200 мл, 250 мл, 400 мл или 500 мл 1 шт. рег. №: ЛП-003091 |
ГРОТЕКС (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 0.5%: фл. 200 мл или 400 мл рег. №: П N015659/01 |
НЕСВИЖСКИЙ ЗАВОД МЕДИЦИНСКИХ ПРЕПАРАТОВ (Республика Беларусь) |
||
|
Новокаин |
Р-р д/инъекц. 1%: амп. 1 мл, 2 мл или 5 мл 10 шт. рег. №: Р N001126/01 |
ФАРМСТАНДАРТ-УФИМСКИЙ ВИТАМИННЫЙ ЗАВОД (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 1%: амп. 1 мл, 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N000353/03-2002 |
БИОСИНТЕЗ (Россия) Группа: БИОТЭК МФПДК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 1%: амп. 1 мл, 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N001052/01 |
ДАЛЬХИМФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 1%: амп. 2 мл или 5 мл 10 шт. рег. №: ЛС-001406 |
БИОХИМИК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 10 мг/1 мл: 2.5 мл, 5 мл или 10 мл амп. 10 шт. рег. №: ЛП-003284 |
ФАРМСИНТЕЗ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 2.5 мг/1 мл: 2.5 мл, 5 мл или 10 мл амп. 10 шт. рег. №: ЛП-003284 |
ФАРМСИНТЕЗ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 2%: амп. 1 мл, 2 мл или 5 мл 10 шт. рег. №: Р N001126/01 |
ФАРМСТАНДАРТ-УФИМСКИЙ ВИТАМИННЫЙ ЗАВОД (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 2%: амп. 1 мл, 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N000353/03-2002 |
БИОСИНТЕЗ (Россия) Группа: БИОТЭК МФПДК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 2%: амп. 1 мл, 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N001052/01 |
ДАЛЬХИМФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 2%: амп. 2 мл 10 шт. рег. №: П N015216/01 |
ФАРМАЦЕВТИЧЕСКАЯ КОМПАНИЯ ЗДОРОВЬЕ (Украина) |
||
|
Новокаин |
Р-р д/инъекц. 2%: амп. 2 мл или 5 мл 10 шт. рег. №: ЛС-001406 |
БИОХИМИК (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 2%: амп. 2 мл, 5 мл или 10 мл 10 шт. рег. №: Р N000423/01 |
АРМАВИРСКАЯ БИОФАБРИКА (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 20 мг/1 мл: 2.5 мл, 5 мл или 10 мл амп. 10 шт. рег. №: ЛП-003284 |
ФАРМСИНТЕЗ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 25 мг/5 мл: амп. 10 шт. рег. №: ЛСР-002696/10 |
MAPICHEM (Швейцария) Произведено: WUHU KANGQI PHARMACEUTICAL (Китай) |
||
|
Новокаин |
Р-р д/инъекц. 5 мг/1 мл: 2.5 мл, 5 мл или 10 мл амп. 10 шт. рег. №: ЛП-003284 |
ФАРМСИНТЕЗ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 5 мг/1 мл: 5 мл или 10 мл амп. 10 шт. рег. №: Р N000634/01 |
МОСХИМФАРМПРЕПАРАТЫ им. Н.А.Семашко (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 5 мг/мл: 2 мл, 5 мл или 10 мл амп. 5 или 10 шт. рег. №: ЛП-005096 Р-р д/инъекц. 20 мг/мл: 2 мл, 5 мл или 10 мл амп. 5 или 10 шт. рег. №: ЛП-005096 |
ВЕЛФАРМ (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 5 мг/мл: 5 или 10 мл амп. 5 или 10 шт. рег. №: ЛП-002112 |
СЛАВЯНСКАЯ АПТЕКА (Россия) |
||
|
Новокаин |
Р-р д/инъекц. 5 мг/мл: 5 мл амп. 10 шт. рег. №: ЛП-001730 |
КОМПАНИЯ ДЕКО (Россия) |
||
|
Новокаин Буфус |
Р-р д/инъекц. 5 мг/1 мл: амп. 5 мл или 10 мл №10 рег. №: ЛСР-009446/08 |
ОБНОВЛЕНИЕ ПФК (Россия) |
||
|
Новокаин-Виал |
Р-р д/инъекц. 25 мг/5 мл: амп. 10 шт. рег. №: ЛСР-007720/08 |
ВИАЛ (Россия) Произведено: SISHUI XIERKANG PHARMACEUTICAL (Китай) |
||
|
Новокаин-Виал |
Р-р д/инъекц. 25 мг/5 мл: амп. 10 шт. рег. №: ЛСР-007720/08 |
ВИАЛ (Россия) Произведено: SHANDONG SHENGLU PHARMACEUTICAL (Китай) |
||
|
Новокаин-Виал |
Р-р д/инъекц. 25 мг/5 мл: амп. 10 шт. рег. №: ЛСР-007720/08 |
ВИАЛ (Россия) Произведено: NORTH CHINA PHARMACEUTICAL (Китай) |
||
|
Новокаин-Виал |
Р-р д/инъекц. 25 мг/5 мл: амп. 10 шт. (упаковано Озон ООО) рег. №: ЛСР-007720/08 |
ВИАЛ (Россия) Произведено: SISHUI XIERKANG PHARMACEUTICAL (Китай) Упаковано: ОЗОН (Россия) |
||
|
Новокаин-Виал |
Р-р д/инъекц. 40 мг/2 мл: амп. 10 шт. рег. №: ЛСР-007720/08 |
ВИАЛ (Россия) Произведено: SISHUI XIERKANG PHARMACEUTICAL (Китай) |
||
|
Новокаин-Виал |
Р-р д/инъекц. 40 мг/2 мл: амп. 10 шт. рег. №: ЛСР-007720/08 |
ВИАЛ (Россия) Произведено: SHANDONG SHENGLU PHARMACEUTICAL (Китай) |
||
|
Новокаин-Виал |
Р-р д/инъекц. 40 мг/2 мл: амп. 10 шт. рег. №: ЛСР-007720/08 |
ВИАЛ (Россия) Произведено: NORTH CHINA PHARMACEUTICAL (Китай) |
||
|
Новокаин-Виал |
Р-р д/инъекц. 40 мг/2 мл: амп. 10 шт. (упаковано Озон ООО) рег. №: ЛСР-007720/08 |
ВИАЛ (Россия) Произведено: SISHUI XIERKANG PHARMACEUTICAL (Китай) Упаковано: ОЗОН (Россия) |
||
|
Ораблок |
Р-р д/инъекц. 40 мг+0.005 мг/1 мл: картриджи 1.8 мл 100 шт. рег. №: ЛСР-004839/10 Р-р д/инъекц. 40 мг+0.01 мг/1 мл: картриджи 1.8 мл 100 шт. рег. №: ЛСР-004839/10 |
PIERREL FARMACEUTICI (Италия) Произведено: PIERREL (Италия) |
||
|
Перкаин |
Раствор д/инъекций 30 мг/мл рег. №: ЛП-008718 |
PIERREL FARMACEUTICI (Италия) |
||
|
Примакаин с адреналином |
Р-р д/инъекц. 40 мг+10 мкг/1 мл: картридж 1.7 мл 50 шт. рег. №: П N011701/01 |
PRODUITS DENTAIRES PIERRE ROLLAND (Франция) |
||
|
Примакаин с адреналином |
Р-р д/инъекц. 40 мг+5 мкг/1 мл: картридж 1.7 мл 50 шт. рег. №: П N011701/01 |
PRODUITS DENTAIRES PIERRE ROLLAND (Франция) |
||
|
Ропивакаин |
Раствор д/инъекций 2 мг/мл рег. №: ЛП-008480 Раствор д/инъекций 5 мг/мл рег. №: ЛП-008480 Раствор д/инъекций 7.5 мг/мл рег. №: ЛП-008480 Раствор д/инъекций 10 мг/мл рег. №: ЛП-008480 |
Химико-фармацевтический концерн МИР (Россия) |
||
|
Септалор |
Спрей д/местн. прим. дозированный спиртовой со вкусом лимона 42.5 мкг+170 мкг/доза: фл. 30 мл рег. №: ЛП-005226 Спрей д/местн. прим. дозированный спиртовой со вкусом ментола 42.5 мкг+170 мкг/доза: фл. 30 мл рег. №: ЛП-005226 |
SANDOZ (Словения) Произведено: QUALIPHAR (Бельгия) |
||
|
Септалор |
Таб. д/рассасывания со вкусом лимона 1 мг+5 мг: 24, 36 или 48 шт. рег. №: ЛП-005228 Таб. д/рассасывания со вкусом клубники 1 мг+5 мг: 24, 36 или 48 шт. рег. №: ЛП-005228 Таб. д/рассасывания со вкусом ментола 1 мг+5 мг: 24, 36 или 48 шт. рег. №: ЛП-005228 Таб. д/рассасывания со вкусом меда 1 мг+5 мг: 24, 36 или 48 шт. рег. №: ЛП-005228 |
SANDOZ (Словения) Произведено: QUALIPHAR (Бельгия) |
||
|
Септанест с адреналином |
Р-р д/инъекц. 40 мг+10 мкг/1 мл: картридж 1.8 мл 10 или 50 шт. рег. №: П N012998/01 |
SEPTODONT (Франция) |
||
|
Септанест с адреналином |
Р-р д/инъекц. 40 мг+5 мкг/1 мл: картридж 1.8 мл 10 или 50 шт. рег. №: П N012998/01 |
SEPTODONT (Франция) |
||
|
Скандинибса |
Р-р д/инъекц. 30 мг/1 мл: картриджи 1.8 мл 10 шт. рег. №: ЛСР-010989/09 |
INIBSA DENTAL (Испания) Произведено: LABORATORIOS INIBSA (Испания) |
||
|
Скандинибса Форте |
Р-р д/инъекц. 20 мг+10 мкг/1 мл: картриджи 1.8 мл 10 шт. рег. №: ЛСР-000001/10 |
LABORATORIOS INIBSA (Испания) |
||
|
Скандонест |
Р-р д/инъекц. 3%: картриджи 1.8 мл 10, 20, 30, 40, 50, 60, 80, 100 или 120 шт. рег. №: П N012996/01 |
SEPTODONT (Франция) |
||
|
Убистезин |
Р-р д/инъекц. 40 мг+0.005 мг/1 мл: картриджи 1.7 мл 50 шт. рег. №: ЛП-(000850)-(РГ-RU ) Предыдущий рег. №: П N016046/01 |
3M DEUTSCHLAND (Германия) |
||
|
Убистезин Форте |
Р-р д/инъекц. 40 мг+0.01 мг/1 мл: картриджи 1.7 мл 50 шт. рег. №: ЛП-(000846)-(РГ-RU ) Предыдущий рег. №: П N016047/01 |
3M DEUTSCHLAND (Германия) |
||
|
Ультракаин® Д |
Р-р д/инъекц. 40 мг/1 мл: амп. 2 мл 10 шт. рег. №: ЛС-001358 Р-р д/инъекц. 40 мг/1 мл: картриджи 1.7 мл 10 или 100 шт. рег. №: ЛС-001358 |
SANOFI-AVENTIS DEUTSCHLAND (Германия) контакты: САНОФИ |
||
|
Ультракаин® Д-С |
Р-р д/инъекц. 40 мг+5 мкг/1 мл: амп. 2 мл 10 шт. рег. №: П N015119/01 Р-р д/инъекц. 40 мг+5 мкг/1 мл: картридж 1.7 мл 100 шт. рег. №: П N015119/01 |
SANOFI-AVENTIS DEUTSCHLAND (Германия) контакты: САНОФИ |
||
|
Ультракаин® Д-С форте |
Р-р д/инъекц. 40 мг+10 мкг/1 мл: амп. 2 мл 10 шт. рег. №: П N015117/01 Р-р д/инъекц. 40 мг+10 мкг/1 мл: картриджи 1.7 мл 100 шт. рег. №: П N015117/01 |
SANOFI-AVENTIS DEUTSCHLAND (Германия) контакты: САНОФИ |
||
|
Цертакаин® |
|
Р-р д/инъекций 40 мг+0.005 мг/1 мл: амп. 2 мл 10, 50 или 100 шт. рег. №: ЛП-(001001)-(РГ-RU ) Предыдущий рег. №: ЛП-004580 Р-р д/инъекций 40 мг+0.01 мг/1 мл: амп. 2 мл 10, 50 или 100 шт. рег. №: ЛП-(001001)-(РГ-RU ) Предыдущий рег. №: ЛП-004580 |
ГРОТЕКС (Россия) контакты: ГРОТЕКС ООО (Россия) |
|
|
Цитокартин |
Р-р д/инъекц. 40 мг+10 мкг/1 мл: картридж 1.7 мл 10 шт. рег. №: П N012062/01 |
MOLTENI FARMACEUTICI (Италия) Произведено: COSMO (Италия) |
||
|
Цитокартин |
Р-р д/инъекц. 40 мг+5 мкг/1 мл: картридж 1.7 мл 10 шт. рег. №: П N012062/01 |
MOLTENI FARMACEUTICI (Италия) Произведено: COSMO (Италия) |
||
|
Эмла |
Крем д/местн. и наружн. прим. 25 мг+25 мг/1 г: тубы 5 г 5 шт. или 30 г 1 шт. рег. №: П N014033/01 |
ASPEN PHARMA TRADING (Ирландия) Произведено: RECIPHARM KARLSKOGA (Швеция) контакты: АСПЕН ХЭЛС ООО (Россия) |
||
|
Эстет-а-тет |
Крем д/местн. и наружн. прим. 2.5 г+2.5 г/100 г: тубы 5 г или 30 г 1 или 5 шт. рег. №: ЛП-007136 |
АТОЛЛ (Россия) Произведено: ОЗОН (Россия) |
Рапинов
(PHARMASYNTEZ AO Россия)
Р-р д/инъекц. 10 мг/мл: 10 мл амп. 5, 10 или 25 шт.
Рапинов
(PHARMASYNTEZ AO Россия)
Р-р д/инъекц. 2 мг/мл: 10 мл амп. 5, 10 или 25 шт.
Р-р д/инъекц. 5 мг/мл: 10 мл амп. 5, 10 или 25 шт.
Р-р д/инъекц. 7.5 мг/мл: 10 мл амп. 5, 10 или 25 шт.
Ропивабин®
(PPHK ALIUM Россия)
(BINNOPHARM AO Россия)
Р-р д/инъекц. 10 мг/мл: амп. 10 мл 5 или 10 шт.
Ропивабин®
(PPHK ALIUM Россия)
Р-р д/инъекц. 2 мг/мл: фл. 100 мл и 200 мл.
Ропивабин®
(PPHK ALIUM Россия)
(BINNOPHARM AO Россия)
Р-р д/инъекц. 5 мг/мл: амп. 10 мл 5 или 10 шт.
Ропивабин®
(PPHK ALIUM Россия)
(BINNOPHARM AO Россия)
Р-р д/инъекц. 7.5 мг/мл: амп. 10 мл 5 или 10 шт.
Ропивакаин
(BIOCAD AO Россия)
Р-р д/инъекц. 10 мг/мл: 10 или 20 мл фл. 5 шт.
Ропивакаин
(BIOCAD AO Россия)
Р-р д/инъекц. 2 мг/мл: 10 или 20 мл фл. 5 шт.
Ропивакаин
(PHARMASYNTEZ-TYUMEN LLC Россия)
Р-р д/инъекц. 2 мг/мл: 100 мл или 200 мл фл.
Ропивакаин
(B-PHARM OOO Россия)
(FGBNU Россия)
Р-р д/инъекц. 2 мг/мл: амп. 10 мл 5 шт.
Р-р д/инъекц. 5 мг/мл: амп. 10 мл 5 шт.
Р-р д/инъекц. 7.5 мг/мл: амп. 10 мл 5 шт.
Р-р д/инъекц. 10 мг/мл: амп. 10 мл 5 шт.
Ропивакаин
(ECOPHARMPLUS AO Россия)
Р-р д/инъекц. 2 мг/мл: амп. 10 мл или 20 мл 5 или 10 шт.
Р-р д/инъекц. 5 мг/мл: амп. 10 мл или 20 мл 5 или 10 шт.
Р-р д/инъекц. 7.5 мг/мл: амп. 10 мл или 20 мл 5 или 10 шт.
Р-р д/инъекц. 10 мг/мл: амп. 10 мл или 20 мл 5 или 10 шт.
Ропивакаин
(KRASPHARMA PJSC Россия)
Р-р д/инъекц. 2 мг/мл: фл. 10 мл 5. 10 или 20 шт.
Р-р д/инъекц. 5 мг/мл: фл. 10 мл 5. 10 или 20 шт.
Р-р д/инъекц. 7.5 мг/мл: фл. 10 мл 5. 10 или 20 шт.
Р-р д/инъекц. 10 мг/мл: фл. 10 мл 5. 10 или 20 шт.
Ропивакаин
(BIOCAD AO Россия)
Р-р д/инъекц. 5 мг/мл: 10 или 20 мл фл. 5 шт.
Ропивакаин
(BIOCAD AO Россия)
Р-р д/инъекц. 7.5 мг/мл: 10 или 20 мл фл 5 шт.
Ропивакаин
(NPC PHARMZASHITA FGUP FMBA Russia Россия)
Р-р д/инъекций 2 мг/мл: амп. 10 мл 5, 10 или 25 шт.
Р-р д/инъекций 5 мг/мл: амп. 10 мл 5, 10 или 25 шт.
Р-р д/инъекций 7.5 мг/мл: амп. 10 мл 5, 10 или 25 шт.
Р-р д/инъекций 10 мг/мл: амп. 10 мл 5, 10 или 25 шт.
Ропивакаин
(PROMOMED OOO Россия)
Раствор д/инъекций 2 мг/мл
Раствор д/инъекций 5 мг/мл
Раствор д/инъекций 7.5 мг/мл
Раствор д/инъекций 10 мг/мл
Ропивакаин Бинергия
(BINERGIYA AO Россия)
(ARMAVIRSKAYA BIOFABRIKA FKP Россия)
Р-р д/инъекц. 10 мг/мл: 10 мл или 20 мл амп. 5 шт.
Ропивакаин Бинергия
(BINERGIYA AO Россия)
(ARMAVIRSKAYA BIOFABRIKA FKP Россия)
Р-р д/инъекц. 2 мг/мл: 5 мл, 10 мл или 20 мл амп. 5 или 10 шт., 100 или 200 мл: фл. 1 или 5 шт.
Ропивакаин Бинергия
(BINERGIYA AO Россия)
(ARMAVIRSKAYA BIOFABRIKA FKP Россия)
Р-р д/инъекц. 5 мг/мл: 10 мл или 20 мл амп. 5 шт.
Ропивакаин Бинергия
(BINERGIYA AO Россия)
(ARMAVIRSKAYA BIOFABRIKA FKP Россия)
Р-р д/инъекц. 7.5 мг/мл: 10 мл или 20 мл амп. 5 шт.
Ропивакаин Велфарм
(VELPHARM OOO Россия)
Р-р д/инъекц. 10 мг/мл: 5 мл, 10 мл или 20 мл амп. 5 или 10 шт.
Ропивакаин Велфарм
(VELPHARM OOO Россия)
Р-р д/инъекц. 2 мг/мл: 5 мл, 10 мл или 20 мл амп. 5 или 10 шт.
Р-р д/инъекц. 5 мг/мл: 5 мл, 10 мл или 20 мл амп. 5 или 10 шт.
Р-р д/инъекц. 7.5 мг/мл: 5 мл, 10 мл или 20 мл амп. 5 или 10 шт.
Ропивакаин Каби
(FRESENIUS KABI DEUTSCHLAND GmbH Германия)
(FRESENIUS KABI NORGE AS Норвегия)
Р-р д/инъекц. 2 мг/1 мл: амп. 10 мл или 20 мл 1 или 5 шт., контейнеры 100 мл или 200 мл 5 шт.
Р-р д/инъекц. 7.5 мг/1 мл: амп. 10 мл или 20 мл 1 или 5 шт.
Р-р д/инъекц. 10 мг/1 мл: амп. 10 мл или 20 мл 1 или 5 шт.
Ропивакаин Каби
(FRESENIUS KABI DEUTSCHLAND GmbH Германия)
(FRESENIUS KABI NORGE AS Норвегия)
Р-р д/инъекц. 5 мг/1 мл: амп. 10 мл 1 или 5 шт.
Ропивакаин НоваМедика
(NOVAMEDICA Россия)
Р-р д/инъекц. 2 мг/мл: фл. 20 мл 5 шт, 100 мл 1 шт.
Р-р д/инъекц. 5 мг/мл: фл. 10 мл 5 шт.
Р-р д/инъекц. 7.5 мг/мл: фл. 10 мл 5 шт.
Р-р д/инъекц. 10 мг/мл: фл. 10 мл 5 шт.
Наропин® (5 мг/мл)
МНН: Ропивакаин
Производитель: Астра Зенека АБ
Анатомо-терапевтическо-химическая классификация: Ropivacaine
Номер регистрации в РК:
№ РК-ЛС-5№020451
Информация о регистрации в РК:
18.03.2019 — бессрочно
- Скачать инструкцию медикамента
Торговое название
Наропин
Международное непатентованное название
Ропивакаин
Лекарственная форма
Раствор для инъекций 5мг/мл, 10 мл
Состав
1 мл раствора содержит
активное вещество — ропивакаина гидрохлорида – 5 мг,
вспомогательные вещества: натрия хлорид для инъекций, натрия гидроксид 2 М раствор или 2 М кислота хлороводородная (до pH 4-6), вода для инъекций.
Описание
Прозрачный бесцветный раствор
Фармакотерапевтическая группа
Анестетики. Анестетики местные. Амиды. Ропивакаин.
Код АТХ N01BB09
Фармакологические свойства
Фармакокинетика
Концентрация ропивакаина в плазме крови зависит от дозы, пути введения и степени васкуляризации области инъекции. Фармакокинетика ропивакаина линейная, максимальная концентрация (Cmax) пропорциональна введенной дозе. После эпидурального введения ропивакаин полностью абсорбируется. Абсорбция носит двухфазный характер, период полувыведения (T1/2) для двух фаз составляет соответственно 14 мин и 4 ч. Замедление элиминации ропивакаина определяется медленной абсорбцией, что объясняет более длительный T1/2 после эпидурального введения по сравнению с внутривенным введением.
Общий плазменный клиренс ропивакаина – 440 мл/мин, плазменный клиренс несвязанного вещества 8 л/мин, почечный клиренс 1 мл/мин, объем распределения в равновесном состоянии 47 л, показатель печеночной экстракции около 0.4, T1/2-1.8 часа.
Ропивакаин интенсивно связывается с белками плазмы крови (главным образом с 1-кислыми гликопротеинами), несвязанная фракция ропивакаина составляет около 6%. Ропивакаин проникает через плацентарный барьер с быстрым достижением равновесия до несвязанной фракции. Степень связывания с белками плазмы у плода ниже, чем у матери, что влечет за собой более низкую общую концентрацию в плазме крови плода. Ропивакаин активно метаболизируется в печени, главным образом путем ароматического гидроксилирования до 3-гидрокси-ропивакаина с помощью цитохрома Р4501A2 и путем N-дезалкилирования до РРХ (N-депропилат ропивакаин — pipecoloxylidide) с помощью CYP3A4.
Около 37% 3-гидрокси-ропивакаина, основного метаболита ропивакаина, выводится с мочой как в связанном, так и в несвязанном виде. Экскреция с мочой PPX и других метаболитов составляет менее 3% всей дозы.
При эпидуральной инфузии основные метаболиты PPX и 3-гидрокси-ропивакаин выводятся с мочой. Общая концентрация PPX в плазме составляет около половины от общей концентрации ропивакаина, однако, значение концентрации несвязанного PPX в 7-9 раз выше, чем концентрация несвязанного ропивакаина при последующей непрерывной эпидуральной инфузии до 72 часов.
Нарушение функции почек не оказывает существенного влияния на фармакокинетику ропивакаина. Почечный клиренс PPX значимо коррелирует с клиренсом креатинина. Отсутствие корреляции между общей экспозицией, выраженной в AUC, и клиренсом креатинина указывает, что общий клиренс PPX включает внепочечную элиминацию в дополнение к почечной экскреции. У некоторых пациентов с нарушенной функцией почек может отмечаться повышение экспозиции PPX в результате низкого почечного клиренса. Из-за пониженной нейротоксичности PPX по сравнению с ропивакаином клинические последствия считаются незначительными при краткосрочном применении.
Свидетельства рацемизации ропивакаина in vivo отсутствуют.
Фармакодинамика
Наропин – первый местный анестетик амидного типа длительного действия, являющийся чистым энантиомером. Oбладает как анестезирующим, так и обезболивающим действием. Высокие дозы препарата применяются для местной анестезии при хирургических вмешательствах, низкие дозы препарата обеспечивают аналгезию (сенсорный блок) с минимальным и не прогрессирующим моторным блоком. На длительность и интенсивность блокады, вызванной ропивакаином, добавление адреналина не влияет. Обратимо блокируя вольтаж-зависимые натриевые каналы, препятствует генерации импульсов в окончаниях чувствительных нервов и проведению импульсов по нервным волокнам.
Наропин может оказывать влияние на другие возбудимые клеточные мембраны (например, в головном мозге и миокарде). Если избыточное количество местного анестетика достигает системного кровотока за короткий промежуток времени, возможно, проявление признаков системной токсичности. Признаки токсичности со стороны центральной нервной системы предшествуют признакам токсичности со стороны сердечно-сосудистой системы, так как наблюдаются при более низких концентрациях препарата в плазме крови.
Прямое действие местных анестетиков на сердце включает замедление проводимости, отрицательный инотропный эффект и, при выраженной передозировке, аритмии и остановку сердца. Внутривенное введение высоких доз Наропина приводит к таким же эффектам со стороны сердечно-сосудистой системы.
Непрямые сердечно-сосудистые эффекты (снижение АД, брадикардия), которые могут возникать после эпидурального введения ропивакаина, обусловлены возникающей симпатической блокадой.
Показания к применению
Анестезия при хирургических вмешательствах:
-
спинномозговая анестезия
-
эпидуральная блокада при хирургических вмешательствах, в том числе при кесаревом сечении
-
блокада крупных нервов и нервных сплетений
-
блокада отдельных нервов и инфильтрационная анестезия
Купирование острого болевого синдрома в педиатрии:
-
блокада переферических нервов у детей с 1 до 12 летнего возраста включительно
Способ применения и дозы
Препарат применяется для эпидуральной, спинальной инфильтрационной и проводниковой анестезии.
Наропин должен использоваться только специалистами, имеющими достаточный опыт проведения регионарной анестезии.
Взрослые и дети старше 12 лет
В целом для анестезии при хирургических вмешательствах (например, при эпидуральном введении) требуются более высокие дозы и более концентрированные растворы препарата. При обезболивании (например, эпидуральное введение для купирования болевого синдрома) рекомендуются более низкие дозы и концентрации препарата.
Рекомендации по дозированию препарата Наропин для взрослых:
|
Концентрация препарата (мг/мл) |
Объем раствора (мл) |
Доза (мг) |
Начало действия (мин) |
Длитель-ность действия (ч) |
|
|
Анестезия при хирургических вмешательствах: |
|||||
|
Спинномозговая анестезия |
5.0 |
3 — 4 |
15 — 20 |
1 — 5 |
2 — 6 |
Указанные в таблице дозы считаются необходимыми для надежной блокады и должны рассматриваться как руководство для применения у взрослых. Может наблюдаться индивидуальная вариабельность начала и продолжительности действия. Цифры отражают средний диапазон ожидаемых дозировок. Для справок о факторах, которые влияют на методы выполнения отдельных блокад и о требованиях, предъявляемых к конкретным группам пациентов, следует использовать стандартные руководства.
Если Наропин дополнительно использовался для других видов анестезии, максимальная доза не должна превышать 225 мг.
Для предотвращения попадания анестетика в сосуд следует обязательно проводить аспирационную пробу до введения и в процессе введения препарата. Случайное внутрисосудистое введение распознается по временному увеличению частоты сердечных сокращений, а случайное интратекальное введение – по признакам спинального блока.
До введения и во время введения Наропина (которое следует проводить медленно или путем увеличения вводимых последовательно доз препарата со скоростью 25-50мг/мин) необходимо тщательно контролировать жизненно важные функции пациента и поддерживать с ним вербальный контакт.
Однократное введение Наропина в дозе до 250 мг при эпидуральной блокаде для проведения хирургического вмешательства обычно хорошо переносилось пациентами. При появлении токсических симптомов следует немедленно прекратить введение препарата. При длительном проведении блокады путем продленной инфузии или повторного болюсного введения следует учитывать возможность создания токсических концентраций анестетика в крови и местного повреждения нерва. Введение Наропина в течение 24 ч в дозе до 800 мг суммарно при хирургических вмешательствах и для послеоперационного обезболивания, а также продленная эпидуральная инфузия после операции со скоростью 28мг/ч в течение 72 ч хорошо переносится взрослыми пациентами.
Рекомендации по дозированию препарата Наропин для детей до 12 лет:
|
Концентрация препарата (мг/мл) |
Объем раствора (мл/кг) |
Доза (мг/кг) |
|
|
Блокада периферических нервов: |
|||
|
Блокада периферических нервов (к примеру, подвздошно-паховая блокада) |
5.0 |
0.6 мг/кг |
3 мг/кг |
Дозы, указанные в таблице, считаются достаточными для достижения надежной блокады и являются руководством к использованию препарата в педиатрической практике. В то же время существует индивидуальная вариабельность скорости развития блока и его длительности.
У детей с избыточным весом часто требуется постепенное снижение дозы препарата; при этом необходимо руководствоваться «идеальным» весом пациента. Для справок о факторах, которые влияют на методы выполнения отдельных блокад и о требованиях, предъявляемых к конкретным группам пациентов, следует использовать стандартные руководства. Объем раствора для каудального эпидурального введения и объем болюса для эпидурального введения не должны превышать 25мл для любого пациента.
Для предотвращения непреднамеренного внутрисосудистого введения анестетика следует тщательно проводить аспирационную пробу до введения и в процессе введения препарата. Во время введения препарата необходимо тщательно контролировать жизненно важные функции пациента. При появлении токсических симптомов следует немедленно прекратить введение препарата.
Независимо от типа анестезии, рекомендуется дозированное введение рассчитанной дозы препарата. Применение препарата в концентрации выше 5мг/мл, а также интратекальное применение Наропина у детей не исследовалось. Применение Наропина у недоношенных детей не изучалось.
Побочные эффекты
Очень часто (>1/10)
— гипотензия
— тошнота
Часто (>1/100)
— парестезия, головокружение, головная боль
— брадикардия, тахикардия
— гипертония
— рвота
— задержка мочеиспускания
— реакции в месте введения (повышение температуры, озноб, боль в спине)
Нечасто (>1/1000)
— беспокойство
— признаки интоксикации со стороны ЦНС (конвульсии, большой
эпилептический припадок, судороги, легкое головокружение, периоральная
парестезия, онемение языка, гиперакузия, звон в ушах, нарушение зрения,
дизартрия, мышечные подергивания, тремор), гипестезия
— синкопе
— одышка
— осложнения общего характера и реакции в месте введения (гипотермия)
Редко (>1/10000)
— остановка сердца, аритмия
— аллергические реакции (анафилактический шок, ангионевротический отек и
крапивница)
Наропин может вызывать острые системные токсические реакции при использовании высоких доз или при быстром повышении концентрации в крови при случайном внутрисосудистом введении препарата либо его передозировке.
Противопоказания
— известная повышенная чувствительность к местным анестетикам амидного типа
Лекарственные взаимодействия
Возможно суммирование токсических эффектов при одновременном назначении с другими местными анестетиками или препаратами структурно сходными с местными анестетиками амидного типа.
Взаимодействие ропивакаина и антиаритмических препаратов класса III (например, амиодарона) специально не изучалось, но следует соблюдать осторожность при совместном назначении.
Клиренс ропивакаина уменьшается на 77% при совместном назначении с флувоксамином, являющимся сильным конкурентным ингибитором цитохрома Р4501А2. Таким образом, одновременное применение сильнодействующих ингибиторов CYP1А2, таких как флувоксамин и эноксацин, с Наропином может послужить причиной метаболического взаимодействия, которое приводит к повышению концентрации ропивакаина в плазме крови. Поэтому пациентам, принимающим лечение сильными ингибиторами CYP1A2, такими как флувоксамин и эноксацин, не следует назначать продолжительное введение ропивакаина.
Повышение рН раствора выше 6.0 может привести к образованию преципитата из-за плохой растворимости ропивакаина при данных условиях.
Особые указания
Регионарная анестезия должна проводиться опытными специалистами. Обязательно наличие оборудования и лекарственных препаратов для проведения реанимационных мероприятий. До начала выполнения больших блокад должен быть установлен внутривенный катетер.
Персонал, обеспечивающий выполнение анестезии, должен быть соответствующим образом подготовлен и знаком с диагностикой и лечением возможных побочных эффектов, системных токсических реакций и других возможных осложнений.
Эпидуральная анестезия может приводить к снижению АД и брадикардии. Введение сосудосуживающих препаратов или увеличение объёма циркулирующей крови может уменьшить риск развития подобных побочных эффектов.
Имеются сообщения о единичных случаях остановки сердца у пожилых пациентов и у пациентов с сопутствующими сердечно-сосудистыми заболеваниями при применении Наропина для эпидуральной анестезии или блокад периферических нервов, особенно после случайного внутрисосудистого попадания препарата. В ряде случаев реанимационные мероприятия были затруднительны. Остановка сердца, как правило, требует более длительных реанимационных мероприятий. Поскольку Наропин метаболизируется в печени, следует проявлять осторожность при применении препарата у больных с тяжелыми заболеваниями печени; в некоторых случаях из-за замедленной элиминации может возникнуть необходимость уменьшения повторно вводимых доз анестетика.
Обычно у больных с почечной недостаточностью при введении препарата однократно или при использовании препарата в течение непродолжительного периода времени не требуется корректировать дозу. Однако, ацидоз и снижение концентрации белков в плазме крови, часто развивающиеся у больных с хронической почечной недостаточностью, могут повышать риск системного токсического действия препарата.
Следует своевременно корректировать гипотензию путем внутривенного введения 5-10 мг эфедрина, с повторным введением, при необходимости. Применение препарата у новорожденных требует учета возможной незрелости органов и физиологических функций, что особенно важно при продленной инфузии. Наропин – может являться порфириногенным и может применяться у пациентов с диагнозом острая порфирия только в случае, если нет более безопасной альтернативы.
Имеются сообщения о случаях хондролиза у пациентов, получавших послеоперационную внутрисуставную продленную инфузию. Большая часть этих сообщений касалась плечевого сустава. Из-за возможности влияния различных факторов и противоречивых литературных данных, точной причинно-следственной связи не установлено. Наропин не показан для продленной внутрисуставной инфузии.
С осторожностью: следует вводить препарат ослабленным пожилым пациентам или пациентам с тяжелыми сопутствующими заболеваниями, такими как блокады сердца (синоатриальная, атриовентрикулярная, внутрижелудочковая), прогрессирующий цирроз печени, тяжелая хроническая почечная недостаточность. Для данных групп пациентов регионарная анестезия является предпочтительной.
Беременность и лактация
Не выявлено влияния ропивакаина на фертильность и репродуктивную функцию, а также тератогенного действия. Не проводились исследования по оценке возможного действия ропивакаина на развитие плода у женщин.
Наропин можно применять при беременности только, если это оправдано клинической ситуацией (в акушерстве использование препарата для анестезии или аналгезии хорошо обосновано).
Экскреция ропивакаина и его метаболитов с грудным молоком не изучена. При необходимости применения препарата в период грудного кормления следует рассмотреть соотношение потенциальной пользы для матери и возможного риска для младенца.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Необходимо воздерживаться от потенциально опасных видов деятельности, требующих повышенного внимания.
Передозировка
Симптомы: нарушение зрения и слуха, онемение вокруг рта, головокружение, парестезии, дизартрия, мышечный гипертонус, мышечные подергивания, аритмии; при прогрессировании интоксикации – снижение АД, брадикардия, аритмия, потеря сознания, генерализованные судороги, остановка сердца.
Лечение: при появлении первых признаков интоксикации следует прекратить введение; при развитии судорог поддерживают адекватное поступление кислорода с помощью кислородного мешка или маски, в/в вводят 100-120мг тиопентала или 5-10мг диазепама; после интубации и начала ИВЛ вводят суксаметоний. Необходимо поддерживать оптимальный газовый состав крови с одновременной коррекцией ацидоза.
Форма выпуска и упаковка
Раствор для инъекций 5мг/мл. По 10 мл препарата разливают в запаянные ампулы из полипропилена. Каждая ампула помещается в контурную ячейковую упаковку. По 5 контурных ячейковых упаковок помещается в картонную пачку вместе с инструкцией по применению на государственном и русском языках.
Условия хранения
Хранить при температуре не выше 25°С. Не замораживать.
Хранить в недоступном для детей месте!
Срок хранения
3 года
Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту
Производитель
АстраЗенека АБ, SE 151 85 Содерталье, Швеция
Наименование и страна организации-упаковщика
АстраЗенека АБ, Швеция
Владелец регистрационного удостоверения
АстраЗенека АБ, Швеция
Наропин товарный знак – собственность группы компаний АстраЗенека
Адрес организации, принимающей претензии от потребителей по качеству продукции (товара) на территории Республики Казахстан
Представительство закрытой акционерной компании «АстраЗенека Ю-Кей Лимитед», в Республике Казахстан
Республика Казахстан, город Алматы, 05000, ул. Наурызбай батыра 31, Бизнес-Центр «Премиум», офис № 84
Телефон: +7 727 226 25 30, факс: +7 727 226 25 29
e-mail: Aigul.Doszhanova@astrazeneca.com
| 377727551477976781_ru.doc | 82 кб |
| 870881591477977954_kz.doc | 120.5 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
-
По рецепту
Внешний вид товара может отличаться
Наропин раствор для инъекций 7,5 мг/мл ампулы 10 мл 5 шт.
Товара нет в наличии.
🏥 Купить Наропин раствор для инъекций 7,5 мг/мл ампулы 10 мл 5 шт. в наших аптеках в Москве
💊 Наропин раствор для инъекций 7,5 мг/мл ампулы 10 мл 5 шт. в интернет-аптеке «WER.RU»
🚚 Доставка со склада в Москве от 1-го дня
⚠ Отпускается по рецепту в торговом зале аптеки
- Форма выпуска:раствор для инъекций
- Дозировка:7.5 мг/мл
Перейти к формам выпуска
-
Производитель
-
Код товара
114404
-
Категория
-
Форма отпуска
по рецепту
Перейти к описанию
все
товары Наропин,
4 шт.
🏥 Купить Наропин раствор для инъекций 7,5 мг/мл ампулы 10 мл 5 шт. в наших аптеках в Москве
💊 Наропин раствор для инъекций 7,5 мг/мл ампулы 10 мл 5 шт. в интернет-аптеке «WER.RU»
🚚 Доставка со склада в Москве от 1-го дня
⚠ Отпускается по рецепту в торговом зале аптеки
Состав и форма выпуска
Наропин — раствор для инъекций:
1 мл содержит ропивакаина гидрохлорид 2, 7,5 и 10 мг; вспомогательные вещества: натрия хлорид — 8,6; 7,5 или 7,1 мг; в упаковке 5 ампул по 10 и 20 мл;
Наропин — раствор для инфузий:1 мл содержит ропивакаина гидрохлорид 2 мг; вспомогательные вещества: натрия хлорид — 8,6 мг; в упаковке 1 мешок по 100 или 200 мл; в картонной коробке 5 упаковок.
Фармакологическое действие
Наропин оказывает местноанестезирующее действие.
Показания
Местная анестезия: эпидуральная, в т.ч. при кесаревом сечении, проводниковая (включая крупные нервы и сплетения), инфильтрационная; купирование острого болевого синдрома (в т.ч. послеоперационное обезболивание и обезболивание родов).
Противопоказания
Гиперчувствительность; детский возраст до 12 лет (т.к. отсутствует достаточное количество клинических наблюдений).
Применение при беременности и кормлении грудью
С осторожностью. Применение для анестезии или аналгезии в акушерстве обосновано.
Побочные действия
Аналогичны действию др. амидных местных анестетиков: гипотензия или гипертензия, брадикардия или тахикардия, головная боль, головокружение, парестезия, нейропатия, нарушение функции спинного мозга (синдром передней спинной артерии, арахноидит), тошнота, рвота, озноб, повышение температуры тела, задержка мочи, аллергические реакции.
Способ применения и дозы
0,2% раствор Наропина. Купирование острого болевого синдрома: эпидуральное введение на поясничном уровне — болюсное введение — 10-20 мл (20-40 мг); интермиттирующее введение (боль во время родов) — по 10-15 мл (20-30 мг) с минимальным интервалом 30 мин; продолжительные инфузии для обезболивания родов — 6-10 мл/ч (12-20 мг/ч); послеоперационное введение — 6-14 мл/ч (12-28 мг/ч); торакальная эпидуральная анальгезия: продолжительные инфузии после операций — 6-14 мл/ч (12-28 мг/ч); проводниковая и инфильтрационная анестезия — 1-100 мл (2-200 мг).
0,75% раствор Наропина. Анестезия при хирургических вмешательствах. Кесарево сечение — 15-20 мл (113-150 мг); торакальная эпидуральная анестезия при послеоперационной боли — 5-15 мл (38-113 мг); эпидуральная анестезия на поясничном уровне — 15-25 мл (113-188 мг); проводниковая и инфильтрация анестезия — 1-30 мл (7,5-225 мг); блокада крупных нервных сплетений (плечевое) — 10-40 мл (75-300 мг).
1% раствор Наропина. Анестезия при хирургических вмешательствах: эпидуральная анестезия на поясничном уровне — 15-20 мл (150-200 мг).
Условия хранения и срок годности
В сухом, защищенном от света месте, при комнатной температуре не выше 20°C. Срок годности — 3 года.