Дата публикации 9 марта 2021Обновлено 26 апреля 2021
Определение болезни. Причины заболевания
B12-дефицитная анемия (B12ДА) — это заболевание, при котором снижается уровень эритроцитов и гемоглобина из-за недостатка в организме витамина В12.
Синонимы: анемия Аддисона — Бирмера, мегалобластная, пернициозная анемия.
Витамин B12 участвует в образовании всех клеток крови (эритроцитов, лейкоцитов, тромбоцитов), клеток желудочно-кишечного тракта и обеспечивает нормальное функционирование клеток нервной системы. Поэтому при анемии, связанной с дефицитом витамина B12, часто наблюдаются признаки поражения желудочно-кишечного тракта и нервной системы, а в анализе крови снижается уровень тромбоцитов и лейкоцитов [3].
Распространённость
B12ДА встречается у 1500 человек на 1 миллион населения, как у детей, так и у взрослых. Однако чаще болеют люди старше 60 лет. У женщин заболеваемость выше, чем у мужчин: соотношение 10:7 [1][2].
Причины B12-дефицитной анемии
Причинами развития B12ДА являются недостаточное поступление витамина в организм, нарушение его высвобождения из пищи, нарушение всасывания, транспорта, обмена (метаболизма) или повышенное его расходование. Разберём подробнее каждую причину.
1. Недостаточное поступление. Витамин B12 содержится только в продуктах животного происхождения. Если с пищей поступает мало витамина В12 или не поступает совсем, например при вегетарианстве или веганстве, через 2-4 года развивается B12ДА. У грудных детей дефицит может развиться при сниженном содержании B12 в грудном молоке из-за дефицита витамина у матери [1][2][3][4][8].
2. Нарушение высвобождения В12 из пищи может быть вызвано следующими причинами:
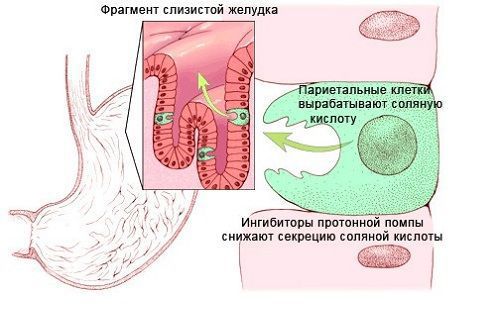
- Утратой или повреждением париетальных клеток желудка. Витамин B12 в пище присутствует в белковой форме. В желудке В12 высвобождается из пищи под воздействием соляной кислоты и ферментов желудочного сока, расщепляющих белок. Соляная кислота вырабатывается париетальными клетками желудка. Причинами нарушения её продукции может быть утрата или повреждение париетальных клеток в результате:
- Хирургического вмешательства на желудке: тотальной или субтотальной резекции, например при раке желудка.
- Атрофического гастрита — хронического воспаления желудка. В том числе аутоиммунного гастрита, при котором иммунная система ошибочно распознаёт париетальные клетки желудка как чужеродные и разрушает их с помощью специфических антител.
- Рака или полипоза желудка, которые повреждают и вытесняют париетальные клетки слизистой оболочки.
- Недостатком ферментов поджелудочной железы. После высвобождения из пищевых белков витамин В 12 связывается с белком слюны гаптокоррином, который защищает витамин от кислой среды желудка. В двенадцатиперстной кишке В12 высвобождается под воздействием ферментов поджелудочной железы. Причинами нехватки ферментов может быть недостаточность поджелудочной железы, хронический панкреатит или синдром Золлингера — Эллисона (опухоль поджелудочной железы) [17].
3. Нарушение всасывания витамина в тонком кишечнике. Возможные причины:
- Недостаток внутреннего фактора Кастла. После высвобождения витамина из белков слюны В12 связывается с внутренним фактором Кастла — белком, который вырабатывают париетальные клетки желудка. Только благодаря этой связи витамин может всасываться в тонком кишечнике. Причины недостатка внутреннего фактора Кастла:
- Врождённый дефицит внутреннего фактора Кастла — наследственное заболевание, которое характеризуется дефектом гена, ответственного за образование этого фактора.
- Утрата париетальных клеток желудка.
- Врождённые и приобретённые болезни кишечника:
- Синдром Имерслунд — Гресбека — редкое наследственное заболевание, вызванное нарушением работы рецептора сubam в подвздошной кишке. С помощью этого рецептора происходит всасывание витамина В12.
- Целиакия — непереносимость глютена, при которой повреждается слизистая оболочка тонкого кишечника.
- Болезнь Крона — хроническое воспалительное заболевание кишечника.
- Опухоли тонкого кишечника, в том числе лимфомы.
- Резекция участка подвздошной кишки.
- Длительный приём некоторых лекарственных препаратов: ингибиторов протонной помпы, аминосалициловой кислоты, метформина, колхицина, неомицина, бигуанидов, циметидина, оральных контрацептивов и др. [1][2][3][4][6][9][10]
4. Нарушение транспорта. После всасывания в кишечнике витамин B12 поступает в кровь, где связывается с белком-транспортёром транскобаламином II. Он доставляет витамин клеткам-потребителям. Врождённый дефект белка-транспортёра либо появление к нему антител приводит к нарушению транспорта витамина B12 и к его дефициту [11].
5. Нарушение метаболизма. Проникая из крови в клетки, витамин B12 принимает участие в сложных биохимических процессах, приводящих к синтезу ДНК, делению и созреванию клеток, обмену жирных кислот и гомоцистеина. Врождённые и приобретённые дефекты ферментов, обеспечивающих эти процессы, могут приводить к развитию B12ДА [2][4].
6. Повышенное расходование витамина В12. Может быть вызвано [4]:
- Состояниями, связанными с повышенным потреблением: многоплодная беременность [18], тиреотоксикоз [19], онкогематологические заболевания (множественная миелома, миелопролиферативные заболевания).
- Конкурентным потреблением витамина: бактериями, например при дивертикулёзе и синдроме «слепой петли»; паразитами — при дифиллоботриозе и власоглаве [3].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы В12-дефицитной анемии
При дефиците внутреннего фактора, дефиците транспортного белка, нарушении внутриклеточного метаболизма и некоторых других врождённых состояниях симптомы B12ДА могут появиться у детей в первые месяцы или годы жизни. При недостаточности поступления с пищей или нарушении всасывания симптомы развиваются постепенно, обычно у детей в возрасте старше 7 лет и у взрослых.
Все проявления B12ДА можно разделить на 3 группы:
- симптомы, связанные со снижением гемоглобина — анемический синдром;
- симптомы поражения желудочно-кишечного тракта — гастроэнтерологический синдром;
- симптомы поражения нервной системы — нейропсихический синдром.
Каждая из этих групп симптомов может присутствовать по отдельности, а может встречаться их сочетание.
Анемический синдром
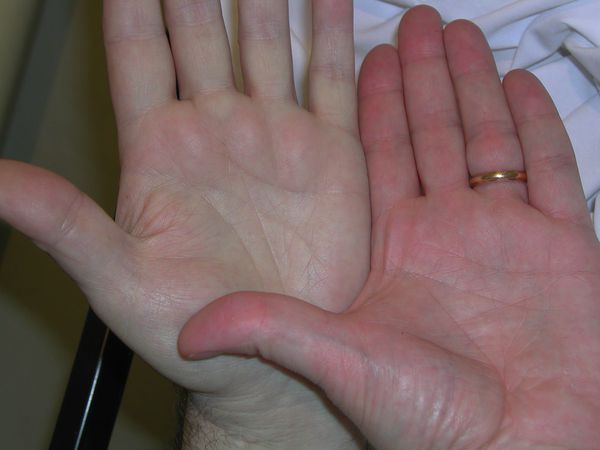
При B12ДА, как и при любой анемии, наблюдается бледность кожи, иногда с желтушным оттенком. Может беспокоить общая слабость, повышенная утомляемость, сонливость, одышка при незначительной физической нагрузке.
Возможно учащённое сердцебиение, шум в ушах, головокружение, потемнение в глазах, мелькание «мушек» перед глазами. Обращает на себя внимание снижение памяти, работоспособности, успеваемости в школе или ВУЗе. У детей на фоне анемического синдрома возможно нарушение роста и развития.
Симптомы поражения желудочно-кишечного тракта
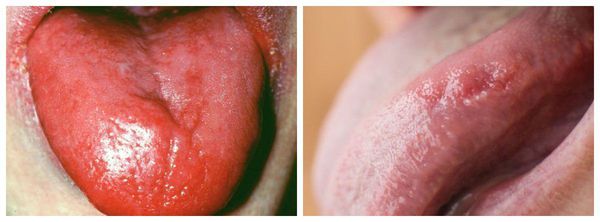
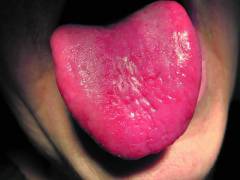
Для больных B12ДА специфичным симптомом является воспаление языка, которое сопровождается неприятными ощущениями и болями. При этом язык ярко-красного цвета, со сглаженными сосочками («лакированный язык», Гунтеровский глоссит), участками воспаления, трещинами и изъязвлениями. Может наблюдаться появление язвочек в углах рта и болей в деснах и губах.
Возможно снижение аппетита и, как следствие, потеря веса, ощущение тяжести в животе, диарея. Иногда незначительно увеличивается печень и селёзенка, что может быть выявлено при пальпации живота врачом либо при УЗИ органов брюшной полости.
Симптомы поражения нервной системы
Поражение нервной системы при B12ДА называется фуникулярным миелозом. Он затрагивает задние и боковые столбы спинного мозга, а также периферические нервы. Чаще встречается у мужчин. Это состояние проявляется онемением, парестезиями (ощущением ползанья мурашек), слабостью в ногах и нарушением походки. Реже наблюдаются подобные жалобы со стороны рук, при этом возникает трудность при выполнении точных движений.
Иногда нарушается слух, обоняние, зрение, возникают психические нарушения от раздражительности до тяжёлой деменции и психоза. Могут возникнуть такие неврологические проявления, как недержание мочи и непроизвольная дефекация. У детей раннего возраста симптомами поражения нервной системы могут быть мышечная слабость, дрожание, непроизвольные сокращения мышц. Возможна задержка психомоторного развития и потеря навыков [1][2][3][4][6][7].
Патогенез В12-дефицитной анемии
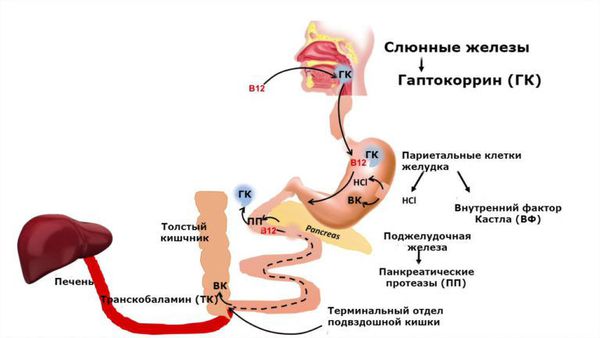
Витамин B12 поступает в организм с продуктами животного происхождения: мясные продукты, яйца, сыр, молоко. Из связи с белками пищи витамин высвобождается сначала под воздействием кулинарной обработки, а затем соляной кислоты и ферментов желудочного сока.
В двенадцатиперстной кишке витамин B12 соединяется с внутренним фактором Кастла, который синтезируется париетальными клетками желудка. Благодаря фактору Кастла витамин B12 поступает в клетки слизистой оболочки подвздошной кишки. После этого он связывается с транспортным белком транскобаламином II и переносится кровью клеткам-потребителям, в основном в печень и костный мозг.
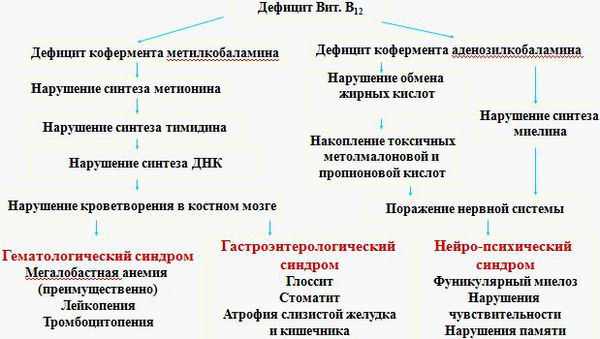
В клетке витамин B12 преобразуется в два кофермента: метилкобаламин и аденозилкобаламин. Коферменты — это соединения, необходимые для функционирования ферментов.
Метилкобаламин является коферментом для фермента метионинсинтазы, который преобразует одну аминокислоту — гомоцистеин в другую — метионин. При сбое этого процесса в организме накапливается гомоцистеин, не образуются пиримидиновые основания, необходимые для формирования ДНК. В результате нарушается синтез ДНК и процессы деления клеток. К этому изменению особенно чувствительны быстроделящиеся клетки — кроветворные клетки костного мозга, из которых образуются клетки крови, а также эпителиальные клетки желудочно-кишечного тракта. Отсюда появление таких изменений в анализе крови, как анемия, лейкопения (снижение количества лейкоцитов), тромбоцитопения (снижение количества тромбоцитов), а также атрофия слизистых оболочек.
Второй кофермент — аденозилкобаламин — принимает участие в обмене жирных кислот, который необходим для метаболизма миелина (вещества, образующего оболочку нервных волокон). Неправильный обмен жирных кислот вследствие недостатка витамина B12 приводит к накоплению токсичных для нервной системы кислот — метилмалоновой и пропионовой. Нарушается синтез миелина в задних и боковых столбах спинного мозга. Как следствие, появляется клиника поражения нервной системы [1][2][3][4][6].
Классификация и стадии развития В12-дефицитной анемии
Классификация В12ДА по причинам развития:
- Наследственные (врождённые) формы. Описаны у детей с генетическими аномалиями, которые приводят к нарушению транспорта и метаболизма витамина B12.
- Приобретённые формы:
- первичная форма обусловлена аутоиммунной причиной дефицита витамина B12, то есть наличием антител к париетальным клеткам желудка или к фактору Кастла. Зачастую первичная форма B12ДА осложняет течение таких заболеваний, как аутоиммунный тиреоидит, витилиго или сахарный диабет 1 типа [6].
- Вторичная форма возникает на фоне строгой веганской диеты [3][7][11].
Стадии развития B12ДА:
- Начальная — латентный дефицит. Уровень витамина в сыворотке крови снижен, однако число эритроцитов и уровень гемоглобина остаются в норме. Клинических проявлений на данной стадии может не наблюдаться. Лабораторно возможно выявить изменение параметров эритроцитов: увеличение среднего объёма эритроцита (параметр MCV в анализе крови) и среднего содержания гемоглобина в эритроците (параметр MCH).
- Стадия клинических проявлений. Наблюдается при снижении уровня гемоглобина, когда появляются симптомы анемии, и при поражении нервной системы.
Степени тяжести В12ДА:
- Лёгкая — снижение уровня гемоглобина до 90 г/л.
- Средней тяжести — уровень гемоглобина в пределах 90-70 г/л.
- Тяжёлая — уровень гемоглобина ниже 70 г/л.
Осложнения В12-дефицитной анемии
Задержка роста и развития у детей возможна в результате снижения гемоглобина при B12ДА.
Сердечная недостаточность. У пожилых пациентов анемия может ухудшить течение сопутствующей сердечно-сосудистой патологии в виде развития сердечной недостаточности [14].
Потеря массы тела может стать результатом снижения аппетита и проявлений со стороны желудочно-кишечного тракта.
Присоединение инфекционных осложнений возможно при развитии глубокой лейкопении (низкого уровня лейкоцитов). Снижение тромбоцитов, как правило, незначительное и не приводит к геморрагическим осложнениям.
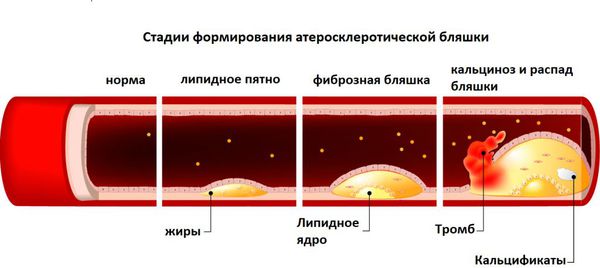
Атеросклероз, тромбоз. Повышение уровня гомоцистеина на фоне дефицита витамина B12 может вызвать атеросклероз и формирование тромбов. Накапливаясь в организме, гомоцистеин повреждает внутреннюю стенку артерий, что приводит к разрывам внутренней оболочки сосудов — эндотелия. В месте повреждения оседает холестерин и кальций — образуется атеросклеротическая бляшка, вследствие чего просвет сосуда сужается, а иногда закупоривается. Это грозит тромбозом или разрывом сосуда [15][16].
Также описано такое тяжёлое осложнение B12ДА, так тромботическая микроангиопатия — заболевание, в основе которого лежит поражение мелких сосудов и формирование в их просвете тромбов, что сопровождается воспалением сосудистой стенки. Как следствие, может развиваться ишемия органов и тканей.
Поражение головного и спинного мозга без лечения может привести к спастичности (чрезмерно высокому мышечному тонусу и непроизвольным движениям) и параплегии (полному параличу обеих рук или ног). С началом лечения B12ДА анемический синдром и неврологические проявления быстро купируются. Однако при выраженном дефиците витамина B12 поражение спинного мозга может быть необратимым [1][6][17].
Диагностика В12-дефицитной анемии
Для правильной постановки диагноза B12ДА важен осмотр врача-гематолога. Для уточнения и коррекции проблем, связанных с работой желудочно-кишечного тракта, потребуется консультация гастроэнтеролога. Для оценки неврологических проявлений может быть необходим осмотр врача-невролога.
Осмотр пациента
При осмотре врач может обратить внимание на бледность и лёгкую желтушность кожи, увеличение частоты сердечных сокращений и расширение границ сердца. Необходимо провести осмотр полости рта, особенно языка. Невролог может оценить тонус мышц и наличие патологических рефлексов.
Лабораторная диагностика
Одним из самых важных этапов диагностики является оценка клинического анализа крови. В анализе наблюдается:
- снижение гемоглобина — анемия;
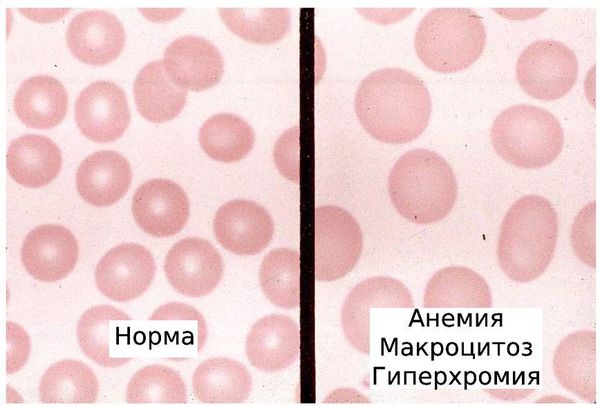
- макроцитоз — наличие в крови большого количества аномально крупных эритроцитов (макроцитов);
- гиперхромия — интенсивное окрашивание эритроцитов, вызванное повышенным количеством гемоглобина в крови;
- может наблюдаться снижение числа лейкоцитов и тромбоцитов.
Необходимо выполнение мазка крови, в котором врач-морфолог может увидеть патологические формы эритроцитов:
- овалоциты (эритроциты овальной формы) и дегенеративные формы;
- увеличение разницы эритроцитов по своему размеру (параметр RDW);
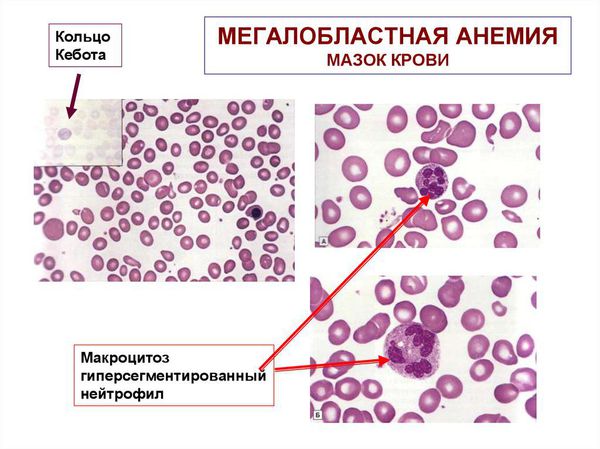
- специфические патологические включения, такие как тельца Жолли и кольца Кебота;
- мегалоциты и мегалобласты — в тяжёлых случаях.
Могут встречаться также патологические формы нейтрофилов:
- гигантские нейтрофилы;
- нейтрофилы с гиперсегментацией ядра (5 и более сегментов);
- метамиелоциты — незрелые нейтрофильные лейкоциты.
Количество молодых форм эритроцитов (ретикулоцитов), как правило, снижено. При наличии лабораторной возможности дополнительную полезную информацию могут предоставить ретикулоцитарные индексы: увеличивается средний объём ретикулоцитов и среднее содержание гемоглобина в ретикулоцитах, повышается фракция незрелых ретикулоцитов [1][2][4][5].
В биохимическом анализе крови:
- снижен уровень витамина B12;
- может быть повышен непрямой билирубин и лактатдегидрогеназа — признак раннего разрушения (гемолиза) эритроцитов в крови и распада предшественников эритроцитов в костном мозге [4];
- уровень железа и ферритина в норме.
Обязательно нужно оценить уровень фолиевой кислоты, поскольку изменения в клиническом анализе при дефиците B12 и фолиевой кислоты схожи, а лечение отличается. При подозрении на B12ДА, но при нормальном уровне витамина B12 и фолиевой кислоты, рекомендовано определение голотранскобаламина сыворотки (активного витамина B12). В случае дефицита B12 его содержание снижено. Может быть выявлено повышение уровня гомоцистеина и метилмалоновой кислоты в сыворотке крови [2][3].
В общем анализе мочи может наблюдаться стойкая протеинурия — появление белка в моче. В ряде случаев отмечается повышение уровня метилмалоновой кислоты и гомоцистеина.
Дополнительные лабораторные исследования, которые могут помочь выявить причину дефицита витамина B12:
- исследование антител к внутреннему фактору Кастла (IgG) и париетальным клеткам желудка в сыворотке крови;
- исследование желудочного сока на выявление внутреннего фактора Кастла и антител к этому фактору (IgA, синтезируются париетальными клетками желудка);
- тест Шиллинга — определяет активность внутреннего фактора Кастла и всасывание витамина B12 в кишечнике;
- тесты на мальабсорбцию (нарушение всасывания питательных веществ) [5].
Возможна пренатальная диагностика генетически обусловленной недостаточности транспортного белка транскобаламина II, поскольку он синтезируется амниоцитами (клетками плодной оболочки).
Инструментальная диагностика
При ультразвуковом исследовании органов брюшной полости можно обнаружить незначительную гепатоспленомегалию — увеличение печени и селезёнки.
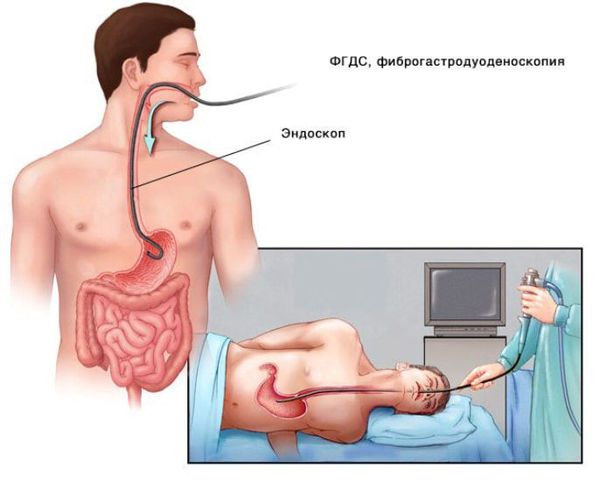
Для выявления заболеваний желудочно-кишечного тракта, которые могут нарушать всасывание витамина B12, всем пациентам с впервые выявленной B12ДА показано выполнение эндоскопических исследований — фиброгастродуоденоскопии (ФГДС) и колоноскопии. При ФГДС может быть выявлен хронический атрофический гастрит, дуоденит, может наблюдаться уменьшение желудочной секреции. При наличии патологических изменений обязательно выполнение биопсии слизистой желудка с дальнейшим гистологическим исследованием [3][4].
Дифференциальная диагностика
Дифференциальный диагноз при В12-дефицитной анемии, особенно со снижением лейкоцитов и тромбоцитов, проводится с такими заболеваниями системы крови:
- Миелодиспластический синдром — группа гематологических заболеваний, при которых костный мозг не производит достаточного количества одного или более типов клеток крови: тромбоцитов, лейкоцитов, эритроцитов.
- Апластическая анемия — это анемия, возникающая вследствие недостаточной продукции эритроцитов из-за уменьшения количества кроветворных стволовых клеток.
Для уточнения диагноза может потребоваться выполнение пункции костного мозга и его морфологическое исследование. При наличии B12ДА специалист морфолог описывает в костном мозге характерные изменения стволовых клеток-предшественников:
- гиперплазию (разрастание) эритроидного ростка — стволовых клеток-предшественников, из которых образуются эритроциты;
- мегалобластный тип кроветворения, при котором образуются крупные клетки с зернистыми ядрами, патологические митозы, тельца Жолли;
- нарушение созревания клеток миелоидного ряда и предшественников тромбоцитов: гигантские метамиелоциты, гиперсегментация нейтрофилов, многоядерные мегакариоциты [1][2][3][4].
Лечение В12-дефицитной анемии
При анемии, которая связана с недостаточностью поступления витамина с пищей, лечение предполагает коррекцию диеты в комбинации с внутримышечным введением витамина B12. Диета с достаточным содержанием витамина B12 предполагает употребление продуктов животного происхождения. Овощи, фрукты, хлеб не содержат витамин B12.
При других причинах коррекция диеты будет неэффективна. Во всех случаях лечение подразумевает введение препарата витамина В12 по стандартным схемам. Дозы препарата могут отличаться в зависимости от возраста больного и от наличия неврологических симптомов.
Лечение обычно проводится в амбулаторных условиях. Показанием для госпитализации в стационар может послужить тяжёлая анемия (уровень гемоглобина менее 70 г/л) и пожилой возраст.
При подозрении на B12ДА без лабораторного её подтверждения категорически не рекомендуется начинать лечение витамином B12 либо поливитаминными комплексами, поскольку введение B12 приводит к быстрому исчезновению морфологических аномалий клеток, что в свою очередь затруднит постановку правильного диагноза. Ошибочное использование фолиевой кислоты при дефиците B12 может привести к усугублению неврологических симптомов. Поэтому очень важно начинать терапию только после лабораторного подтверждения диагноза.
Первый этап терапии — насыщение. Он длится 4-6 недель и предполагает внутримышечное введение препарата цианокобаламин в лечебной дозе. В некоторых случаях может быть эффективно использование сублингвальных форм витамина B12. Признаки улучшения состояния наблюдаются после первых 3-5 инъекций препарата.
Первым лабораторным признаком эффективности терапии является ретикулярный криз — повышение уровня ретикулоцитов в крови в 2-3 раза по сравнению с исходным на 4-7 день от начала терапии. Нормализация уровня гемоглобина достигается через 1-2 месяца, периферическая нейропатия купируется медленнее.
На фоне терапии цианокобаламином в связи с активным делением клеток-предшественников в костном мозге возможно присоединение дефицита фолиевой кислоты и железа, поэтому спустя 7-10 дней от начала терапии витамином B12 необходимо дополнительно назначить фолиевую кислоту, а при снижении уровня ферритина — препараты железа.
Второй этап — закрепляющая терапия: витамин B12 вводится в той же дозе, но кратность введения уменьшается.
Третий этап — поддерживающая терапия. Она проводится пожизненно. Переливание эритроцитарной взвеси показано при тяжёлой анемии с признаками гипоксии и недостаточности кровообращения. При развитии нейтропении (снижения количества нейтрофилов) и присоединении инфекционных осложнений может потребоваться проведение антибактериальной терапии [1][3][4][6].
Прогноз. Профилактика
Независимо от возраста больного, при ранней постановке диагноза, своевременном начале лечения и правильном наблюдении после выздоровления прогноз при B12ДА благоприятный. Ухудшению прогноза могут способствовать сопутствующие сердечно-сосудистые заболевания у пожилых больных, а также поражение нервной системы (фуникулярный миелоз).
Профилактика B12ДА сводится к коррекции рациона питания. При невозможности ликвидировать причину заболевания (например, при удалении части желудка или при недостаточности внутреннего фактора Кастла) профилактика сводится к регулярному пожизненному введению препарата витамина B12. Анализ крови необходимо контролировать 1 раз в 3-4 месяца. Больным с атрофическим гастритом рекомендовано ежегодное выполнение ФГДС, поскольку у них повышен риск новообразований желудка [3][6].
Пернициозная анемия (Болезнь Аддисона-Бирмера, В12-дефицитная анемия)
Пернициозная анемия – нарушение красного ростка кроветворения, обусловленное недостатком в организме цианокобаламина (витамина В12). При В12-дефицитной анемии развивается циркуляторно-гипоксический (бледность, тахикардия, одышка), гастроэнтерологический (глоссит, стоматит, гепатомегалия, гастроэнтероколит) и неврологический синдромы (нарушение чувствительности, полиневриты, атаксия). Подтверждение пернициозной анемии производится по результатам лабораторных исследований (клинического и биохимического анализа крови, пунктата костного мозга). Лечение пернициозной анемии включает сбалансированную диету, внутримышечное введение цианокобаламина.
Общие сведения
Пернициозная анемия – разновидность мегалобластной дефицитной анемии, развивающаяся при недостаточном эндогенном поступлении или усвоении в организме витамина В12. «Пернициозная» в переводе с латинского означает «опасная, гибельная»; в отечественной традиции такая анемия раньше называлась «злокачественным малокровием». В современной гематологии синонимами пернициозной анемии также служат В12-дефицитная анемия, болезнь Аддисона-Бирмера. Заболевание чаще возникает у лиц старше 40-50 лет, несколько чаще у женщин. Распространенность пернициозной анемии составляет 1%; вместе с тем, дефицитом витамина В12 страдает около 10% пожилых людей в возрасте старше 70 лет.
Пернициозная анемия
Причины пернициозной анемии
Ежесуточная потребность человека в витамине B12 равняется 1-5 мкг. Она удовлетворяется за счет поступления витамина с пищей (мясом, кисломолочными продуктами). В желудке под действием ферментов витамин В12 отделяется от пищевого белка, однако для усвоения и всасывания в кровь он должен соединиться с гликопротеином (фактором Касла) или другими связывающими факторами. Всасывание цианокобаламина в кровоток происходит в средней и нижней части подвздошной кишки. Последующий транспорт витамина В12 к тканям и гемопоэтическим клеткам осуществляется белками плазмы крови — транскобаламинами 1, 2, 3.
Развитие В12-дефицитной анемии может быть связано с двумя группами факторов: алиментарными и эндогенными. Алиментарные причины обусловлены недостаточным поступлением витамина В12 с пищей. Это может происходить при голодании, вегетарианстве и диетах с исключением животного белка.
Под эндогенными причинами подразумевается нарушение усвоения цианокобаламина вследствие дефицита внутреннего фактора Касла при его достаточном поступлении из вне. Такой механизм развития пернициозной анемии встречается при атрофическом гастрите, состоянии после гастрэктомии, образовании антител к внутреннему фактору Касла или париетальным клеткам желудка, врожденном отсутствии фактора.
Нарушение абсорбции цианокобаламина в кишечнике может отмечаться при энтерите, хроническом панкреатите, целиакии, болезни Крона, дивертикулах тонкого кишечника, опухолях тощей кишки (карциноме, лимфоме). Повышенное расходование цианокобаламина может быть связано с гельминтозами, в частности, дифиллоботриозом. Существуют генетические формы пернициозной анемии.
Всасывание витамина В12 нарушено у пациентов, перенесших резекцию тонкой кишки с наложением желудочно-кишечного анастомоза. Пернициозная анемия может быть ассоциирована с хроническим алкоголизмом, применением некоторых лекарственных средств (колхицина, неомицина, пероральных контрацептивов и др.). Поскольку в печени содержится достаточный резерв цианкобаламина (2,0-5,0 мг), пернициозная анемия развивается, как правило, только лишь спустя 4-6 лет после нарушения поступления или усвоения витамина В12.
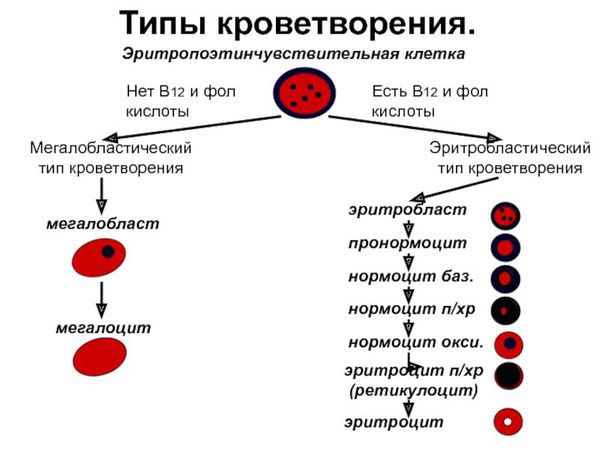
В условиях недостаточности витамина В12 возникает дефицит его коферментных форм – метилкобаламина (участвует в нормальном протекании процессов эритропоэза) и 5-дезоксиаденозилкобаламина (участвует в метаболических процессах, протекающих в ЦНС и периферической нервной системе). Недостаток метилкобаламина нарушает синтез незаменимых аминокислот и нуклеиновых кислот, что приводит к расстройству образования и созревания эритроцитов (мегалобластному типу кроветворения). Они принимают форму мегалобластов и мегалоцитов, которые не выполняют кислородтранспортную функцию и быстро разрушаются. В связи с этим количество эритроцитов в периферической крови существенно сокращается, что приводит к развитию анемического синдрома.
С другой стороны, при дефиците кофермента 5-дезоксиаденозилкобаламина нарушается обмен жирных кислот, в результате чего накапливаются токсичные метилмалоновая и пропионовая кислоты, оказывающие непосредственное повреждающее действие на нейроны головного и спинного мозга. Кроме этого, нарушается синтез миелина, что сопровождается дегенерацией миелинового слоя нервных волокон – этим обусловлено поражение нервной системы при пернициозной анемии.
Симптомы пернициозной анемии
Тяжесть течения пернициозной анемии определяется выраженностью циркуляторно-гипоксического (анемического), гастроэнтерологического, неврологического и гематологического синдромов. Признаки анемического синдрома неспецифичны и являются отражением нарушения кислородтранспортной функции эритроцитов. Они представлены слабостью, снижением выносливости, тахикардией и ощущением сердцебиения, головокружением и одышкой при движении, субфебрилитетом. При аускультации сердца может выслушиваться шум «волчка» или систолические (анемические) шумы. Внешне отмечается бледность кожи с субиктеричным оттенком, одутловатость лица. Длительный «стаж» пернициозной анемии может приводить к развитию миокардиодистрофии и сердечной недостаточности.
Гастроэнтерологическими проявлениями В12-дефицитной анемии служат пониженный аппетит, неустойчивость стула, гепатомегалия (жировая дистрофия печени). Классический симптом, выявляемый при пернициозной анемии – «лакированный» язык малинового цвета. Характерны явления ангулярного стоматита и глоссита, жжение и болевые ощущения в языке. При проведении гастроскопии обнаруживаются атрофические изменения слизистой желудка, которые подтверждаются эндоскопической биопсией. Желудочная секреция резко снижается.
Неврологические проявления пернициозной анемии обусловлены поражением нейронов и проводящих путей. Больные указывают на онемение и скованность конечностей, мышечную слабость, нарушение походки. Возможно недержание мочи и кала, возникновение стойкого парапареза нижних конечностей. Осмотр невролога выявляет нарушение чувствительности (болевой, тактильной, вибрационной), повышение сухожильных рефлексов, симптомы Ромберга и Бабинского, признаки периферической полиневропатии и фуникулярного миелоза. При В12-дефицитной анемии могут развиваться психические нарушения – бессонница, депрессия, психозы, галлюцинации, деменция.
Лакированный язык при пернициозной анемии
Диагностика пернициозной анемии
Кроме гематолога, к диагностике пернициозной анемии должны быть привлечены гастроэнтеролог и невролог. Дефицит витамина В12 (менее 100 пг/мл при норме 160-950 пг/мл) устанавливается при проведении биохимического исследования крови; возможно обнаружение Ат к париетальным клеткам желудка и к внутреннему фактору Касла. Для общего анализа крови типична панцитопения (лейкопения, анемия, тромбоцитопения). При микроскопии мазка периферической крови обнаруживаются мегалоциты, тельца Жолли и Кэбота. Исследование кала (копрограмма, анализ на яйца глистов) могут выявлять стеаторею, фрагменты или яйца широкого лентеца при дифиллоботриозе.
Проба Шиллинга позволяет определить нарушение всасывания цианокобаламина (по экскреции с мочой меченного радиоактивным изотопом витамина В12, принятого внутрь). Пункция костного мозга и результаты миелограммы отражают характерное для пернициозной анемии увеличение числа мегалобластов.
Для определения причин нарушения абсорбции витамина В12 в ЖКТ проводится ФГДС, рентгенография желудка, ирригография. В диагностике сопутствующих нарушений информативны ЭКГ, УЗИ органов брюшной полости, электроэнцефалография, МРТ головного мозга и др. В12-дефицитную анемию необходимо отличать от фолиеводефицитной, гемолитической и железодефицитной анемии.
Лечение пернициозной анемии
Установление диагноза пернициозной анемии означает, что пациент будет нуждаться в пожизненном патогенетическом лечении витамином В12. Кроме этого, показано регулярное (каждые 5 лет) проведение гастроскопии для исключения развития рака желудка.
С целью восполнения дефицита цианокобаламина назначаются внутримышечные инъекции витамина В12. Требуется коррекция состояний, приведших к В12-дефицитной анемии (дегельминтизация, прием ферментных препаратов, хирургическое лечение), а при алиментарном характере заболевания — диета с повышенным содержанием животного белка. При нарушении выработки внутреннего фактора Касла назначаются глюкокортикоиды. К гемотрансфузиям прибегают только при анемии тяжелой степени или признаках анемической комы.
На фоне терапии пернициозной анемии показатели крови обычно нормализуются через 1,5-2 месяца. Дольше всего (до 6 мес.) сохраняются неврологические проявления, а при поздно начатом лечении они становятся необратимыми.
Пернициозная анемия
Профилактика
Первым шагом на пути предотвращения пернициозной анемии должно стать полноценное питание, обеспечивающее достаточное поступление в организм витамина В12 (употребление мяса, яиц, печени, рыбы, молочных продуктов, сои). Необходима своевременная терапия патологий ЖКТ, нарушающих усвоение витамина. После хирургических вмешательств (резекции желудка или кишечника) необходимо проведение поддерживающих курсов витаминотерапии.
Больные с В12-дефицитной анемией входят в группу риска по развитию диффузного токсического зоба и микседемы, а также рака желудка, поэтому нуждаются в наблюдении эндокринолога и гастроэнтеролога.
Пернициозная анемия — лечение в Москве
Что такое мегалобластная анемия?
Мегалобластная анемия (болезнь Аддисона-Бирмера или пернициозная анемия) — это состояние, при котором костный мозг производит необычно крупные, структурно аномальные, незрелые эритроциты (мегалобласты).
Костный мозг, мягкий губчатый материал, содержащийся в определенных костях, производит основные кровяные клетки тела — красные клетки, белые клетки и тромбоциты.
Анемия — это состояние, характеризующееся низким уровнем циркулирующих эритроцитов (красные кровяные тельца). Эритроциты высвобождаются из костного мозга в кровоток, где они перемещаются по всему организму, доставляя кислород к тканям. Дефицит здоровых, полностью созревших эритроцитов может привести к усталости, бледности кожи, проблемы с памятью и концентрацией внимания и дополнительным признакам.
Мегалобластная анемия имеет несколько различных причин, — из которых две наиболее распространенные — дефицит кобаламина (витамин B12) или фолиевой кислоты (витамин B9).
Признаки и симптомы
В большинстве случаев мегалобластная анемия развивается медленно, и больные люди не испытывают явных симптомов (т.е. бессимптомное течение) многие годы. Симптомы, общие для анемии, обычно развиваются внезапно, в определенный момент жизни и включают:
- усталость;
- бледность кожи;
- одышку;
- головокружение;
- проблемы с памятью;
- учащенное или нерегулярное сердцебиение.
Специфические симптомы, присутствующие у каждого человека, могут сильно различаться.
Дополнительные общие симптомы включают боли и недомогания, мышечную слабость и затрудненное дыхание. У людей с заболеванием могут также развиться желудочно-кишечные нарушения, включая:
- диарею;
- тошноту;
- потерю аппетита.
У некоторых больных краснеет и воспаляется язык. Эти нарушения (диарея, отсутствие аппетита…) могут привести к непреднамеренной потере веса. Может также произойти легкое увеличение печени (гепатомегалия) и небольшое пожелтение кожи или склеры глаз (желтуха).
Мегалобластная анемия, вызванная дефицитом кобаламина (витамина B12), также может быть связана с неврологическими симптомами. Первоначальный неврологический симптом могут включать покалывание или онемение в руках или ногах. Со временем развиваются дополнительные симптомы, включая:
- нарушение равновесия или проблемы с походкой;
- потеря зрения из-за дегенерации (атрофии) нерва, передающего импульсы от сетчатки к мозгу (зрительный нерв);
- спутанность сознания;
- потеря памяти;
- проблемы с концентрацией внимания.
У лиц с дефицитом кобаламина также сообщалось о различных психических расстройствах, включая:
- депрессию;
- бессонницу;
- вялость;
- приступы паники.
Спектр потенциальных нейропсихологических симптомов, потенциально связанных с дефицитом кобаламина, велик и разнообразен.
В редких случаях дефицита кобаламина неврологические симптомы могут возникать до характерных признаков анемии. Обычно считается, что дефицит фолиевой кислоты не приводит к неврологическим симптомам, хотя некоторые недавние исследования показывают, что в редких случаях недостаток витамина B9 может вызывать некоторые неврологические симптомы.
Причины мегалобластной анемии
Наиболее распространенными причинами мегалобластной анемии являются дефицит кобаламина (витамин B12) или фолиевой кислоты (фолат, витамин B9). Эти два витамина служат строительными блоками и необходимы для производства здоровых клеток, например, предшественников эритроцитов. Без этих необходимых витаминов создание (синтез) дезоксирибонуклеиновой кислоты (ДНК), генетического материала, обнаруженного во всех клетках, затруднен.
Дефицит витаминов, приводящий к мегалобластной анемии, может быть результатом недостаточного потребления кобаламина и фолиевой кислоты с питанием, плохой абсорбции витаминов кишечником или неправильного использования витаминов организмом. Дефицит фолата также может быть результатом состояний, требующих чрезмерного количества фолата.
Кобаламин содержится в мясе, рыбе и яйцах. Дефицит кобаламина из-за плохого рациона питания встречается крайне редко, но наблюдается у некоторых вегетарианцев (веганов). Наиболее частой причиной дефицита кобаламина является нарушение всасывания витамина в тонкой кишке (мальабсорбция). В таких случаях организм содержит достаточное количество витамина, но не может усваивать и впоследствии использовать витамин. Нарушение всасывания может быть результатом:
- операции на кишечнике;
- кишечных заболеваний, таких как болезнь Крона или тропический спру;
- инфекции (рост бактерий) в желудочно-кишечном тракте.
Пагубная анемия может также вызвать дефицит кобаламина. Эта форма анемии характеризуется отсутствием внутреннего фактора, белка, который связывается с кобаламином и способствует его всасыванию в тонкой кишке. Без достаточного внутреннего фактора, организм не может поглотить достаточно кобаламинов.
В редких случаях рыбий ленточный червь, известный как Широкий лентец, может укорениться в тонкой кишке и израсходовать кобаламин, тем самым лишив организм необходимого количества этого необходимого витамина. В некоторых случаях бактерии могут конкурировать с организмом за кобаламин, как при синдром слепой кишечной петли, расстройстве, при котором обструкция тонкого кишечника приводит к ненормальному скоплению бактерий в желудочно-кишечном тракте.
Фолиевая кислота обычно содержится в зеленых листовых овощах, цитрусах и некоторых зернах и орехах. Дефицит фолата может возникнуть при недостаточном количестве потреблении этих продуктов. У алкоголиков может развиться дефицит фолата, потому что алкоголь не содержит фолат и может нарушить распад (метаболизм) данного вещества в организме. Хирургические вмешательства на желудке или кишечнике может привести к нарушению всасывания фолата. Определенные кишечные расстройства, такие как болезнь Крона или тропический спру, могут вызвать нарушение всасывания и последующий дефицит фолата.
Беременные женщины, женщины кормящие грудью, больные с хроническими гемолитическими анемиями и люди, подвергающиеся гемодиализу при заболеваниях почек, имеют более высокие, чем обычно, потребности в фолате. Неспособность адекватно пополнить фолат у этих людей может привести к дефициту витамина.
Некоторые лекарства могут ухудшить способность организма поглощать фолат, в том числе многие препараты, применяемые для лечения рака. Лекарства также могут нарушать синтез ДНК, что приводит к мегалобластной анемии.
Выявлены гораздо более редкие причины мегалобластной анемии (не связанной с дефицитом витаминов), в том числе редкие ферментные дефициты, известные как врожденные нарушения обмена веществ и первичные нарушения костного мозга, включая миелодиспластические синдромы и острый миелоидный лейкоз.
В некоторых случаях причина заболевания неизвестна (идиопатическая).
Затронутые группы населения
Заболевание поражает мужчин и женщин в равных количествах. Состояние может возникнуть у людей любого расового или этнического происхождения. Поскольку причины мегалобластной анемии различны и у некоторых людей могут не проявляться какие-либо очевидные симптомы (бессимптомное течение), определить их истинную частоту в общей популяции сложно.
Диагностика
Диагноз мегалобластной анемии ставится на основании тщательной клинической оценки, подробного анамнеза пациента, выявления характерных признаков и различных анализов крови. Анализы крови могут выявить аномально большие, деформированные эритроциты, которые характеризуют мегалобластную анемию.
Анализы крови также могут подтвердить дефицит кобаламина или фолата как причину мегалобластной анемии. Могут потребоваться дополнительные исследования, например, проба Шиллинга, подтверждающая плохую абсорбцию как причину дефицита кобаламина.
Схожие по симптомам расстройства
Симптомы следующих расстройств могут быть похожи на симптомы мегалобластной анемии. Сравнения могут быть полезны для дифференциальной диагностики.
- Пагубная анемия — редкое заболевание крови, характеризующееся неспособностью организма правильно использовать витамин B12, который необходим для развития эритроцитов. В большинстве случаев из-за недостатка желудочного белка, известного как внутренний фактор, без которого витамин B12 не усваивается. Симптомы пагубной анемии могут включать слабость, усталость, расстройство желудка, аномально быстрое сердцебиение (тахикардия) и/или боли в груди. Периодические эпизоды бледности и желтизны кожи (желтуха) также распространены. Считается, что пагубная анемия является аутоиммунным заболеванием, и некоторые люди могут иметь генетическую предрасположенность к расстройству. Существует редкая врожденная форма пагубной анемии, при которой дети рождаются без способности вырабатывать эффективный внутренний фактор. Существует также ювенильная форма заболевания, однако редко, обычно болезнь не проявляется до возраста 30 лет. Начало заболевания протекает медленно и может длиться десятилетия. Когда заболевание не диагностируется и не лечится в течение длительного периода времени, это может привести к неврологическим осложнениям. Нервным клеткам и клеткам крови необходим витамин B12 для правильной работы.
В некоторых случаях структурные изменения в аномальных эритроцитах (мегалобластах), которые характеризуют мегалобластную анемию, были ошибочно приняты за некоторые первичные нарушения костного мозга, такие как:
- острый миелоидный лейкоз;
- миелодиспластические синдромы;
- апластическая анемия.
Лечение
Лечение мегалобластной анемии зависит от первопричины заболевания. Диетическую недостаточность кобаламина и фолата можно лечить с помощью соответствующих изменений в рационе и приеме добавок. У людей, которые не могут усваивать кобаламин или фолиевую кислоту должным образом, может потребоваться дополнительное введение этих витаминов в течение всей жизни. Оперативное лечение дефицита кобаламина важно из-за риска неврологических симптомов.
Если лежащие в основе расстройства (например, болезнь Крона, тропический спру, целиакия, синдром слепой кишечной петли, врожденные нарушения обмена веществ) являются причиной недостатков витаминов, требуется соответствующее лечение для конкретного расстройства. Может также потребоваться добавка кобаламина или фолата.
Если лекарственное средство стало причиной дефицита витаминов, то следует прекратить применение или уменьшить дозировку конкретного лекарства.
Прогноз
Прогноз благоприятный, если выявлена этиология мегалобластоза и назначено соответствующее лечение. Однако пациенты подвергаются риску гипокалиемии (пониженная концентрация ионов калия в крови) и сердечных осложнений, связанных с анемией, во время терапии дефицита кобаламина.
Дефицит фолиевой кислоты во время беременности может привести к дефектам нервной трубки и другим нарушениям развития у плода. Однако прием фолиевой кислоты в добавках во время беременности, снижает эти заболевания.
Сайт предоставляет справочную информацию. Адекватная диагностика и лечение болезни возможны под наблюдением добросовестного врача. У любых препаратов есть противопоказания. Необходима консультация специалиста, а также подробное изучение инструкции!
Данное заболевание крови встречается у 0,1% всего населения, однако среди пожилых людей данный показатель повышается до 1%. Чаще болеют женщины, причем развитие дефицита витамина В12 обычно связано с беременностью и может самостоятельно исчезать после рождения ребенка.
Интересные факты
- Дефицит витамина В12 отмечается у 10% людей в возрасте старше 70 лет, однако не у всех из них развиваются клинические проявления В12 дефицитной анемии.
- Ни одно животное или растение на земле не способно синтезировать витамин В12.
- Витамин В12 вырабатывается исключительно микроорганизмами (бактериями), обитающими в конечном отделе пищеварительного тракта животных и человека, однако он неспособен попасть в кровоток, так как его всасывание происходит в тощей кишке, которая расположена в начальных отделах кишечника.
Что такое эритроциты?
Образование эритроцитов
Образование эритроцитов начинается еще на ранних стадиях эмбрионального развития. Первые клетки крови у эмбриона образуются из мезенхимы (особой эмбриональной ткани) в конце 3 недели беременности. По мере роста и развития выделяются основные органы, которые обеспечивают кроветворение.
Основными кроветворными органами являются:
- Печень – выполняет кроветворную функцию с 6 недели внутриутробного развития и до рождения ребенка.
- Селезенка – участвует в процессе кроветворения с 12 недели внутриутробного развития и до рождения ребенка.
- Красный костный мозг – начинает выполнять кроветворную функцию с 12 недели внутриутробного развития и является единственным кроветворным органом после рождения ребенка.
Образование эритроцитов происходит из так называемых полипотентных стволовых клеток (ПСК). В организме человека имеется около 40 тысяч ПСК, которые образуются в периоде внутриутробного развития. Они содержат ядро, в котором располагается ДНК (дезоксирибонуклеиновая кислота), регулирующая процессы клеточного деления и дифференцировки (приобретения клеткой специфической функции). Кроме ядра в стволовых клетках имеется множество других структур (органелл), которые нужны для обеспечения процессов их жизнедеятельности и размножения.
Молекула ДНК человека имеет форму двух нитей, спирально перекрученных между собой. Каждая нить состоит из множества особых химических соединений – нуклеозидов. Нуклеозиды могут соединяться друг с другом в различных комбинациях, от чего в конечном итоге и зависит вид клетки, ее форма, состав и выполняемые ею функции. Другими словами, любые проявления живой клетки зависят от того, какие нуклеозиды и в какой последовательности будут взаимодействовать в каждой определенной молекуле ДНК.
Уникальной особенностью ПСК является то, что под действием различных регуляторных факторов они могут превращаться в любую клетку крови — эритроцит (обеспечивающий транспорт газов), тромбоцит (отвечающий за остановку кровотечений), лейкоцит или лимфоцит (выполняющие защитные функции).
Процесс роста и развития эритроцитов регулируется эритропоэтином – особым веществом, которое вырабатывается почками, если ткани организма испытывают недостаток в кислороде (кислородное голодание). Эритропоэтин активирует образование эритроцитов в красном костном мозге, в результате чего увеличивается их количество в периферической крови, что улучшает доставку кислорода к органам и тканям организма. Устранение кислородного голодания на тканевом уровне уменьшает продукцию эритропоэтина, что приводит к уменьшению синтеза эритроцитов.
Процесс дифференцировки (образования эритроцита из стволовой клетки) можно представить следующим образом:
- Полипотентная стволовая клетка через несколько промежуточных делений превращается в клетку-предшественницу эритропоэза, которая также содержит ядро и органеллы.
- Под воздействием эритропоэтина клетка-предшественница эритропоэза начинает активно делиться, при этом в ней происходит ряд структурных и функциональных изменений — она в несколько раз уменьшается в размерах, теряется ядро и большинство органелл (следовательно, и способность к дальнейшему размножению) и накапливает гемоглобин.
- Все описанные выше процессы происходят в красном костном мозге, а их результатом является образование ретикулоцитов (незрелых форм эритроцитов). За сутки в костном мозге образуется около 3 х 109 ретикулоцитов, которые выделяются в периферический кровоток. Они содержат некоторые органеллы и способны в небольших количествах образовывать гемоглобин.
- В течение 24 часов происходит полная утрата всех оставшихся органелл, в результате чего формируется зрелый эритроцит.
Для образования эритроцитов необходимы:
- Железо – включается в состав гемоглобина, являясь основным микроэлементом, обеспечивающим транспорт кислорода в организме.
- Витамин В12 (кобаламин) – принимает участие в образовании ДНК.
- Витамин В9 (фолиевая кислота) – также участвует в процессе образования ДНК.
- Витамин В6 (пиридоксин) – участвует в процессе образования гемоглобина.
- Витамин В2 (рибофлавин) – участвует в процессе дифференцировки эритроцитов.
Строение и функция эритроцитов
Конечным этапом эритропоэза является зрелый эритроцит. Он не содержит ядра, практически полностью лишен органелл и не способен делиться. Его красный цвет обусловлен наличием железа, входящего в состав гемоглобина, который заполняет почти все внутреннее пространство клетки (в каждом эритроците содержится от 250 до 400 миллионов молекул гемоглобина, что равняется 25 – 40 пикограммам).
Эритроцит имеет форму уплощенного двояковогнутого диска с более толстыми краями и углублением в центре. Внутренняя поверхность его клеточной мембраны выстлана специальным белком – спектрином, который отвечает за поддержание формы клетки. Диаметр клетки равен в среднем 7,5 – 8,3 мкм.
Перечисленные особенности строения позволяют эритроциту видоизменяться и проходить через мельчайшие кровеносные сосуды организма, диаметр которых в 2 – 3 раза меньше диаметра самих эритроцитов, возвращаясь после этого к первоначальной форме (благодаря наличию спектрина).
Эритроциты не способны передвигаться самостоятельно и транспортируются в организме с током крови. Наружные поверхности их мембран обладают определенным отрицательным зарядом, в результате чего отталкиваются друг от друга, от остальных клеток крови и от стенок сосудов (которые также заряжены отрицательно). Это обеспечивает поддержание всех клеток крови во взвешенном состоянии, предотвращая их слипание и образование сгустков.
Старение и разрушение эритроцитов
Средний срок жизни эритроцитов составляет 120 дней, в течение которых они циркулируют в крови, выполняя свои функции. Так как данные клетки практически лишены органелл, их способности к устранению повреждений (неизменно возникающих в процессе циркуляции в организме) довольно ограничены.
С течением времени эритроциты несколько уменьшаются в объеме (однако количество гемоглобина в них остается прежним), клеточная мембрана утрачивает эластичность и способность видоизменяться. Кроме того, наружная поверхность мембран старых эритроцитов теряет свой отрицательный заряд. Результатом этих процессов является уменьшение прочности и изменение формы красных клеток крови, что способствует их разрушению.
Разрушение эритроцитов (гемолиз) происходит:
- в селезенке;
- в сосудистом русле.
Разрушение эритроцитов в селезенке (внутриклеточный гемолиз)
Селезенка является основным органом, в котором разрушается до 90% эритроцитов, а также других клеток крови. Этому процессу способствует наличие большого количества так называемых синусоидных капилляров, имеющих в своей стенке небольшие отверстия. Эритроциты при прохождении через такие капилляры выходят из них и проходят через узкие щели в ткани селезенки (диаметр которых составляет 0,5 – 0,7 мкм). Старые или деформированные клетки не способны пройти через эти щели, поэтому задерживаются в них и разрушаются специальными клетками – макрофагами, которые находятся в данном органе в большом количестве.
При разрушении эритроцита железо, входящее в состав гемоглобина, высвобождается в кровоток, связывается с особым транспортным белком трансферрином и переносится в костный мозг, где вновь используется для образования эритроцитов. Оставшийся гемоглобин в результате нескольких химических реакций превращается в билирубин (несвязанную фракцию) – вещество желтого цвета, которое выделяется в кровоток при разрушении эритроцитов. Билирубин транспортируется в печень, где связывается с глюкуроновой кислотой, образуя связанную фракцию билирубина, которая включается в состав желчи и выводится из организма с калом.
Разрушение эритроцитов в сосудистом русле (внеклеточный гемолиз)
Данный термин подразумевает разрушение эритроцитов (и других клеток крови) непосредственно в просвете кровеносных сосудов. Примерно 10% эритроцитов разрушается путем внеклеточного гемолиза. Гемоглобин, попадающий при этом в кровоток, связывается с особым белком плазмы – гаптоглобином. Образующийся комплекс переносится в селезенку и разрушается ее макрофагами.
Что такое В12 дефицитная анемия?
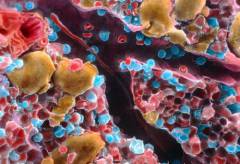
Обмен витамина В12 в организме
Организм человека не в состоянии синтезировать витамин В12, поэтому его количество полностью зависит от поступления с пищей (преимущественно животного происхождения).
Всасывание кобаламина происходит в кишечнике и только в присутствии особого фермента – внутреннего фактора Касла, который вырабатывается париетальными клетками слизистой оболочкой желудка. Поступающий с пищей витамин В12 связывается с данным ферментом в желудке. Образовавшийся комплекс взаимодействует (в присутствии ионов кальция) со специфическими рецепторами клеток слизистой оболочки тощей кишки (являющейся частью тонкого кишечника), в результате чего кобаламин переносится в кровоток, а внутренний фактор Касла остается в просвете кишечника.
Попавший в кровоток витамин В12 связывается со специальным транспортным белком – транскобаламином I или II и в таком виде доставляется в костный мозг, где принимает участие в процессе кроветворения, и в печень, являющуюся местом его депонирования. Важно отметить, что в клетки организма витамин В12 может попасть, только находясь в комплексе с транскобаламином II.
При сбалансированном питании и прочих нормальных условиях в кишечнике ежедневно всасывается 30 – 50 мкг витамина В12. Он депонируется в печени, которая у взрослого человека может содержать до 3 – 5 миллиграмм витамина. Если учесть, что суточная потребность организма в нем составляет 3 – 5 мкг, то становится понятным, почему первые признаки В12 дефицитной анемии начинают появляться не ранее чем через 2 – 3 года после нарушения процессов поступления кобаламина в организм.
Механизм развития В12 дефицитной анемии
Недостаток витамина В12 приводит к нарушению синтеза ДНК во всех клетках организма. В первую очередь это проявляется в тканях, в которых процессы клеточного деления происходят наиболее интенсивно — в кроветворной ткани и в слизистых оболочках.
Попавший в клетку кобаламин превращается в одну из двух активных форм:
- Дезоксиаденозилкобаламин (ДА-В12). Участвует в образовании жирных кислот. При их недостатке в организме поражается нервная система.
- Метил-кобаламин (метил-В12). Принимает активное участие в процессе образования компонентов ДНК, а именно в синтезе тимидина – одного из пиримидиновых нуклеозидов. Недостаток витамина В12 в организме приводит к остановке синтеза данного нуклеозида, в результате чего образуется структурно неполноценная молекула ДНК. Она быстро разрушается, что делает невозможным дальнейшее деление и дифференцировку клеток. Кроме того, метил-В12 также необходим для образования миелина, из которого состоят оболочки нервных волокон. При недостатке данного вещества нарушается проведение нервного импульса по нервам, что может проявляться разнообразными неврологическими симптомами.
Нарушение синтеза ДНК в процессе кроветворения происходит в начальных стадиях эритропоэза, в результате чего дальнейшее развитие эритроцитов становится невозможным. Образующиеся при этом кроветворные клетки (называемые мегалобластами) имеют большие размеры (10 – 20 мкм), содержат остатки разрушенного ядра и множество органелл, а также большое количество гемоглобина. Большинство из них разрушается прямо в костном мозге – развивается так называемый неэффективный эритропоэз. Те мегалобласты, которые все-таки выделяются в кровоток, неспособны выполнять транспортную функцию и при первом же прохождении через селезенку задерживаются и разрушаются в ней.
Важно отметить, что при недостатке витамина В12 в костном мозге нарушается образование не только эритроцитов, но и других клеток – лейкоцитов и тромбоцитов. Обычно эти изменения выражены менее значительно, чем дефицит эритроцитов, однако при длительном течении заболевания и отсутствии адекватного лечения может развиться панцитопения – клинический синдром, характеризующийся недостатком всех клеточных элементов в крови.
Причины В12 дефицитной анемии

Причинами развития дефицита витамина В12 являются:
- недостаточное поступление с пищей;
- нарушение всасывания в кишечнике;
- повышенное использование витамина В12 в организме;
- наследственные заболевания, нарушающие обмен витамина В12.
Недостаточное поступление витамина В12 с пищей
Как было сказано ранее, организм человека неспособен самостоятельно синтезировать кобаламин, поэтому он должен присутствовать в потребляемой пище. Растения не содержат витамин В12, поэтому единственным его источником являются продукты животного происхождения — мясо, рыба, кисломолочные продукты и так далее. В нормальных условиях данные продукты включены в рацион почти каждого человека, поэтому дефицита витамина В12 не развивается.
Причинами недостаточного поступления витамина В12 с пищей могут быть:
- нарушение питания;
- хронический алкоголизм.
Нарушение питания
Одной из частых причин дефицита кобаламина в организме может быть вегетарианство. Вегетарианцами называется определенная группа людей, которые полностью отказались не только от мяса, но и от всех продуктов животного происхождения (яиц, рыбы, молока, сливочного масла и других). Так как данные продукты являются единственным источником кобаламина, вполне логично, что в скором времени у таких людей может развиться дефицит витамина В12 в организме.
Кроме вегетарианцев риск развития В12 дефицитной анемии повышен у бедных слоев населения, которые из-за недостатка средств не могут позволить себе употребление достаточного количества продуктов животного происхождения.
Хронический алкоголизм
Употребление больших доз алкоголя препятствует взаимодействию кобаламина с внутренним фактором Касла, а также повреждает слизистую оболочку желудка, нарушая выработку данного фактора париетальными клетками. Результатом этого становится резкое уменьшение количества кобаламина, поступающего в кровь.
Кроме того, длительное злоупотребление алкогольными напитками может привести к развитию таких заболеваний как алкогольный гепатит и цирроз. Результатом этого является уменьшение запасов кобаламина в печени, что снижает компенсаторные возможности организма при нарушении поступления данного витамина с пищей.
Нарушение всасывания витамина В12 в кишечнике
В данном случае с пищей поступает достаточное количество кобаламина, однако нарушены процессы его транспортировки из просвета кишечника в кровь.
Причинами нарушения всасывания витамина В12 могут быть:
- нарушение образования внутреннего фактора Касла;
- поражение тонкого кишечника;
- паразитарные инфекции.
Нарушение образования внутреннего фактора Касла
Как уже говорилось, наличие данного фактора является необходимым условием для всасывания витамина В12. При его недостатке поступающий с пищей кобаламин не способен пройти через слизистую оболочку кишечника и полностью выделяется с калом.
Причинами недостатка внутреннего фактора Касла могут быть:
- Атрофический гастрит. Данное заболевание характеризуется атрофией (уменьшением размеров и снижением функциональной активности) всех клеток слизистой оболочки желудка, что приводит к снижению или полному прекращению синтеза внутреннего фактора Касла париетальными клетками.
- Аутоиммунный гастрит. Характеризуется нарушением деятельности иммунной (защитной) функции организма, в результате чего собственные клетки начинают восприниматься как чужеродные, к ним образуются специфические антитела, которые их разрушают. При аутоиммунном гастрите антитела могут образовываться как к париетальным клеткам слизистой оболочки желудка, так и к самому фактору Касла.
- Рак желудка. Это опухолевое заболевание, в процессе которого происходит неконтролируемый рост и размножение опухолевых клеток, что приводит к постепенному разрушению и вытеснению париетальных клеток слизистой оболочки.
- Удаление желудка. Лечение некоторых заболеваний (прободной язвы, рака) заключается в частичном или полном удалении желудка, что приводит к уменьшению либо полному исчезновению париетальных клеток и, следовательно, к уменьшению количества образующегося внутреннего фактора Касла.
- Врожденный дефицит внутреннего фактора Касла. Данное заболевание передается по наследству и характеризуется дефектом гена, ответственного за образование этого фактора, что приводит к нарушению его секреции железами желудка.
Поражение тонкого кишечника
Всасывание витамина В12 происходит в тощей кишке. Различные повреждения данного отдела тонкого кишечника могут привести к нарушению процессов всасывания в нем.
Причинами поражения тощей кишки могут быть:
- Воспалительные заболевания (энтериты). Воспалению тонкого кишечника могут способствовать инфекции желудочно-кишечной системы, пищевые отравления, различные аллергии. При длительном течении воспалительных процессов происходит атрофия клеток слизистой оболочки кишечника, что делает невозможным всасывание кобаламина.
- Опухоли. Опухоли кишечника, по описанному ранее механизму, могут приводить к разрушению его слизистой оболочки.
- Удаление тонкой кишки (из-за опухоли или по другой причине).
Паразитарные инфекции
Исследованиями последних лет установлено, что более чем у 90% населения в кишечнике обитают различные паразиты (глисты). Им, как любым живым организмам, для роста и развития требуются определенные питательные вещества, в том числе и витамины. Некоторые глисты (например, широкий ланцет, вызывающий развитие дифиллоботриоза) могут достигать огромных размеров, в результате чего практически весь витамин В12, поступающий с пищей, не всасывается, а потребляется паразитом.
Повышенное использование витамина В12 в организме
Как упоминалось ранее, взрослому человеку необходимо всего лишь 3 – 5 мкг кобаламина в сутки. Однако при определенных условиях и заболеваниях потребность в данном витамине может значительно увеличиваться.
Причинами усиленного использования витамина В12 в организме могут быть:
- Беременность. В развивающемся плоде процессы роста и деления клеток происходят максимально интенсивно, что увеличивает потребность матери в витамине В12 в несколько раз.
- Гипертиреоз. Данное заболевание характеризуется увеличенным образованием и поступлением в кровоток гормонов щитовидной железы (трийодтиронина и тироксина). Это приводит к повышению обмена веществ в организме, что характеризуется усилением процессов клеточного деления во многих органах и требует больших количеств кобаламина.
- Злокачественные опухоли. Злокачественный процесс характеризуется неконтролируемым и непрерывным размножением опухолевой клетки, в результате чего образуется множество ее копий. При массивных опухолях большая часть кобаламина может потребляться опухолевой тканью, в результате чего другие органы будут испытывать недостаток в данном витамине.
Наследственные заболевания, нарушающие обмен витамина В12
Это довольно большая группа патологических состояний, характеризующаяся нарушением образования определенных веществ, которые в норме обеспечивают всасывание и утилизацию кобаламина в организме.
Нарушение обмена витамина В12 может быть обусловлено:
- Наследственным дефицитом транскобаламина II. Заболевание наследуется по аутосомно-рецессивному типу, то есть ребенок будет болеть только в том случае, если оба родителя страдали данным заболеванием (либо являлись его бессимптомными носителями). Характеризуется уменьшением образования или полным отсутствием транскобаламина II в организме. В этом случае количество витамина В12 в крови нормальное или даже увеличенное, однако он не может попасть в клетки организма, в результате чего развивается клиническая картина В12 дефицитной анемии.
- Синдромом Имерслунд-Гресбека. Данное заболевание также передается по аутосомно-рецессивному типу и характеризуется нарушением всасывания витамина В12 в кишечнике. Механизм этого процесса окончательно не установлен, так как секреция и взаимодействие внутреннего фактора Касла с кобаламином происходят нормально, и никаких органических поражений тонкого кишечника не наблюдается. Предполагается нарушение транспортных систем в клетках слизистой оболочки тощей кишки.
- Нарушением использования витамина В12 в клетках. Как говорилось ранее, в клетках организма кобаламин превращается в метил-кобаламин и дезоксиаденозилкобаламин. Эти процессы требуют наличия определенных веществ (ферментов), при отсутствии которых использование витамина В12 клетками становится невозможным.
Симптомы В12 дефицитной анемии

Заболевание развивается медленно и в начальных стадиях характеризуется неспецифическими симптомами – слабостью, повышенной утомляемостью. С течением времени состояние пациента ухудшается, а проявления дефицита витамина В12 становятся более явными.
Основные клинические проявления В12 дефицитной анемии обусловлены:
- нарушением образования клеток крови;
- поражением пищеварительной системы;
- поражением нервной системы.
Нарушение образования клеток крови
В результате нарушения процесса кроветворения в циркулирующей крови снижается количество эритроцитов. Это ухудшает транспорт газов в организме и приводит к кислородному голоданию всех тканей и органов.
Нарушение кроветворения проявляется:
- Бледностью и желтушностью кожи и слизистых оболочек. Розоватый цвет кожи и слизистых оболочек обусловлен белково-пигментным комплексом – гемоглобином, входящим в состав эритроцитов. При В12 дефицитной анемии бледность развивается постепенно, усиливаясь в течение нескольких месяцев. Кроме того, из-за усиленного разрушения эритроцитов (происходящего в костном мозге и в селезенке), в кровь выделяется большое количество пигмента билирубина, который придает коже и слизистым оболочкам желтоватый оттенок.
- Учащенным сердцебиением. Если организм испытывает недостаток в кислороде – активируются определенные защитные реакции, одной из которых является увеличение частоты сердечных сокращений (ЧСС). Это приводит к увеличению объема крови, проходящей через каждый орган за единицу времени, что улучшает доставку кислорода.
- Болями в сердце. Увеличение частоты сердечных сокращений улучшает доставку кислорода ко всем органам. Однако само сердце при этом выполняет большую работу и получает меньше кислорода, что может привести к появлению колющих болей в груди, которые могут распространяться в область левого плеча и живота.
- Непереносимостью физических нагрузок. При физических нагрузках увеличивается потребность мышц в энергии, которая образуется только при достаточном количестве поступающего кислорода. В нормальных условиях эти потребность восполняются за счет увеличения частоты сердечных сокращений. Однако при В12 дефицитной анемии ЧСС и так увеличена, что усугубляется нарушенной транспортной функцией эритроцитов, в результате чего физические нагрузки различной интенсивности приводят к быстрой утомляемости, появлению чувства нехватки воздуха, головокружениям или потере сознания.
- Головокружениями и частыми обмороками. Данные симптомы являются признаками выраженного дефицита эритроцитов в крови, когда головной мозг начинает испытывать недостаток в кислороде.
- Появлением «мушек» перед глазами. Это обусловлено недостаточным кровоснабжением сетчатки глаза (которая весьма чувствительна к кислородному голоданию) и стекловидного тела, что приводит к нарушению в них обмена веществ, ухудшению остроты зрения и появлению перед глазами маленьких темных пятен в форме колец, молний, ниточек и др.
- Увеличением селезенки. Большие эритроциты, попадающие в кровоток, задерживаются в капиллярах селезенки, закупоривая их. Это приводит к скоплению большого количества клеток крови в органе и увеличению его в размерах.
Поражение пищеварительной системы
Поражение желудочно-кишечной системы является наиболее ранним признаком дефицита витамина В12 в организме, что обусловлено интенсивным клеточным делением в слизистых оболочках полости рта, желудка, кишечника. При нарушении данных процессов быстро развиваются атрофические изменения и нарушение функции органов.
Поражение пищеварительной системы может проявляться:
- Нарушением пищеварения. Процесс пищеварения полностью зависит от нормального функционирования слизистых оболочек полости рта, желудка и кишечника. В них располагается множество желез, выделяющих особые пищеварительные соки, которые способствуют переработке пищевых продуктов. При недостаточности данных соков пища не проходит должной обработки, в результате чего нарушаются процессы всасывания питательных веществ, витаминов, микроэлементов.
- Неустойчивым стулом. В результате нарушения процессов пищеварения пища может дольше задерживаться в желудке или в кишечнике, приводя к вздутию живота, изжоге, запорам, которые могут чередоваться с диареей (поносом).
- Снижением аппетита. Появляется в результате снижения секреции желудочного сока атрофированной слизистой оболочкой желудка.
- Снижением массы тела. Является результатом снижения аппетита и нарушения пищеварения.
- Изменением цвета и формы языка. Поверхность языка образована огромным множеством мелких ворсинок, называемых сосочками. При В12 дефицитной анемии происходит атрофия слизистой оболочки языка, то есть постепенное уменьшение и исчезновение всех сосочков. В результате язык становится гладким, ярко-малинового цвета.
- Нарушением вкуса. Человек чувствует вкус различных продуктов благодаря наличию множества вкусовых рецепторов, расположенных в слизистой оболочке языка (преимущественно в сосочках). Следствием ее поражения является снижение или полная утрата вкусовых ощущений. Кроме того, у человека может появляться различные вкусовые отклонения – он может испытывать отвращение к различным продуктам питания (например, к мясу, рыбным изделиям и т. д.).
- Частыми инфекциями ротовой полости. Слизистая оболочка ротовой полости играет важную защитную роль, предотвращая рост и развитие патогенной микрофлоры. При ее атрофии увеличивается частота инфекционных заболеваний полости рта, может развиваться глоссит (воспаление языка), гингивит (воспаление десен).
- Болью и жжением в полости рта. Возникает в результате атрофических изменений слизистой оболочки и поражения нервных окончаний ротовой полости.
- Болью в животе после еды. Нормальная слизистая оболочка желудка выполняет защитную функцию, предохраняя желудок от агрессивного воздействия пищевых продуктов. При нарушении процессов клеточного деления повышается риск ее воспаления (развития гастрита) и образования язв, что может проявляться режущими болями в животе, усиливающимися после приема пищи (особенно острой, грубой, плохо обработанной).
Стоит отметить, что большинство из перечисленных симптомов неспецифичны и могут проявляться при других заболеваниях, поэтому их стоит оценивать только в комплексе с другими проявлениями В12 дефицитной анемии.
Поражение нервной системы
Поражения нервной системы при дефиците витамина В12 обусловлены участием кобаламина в образовании миелиновых оболочек, которые являются составной частью большинства нервных волокон организма и обеспечивают передачу нервного импульса по ним. При нарушении образования миелина происходит повреждение и склероз (замещение рубцовой тканью) нервных клеток и нервных волокон, что может проявляться всевозможными неврологическими нарушениями (в зависимости от того, какие нервы были поражены).
Наиболее опасным считается поражение головного мозга, являющегося центром всей нервной системы, и спинного мозга, который представляет собой совокупность нервных волокон, идущих от головного мозга ко всем органам и тканям организма и в обратном направлении.
Симптомами поражения нервной системы при В12 дефицитной анемии могут быть:
- Нарушение чувствительности. Одно из первых проявлений поражения нервной системы. Чувствительность может нарушаться в любых участках тела, однако это наиболее заметно, когда поражаются пальцы рук, запястья. Больной человек может не ощущать прикосновение, тепло, холод и даже боль. Чаще поражение носит двусторонний характер и без соответствующего лечения постоянно прогрессирует.
- Парестезии. Один из видов нарушения чувствительности, характеризующийся онемением, покалыванием, «ползанием мурашек» в определенной области кожи.
- Атаксия. Данный термин подразумевает нарушение согласованной работы мышц. Это может проявляться нарушением равновесия, неуклюжестью и несогласованностью движений рук и ног, туловища.
- Снижение мышечной силы. Чтобы мышца сокращалась, необходимо поступление достаточного количества нервных импульсов из головного мозга. Кроме того, даже в покое головной мозг постоянно посылает к мышцам небольшое количество импульсов, что обеспечивает поддержание мышечного тонуса. При поражении спинного мозга импульсы не могут достичь мышц, в результате чего происходит их атрофия (уменьшение массы и размеров). При отсутствии своевременного лечения данное состояние может прогрессировать и привести к параличу – полной утрате способности выполнять произвольные движения.
- Нарушение процессов дефекации и мочеиспускания. Развиваются при длительном недостатке витамина В12 в организме и могут проявляться задержкой или, наоборот, недержанием кала и/или мочи (в зависимости от того, какие участки спинного мозга поражены).
- Нарушения психики. Является одним из наиболее неблагоприятных (в прогностическом плане) симптомов заболевания и характеризуется поражением коры головного мозга. Выраженность психических расстройств варьирует в зависимости от пораженного участка и выраженности склеротических изменений и может проявляться как бессонницей, незначительным ухудшением памяти или легкой депрессией, так и тяжелыми психозами, судорогами, галлюцинациями.
При В12 дефицитной анемии неврологические симптомы появляются в определенной последовательности — вначале происходит симметричное поражение ног, затем живота и туловища. В более поздних стадиях в процесс вовлекаются пальцы рук, плечевой пояс, шея, может поражаться область лица и головы. В последнюю очередь появляются психические расстройства.
Диагностика В12 дефицитной анемии
Диагностикой и лечением В12 дефицитной анемии занимается врач-гематолог, который, при необходимости, может привлекать других специалистов (гастролога, невролога).
Процесс диагностики В12 дефицитной анемии включает:
- общий анализ крови;
- биохимический анализ крови;
- пункцию костного мозга;
- установление причины В12 дефицитной анемии.
Общий анализ крови
Целью данного исследования является определение клеточного состава периферической крови, а также детальное исследование полученного материала под микроскопом, что позволяет выявить отклонения в размерах, форме или составе клеток в крови.
Забор крови для анализа
Процедуру производит медсестра в специальном процедурном кабинете. Кровь берется утром, натощак. За 2 – 3 часа до сдачи анализа рекомендуется исключить курение и тяжелые физические нагрузки.
Для клинического анализа кровь могут брать:
- Из пальца (капиллярную). Капиллярную кровь берут из кончика пальца руки. Вначале с целью дезинфекции медсестра обрабатывает палец пациента ватой, смоченной в 70% спирте. После этого скарификатором (тонкой одноразовой стерильной пластинкой, которая заточена с обеих сторон) делается прокол кожи на глубину 2 – 4 мм. Первая появившаяся капля крови удаляется ватным тампоном, после чего в специальную промаркированную стеклянную трубку набирается несколько миллилитров крови. По окончании процедуры к месту прокола на 2 – 3 минуты прикладывается ватный тампон, пропитанный спиртом.
- Из вены. Кровь обычно берут из вен локтевой области, которые наиболее хорошо определяются под кожей. Если определить расположение вены в данной области не удается, кровь можно взять из любой другой вены. Пациент садится на стул и кладет руку на его спинку таким образом, чтобы локтевой сустав оказался в разогнутом состоянии. Медсестра накладывает тугой жгут на область плеча и определяет местоположение вены. Локтевая область дважды обрабатывается ватой, смоченной в спирте, после чего одноразовой стерильной иглой, присоединенной к шприцу, производится прокол вены и забор нескольких миллилитров крови. Потом игла извлекается, а к месту прокола на 5 – 7 минут прикладывается пропитанный спиртом ватный тампон.
Микроскопическое исследование
Для определения формы и размеров различных клеток в исследуемой крови, одну или несколько капель переносят на специально стекло, окрашивают специальными красителями и исследуют в световом микроскопе. Таким же способом можно подсчитать примерное содержание клеток в исследуемом образце.
Нормальный размер эритроцитов – 7,5 – 8,3 мкм. При микроскопическом исследовании они определяются как клетки красного цвета, одинаковых размеров, кольцевидной формы, не содержащие ядра или других включений.
При дефиците витамина В12 в костном мозге образуются мегалобласты. Часть из них сразу разрушается, а остальные поступают в кровоток.
При В12 дефицитной анемии микроскопическая картина периферической крови характеризуется:
- Пойкилоцитозом – наличием эритроцитов различной формы.
- Анизоцитозом – наличием эритроцитов различных размеров.
- Макроцитозом – наличием эритроцитов, увеличенных в диаметре (более 8,5мкм).
- Внутриклеточными включениями – в эритроцитах определяются остатки разрушенного ядра и некоторые органеллы.
- Гиперхромией – эритроциты имеют более выраженную окраску, чем в норме (что обусловлено большой концентрацией гемоглобина и отсутствием сужения в центре клетки).
Исследование в гематологическом анализаторе
В большинстве современных лаборатории имеются специальные гематологические анализаторы, которые позволяют в довольно короткие сроки получить точную информацию о количестве клеточных элементов в исследуемой крови, а также некоторые другие показатели.
Изменения в общем анализе крови при В12 дефицитной анемии
| Исследуемый показатель | Что обозначает | Норма | Изменения при В12 дефицитной анемии |
|
Средний объем эритроцита |
Данный показатель более точно отображает средние размеры эритроцитов в исследуемой крови, так как оценивает большее количество клеток, чем то, которое исследует врач при обычной микроскопии. | 75 – 100 кубических микрометров (мкм3). | 100 – 110 мкм3 и более. |
| Концентрация эритроцитов (RBC) |
В результате усиленного разрушения эритроцитов в костном мозге и в селезенке количество их в периферической крови будет снижено. | Мужчины (М): 4,0 – 5,0 х 1012/л. |
Менее 4,0 х 1012/л. |
| Женщины (Ж): 3,5 – 4,7 х 1012/л. |
Менее 3,5 х 1012/л. | ||
| Концентрация тромбоцитов (PLT) |
При в12 дефицитной анемии нарушается образование не только эритроцитов, но и остальных клеток крови. | 180 – 320 х 109/л. | Менее 180 х 109/л. |
| Концентрация лейкоцитов (WBC) |
Лейкоциты выполняют защитную функцию. В норме их концентрация увеличивается при различных инфекциях. При дефиците витамина В12 образование лейкоцитов нарушается, и их количество в крови может быть уменьшено даже при тяжелых инфекционных заболеваниях. | 4,0 – 9,0 х 109/л. | Менее 4,0 х 109/л. |
| Концентрация ретикулоцитов (RET) |
При дефиците витамина В12 кроветворение в костном мозге неэффективно, клетки не созревают до стадии ретикулоцитов, в результате чего их количество в крови будет снижено. | М: 0,24 – 1,7%. | Может быть в несколько раз ниже нормы. |
| Ж: 0,12 – 2,05%. | |||
| Общий уровень гемоглобина (HGB) |
При В12 дефицитной анемии количество эритроцитов снижено, однако концентрация гемоглобина в каждом из них увеличена, что может поддерживать общий уровень гемоглобина в крови на нормальном уровне. | М: 130 – 170 г/л. | Может быть нормальным или слегка сниженным. |
| Ж: 120 – 150 г/л. | |||
| Средняя концентрация гемоглобина в эритроцитах (MCHC) |
Дает более точную информацию о насыщении эритроцитов гемоглобином, так как не учитывается объем плазмы, в которой находятся клетки крови. | 320 – 360 г/л. | Более 400 г/л. |
| Среднее содержание гемоглобина в одном эритроците (MCH) |
Определяется посредством деления уровня гемоглобина на количество эритроцитов (вычисления производятся гематологическим анализатором автоматически). | 27 – 33 пикограмм (пг). | Более 35 пг. |
| Гематокрит (Hct) |
Данный показатель выражается в процентах и определяет долю клеточных элементов в общем объеме крови. | М: 42 – 50%. | Снижен из-за значительного уменьшения количества эритроцитов в крови. |
| Ж: 38 – 47%. | |||
| Цветовой показатель (ЦП) |
Характеризует степень насыщения эритроцитов гемоглобином — чем его больше, тем выше будет цветовой показатель. | 0,85 – 1,05. | Более 1,1. |
| Скорость оседания эритроцитов (СОЭ) |
Так как наружные поверхности эритроцитов заряжены отрицательно, они отталкиваются друг от друга, что препятствует их склеиванию. Суть определения СОЭ заключается в склеивании эритроцитов в крови и оседании их на дно пробирки под действием силы тяжести. Скорость данного процесса зависит от концентрации клеток в крови — чем их меньше, тем слабее они отталкиваются друг от друга, и тем быстрее будет СОЭ. | М: 3 – 10 мм/час. | Более 15 мм/час. |
| Ж: 5 – 15 мм/час. | Более 20 мм/час. |
Биохимический анализ крови
Данное исследование позволяет определить наличие растворенных в крови веществ (белков, ферментов, витаминов и других). Практически любое заболевание (в том числе и В12 дефицитная анемия) характеризуется увеличением или снижением концентрации различных веществ в крови, что позволяет судить о выраженности патологического процесса и степени повреждения внутренних органов, а также контролировать эффективность проводимого лечения.
Кровь для биохимического исследования берется из вены (подготовка пациента и методика забора материала были описаны выше), после чего в специальной пробирке направляется в лабораторию.
Изменения биохимического анализа крови при В12 дефицитной анемии
| Исследуемый показатель | Что обозначает | Норма | Изменения при В12 дефицитной анемии |
| Содержание кобаламина в крови | Обычно заболевание характеризуется снижением уровня витамина В12. Однако в некоторых случаях (при нарушениях обмена кобаламина в организме) концентрация данного витамина в крови будет увеличена, несмотря на клинические проявления В12 дефицитной анемии, поэтому данный показатель необходимо оценивать, учитывая данные других анализов. | 200 – 900 пг/мл. |
|
| Уровень метилмалоновой кислоты в крови | Данное вещество участвует в процессах жизнедеятельности клеток. Для его использования необходимо наличие активной формы кобаламина (ДА-В12), в отсутствии которой метилмалоновая кислота не может использоваться клетками организма, в результате чего ее концентрация в крови повышается. | 73 – 270 нмоль/мл. | Значительно выше нормы. |
| Уровень гомоцистеина в крови | Гомоцистеин – аминокислота, которая участвует в образовании вещества метионина, входящего в состав миелиновых оболочек нервных клеток. Этот процесс также требует присутствия активной формы кобаламина (метил-В12). При его недостатке количество свободного гомоцистеина в плазме крови повышается. | 5 – 16 мкмоль/л. | Значительно выше нормы. |
| Концентрация билирубина (несвязанной фракции). | Уровень несвязанного билирубина может повышаться при массивном разрушении мегалобластов в красном костном мозге и в селезенке. | 4,5 – 17,1 мкмоль/л. | Может быть увеличен в несколько раз, особенно при длительном течении заболевания. |
| Концентрация сывороточного железа | При интенсивном разрушении эритроцитов и их предшественников из них выделяется большое количество железа. В нормальных условиях оно используется для синтеза новых эритроцитов, однако при В12 дефицитной анемии данный процесс нарушен, в результате чего концентрация железа в крови может повышаться. | М: 17,9 – 22,5 мкмоль/л. | Может повышаться при длительном течении заболевания. |
| Ж: 14,3 – 17,9 мкмоль/л. |
Пункция костного мозга
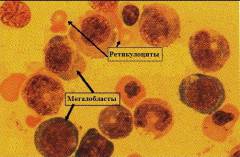
Обычно костный мозг берут из грудины. Процедура выполняется только специально обученным врачом в условиях стерильной операционной. Место пункции дважды обрабатывается 70% спиртовым или йодным раствором. После этого специальным шприцем с полой иглой, установленной под прямым углом к грудине, прокалывают кожу и надкостницу и продвигают иглу на 1 – 2 см в вещество кости. Убедившись, что игла находится в полости кости, производится забор нескольких миллилитров костного мозга, который имеет вид густого, желтовато-красно вещества. Полученный материал направляется в лабораторию для микроскопического исследования.
При В12 дефицитной анемии в костном мозге определяется увеличение клеточных элементов (преимущественно за счет предшественников эритроцитов). Клетки увеличены в размерах, содержат слишком большое количество гемоглобина (по сравнению с нормой). Также отмечается нарушение созревания мегакариоцитов (предшественников тромбоцитов) и промиелоцитов (предшественников лейкоцитов).
Установление причины В12 дефицитной анемии
При подтверждении диагноза не менее важным моментом является выявление его причины, так как ее устранение (если оно возможно) может привести к излечению пациента.
Для выявления причины В12 дефицитной анемии используется:
- Оценка рациона пациента. Уточняется, как питается пациент, потребляет ли достаточное количество животных продуктов, как часто употребляет алкогольные напитки.
- Фиброгастродуоденоскопия (ФГДС). Метод исследования внутренней поверхности желудка и начального отдела кишечника посредством введения специальной трубки с видеокамерой на конце. Позволяет выявить атрофию слизистой, наличие рака или язвы.
- Биопсия слизистой оболочки желудка и/или кишечника. Подразумевает прижизненное взятие кусочка ткани слизистой оболочки и исследование его клеточного строения. Позволяет выявить атрофические процессы, а также различить доброкачественные и злокачественные опухоли.
- Анализ кала на яйца гельминтов (глистов). С помощью данного метода можно установить само наличие паразитов, а также определить их чувствительность к различным противопаразитарным препаратам, что позволит назначить максимально эффективное лечение.
- Определение специфических антител. В крови могут определяться антитела к внутреннему фактору Касла либо к париетальным клеткам слизистой оболочки, которые его продуцируют.
- Оценка функции печени. Определяется уровень печеночных ферментов в крови, проводится ультразвуковое исследование (УЗИ) органа.
- Определение уровня гормонов щитовидной железы в крови. При их увеличении потребление кобаламина организмом возрастает, что со временем может привести к развитию В12 дефицитной анемии.
Лечение В12 дефицитной анемии
Лечение В12 дефицитной анемии медикаментами
Суть медикаментозной терапии данного недуга заключается в ведении витамина В12 извне. Поступив в организм, кобаламин быстро включается в процессы кроветворения, что приводит к устранению симптомов анемии в довольно короткие сроки.
Показаниями к началу лечения витамином В12 являются:
- подтвержденный (лабораторно) диагноз В12 дефицитной анемии;
- концентрация кобаламина в плазме крови менее 220 пг/мл;
- выраженная клиническая картина анемии (даже при более высокой концентрации кобаламина в крови).
Способ применения и дозировка
В большинстве случаев препарат витамина В12 (цианокобаламин) вводится внутримышечно. Прием внутрь (в виде таблеток) допускается, если достоверно установлено, что причиной дефицита витамина является недостаточное его количество в пище, а общее состояние организма не критично (легкое снижение показателей крови, отсутствие неврологических проявлений).
Лечение начинают с внутримышечного введения 500 – 1000 мкг цианокобаламина 1 раз в сутки. Минимальный курс лечения – 6 недель, после чего переходят на поддерживающую терапию. Дозировка препарата на данном этапе лечения зависит от причины и выраженности дефицита витамина В12 в организме. Обычно назначается внутримышечное введение 200 – 400 мкг цианокобаламина 2 – 4 раза в месяц. Поддерживающая терапия может проводиться пожизненно.
Контроль эффективности лечения
В период лечения рекомендуется сдавать общий анализ крови 2 – 3 раза в неделю.
Первым признаком эффективности терапии, а также достоверным подтверждением диагноза является «ретикулоцитарный криз», возникающий на 3 – 5 день после начала введения витамина В12 в организм. Данное состояние характеризующийся резким увеличением количества ретикулоцитов в крови (в 10 – 20 раз), что свидетельствует о начале нормального кроветворения в косном мозге.
В течение 1 – 1,5 месяцев происходит постепенная нормализация состава периферической крови, ослабление неврологических проявлений, нормализация работы пищеварительной системы, что свидетельствует об эффективности проводимого лечения. На этапе поддерживающей терапии рекомендуется ежемесячное проведение общего анализа крови и определение уровня кобаламина в крови.
Переливание крови
Суть метода заключается в переливании пациенту крови или, чаще, отдельной эритроцитарной массы. Переливание крови является опасной процедурой, поэтому данный метод используется только при угрожающих жизни состояниях.
Показаниями к переливанию эритроцитов при В12 дефицитной анемии являются:
- Тяжелая анемия – уровень гемоглобина менее 70 г/л;
- Анемическая кома – потеря сознания, обусловленная выраженным нарушением доставки кислорода к мозгу.
Перед началом процедуры проводятся тесты на совместимость крови донора и реципиента (того, кому переливается кровь), после чего в одну из больших вен организма вводится катетер, через который переливается эритроцитарная масса. Так как данная процедура сопряжена с риском развития множества побочных реакций, в течение всего периода переливания крови в палате должен присутствовать врач.
При подтвержденном диагнозе В12 дефицитной анемии одновременно с переливанием донорских эритроцитов начинают внутримышечное введение витамина В12. Переливание крови следует прекратить как можно раньше, как только устранено угрожающее жизни состояние.
Диета при В12 дефицитной анемии
Как говорилось ранее, суточная потребность в витамине В12 составляет 3 – 5 мкг, а запасы данного витамина в печени настолько велики, что даже при прекращении поступления кобаламина в организм признаки его дефицита появятся не ранее, чем через 2 – 3 года. Тем не менее, диета играет определенную роль в процессе лечения заболевания, особенно когда запасы витаминов В12 в организме снижаются.
Причинами снижения запасов витамина В12 в организме могут быть:
- Заболевания печени. Такие заболевания как цирроз и рак печени, приводят к уменьшению количества нормальных клеток органа, и замещению их соединительно тканью, которая неспособна депонировать витамин В12. В результате запасы данного витамина в организме снижаются, а при нарушении его поступления признаки заболевания могут появляться в более ранние сроки.
- Беременность. В данном случае матери необходимо обеспечивать витамином В12 не только свой, но и быстро развивающийся организм ребенка, поэтому суточная потребность в витамине В12 может увеличиваться на 50%, а в случае многоплодной беременности – еще больше. В нормальных условиях (при отсутствии заболеваний печени) запасов кобаламина в организме достаточно, чтобы покрыть потребности матери и плода в данном веществе. Однако при частых беременностях запасы кобаламина могут истощаться, особенно если у матери имеются какие-либо заболевания печени, поэтому беременным женщинам особенно важно потреблять достаточное количество этого витамина с пищей.
Содержание витамина В12 в некоторых продуктах питания
| Наименование продукта | Содержание витамина В12 в 100г продукта |
| Печень говяжья | 60 мкг |
| Печень свиная | 30 мкг |
| Печень куриная | 16 мкг |
| Скумбрия | 12 мкг |
| Мясо кролика | 4,3 мкг |
| Говядина | 2,6 мкг |
| Морской окунь | 2,4 мкг |
| Свинина | 2 мкг |
| Треска | 1,6 мкг |
| Карп | 1,5 мкг |
| Куриное яйцо | 0,5 мкг |
| Сметана | до 0,4 мкг |
Прогноз при В12 дефицитной анемии

С тех пор как в лечении В12 дефицитной анемии начали применять внутримышечное введение цианокобаламина прогноз для жизни и здоровья пациентов значительно улучшился. При соблюдении режима приема препарата люди могут доживать до глубокой старости без каких-либо проявлений заболевания.
Прогноз при В12 дефицитной анемии
| Благоприятные прогностические признаки | Неблагоприятные прогностические признаки |
|
|
Также:
Витамин В12-дефицитная анемия, мегалобластная анемия, пернициозная анемия, болезнь Аддисона-Бирмера
Версия: Клинические рекомендации РФ 2021 (Россия)
Категории МКБ:
Витамин-b12-дефицитная анемия (D51)
Разделы медицины:
Эндокринология, Эндокринология детская
Общая информация
Краткое описание
Разработчик клинической рекомендации
- Национальное гематологическое общество
- Национальное общество детских гематологов, онкологов
Одобрено Научно-практическим Советом Минздрава РФ
Витамин В12 дефицитная анемия
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем:D51.0, D51.1, D51.3, D51.8, D51.9
Год утверждения (частота пересмотра):2021
Возрастная категория:Взрослые,Дети
Год окончания действия:2023
ID:536
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
В12-дефицитная анемия (мегалобластная анемия, пернициозная анемия, болезнь Аддисона-Бирмера), характеризуется прогрессирующей гиперхромной, макроцитарной анемией, гиперсегментацией ядер нейтрофилов, мегалобластным эритропоэзом и морфологическими аномалиями других ростков кроветворения в костном мозге; в отличие от других анемий, В12-дефицитная анемия часто ассоциируется с развитием патологических психо-неврологических симптомов (фуникулярный миелоз) [1–4].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статической класификации болезней и проблем, связанных со здоровьем
D51.0 Витамин-B12-дефицитная анемия вследствие дефицита внутреннего фактора
D51.1 Витамин-B12-дефицитная анемия вследствие избирательного нарушения всасывания витамина B12 с протеинурией
D51.3 Другие витамин-B12-дефицитные анемии, связанные с питанием
D51.8 Другие витамин-B12-дефицитные анемии
D51.9 Витамин-B12-дефицитная анемия неуточненная
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 500 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
В12-дефицитные анемии разделяют на:
- приобретенные
- наследственные (врожденные)
Среди приобретенных В12-дефицитных анемий выделяют первичную форму, обусловленную наличием аутоантител к внутреннему фактору Кастла (пернициозная анемия), и вторичные, ассоциированные с одним или несколькими факторами риска развития В12-дефицита, например, наличие врожденной гемолитической анемии и строгая веганская диета. Первичная форма, обусловленная аутоиммунным характером дефицита В12, зачастую осложняет течение аутоиммунного тиреоидита и сахарного диабета 1 типа. Наследственные формы В12-дефицита описаны у детей с врожденными генетическими дефектами, приводящими к нарушению транспорта витамина В12 [3,4,8–10,16].
Этиология и патогенез
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Дефицит витамина В12 приводит к нарушению синтеза тимидина и метаболизма жирных кислот, что, в свою очередь, имеет следствием нарушение синтеза ДНК, накопление токсичного для нервных клеток метаболита — метилмалоновой кислоты, и уменьшению содержания миелина в нервных волокнах. Клиническими проявлениями В12-дефицита служат многочисленные нарушения в кроветворной, нервной и эндокринной системе, атрофия слизистых оболочек желудочно-кишечного тракта и развитие характерной клиники фуникулярного миелоза.
Основная причина развития дефицита витамина В12 – нарушение его всасывания в кишечнике. Париетальные клетки тела и дна желудка секретируют белок, т.н. «внутренний фактор Кастла» (открыт W.Castle в 1930), необходимый для всасывания витамина В12 (кобаламин, «внешний фактор»). Образование стойкого комплекса «кобаламин — внутренний фактор Кастла» начинается в щелочной среде 12-перстной кишки, далее всасывание витамина В12 происходит в тонком кишечнике, в основном, в подвздошной кишке, где локализуется кубулин — специфический белок-рецептор для «внутреннего фактора». В процессе всасывания «комплекс» распадается, витамин В12 проникает через стенку тонкой кишки в кровоток, где связывается с транскобаламином, который доставляет его клеткам-потребителям, в том числе клеткам костного мозга и печени.
К нарушению всасывания витамина В12 могут приводить следующие патологические процессы:
— снижение продукции или отсутствие «внутреннего фактора Кастла» вследствие наличия аутоантител к нему или к париетальным клеткам желудка, другие атрофические гастриты, резекция желудка;
— заболевания тонкой кишки (хронические энтериты с синдромом нарушенного всасывания, опухоли, в том числе лимфомы);
— конкурентное поглощение (дивертикулез с изменением флоры, дифиллоботриоз, синдром «слепой петли» при анастомозе тонкой кишки);
— заболевания поджелудочной железы, способствующие повышению кислотности кишечного содержимого (опухоль с образованием гастрина, синдром Золлингера- Эллисона),
— длительный прием некоторых лекарственных препаратов (ингибиторы протонного насоса [группаА02ВС по АТХ классификации], метформин** и др.) [5,6]
Алиментарный дефицит витамина В12 может развиться у лиц, придерживающихся вегетарианской или веганской диеты. Все вышеперечисленные факторы-риска развития дефицита кобаламина необходимо учитывать у пациентов, имеющих наследственные формы гемолитических анемий.
У детей основными причинами дефицита В12 являются:
— снижение поступления витамина В12 с питанием (у грудных детей, чьи матери имеют дефицит витамина В12 или соблюдают строгую вегетарианскую диету [2,7]
— снижение всасывания (дефицит внутреннего фактора Кастла, резекция желудка, нарушение всасывания в подвздошной кишке вследствие врожденных болезней тонкого кишечника, резекции кишечника)
— повышенные потери цианокобаламина в кишечнике (глистная инвазия, синдром слепой кишки)
— врожденные генетические дефекты, приводящие к нарушению транспорта витамина В12 [8–10].
Эпидемиология
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
В12-дефицитная анемия является одной из самых распространенных анемий, частота выявления которой варьирует в разных возрастных группах: после 60 лет дефицит витамина В12 обнаруживают у одного из 50 человек, а после 70 лет — у каждого 15-ого. В соответствии с этим, в некоторых странах концентрацию витамина В12 в сыворотке крови определяют пожилым лицам в порядке диспансеризации [11–15].
Клиническая картина
Cимптомы, течение
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Основные клинические проявления В12-дефицитной анемии включают постепенно нарастающую слабость, апатию, непереносимость физических нагрузок, сердцебиение, боли в сердце, диспепсические расстройства, а также — слабость в ногах и парестезии, мигрирующие боли, «онемение» конечностей и постепенную утрату чувствительности пальцев рук. Типичны — одутловатость лица и амимичность, бледно-желтушный цвет кожи, сглаженность сосочков языка («малиновый лаковый язык»). У молодых — часто раннее поседение волос. Нередко отмечается субфебрильная температура и увеличение размеров селезенки, которые зачастую приводят к диагностическим ошибкам. При отсутствии своевременной диагностики и лечения В12-дефицита развиваются нарушение поверхностной и глубокой мышечной чувствительности, снижение слуха, зрения, арефлексия, в запущенных случаях — нарушение функции тазовых органов и выраженные когнитивные нарушения. В тяжелых случаях В12- дефицита доминирует поражение периферической нервной системы (фуникулярный миелоз): атаксия, гипорефлексия, появление патологических знаков — рефлекс Бабинского [1–4,17]
Диагностика
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза: клинико-гематологической картины заболевания и наличии лабораторных критериев дефицита В-12.
Для В12-дефицитной анемии характерно сочетание гематологических нарушений с патологией желудочно-кишечного тракта и наличием симптомов поражения нервной системы.
Несмотря на значительную вариабельность клинических проявлений дефицита кобаламина, комплексный анализ анамнестических данных и клинических симптомов позволяет предположить диагноз В12-дефицитной анемии и минимизирует выбор лабораторных исследований необходимых для верификации диагноза.
2.1 Жалобы и анамнез
См. раздел «Клиническая картина»
2.2 Физикальное обследование
См. раздел «Клиническая картина»
2.3 Лабораторные диагностические исследования
Основными лабораторными критериями диагноза В12-дефицитной анемии являются:
- В общем (клиническом) анализе крови:
- гиперхромия, макроцитоз, анизопойкилоцитоз;
- гиперсегментация ядер нейтрофилов;
- эритроцитопения и абсолютная ретикулоцитопения
- В анализе крови биохимическом общетерапевтическом:
- высокая активность ЛДГ;
- умеренное повышение свободного билирубина;
- низкий уровень витамина В12 в крови (менее 140 пг/мл);
- нормальный уровень фолиевой кислоты в сыворотке крови (более 5 нг/мл);
- В пунктате костного мозга:
- мегалобластический тип кроветворения;
- наличие гигантских миелоцитов, метамиелоцитов и палочкоядерных нейтрофилов.
Дифференциальная диагностика В12-дефицитной анемии проводится с другими видами макроцитарных анемий, ассоциированных с:
— дефицитом фолиевой кислоты;
— дефицитом витамина В6;
— некоторыми формами латентного гемолиза, при которых макроцитоз обусловлен увеличенным содержанием ретикулоцитов в циркуляции;
— миелодиспластическими синдромами;
— апластической анемией.
- Рекомендуется всем пациентам с подозрением на В12-дефицитную анемию проведение общего (клинического) анализа крови с определением абсолютного и относительного числа ретикулоцитов и эритроцитарных индексов (МСV, МСН, МСНС) для верификации диагноза [1,2,18].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: При В12-дефицитной анемии в общем (клиническом) анализе крови выявляется макроцитарная, гиперхромная анемия, с увеличением среднего объема эритроцитов (MCV), среднего содержания гемоглобина (MCH) в эритроцитах и выраженным анизо-пойкилоцитозом. МСНС остается в пределах референтных значений. Характерными изменениями в общем (клиническом) анализе крови являются базофильная пунктация эритроцитов, тельца Жолли и кольца Кебота в эритроцитах, наличие овалоцитов и единичных нормобластов. Абсолютное число ретикулоцитов снижено, в то время как относительное их количество может быть нормальным или повышенным. При наличии технической возможности дополнительную информацию может предоставить определение ретикулоцитарных индексов: отмечается увеличение среднего объема ретикулоцитов (макроретикулоциты), среднего содержания гемоглобина в ретикулоцитах и, зачастую, повышение фракции незрелых ретикулоцитов. Ранним признаком дефицита В12 является гиперсегментация ядер нейтрофилов, иногда нейтропения. Часто наблюдается умеренная тромбоцитопения, редко — глубокая, обычно без геморрагического синдрома [19,20].
- Рекомендуется пациентам с подозрением на В12-дефицитную анемию проведение анализа крови биохимического общетерапевтического, включающего определение общего белка, альбумина, АЛТ, АСТ, мочевины, креатинина, ЛДГ, общего билирубина, свободного билирубина, ферритина, железа сыворотки, ОЖСС, трансферрина, НТЖ, для определения функционального состояния печени, почек, поджелудочной железы [1–4,21].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
Комментарии: в анализе крови биохимическом общетерапевтическом отмечается характерное, резкое увеличение активности ЛДГ и гипербилирубинемия, в начальной стадии — неконъюгированная, при тяжелой степени анемии — за счёт обеих фракций.
При В12-дефицитной анемии показатели сывороточного железа и ферритина, как правило, высокие. Однако у пациентов с синдромом мальабсорбции может наблюдаться сочетание дефицита кобаламина и железа. В этих случаях типичная лабораторная картина В12-дефицитной анемии может нивелироваться, что препятствует своевременной диагностике заболевания и приводит к отсрочке назначения патогенетической терапии. В подобных случаях возрастает диагностическая значимость клинической картины, анамнеза, а также других диагностических маркеров (ММК, голотранскобаламин) [1–4,21].
- Рекомендуется пациентам с подозрением на В12-дефицитную анемию определение уровня витамина В12 (цианокобаламин) в крови, исследование уровня фолиевой кислоты в сыворотке крови [1–4,18,21–23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Содержание витамина В12 в сыворотке, как правило, существенно снижено. Фолаты сыворотки — в норме или повышены, но может встречаться и сочетание дефицита обоих витаминов.
В случае нормального содержания В12 и фолатов в сыворотке крови целесообразно определение голотранскобаламина сыворотки (активный В12), содержание которого в случае В12-дефицита снижено.
- Рекомендуется пациентам с подозрением на В12-дефицитную анемию и/или пациентам с глубокой макроцитарной анемией неясного генеза проведение цитологического исследования мазка костного мозга (миелограмма) для подтверждения или исключения диагноза В12-дефицитной анемии [1–4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: характерным диагностическим признаком В12-дефицитной анемии служит повышенная клеточность костного мозга и обилие мегалобластов, которые зачастую имеют причудливую форму ядра. Типичными морфологическими признаками являются также наличие гигантских миелоцитов, метамиелоцитов, палочкоядерных нейтрофилов (гранулоцитов), а также гиперсегментация ядер нейтрофилов.
- Рекомендуется пациентам при госпитализации в связи с подозрением на В12- дефицитную анемию или по поводу диагностированной В12-дефицитной анемии определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови; определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови для диагностики сопутствующей патологии [24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
2.4 Инструментальные диагностические исследования
Выявление В12-дефицитной анемии требует проведения стандартного комплекса инструментальных исследований для выяснения причины развития анемии.
-
Рекомендуется всем пациентам с подозрением или с впервые установленным диагнозом В12-дефицитной анемии проведение следующих инструментальных исследований для выяснения причины анемии и/или диагностики сопутствующей патологии [25–27]:
- эзофагастродуоденоскопия и колоноскопия – для выявления патологии желудочно-кишечного тракта, как причины нарушения всасывания витамина В12;
- рентгенография или КТ органов грудной клетки для диагностики сопутствующей патологии;
- УЗИ органов брюшной полости, забрюшинного пространства и малого таза, щитовидной железы – для диагностики сопутствующей патологии.
- ЭКГ –для диагностики нарушений внутрисердечной проводимости, для измерения электрической активности сердца.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: патология щитовидной железы, в первую очередь, аутоиммунный тиреоидит, является пре- или коморбидным состоянием при В12 -дефицитной анемии или латентном дефиците витамина В12, выявленном при определении концентрации В12 в сыворотке крови.
2.5 Иные диагностические исследования
- Рекомендуется пациентам с подозрением или с впервые установленным диагнозом В12-дефицитной анемии проведение осмотра врача-невролога для выявления и документации возможных неврологических нарушений, обусловленных дефицитом витамина В12 [1,2,17].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: при обследовании пожилых пациентов следует учитывать психо- неврологические жалобы и когнитивные нарушения, которые могут предшествовать развитию анемического синдрома [17].
Лечение
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1 Консервативное лечение»
Суточная потребность в витамине В12 составляет 2,4 мкг. Большинство пациентов с дефицитом витамина B12, манифестирующим мегалобластной анемией и/или неврологической симтоматикой (фуникулярного миелоза), имеют синдром мальабсорбции и требуют неотложного введения цианкоболамина** (витамина В12) парентерально. Отсутствие своевременной заместительной терапии может привести к развитию необратимой полиорганной недостаточности [28].
- Не рекомендуется пациентам с подозрением на В12-дефицитную анемию начинать лечение цианокобаламином** до взятия крови для проведения лабораторных исследований необходимых для верификации дефицита витамина В12 [29].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: залогом правильной и своевременной диагностики В12-дефицитной анемии является исследование лабораторных параметров, необходимых для верификации дефицита кобаламина до назначения лечения цианокобаламином**, в том числе в составе поливитаминов в комбинации с минеральными веществами (группа А11А по АТХ классификации), поливитаминов (группа А11В по АТХ классификации), витамина В1 в комбинации с витаминами В6 и/или В12 (группа А11DB про АТХ классификации), и витаминов группы В, включая их комбинации с другими препаратами (группа А11Е по АТХ классификации). Так как даже одна инъекция цианокобаламина** приводит к исчезновению диагностически значимых морфологических аномалий клеток эритроидного ряда.
- Рекомендуется всем пациентам с установленным диагнозом В12-дефицитной анемии проведение терапии цианокобаламином** в дозе 100-200 мкг/сут через день; в случае присоединения нарушения функции нервной системы – 400-500 мкг/ сут в первую неделю ежедневно, далее – с интервалами между введениями до 5-7 дней [1–4,18,30].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: лишь небольшая часть (до 10%) введенного парентерально цианокобаламина** связывается с транскобаламином и усваивается клетками; излишки препарата выводятся с мочой [30]. При В12-дефицитной анемии без явных неврологических проявлений суточная доза цианкобаламина** не превышает 200-500 мкг/ сутки.
В случае развития лекарственного аллергического дерматита введение цианокобаламина** сочетают с глюкокортикоидами (группа Н02АВ по АХТ классификации) и антигистаминными средствами системного действия (группа R06A по АТХ классификации). При повторных введениях препарата удается избежать развития нежелательных аллергических реакций путем уменьшения дозы цианокобаламина** до 100-200 мг/сутки, что не снижает эффективность терапии [1–4].
Длительность терапии цианкоболамином** определяется тяжестью В12-дефицитной анемии. После регресса анемии, лейкопении, тромбоцитопении и всех морфологических аномалий эритроцитов курс лечения цианкоболамином** продолжается еще 10-14 дней с целью создания «запасов» витамина В12 в печени [1–4].
3.2 Диагностика на этапе лечения
- Рекомендуется пациентам с В12-дефицитной анемией проводить контроль эффективности лечения с помощью мониторинга клинических показателей, общего (клинического) анализа крови, анализа крови биохимического общетерапевтического, включающего определение общего белка, альбумина, АЛТ, АСТ, мочевины, креатинина, ЛДГ, общего билирубина, свободного билирубина [1–4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: признаки улучшения состояния пациента в виде уменьшения анемических симптомов появляются после первых 3-5 инъекций цианокобаламина**. Повышение уровня гемоглобина достигается через 7-10 дней, восстановление других гематологических показателей — через 3-5 недель. Адекватность терапии можно оценить по нормализации показателя ЛДГ, развитию ретикулоцитарного криза на 5-7 дни лечения и изменениям ретикулоцитарных индексов, которые опережают развитие ретикулоцитарного криза. После начала терапии стремительно снижается средний объем и содержание гемоглобина в ретикулоцитах, а фракция незрелых ретикулоцитов резко повышается, отражая эффективность терапии. По окончании курса лечения цианокобаламином** общий (клинический) анализ крови развернутый с учетом ретикулоцитов и, по-возможности, ретикулоцитарных индексов необходимо контролировать каждые 3-4 месяца. Дополнительную информацию об эффективности лечения может представить положительная динамика сывороточных показателей обмена железа (снижение или нормализация показателей ферритина и железа) и, при возможности, гомоцистеина (нормализация показателя) [1–4].
3.3 Иное лечение
- Рекомендуется пациентам с В12-дефицитной анемией и признаками плохой адаптации к анемии проводить оксигенотерапию и заместительные трансфузии эритроцит-содержащих компонентов крови (1-2 дозы) по индивидуальным показаниям в качестве дополнительных мер для достижения ремиссии и улучшения общего состояния пациента [31].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: пациенты с мегалобластной анемией всегда плохо адаптированы к анемии, поскольку метаболические нарушения касаются не только кроветворения, но и всех органов и систем, где проявляется клеточная дистрофия (вследствие нарушения синтеза ДНК). В соответствии с этим вопрос назначения заместительной терапии эритроцит-содержащими компонентами крови решается на индивидуальной основе. Пациенты пожилого и старческого возраста зачастую требуют проведения гемокомпонентной терапии даже при умеренном снижении гемоглобина (до 75-85 г/л).
У многих пациентов на фоне лечения цианокобаламином** и активизации эритропоэза может проявиться дефицит железа, который препятствует полной нормализации показателей красной крови и требует стандартного лечения препаратами железа.
Диетотерапия и обезболивание не применяется.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Возможные причины развития В12-дефицитной анемии
I. Нарушения всасывания витамина В12
Приобретенные формы дефицита витамина В12
Нарушение секреции гастромукопротеина (внутреннего фактора) в желудке:
- Атрофия париетальных клеток слизистой оболочкой желудка (атрофические гастриты)
- Антитела к париетальным клеткам слизистой оболочкой желудка
- Антитела к гастромукопротеину или к комплексу гастромукопротеин + витамин В12
- Органические поражения желудка и кишечника (опухоли, распространенный полипоз), состояние после резекции желудка или кишечника
- Органические болезни тонкого кишечника (спру, илеит, болезнь Крона)
Наследственные формы дефицита витамина В12
- Дефицит «внутреннего фактора»
- Болезнь Имерслунд – Гресбека
- Дефицит и аномалии транскобаламина II
II. Повышенный расход витамина В12
- Беременность
- Избыточная кишечная флора при дивертикулезе кишечника, инвазия широкого лентеца и другие паразитозы
III. Уменьшенное потребление витамина В12
- Неполноценное питание
- Отсутствие продуктов животного происхождения
При подозрении на В12-дефицитную анемию в детской практике следует:
- обратить внимание на возможные проявления синдрома мальабсорбции;
- подробно выяснить характер питания ребенка и родителей;
- в случае обследования грудных детей — выяснить характер питания матери до и во время беременности, а также в период кормления грудью.
Дети, в питании которых недостаточно витамина В12, с большой вероятностью имеют дефицит других витаминов и микроэлементов (в том числе фолиевой кислоты, железа). Таких детей необходимо ставить на диспансерный учет, получив результаты первичного обследования.
Прогноз В12-дефицитной анемии
Ранняя диагностика В12-дефицитной анемии, своевременное начало лечения и адекватное диспансерное наблюдение после ликвидации анемии, обеспечивают благоприятный прогноз заболевания вне зависимости от возраста пациента.
У пожилых пациентов с глубокой анемией прогноз может определяться наличием и характером сопутствующих, в том числе сердечно-сосудистых, заболеваний. Развитие клиники фуникулярного миелоза резко ухудшает прогноз.
Медицинская реабилитация
4. Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
Специфических реабилитационных мероприятий в отношении пациентов с В12- дефицитной анемией нет.
Госпитализация
6. Организация оказания медицинской помощи
Показания для экстренной госпитализации в медицинскую организацию:
1. глубокая анемия с выраженными гипоксическими проявлениями и/или отсутствие адаптации к сниженному уровню гемоглобина (декомпенсация анемии).
Показания для плановой госпитализации в медицинскую организацию:
1. диспансерное обследование, в том числе при первичной диагностике В12- дефицитной анемии умеренной или тяжелой степени.
Показания к выписке пациента из медицинской организации:
1. регресс симптомов декомпенсации анемии, окончание обследования с целью выявления причины развития дефицита витамина В12.
Профилактика
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Диспансерное наблюдение проводится с учетом возможности устранения причины дефицита В12.
К группе риска развития В12-дефицитной анемии относятся пациенты с синдромом мальабсорбции (целиакия, хронические воспалительные заболевания кишечника), с резекцией желудка и кишечника в анамнезе, находящиеся на программном гемодиализе, а также беременные женщины, соблюдающие вегетарианскую диету.
Информация
Источники и литература
-
Клинические рекомендации Российской ассоциации эндокринологов
- Клинические рекомендации Российской ассоциации эндокринологов — 1. Воробьев АИ, editor. Руководство по гематологии: в 3 т. М.: “Ниюдиамед”; 2005.
2. Румянцев АГ, Масчан АА, Жуковская ЕВ. Детская гематология. 2015.
3. Green R, Allen LH, Bjørke-Monsen A-L, Brito A, Guéant J-L, Miller JW, et al. Vitamin B12 deficiency. Nat Rev Dis Prim 2017;3:17040.
4. Green R., Folate, cobalamin, and megaloblastic anemias, Williams Hematology, 9th ed., Chapter 41, p. 583-615, n.d.
5. Lam JR, Schneider JL, Zhao W, Corley DA. Proton Pump Inhibitor and Histamine 2 Receptor Antagonist Use and Vitamin B 12 Deficiency. JAMA 2013;310:2435. https://doi.org/10.1001/jama.2013.280490.
6. Ahmed MA, Muntingh G, Rheeder P. Vitamin B12 deficiency in metformin-treated type-2 diabetes patients, prevalence and association with peripheral neuropathy. BMC Pharmacol Toxicol 2016;17:44. https://doi.org/10.1186/s40360-016-0088-3.
7. Specker BL, Black A, Allen L, Morrow F. Vitamin B-12: low milk concentrations are related to low serum concentrations in vegetarian women and to methylmalonic aciduria in their infants. Am J Clin Nutr 1990;52:1073–6. https://doi.org/10.1093/ajcn/52.6.1073.
8. Michael Whitehead V. Acquired and inherited disorders of cobalamin and folate in children. Br J Haematol 2006;134:125–36. https://doi.org/10.1111/j.1365-2141.2006.06133.x.
9. Kozyraki R, Kristiansen M, Silahtaroglu A, Hansen C, Jacobsen C, Tommerup N, et al. The human intrinsic factor-vitamin B12 receptor, cubilin: Molecular characterization and chromosomal mapping of the gene to 10p within the autosomal recessive megaloblastic anemia (MGA1) region. Blood 1998;91:3593–600. https://doi.org/10.1182/blood.v91.10.3593.3593_3593_3600.
10. Tanner SM, Li Z, Perko JD, Oner C, Cetin M, Altay C, et al. Hereditary juvenile cobalamin deficiency caused by mutations in the intrinsic factor gene. Proc Natl Acad Sci 2005;102:4130–3. https://doi.org/10.1073/pnas.0500517102.
11. Borch K, Liedberg G. Prevalence and incidence of pernicious anemia. An evaluation for gastric screening. Scand J Gastroenterol 1984;19:154–60. https://doi.org/10.1080/00365521.1984.12005702.
12. Kocak R, Paydas S. Pernicious anemia in Turkey. Int J Hematol 1992;55:117–9.
13. Stabler SP, Allen RH. VITAMIN B12 DEFICIENCY AS A WORLDWIDE PROBLEM. Annu Rev Nutr 2004;24:299–326. https://doi.org/10.1146/annurev.nutr.24.012003.132440.14. Allen LH. How common is vitamin B-12 deficiency? Am J Clin Nutr 2009;89:693S-696S. https://doi.org/10.3945/ajcn.2008.26947A.
15. Yildirim T, Yalcin A, Atmis V, Cengiz OK, Aras S, Varlı M, et al. The prevalence of anemia, iron, vitamin B12, and folic acid deficiencies in community dwelling elderly in Ankara, Turkey. Arch Gerontol Geriatr 2015;60:344–8. https://doi.org/10.1016/j.archger.2015.01.001.
16. De Block CEM, De Leeuw IH, Van Gaal LF. Autoimmune Gastritis in Type 1 Diabetes: A Clinically Oriented Review. J Clin Endocrinol Metab 2008;93:363–71. https://doi.org/10.1210/jc.2007-2134.
17. Moore E, Mander A, Ames D, Carne R, Sanders K, Watters D. Cognitive impairment and vitamin B12: a review. Int Psychogeriatrics 2012;24:541–56. https://doi.org/10.1017/S1041610211002511.
18. Devalia V, Hamilton MS, Molloy AM. Guidelines for the diagnosis and treatment of cobalamin and folate disorders. Br J Haematol 2014;166:496–513. https://doi.org/10.1111/bjh.12959.
19. Buttarello M. Laboratory diagnosis of anemia: are the old and new red cell parameters useful in classification and treatment, how? Int J Lab Hematol 2016;38:123–32. https://doi.org/10.1111/ijlh.12500.
20. Долгов В.В., Луговская С.А., Морозова В.Т., Почтарь М.Е. Лабораторная диагностика анемий. Москва, Триада. 2009; 147 с. n.d.
21. Егорова М.О., Цветаева Н.В., Сухачева Е.А., Комолова Е.Н. Практические рекомендации по скрининговой лабораторной диагностике анемии. Гематология и трансфузиология. 2011; 56; 5: 24-36. n.d.
22. Snow CF. Laboratory Diagnosis of Vitamin B12 and Folate Deficiency. Arch Intern Med 1999;159:1289. https://doi.org/10.1001/archinte.159.12.1289.
23. Yuen M-F, Lai C-L. Hbsag seroclearance in the natural history of chronic hepatitis b infection. Curr Hepat Rep 2006;5:23–6. https://doi.org/10.1007/s11901-006-0019-7.
24. CA B. An investigation of the relationship between vitamin B12 deficiency and HIV infection. J Assoc Nurses AIDS Care 2000;11. https://doi.org/10.1016/S1055-3290(06)60419- 6.
25. A S-M, E D, A M, KR A, DJ H. Vitamin B 12 status in health and disease: a critical review. Diagnosis of deficiency and insufficiency — clinical and laboratory pitfalls. Crit Rev Clin Lab Sci 2021. https://doi.org/10.1080/10408363.2021.1885339.26. E O, K O, H T, K A, K E, G T, et al. Hyperhomocysteinemia is a risk factor for coronary arteriosclerosis in Japanese patients with type 2 diabetes. Diabetes Care 1999;22:484–90. https://doi.org/10.2337/DIACARE.22.3.484.
27. Dani SI, Thanvi S, Shah JM, Prajapti J, Jain S, Joshi H. Hyperhomocysteinemia masquerading as pulmonary embolism. J Assoc Physicians India 2003;51:914–5.
28. Toh B-H. Pathophysiology and laboratory diagnosis of pernicious anemia. Immunol Res 2017;65:326–30. https://doi.org/10.1007/s12026-016-8841-7.
29. Carmel R. How I treat cobalamin (vitamin B12) deficiency. Blood 2008;112:2214–21. https://doi.org/10.1182/blood-2008-03-040253.
30. Vidal-Alaball J, Butler C, Cannings-John R, Goringe A, Hood K, McCaddon A, et al. Oral vitamin B12 versus intramuscular vitamin B12 for vitamin B12 deficiency. Cochrane Database Syst Rev 2005. https://doi.org/10.1002/14651858.CD004655.pub2.
31. Cortés Buelvas A. Anemia and transfusion of red blood cells. Colomb Med 2013;44:236–42. https://doi.org/10.25100/cm.v44i4.1504.
- Клинические рекомендации Российской ассоциации эндокринологов — 1. Воробьев АИ, editor. Руководство по гематологии: в 3 т. М.: “Ниюдиамед”; 2005.
Информация
Список сокращений
В12 – витамин В12, цианокобаламин
MCV – средний объём эритроцитов
MCH – среднее содержание гемоглобина в эритроците
MCHС – средняя концентрация гемоглобина в эритроците
ЛДГ – лактатдегидрогеназа
ЭКГ – электрокардиограмма
АЛТ – аланинаминотрансфераза
АСТ – аспартатаминотрансфераза
УЗИ – ультразвуковое исследование
ОЖСС – общая железосвязывающая способность сыворотки
НТЖ – насыщение трансферрина железом
ММК – метилмалоновая кислота
Термины и определения
В12-дефицитная анемия
– макроцитарная анемия, обусловленная дефицитом витамина В12, отличительными морфологическими признаками которой являются гиперхромия эритроцитов и мегалобластный эритропоэз; характерны также морфологические аномалии других ростков кроветворения в костном мозге, цитопении и гиперсегментация ядер нейтрофилов в крови, частое развитие психо- неврологических симптомов (фуникулярный миелоз).
Кобаламин – биохимическое название витамина В12.
Внутренний фактор Кастла – белок, продуцирующийся париетальными клетками тела и дна желудка (открыт W.Castle в 1930), необходимый для всасывания витамина В12.
Кубулин — специфический белок-рецептор, необходимый для связывания комплекса витамина В12 с внутренним фактором Кастла, обеспечивающий поступление данного комплекса в стенку подвздошной кишки.
Метилмалоновая кислота (ММК) – субстрат для фермента метилмалонил-КоА, кофактором которого является витамин В12.
Фуникулярный миелоз — комплекс неврологических нарушений (парестезии, гипорефлексии, рефлекс Бабинского), характерный для дефицита витамина В12.
Ретикулоцитарный криз – повышение количества ретикулоцитов более, чем на 20- 25% от исходного.
Критерии оценки качества медицинской помощи
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Члены Национального гематологического общества:
- Лукина Е.А.1, д.м.н., профессор, зав. отделением орфанных заболеваний ФГБУ НМИЦ гематологии Минздрава России
- Цветаева Н.В.1, к.м.н., старший научный сотрудник отделения орфанных заболеваний ФГБУ НМИЦ гематологии Минздрава России
- Двирнык В.Н.1, к.м.н., зав. Централизованной клинико-диагностической лабораторией ФГБУ НМИЦ гематологии Минздрава России
Члены Национального общества детских гематологов и онкологов:
- Румянцев А.Г. доктор медицинских наук, профессор, главный детский гематолог Министерства здравоохранения Российской Федерации, директор Федерального научно-клинического центра детской гематологии, онкологии и иммунологии им. Дмитрия Рогачёва, член правления Союза педиатров России, академик РАМН.
- Масчан А.А. д.м.н., профессор, член-корреспондент РАН, заместитель генерального директора, директор Института гематологии, иммунологии и клеточных технологий ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России
- Демихов В. Г. — д.м.н., профессор, директор Научно-клинического центра гематологии, онкологии и иммунологии ГБОУ ВПО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, член НОДГО, член Европейской гематологической ассоциации (EHA).
- Скобин В.Б., к.м.н., врач-гематолог Научно-клинического центра гематологии, онкологии и иммунологии ГБОУ ВПО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, член НОДГО.
- Журина О.Н., к.м.н., зав. лабораторией Научно-клинического центра гематологии, онкологии и иммунологии ГБОУ ВПО «Рязанский государственный медицинский университет им. акад. И.П. Павлова» Минздрава России, член НОДГО.
Члены Федерации лабораторной медицины:
- Луговская С.А., д.м.н., профессор кафедры клинической лабораторной диагностики ФГБОУ ДПО РМАНПО Минздрава России
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Приложение А2. Методология разработки клинических рекомендаций
Целевая а
уд
ито
р
ия
д
анных клинических
р
екомен
д
аций:
- Врачи-Терапевты
- Врачи-Педиатры
- Врачи-Гематологи
- Врачи-Неврологи
- Врачи-Гастроэнтерологи
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Нет.
Приложение Б. Алгоритмы действий врача
Приложение В. Информация для пациента
Нехватка витамина В12 может наблюдаться у взрослых и детей при редких заболеваниях: глистной инвазии широким лентецом, при редких врожденных заболеваниях, связанных с нарушением образования внутреннего фактора Кастла (белка, ответственного за перенос витамина В12 из пищи в кровь), а также иммунном заболевании, причиной которого является выработка антител к внутреннему фактору (пернициозная анемия). Причина может заключаться в неправильном питании, строгой вегетарианской диете, удалении желудка или части кишки. Для уточнения причины всегда необходимо индивидуальное полноценное обследование, которое должно включать определение концентрации витамина В12 в крови. При нехватке в организме витамина В12 развивается анемия, потеря веса, бледность, хронический гастрит, воспаление языка (глоссит), появляются слабость в конечностях и другие неврологические нарушения, последние в большей мере свойственны людям пожилого и старческого возраста. В случаях упорного ухудшения самочувствия, депрессии, снижения работоспособности, а у детей ухудшения успеваемости, отставания в развитии необходимо обратиться к врачу по месту жительства для проведения обследования. Очень важно сдать анализ крови. При своевременном распознавании В12-дефицитная анемия легко поддается лечению витамином В12. Через месяц после начала лечения уровень гемоглобина нормализуется. Если причину дефицита витамина В12 можно устранить (глисты, неправильное питание), поддерживающее лечение не проводится. Если причину устранить невозможно (сохраняется пониженное всасывание в кишечнике, нежелание отказаться от вегетарианской диеты, наличие антител к внутреннему фактору или его врожденная недостаточность), поддерживающее введение витамина В12 в приемлемом для пациентов режиме проводится пожизненно. Самостоятельное использование препарата недопустимо. Назначается лечение врачом с учетом всех показаний и противопоказаний.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Нет.
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.