Содержание
-
Структурная формула
-
Русское название
-
Английское название
-
Латинское название
-
Химическое название
-
Брутто формула
-
Фармакологическая группа вещества Гликопиррония бромид
-
Код CAS
-
Применение при беременности и кормлении грудью
-
Торговые названия с действующим веществом Гликопиррония бромид
Структурная формула
Русское название
Гликопиррония бромид
Английское название
Glycopyrronium bromide
Латинское название
Glycopyrronii bromidum (род. Glycopyrronii bromidi)
Химическое название
3-(2-Циклопентил-2-гидрокси-2-фенилацетокси)-1,1-диметилпирролидиниум бромид
Брутто формула
C19H28BrNO3
Фармакологическая группа вещества Гликопиррония бромид
Код CAS
596-51-0
Применение при беременности и кормлении грудью
Категория действия на плод по FDA — C.
Торговые названия с действующим веществом Гликопиррония бромид
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Сибри® Бризхалер® |
от 1315.00 до 1850.00 |
Респинекс — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-№(000743)-(РГ-RU)
Листок-вкладыш – информация для пациента
Респинекс®, 50 мкг/доза, капсулы с порошком для ингаляций
Действующее вещество: гликопиррония бромид
Перед применением препарата полностью прочитайте листок-вкладыш, поскольку в нем содержатся важные для Вас сведения.
Сохраните листок-вкладыш. Возможно, Вам потребуется прочитать его еще раз.
Если у Вас возникли дополнительные вопросы, обратитесь к лечащему врачу или работнику аптеки, или медицинской сестре.
Препарат назначен именно Вам. Не передавайте его другим людям. Он может навредить им, даже если симптомы их заболевания совпадают с Вашими.
Если у Вас возникли какие-либо нежелательные реакции, обратитесь к лечащему врачу или работнику аптеки, или медицинской сестре. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в разделе 4 листка-вкладыша.
Содержание листка-вкладыша
- Что из себя представляет препарат Респинекс® и для чего его применяют.
- О чем следует знать перед применением препарата Респинекс®.
- Применение препарата Респинекс®.
- Возможные нежелательные реакции.
- Хранение препарата Респинекс®.
- Содержимое упаковки и прочие сведения.
1. Что из себя представляет препарат Респинекс® и для чего его применяют
Препарат Респинекс® содержит действующее вещество гликопиррония бромид и является средством для лечения обструктивных заболеваний дыхательных путей.
Показания к применению
Поддерживающее лечение нарушений бронхиальной проводимости при хронической обструктивной болезни легких (ХОБЛ).
Способ действия препарата Респинекс®
Гликопиррония бромид вызывает расслабление мускулатуры бронхов и их расширение, что улучшает дыхательную функцию и облегчает симптомы заболевания. Продолжительность действия препарата после ингаляции обусловлена длительным поддержанием лечебной концентрации препарата в легких.
Если улучшение не наступило или Вы чувствуете ухудшение, необходимо немедленно обратиться к врачу.
2. О чем следует знать перед применением препарата Респинекс®
Противопоказания
Не применяйте препарат Респинекс®:
- Если у Вас аллергия на гликопиррония бромид или любые другие компоненты препарата (перечисленные в разделе 6 листка-вкладыша).
- Если Вы младше 18 лет.
- Если у Вас есть непереносимость галактозы, дефицит лактазы или глюкозо-галактозная мальабсорбция (препарат содержит лактозу).
- Противопоказан одновременный прием с ингаляционными лекарственными средствами, содержащими другие м-холиноблокаторы.
Особые указания и меры предосторожности
Перед применением препарата Респинекс® проконсультируйтесь с лечащим врачом.
С осторожностью
Препарат Респинекс® необходимо применять с осторожностью при наличии следующих заболеваний: закрытоугольная глаукома, заболевания, сопровождающиеся задержкой мочи, тяжелая почечная недостаточность, включая терминальную стадию почечной недостаточности, требующую проведения гемодиализа (препарат Респинекс® должен применяться только в случае, если ожидаемая польза превышает потенциальный риск); нестабильная ишемическая болезнь сердца (ИБС), инфаркт миокарда в анамнезе, нарушения сердечного ритма, удлинение интервала QTc.
Сообщите Вашему врачу, если у Вас есть или ранее было какое-либо из этих заболеваний. Ваш врач при назначении препарата оценит предполагаемый риск, связанный с применением препарата конкретно у Вас, и, при необходимости, проведет дополнительные обследования.
Бронхоспазм
Препарат Респинекс® не рекомендован для купирования острых эпизодов бронхоспазма. Такие эпизоды могут наблюдаться при обострении Вашего заболевания. Ваш врач может назначить Вам дополнительный препарат для применения при острых эпизодах бронхоспазма.
Реакции гиперчувствительности
При применении препарата возможно развитие аллергических реакций. При развитии у Вас симптомов аллергической реакции (затрудненное дыхание или глотание, отек языка, губ и лица, крапивница, кожная сыпь, зуд) немедленно прекратите прием препарата и обратитесь за медицинской помощью. Затем Ваш врач подберет для Вас альтернативное лечение.
Парадоксальный бронхоспазм
Как и в случаях другого ингаляционного лечения, при применении препарата Респинекс® возможно развитие парадоксального бронхоспазма, что может представлять угрозу для жизни. Симптомы парадоксального бронхоспазма возникают сразу после ингаляции. К ним относятся затрудненное дыхание, одышка, хрипы при дыхании, чувство дискомфорта и сдавления в груди.
В случае развития парадоксального бронхоспазма немедленно прекратите прием препарата и обратитесь за медицинской помощью. Вам потребуется другое лечение.
Закрытоугольная глаукома
Препарат Респинекс® может влиять на внутриглазное давление и должен с осторожностью применяться у пациентов с закрытоугольной (узкоугольной) глаукомой.
При развитии у Вас симптомов приступа закрытоугольной глаукомы (боль или дискомфорт в глазах, нечеткость зрения, появление ореолов вокруг источников света, покраснение глаз) немедленно прекратите прием препарата и обратитесь за медицинской помощью.
Задержка мочи
Сообщите Вашему врачу, если у Вас есть какие-либо заболевания почек или другие состояния, которые могут вызвать задержку мочи.
Тяжелая почечная недостаточность
Если у Вас нарушена работа почек, в том числе в связи с терминальной стадией почечной недостаточности, и если Вам необходим гемодиализ, Ваш врач будет особенно тщательно следить за Вашим состоянием в период применения препарата и, при необходимости, проводить дополнительные обследования.
Лактоза
Препарат Респинекс® содержит лактозу.
Пациентам с редко встречающейся наследственной непереносимостью галактозы, дефицитом лактазы лопарей или глюкозно-галактозной мальабсорбцией не следует применять этот препарат.
Дети и подростки
Детям и подросткам до 18 лет не следует применять препарат Респинекс®.
Другие препараты и препарат Респинекс®
Сообщите лечащему врачу о том, что Вы принимаете, недавно принимали или можете начать принимать какие-либо другие препараты.
Одновременное применение препарата с другими лекарственными средствами для ингаляционного применения, содержащими м-холиноблокаторы (такими как тиотропий, ипратропий), не изучено, в связи с чем одновременное применение вышеуказанных средств противопоказано.
При одновременном ингаляционном применении гликопиррония бромида и индакатерола (бронхорасширяющий препарат из группы бета2-адреномиметиков) не наблюдалось изменения эффективности и безопасности обоих препаратов. Кроме того, при одновременном применении гликопиррония бромида с другими препаратами для лечения ХОБЛ, в т.ч. бета-адреномиметиками (такими как, например, формотерол), метилксантинами (такими как, например, теофиллин), глюкокортикостероидами (такими как, например, будесонид), не наблюдалось признаков взаимодействия и изменения эффективности и безопасности препаратов.
При одновременном применении гликопиррония бромида с циметидином и другими препаратами группы ингибиторов транспортеров катионов (препараты для лечения язвенной болезни желудка и двенадцатиперстной кишки) маловероятно изменение эффективности и безопасности препаратов.
Беременность и грудное вскармливание
Если Вы беременны или кормите грудью, предполагаете, что Вы можете быть беременны или планируете в скором времени завести ребенка, обратитесь к врачу за консультацией, прежде чем начать применение препарата Респинекс®
Данных о применении гликопиррония бромида у беременных женщин нет.
В доклинических исследованиях было показано, что гликопиррония бромид не влияет на развитие плода.
В связи с отсутствием клинических данных по применению препарата Респинекс® у беременных женщин, применение препарата во время беременности возможно только если предполагаемая польза применения для матери превышает потенциальный риск для плода.
Неизвестно, проникает ли гликопирроний в грудное молоко у человека. Учитывая это обстоятельство, применение препарата Респинекс® у кормящих грудью женщин допустимо, только если предполагаемая польза для матери превышает возможный риск для ребенка.
Управление транспортными средствами и работа с механизмами
Препарат Респинекс® не оказывает влияние на способность управлять транспортными средствами и выполнение потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
Препарат Респинекс® содержит лактозу.
Если у Вас непереносимость некоторых сахаров, обратитесь к лечащему врачу перед применением данного лекарственного препарата.
3. Применение препарата Респинекс®
Всегда применяйте препарат в полном соответствии с рекомендациями лечащего врача. При появлении сомнений посоветуйтесь с лечащим врачом.
Рекомендуемая доза
Рекомендуемая доза препарата Респинекс® составляет 50 мкг (содержимое 1 капсулы) 1 раз в сутки. Ингаляцию препарата необходимо проводить в одно и то же время. Недопустимо применять более 1 дозы препарата в сутки.
Режим дозирования у особых групп пациентов
Пациенты пожилого возраста
Не требуется коррекции дозы препарата, если Вам больше 75 лет.
Пациенты с нарушением функции почек
Не требуется коррекции дозы при применении препарата, если у Вас нарушения функции почек легкой или средней степени. Если у Вас нарушение функции почек тяжелой степени или терминальная стадия хронической болезни почек (ХБП), требующая проведения гемодиализа, Ваш врач оценит потенциальную пользу и риски применения препарата Респинекс® в рекомендуемой дозе конкретно у Вас.
Пациенты с нарушением функции печени
Не требуется коррекции дозы при применении препарата, если у Вас нарушения функции печени легкой и средней степени тяжести. Специальных клинических исследований у пациентов с нарушением функции печени не проводилось.
Путь и (или) способ введения
Ингаляционно.
Перед началом применения препарата Респинекс® необходимо ознакомиться с техникой использования устройства для ингаляций (ингалятора), которая представлена в конце данного листка-вкладыша.
Препарат представляет собой капсулы с порошком для ингаляций, которые следует применять только для ингаляций через рот с помощью ингалятора, который входит в комплект. Капсулы нельзя принимать внутрь.
Препарат следует вдыхать, а не глотать.
Капсулы с порошком для ингаляций следует хранить в блистере и извлекать из него непосредственно перед применением.
Перед началом применения препарата Ваш врач расскажет Вам о том, как правильно пользоваться устройством для ингаляций (ингалятором).
При отсутствии улучшения Вашего состояния Ваш врач, возможно, захочет проверить, правильно ли Вы пользуетесь ингалятором.
Если Вы забыли принять препарат Респинекс®
Если Вы пропустили прием дозы препарата Респинекс®, следующую дозу необходимо принять как можно быстрее. Если Вы вспомнили о пропущенной дозе только на следующий день, примите следующую дозу в обычное время; не следует принимать две дозы в один день.
Если Вы приняли препарата Респинекс® больше, чем следовало
Применение высоких доз может привести к развитию характерных симптомов и потребовать соответствующего лечения.
Если Вы приняли больше препарата Респинекс®, чем следовало, или если кто-то другой по ошибке принял Ваш препарат, немедленно обратитесь к своему лечащему врачу или в отделение скорой помощи. При обращении покажите пачку препарата Респинекс®. Вам может потребоваться срочная медицинская помощь. Специального лечения при передозировке препарата Респинекс® не существует, но Вам может быть назначено лечение для устранения симптомов.
При случайном проглатывании капсулы препарата Респинекс® развитие острых симптомов передозировки маловероятно.
При наличии вопросов по применению препарата обратитесь к лечащему врачу.
4. Возможные нежелательные реакции
Подобно всем лекарственным препаратам, препарат Респинекс® может вызывать нежелательные реакции, однако они возникают не у всех.
Немедленно прекратите применение препарата и обратитесь за медицинской помощью, если:
- у Вас появилось затрудненное дыхание или глотание, отек языка, губ и лица, крапивница, кожная сыпь, зуд и так далее (симптомы аллергических реакций).
- у Вас появилось затрудненное дыхание, одышка, хрипы при дыхании, чувство дискомфорта и сдавления в груди сразу после ингаляции (симптомы парадоксального бронхоспазма).
- у Вас появились боль или дискомфорт в глазах, нечеткость зрения, появление ореолов вокруг источников света, покраснение глаз (симптомы приступа закрытоугольной глаукомы).
- у Вас появилась сильная жажда, повышенный аппетит, увеличение частоты мочеиспускания и объема мочи, усталость (симптомы повышения уровня глюкозы в крови).
- у Вас появились боли в груди, нарушения ритма сердечных сокращений (симптомы со стороны сердца).
Другие нежелательные реакции, которые могут возникать при лечении препаратом Респинекс®, описаны ниже.
Частые нежелательные реакции (могут возникать не более чем у 1 человека из 10):
- насморк в сочетании с болью в горле (назофарингит)
- бессонница
- головная боль
- сухость слизистой оболочки полости рта
- воспаление слизистой желудка и кишечника (гастроэнтерит)
- инфекция мочевыводящих путей
Нечастые нежелательные реакции (могут возникать не более чем у 1 человека из 100):
- воспаление слизистой носа (ринит)
- воспаление слизистой мочевого пузыря (цистит)
- снижение тактильной чувствительности (гипестезия)
- ощущение сердцебиения
- застойные явления в придаточных пазухах носа
- кашель с мокротой (продуктивный кашель)
- першение в горле
- носовое кровотечение
- расстройство пищеварения (диспепсия)
- кариес зубов
- кожная сыпь
- боль в конечностях
- скелетно-мышечная боль в грудной клетке
- боли или жжение при мочеиспускании (дизурия)
- задержка мочи
- усталость
- повышенная утомляемость (астения)
- повышение уровня глюкозы в крови по результатам лабораторных анализов (гипергликемия)
Нежелательные реакции с неизвестной частотой (исходя из имеющихся данных частоту определить невозможно):
- изменение голоса (дисфония)
- кожный зуд
Особые группы пациентов
У пожилых пациентов в возрасте старше 75 лет к частым нежелательным реакциям также относятся инфекции мочевыводящих путей и головная боль.
Если любые из указанных в инструкции нежелательных реакций ухудшаются, или доставляют выраженный дискомфорт, а также в случае, если Вы отметили появление других нежелательных реакций, не указанных в инструкции, сообщите об этом врачу.
Сообщение о нежелательных реакциях
Если у Вас возникают какие-либо нежелательные реакции, проконсультируйтесь с врачом. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в листке-вкладыше Вы также можете сообщить о нежелательных реакциях в информационную базу по нежелательным реакциям (действиям) на лекарственные препараты, включая сообщения о неэффективности лекарственных препаратов, выявленным на территории государства – члена Евразийского экономического союза.
Российская Федерация:
Федеральная служба по надзору в сфере здравоохранения
109074, г. Москва, Славянская площадь, д. 4, стр. 1
roszdravnadzor.gov.ru.
Республика Беларусь:
УП «Центр экспертиз и испытаний в здравоохранении»
220037, г. Минск, Товарищеский пер., 2а
http://www.rceth.bv.
Республика Казахстан:
РГП на ПХВ «Национальный Центр экспертизы лекарственных средств и медицинских изделий» Комитета медицинского и фармацевтического контроля Министерства здравоохранения Республики Казахстан
010000, г. Нур-Султан, район Алматы, пр. Бауыржана Момышулы, 2/3
ndda.kz.
Кыргызская Республика:
Департамент лекарственного обеспечения и медицинской техники при Министерстве Здравоохранения Кыргызской Республики
720044, г. Бишкек, ул. 3-я Линия, 25
pharm.kg.
Республика Армения:
АОЗТ «Научный центр экспертизы лекарств и медицинских технологий им. Академика Э. Габриеляна»
0051, г. Ереван, пр. Комитаса, 49/4
pharm.am.
Сообщая о нежелательных реакциях, Вы помогаете получить больше сведений о безопасности препарата.
5. Хранение препарата Респинекс®
Храните препарат в недоступном для ребенка месте так, чтобы ребенок не мог увидеть его.
Не применяйте препарат после истечения срока годности (срока хранения), указанного на картонной пачке после слов «Годен до:».
Датой истечения срока годности является последний день данного месяца.
Храните препарат Респинекс® в оригинальной упаковке (блистер в пачке) при температуре не выше 25 °С. Берегите препарат от воздействия влаги.
Срок годности препарата: 2 года.
6. Содержимое упаковки и прочие сведения
Препарат Респинекс® содержит
Действующим веществом является гликопиррония бромид.
Каждая капсула с порошком для ингаляций содержит 0,05 мг гликопиррония основания, что эквивалентно 0,0626 мг1 гликопиррония бромида.
1 В состав включен 5% избыток действующего вещества гликопиррония бромида для компенсации потерь во время производства и внутри ингалятора при применении. Количество гликопиррония бромида с учетом избытка составляет 0,0657 мг.
Вспомогательные вещества.
Содержимое капсулы: лактозы моногидрат, магния стеарат.
Корпус капсулы: каррагинан, гипромеллоза, калия ацетат, вода очищенная.
Крышечка капсулы: каррагинан, гипромеллоза, калия ацетат, вода очищенная, краситель зеленый прочный, краситель хинолиновый желтый, титана диоксид.
Внешний вид Респинекс® и содержимое упаковки
Капсулы с порошком для ингаляций.
Препарат представляет собой твердые капсулы № 3 с бесцветным прозрачным корпусом и крышечкой зеленого цвета.
Содержимое капсул: белый или почти белый порошок.
По 10 капсул в контурную ячейковую упаковку (блистер) из фольги алюминиевой и материала комбинированного ОПА/АЛ/ПВХ.
По 3 блистера вместе с устройством для ингаляций производства Taian Dalu Medical Instrument Co., Ltd., Китай, с листком-вкладышем помещают в картонную пачку или в пачку из картона гофрированного.
Картонная пачка может быть снабжена этикеткой контрольного вскрытия.
Держатель регистрационного удостоверения и производитель
Российская Федерация.
ООО «ПСК Фарма», 141983, Московская область, г.о. Дубна, г. Дубна, ул. Программистов, д. 5, стр. 1.
Производитель, ответственный за выпускающий контроль качества
ООО «ПСК Фарма»
Московская область, г.о. Дубна, г. Дубна, ул. Программистов, д. 5, стр. 1.
За любой информацией о препарате, а также в случаях возникновения претензий следует обращаться к местному представителю держателя регистрационного удостоверения:
Российская Федерация
ООО «ПСК Фарма»
Адрес: 141983, Московская область, г.о. Дубна, г. Дубна, ул. Программистов, д. 5, стр. 1.
Республика Беларусь
ООО «ФармАссистенс», 220131, г. Минск, 4-ый пер. Кольцова, дом 51, 4 этаж, оф. 54.
Республика Казахстан
ТОО «Prime Asia», 050000, г. Алматы, мкр-н Нур Алатау, ул. Темирбек Кожакеев, дом 70.
Республика Киргизия
ОсОО «Медсервис.КО», 720051, г. Бишкек, ул. Курманжан Датка, д. 131-133.
Республика Армения
ООО «Рудиум Традинг», г. Ереван, ул. Кочарян, д. 18/52.
Листок-вкладыш пересмотрен
Прочие источники информации
Подробные сведения о данном препарате содержатся на веб-сайте Союза eec.eaeunion.org/.
Инструкция по использованию ингалятора
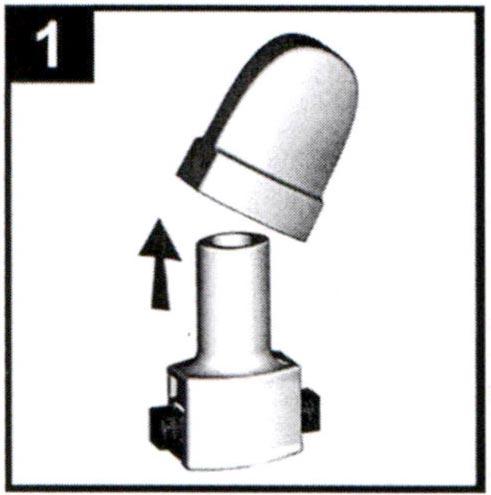
1. Снимите защитный колпачок с ингалятора.
2. Возьмитесь за середину мундштука и основание ингалятора, поверните мундштук по направлению, указанному стрелкой на корпусе, и откройте ячейку для капсулы в основании ингалятора.
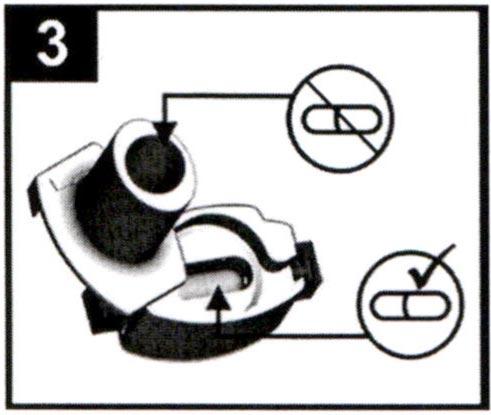
3. Сухими руками возьмите одну капсулу из блистера и поместите капсулу в ячейку для капсул. Никогда не кладите капсулу непосредственно в мундштук, в противном случае возникает угроза попадания капсулы в дыхательные пути и удушья. Не глотайте капсулу.
4. Закройте мундштук, вращая его в противоположную сторону от указания стрелки, удерживайте ингалятор в вертикальном положении.
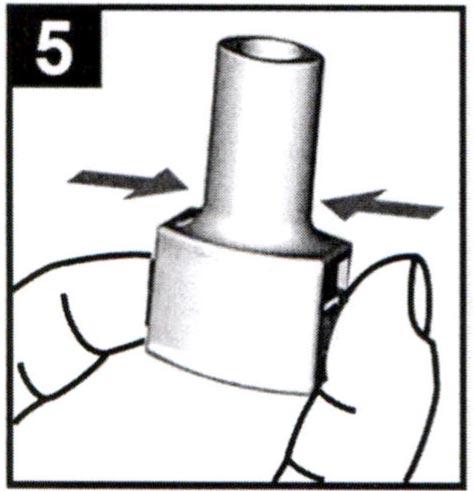
5. Удерживая ингалятор в вертикальном положении, нажмите на кнопки в основании ингалятора и проткните капсулу. Полностью отпустите обе кнопки.
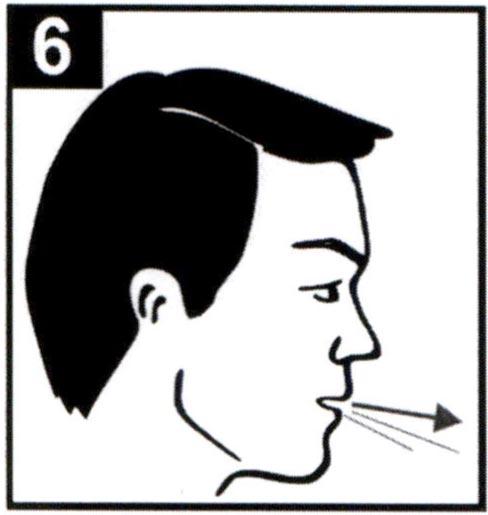
6. Перед тем как поместить мундштук ингалятора в рот, сделайте полный, насколько это возможно, выдох в сторону. Не выдыхайте в ингалятор.
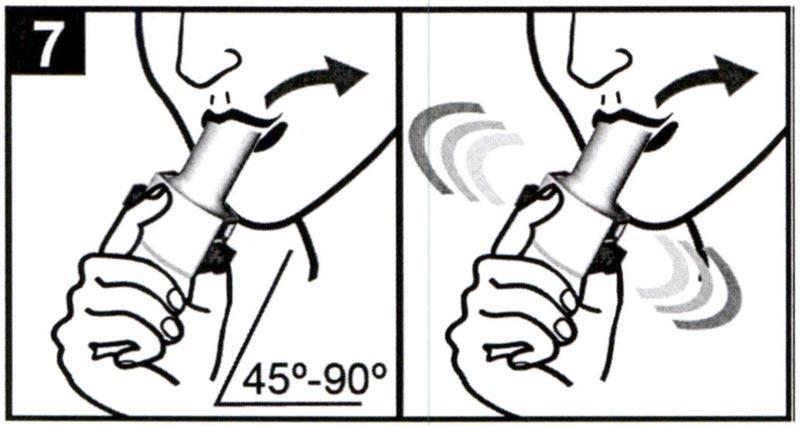
7. Держите ингалятор в руке, как показано на рисунке, не задевая кнопки и не закрывая отверстия для входа воздуха. Вложите мундштук ингалятора в рот и плотно сожмите губы вокруг него. Сделайте быстрый, равномерный, максимально глубокий, насколько это возможно, вдох.
Во время вдоха должен быть характерный дребезжащий звук, издаваемый капсулой при вращении и рассеивании препарата.
Отсутствие дребезжащего звука свидетельствует о блокировке капсулы, в результате чего препарат не рассеивается из капсулы. Если Вы не слышите этот звук, следует немного изменить положение ингалятора или слегка постучать пальцем по основанию ингалятора, после чего повторить вдох.
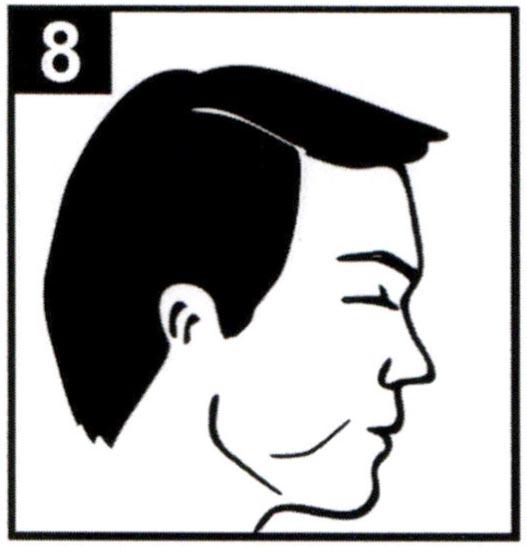
8. Выньте мундштук изо рта и задержите дыхание как можно дольше. Затем медленно выдохните. Никогда не выдыхайте через мундштук.
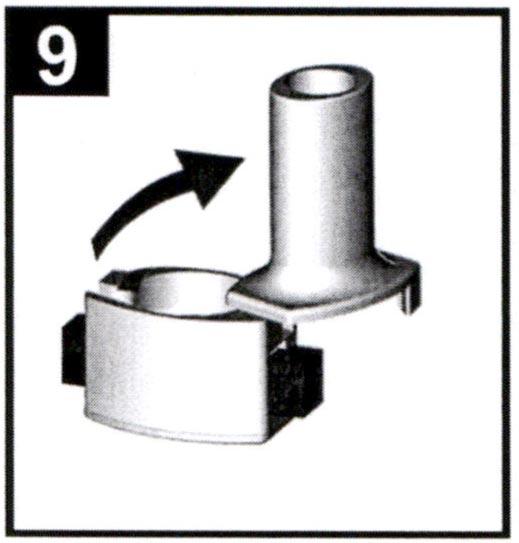
9. Откройте ячейку для капсул: возьмитесь за середину мундштука и основание ингалятора, поверните мундштук по направлению, указанному стрелкой на корпусе.
10. Извлеките капсулу и визуально проверьте ее на наличие проколов и порошка внутри:
- если капсула не проколота и содержит порошок, повторно вставьте ее в ячейку для капсул и повторите процедуру ингаляции, начиная с пункта 4.
- если капсула проколота, но не пустая, повторно вставьте ее в ячейку для капсул, закройте мундштук, как указано в пункте 4, и повторите процедуру ингаляции, начиная с пункта 6. Не нажимайте кнопки повторно.
- если капсула пустая, то Вы получили полную дозу препарата, и эту капсулу можно выбросить.
11. После каждого применения прополощите рот водой, а затем выплюньте.
Воду нельзя глотать!
12. После использования, при необходимости, протрите мундштук сухой салфеткой, закройте мундштук и наденьте на ингалятор защитный колпачок.
Поскольку количество вдыхаемого порошка очень мало, Вы, возможно, не почувствуете вкус порошка после ингаляции. Однако, если Вы следовали инструкции, то можете быть уверены в том, что вдохнули необходимую дозу препарата.
Как очищать ингалятор
Регулярно (не реже 1 раза в неделю) очищайте мундштук снаружи сухой салфеткой. Не используйте воду или другие жидкости для очистки мундштука.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Фармакологическое действие
Бронходилатирующее средство, м-холиноблокатор. Механизм действия основан на блокировании действия ацетилхолина на гладкомышечные клетки дыхательных путей, что приводит к бронходилатирующему эффекту.
Гликопиррония бромид, являясь м-холиноблокатором, обладает высоким сродством к м-холинорецепторам подтипа M1-3. При этом гликопиррония бромид обладает в 4-5 раз большей селективностью в отношении M1 и М3 подтипа рецепторов, по сравнению с М2 подтипом рецепторов.
Продолжительность действия гликопиррония бромида после ингаляции обусловлена длительным поддержанием его терапевтической концентрации в легких, что подтверждается более длительным T1/2 активного вещества после ингаляционного применения, по сравнению с в/в введением. В многочисленных клинических исследованиях было показано, что на фоне применения гликопиррония бромида у пациентов с ХОБЛ существенно улучшается легочная функция (оценка проводилось с помощью изменения ОФВ1): терапевтический эффект возникает в течение первых 5 мин после ингаляции, со значимым повышением ОФВ1 от исходных показателей в пределах 0.091 л до 0.094 л, бронходилатирующий эффект гликопиррония бромида после ингаляции сохраняется более 24 ч.
Фармакокинетика
После ингаляции гликопиррония бромид быстро абсорбируется в системный кровоток и достигает Cmax через 5 мин.
Абсолютная биодоступность гликопиррония бромида после ингаляционного применения составляет примерно 40%. Около 90% системной экспозиции гликопиррония бромида приходится на абсорбцию в легких, и 10% на абсорбцию из ЖКТ. Абсолютная биодоступность после перорального применения гликопиррония бромида оценивается в 5%. На фоне регулярных ингаляций (1 раз/сут) равновесное состояние гликопиррония бромида достигается в течение 1 недели. Cssmax гликопиррония бромида (ингаляция 50 мкг 1 раз/сут) и концентрация гликопиррония бромида в плазме крови непосредственно перед приемом следующей дозы составляют 166 пг/мл и 8 пг/мл соответственно.
После в/в введения Vss гликопиррония бромида составил 83 л и объем распределения в терминальной фазе (Vz) — 376 л. Кажущийся Vz после ингаляции (Vz/F) составил 7310 л, что отражает более медленное выведение гликопиррония бромида после ингаляции.
Связывание гликопиррония бромида с белками плазмы крови человека in vitro составила 38-41% при концентрации 1-10 нг/мл. Эти концентрации как минимум в 6 раз выше, чем Css, достигаемые в плазме на фоне применения препарата в дозе 50 мкг 1 раз/сут.
Было отмечено, что гидроксилирование гликопиррония бромида приводит к образованию различных моно- и бис-гидроксилированных метаболитов, а прямой гидролиз приводит к образованию производных карбоновой кислоты (М9). Исследования in vitro показали, что изоферменты CYP450 вносят свой вклад в окислительную биотрансформацию гликопиррония бромида. Гидролиз до М9, по-видимому, катализируется ферментами семейства холинэстераз. Т.к. в исследованиях in vitro не выявлен метаболизм активного вещества в легких, и М9 вносит незначительный вклад в циркуляцию (4% от Cmax и AUC гликопиррония бромида) после в/в введения, предполагается, что М9 образуется из абсорбируемой из ЖКТ (после ингаляции) фракции действующего вещества путем пресистемного гидролиза и/или при «первом прохождении» через печень. После ингаляции или в/в введения только минимальное количество М9 было обнаружено в моче (<0.5% введенной дозы). Глюкуроновые конъюгаты и/или сульфаты гликопиррония бромида были обнаружены в моче человека после повторных ингаляций в количестве приблизительно 3% от дозы. Исследования ингибирования in vitro продемонстрировали, что гликопиррония бромид не вызывал существенного ингибирования изоферментов CYP1A2, CYP2A6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 или CYP3A4/5, транспортеров MDR1, MRP2 или MXR, и транспортеров ОСТ1 или ОСТ2. В исследованиях индукции ферментов in vitro не выявлено значимой индукции гликопиррония бромидом какого-либо из протестированных изоферментов цитохрома Р450, а также в отношении UGT1A1 и транспортеров MDR1 и MRP2.
Выведение гликопиррония бромида почками достигает 60-70% от общего плазменного клиренса, 30-40% выводится другими путями — с желчью или за счет метаболизма. После однократной и повторных ингаляций гликопиррония бромида в диапазоне от 50 до 200 мкг 1 раз/сут здоровым добровольцам и пациентам с ХОБЛ, средний почечный клиренс находился в пределах 17.4-24.4 л/ч. Активная тубулярная секреция вносит свой вклад в выведение почками гликопиррония бромида. До 20% от принятой дозы обнаруживается в моче в неизмененном виде. Плазменная концентрация гликопиррония бромида снижается многофазно. Средний конечный T1/2 более продолжителен после ингаляционного пути введения (33-57 ч) чем после в/в введения (6.2 ч) и перорального применения (2.8 ч). Характер элиминации позволяет предположить длительную абсорбцию в легких и/или проникновение гликопиррония бромида в системный кровоток во время и после 24 ч после ингаляции.
У пациентов с ХОБЛ системная экспозиция, а также общая экскреция с мочой гликопиррония бромида в равновесном состоянии повышалась пропорционально дозе в диапазоне от 50 мкг до 200 мкг.
Показания активного вещества
ГЛИКОПИРРОНИЯ БРОМИД
Поддерживающая терапия нарушений бронхиальной проходимости у пациентов с ХОБЛ.
Режим дозирования
Предназначен только для ингаляционного применения в соответствующей лекарственной форме.
Рекомендуемая доза — 50 мкг 1 раз/сут.
Побочное действие
Со стороны дыхательной системы: часто — назофарингит; нечасто — ринит, застойные явления в пазухах, продуктивный кашель, раздражение глотки, носовое кровотечение.
Со стороны пищеварительной системы: часто — сухость во рту, гастроэнтерит, рвота; нечасто — диспепсия, зубной кариес.
Со стороны нервной системы: часто — головная боль, бессонница; нечасто — гипестезия.
Со стороны обмена веществ: нечасто — гипергликемия, сахарный диабет.
Со стороны сердечно-сосудистой системы: нечасто — фибрилляция предсердий, ощущение сердцебиения.
Со стороны кожи и подкожных тканей: нечасто — кожная сыпь.
Со стороны костно-мышечной системы: часто — мышечная боль; нечасто — боль в конечностях, боль в скелетных мышцах грудной клетки.
Со стороны мочевыделительной системы: часто — инфекция мочевыводящих путей; нечасто — цистит, дизурия, задержка мочи.
Общие нарушения: часто — боль в области шеи; нечасто — усталость, астения.
Противопоказания к применению
Одновременное применение с ингаляционными лекарственными средствами, содержащими другие м-холиноблокаторы; детский и подростковый возраст до 18 лет; повышенная чувствительность к гликопиррония бромиду.
Применение при беременности и кормлении грудью
Применение при беременности и в период лактации (грудного вскармливания) возможно только в случаях, когда ожидаемая польза терапии для матери превышает потенциальный риск для плода или грудного ребенка.
Клинические данные по применению гликопиррония бромида при беременности отсутствуют. Неизвестно, выделяется ли гликопиррония бромид с грудным молоком у человека.
В доклинических исследованиях было показано отсутствие у препарата тератогенного эффекта после ингаляционного применения. Ни исследования репродуктивной токсичности, ни другие исследования на животных не дают оснований полагать, что гликопиррония бромид может влиять на фертильность у мужчин или женщин.
Особые указания
С осторожностью следует применять при закрытоугольной глаукоме, заболеваниях, сопровождающихся задержкой мочи, почечной недостаточности тяжелой степени (СКФ ниже 30 мл/мин/1.73 м2), включая терминальную стадию, при которой требуется проведение гемодиализа, при нестабильной ИБС, инфаркте миокарда в анамнезе, нарушениях сердечного ритма, удлинении интервала QTc (QT скорректированный >0.44 с). При необходимости применения в таких случаях требуется наблюдение врача.
Гликопиррония бромид не рекомендован для купирования острых эпизодов бронхоспазма.
В общей популяции ХОБЛ существенно преобладают пациенты в возрасте старше 40 лет, поэтому при необходимости применения у пациентов в возрасте до 40 лет требуется спирометрическое подтверждение диагноза ХОБЛ.
Лекарственное взаимодействие
В клинических исследованиях у здоровых добровольцев циметидин, ингибитор транспортеров органических катионов, влияющих на почечный клиренс гликопиррония бромида, увеличивал AUC гликопиррония бромида на 22% и снижал почечный клиренс на 23%. Основываясь на данных показателях, не предполагается клинически значимого взаимодействия при одновременном применении гликопиррония бромида с циметидином или другими ингибиторами транспортеров катионов.
-
Рецептурный.
Действующее вещество (МНН): Гликопиррония бромид, Индакатерол
Производитель: Зигфрид Барбера С.Л./Новартис Фарма ГмбХ
Забрать в аптеке через час
-
Рецептурный.
Действующее вещество (МНН): Гликопиррония бромид
Производитель: ООО ПСК Фарма
-
Рецептурный.
Действующее вещество (МНН): Гликопиррония бромид
Производитель: Зигфрид Барбера С.Л./Новартис Фармасьютика С.А
Забрать в аптеке через час
-
Рецептурный.
Действующее вещество (МНН): Гликопиррония бромид, Индакатерол, Мометазон
Производитель: Новартис Фарма Штейн АГ/ Новартис Фармасьютика С.А.
Забрать в аптеке через час
-
Рецептурный.
Действующее вещество (МНН): Гликопиррония бромид
Производитель: Новартис Фарма Штейн АГ/ Новартис Фармасьютика С.А.
-
Рецептурный.
Действующее вещество (МНН): Беклометазон, Гликопиррония бромид, Формотерол
Производитель: Кьези Фармасьютика Лтда
-
Рецептурный.
Действующее вещество (МНН): Гликопиррония бромид, Индакатерол, Мометазон
Производитель: Новартис Фарма Штейн АГ/ Новартис Фармасьютика С.А.
Нет в наличии
Последняя цена продажи 4 331.00₽
В статье рассмотрено применения гликопиррония бромида в терапии хронической обструктивной болезни легких
Бронхолитики длительного действия занимают центральное место в фармакологическом лечении хронической обструктивной болезни легких (ХОБЛ) стабильного течения [1]. Длительно действующие антихолинергические препараты (ДДАХП), длительно действующие β2-агонисты и их комбинации являются препаратами выбора в современной базисной терапии этого заболевания. Тиотропия бромид длительное время был единственным ДДАХП и остается наиболее изученным лекарственным средством в своем классе. Но в последние годы в этом классе появились 2 других препарата: аклидиния бромид и гликопиррония бромид. Гликопиррония бромид характеризуется наиболее быстрым началом действия, отличаясь при этом более длительным, чем у аклидиния бромида, эффектом и более быстрым временем достижения максимального бронходилатационного эффекта по сравнению с тиотропием (табл. 1) [2].
Фармакокинетика гликопиррония
Бронхоконстрикция в дыхательных путях обусловлена, главным образом, холинергическим тонусом парасимпатической системы. При стимуляции холинергических нервных волокон высвобождается ацетилхолин, который действует на мускариновые рецепторы. В легких присутствуют 3 типа мускариновых рецепторов (М1, М2 и М3). В механизмы бронхоконстрикции вовлечены те М3-рецепторы, которые расположены в гладкомышечных клетках бронхов. Кроме того, M3-рецепторы располагаются в секреторных клетках бронхов, поэтому их стимуляция также обеспечивает секрецию бронхиальной слизи [3].
Гликопирроний обладает значительно более высокой селективностью к М3-холинорецепторам бронхов, чем к М2-холинорецепторам , поэтому оказывает гораздо меньшее влияние на сердечно-сосудистую систему. Способность гликопиррония связываться с М3-рецепторами в 7,8 раза выше, его связи с M2-рецепторами. Кроме того, гликопирроний в 10 раз быстрее диссоциирует с М2-рецепторами, чем с М1 и М3-рецепторами. Это обеспечивает благоприятный фармакологический профиль препарату, его безопасность, в т. ч. в отношении сердечно-сосудистой системы. При этом селективность гликопиррония по отношению к М3-рецепторам по сравнению с М2-рецепторами выше, чем у тиотропия бромида. Также было показано, что гликопирроний более быстро связывается с М3-рецепторами, чем другие ДДАХП, что обусловливает его более быстрое, чем у других ДДАХП, начало действия [4, 5].
При ингаляционном пути введения около половины (52%) ингаляционной дозы гликопиррония депонируется в легких, 4–7% проглатывается и абсорбируется в желудочно-кишечном тракте. Депонированная в легких доля препарата сохраняется там более 3-х суток, медленно абсорбируясь в системный кровоток (период полувыведения составляет 80 ч, или около 3,5 сут). Именно это свойство гликопиррония обеспечивает стабильный пролонгированный бронходилатационный эффект, наблюдаемый при ингаляции 1 раз в сутки. Гликопирроний для базисной терапии ХОБЛ назначается 1 р./сут по 50 мкг ингаляционно через дозирующий порошковый ингалятор Бризхалер® [6].
Программа исследований GLOW
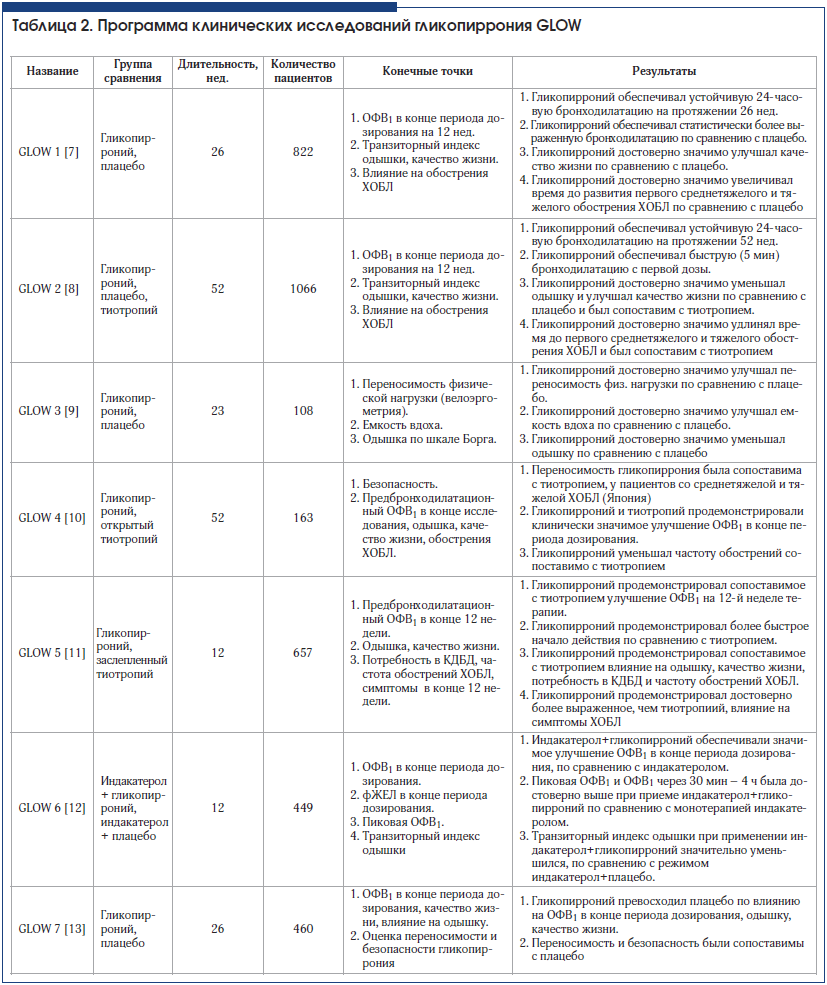
Для оценки эффективности и безопасности гликопиррония, выполнен ряд клинических исследований, объединенных в программу GLOW (GLycopyrronium bromide in COPD airWays). Суммарные данные об этих клинических исследованиях представлены в таблице 2.
В исследовании GLOW 1 оценивали эффективность, безопасность и переносимость лечения гликопирронием в дозе 50 мкг, ингалируемой однократно в сутки в течение 26 нед, по сравнению с плацебо у 822 больных. В исследовании GLOW 2 оценивали эффективность и безопасность гликопиррония в той же дозе в течение 52 нед у 1066 больных по сравнению с плацебо и тиотропием в суточной дозе 18 мкг (который назначался открыто в качестве препарата активного сравнения) [7, 8]. В исследовании GLOW3 изучалось влияние гликопиррония на переносимость физической нагрузки больными среднетяжелой и тяжелой ХОБЛ [9]. Исследование GLOW4 (сравнение гликопиррония и тиотропия) проводилось в течение 1 года и продемонстрировало высокую эффективность и безопасность гликопиррония у пациентов со среднетяжелой и тяжелой ХОБЛ из Японии [10]. В исследовании GLOW5 гликопирроний сравнивался с тиотропием в слепом режиме с двойным плацебо-контролем, оценивались данные спирометрии, показатели качества жизни, одышка, уровень симптомов, потребность в короткодействующих бронходилататорах (КДБД) [11]. Целью исследования GLOW6 являлась оценка эффективности комбинированной терапии гликопирронием и индакатеролом по сравнению с монотерапией индакатеролом по тем же основным критериям, которые применялись в предыдущих исследованиях: объем форсированного выдоха за 1-ю минуту (ОФВ1) в конце периода дозирования, выраженность одышки, качество жизни, потребность в применении КДБД и частота обострений. Было показано, что добавление гликопиррония к индакатеролу достоверно улучшает показатели спирометрии (р<0,01) и уменьшает проявления одышки (р<0,05) [12]. Исследование GLOW7 проводилось на популяции китайских пациентов со среднетяжелым и тяжелым течением ХОБЛ и продемонстрировало эффективность и достоверные преимущества гликопиррония по сравнению с плацебо в отношении показателей легочной функции, одышки и качества жизни при сходных показателях безопасности [13].
Бронхолитическое действие гликопиррония
ХОБЛ характеризуется, как правило, прогрессированием бронхиальной обструкции, что приводит к развитию гиперинфляции легких, которая является основным механизмом формирования одышки при физической нагрузке. Бронхолитическая терапия препаратами длительного действия обеспечивает фармакологическое стентирование бронхов, что приводит к снижению гиперинфляции и нормализации объемов легких, уменьшая легочную симптоматику и улучшая переносимость физической нагрузки. Минимальным клинически значимым приростом в отношении показателя ОФВ1 является его увеличение на 100 мл [14]. Гликопирроний в исследованиях GLOW1 и GLOW2 значительно улучшал показатели спирометрии, демонстрируя, по сравнению с плацебо как статистически значимое улучшение ОФВ1 в конце периода дозирования, так и клинически значимое превосходство уже через 12 нед. терапии, сохраняя эти показатели на протяжении всех 52 нед. терапии (рис. 1). ОФВ1 до ингаляции в группе больных, получавших гликопирроний, через 26 и 52 нед. терапии составил 125 мл и 108 мл соответственно (т. е. более 100 мл), в группе больных на терапии тиотропием этот показатель составил 78 мл и 89 мл соответственно [15, 17].
![Рис. 1. Динамика показателей ОФВ1 в конце периода дозирования при применении гликопиррония и тиотропия бромида по сравнению с плацебо [15] Рис. 1. Динамика показателей ОФВ1 в конце периода дозирования при применении гликопиррония и тиотропия бромида по сравнению с плацебо [15]](https://www.rmj.ru/upload/medialibrary/77a/808-2.png)
Гликопирроний также продемонстрировал более быстрое, по сравнению с тиотропием, начало бронхолитического эффекта (рис. 2): в первый день терапии прирост ОФВ1 через 5 мин в группе гликопиррония составил 87 мл, в группе тиотропия – 45 мл, через 15 мин эти показатели составили 143 мл и 78 мл соответственно (p<0,001 для всех показателей).
При серийных спирографиях наблюдалось статистически значимое превосходство гликопиррония над тиотропием по ОФВ1 через 5, 15, 30 мин, а также через 1 и 2 ч (р<0,05) [8].
Терапия гликопирронием увеличивала емкость вдоха на 97–129 мл (по сравнению с плацебо) через 12–52 нед. терапии (p≤0,01 во всех точках), и эти данные были сопоставимы с аналогичными показателями в группе тиотропия [7, 8]. Остаточный объем через 3 нед. терапии уменьшался в группе гликопиррония по сравнению с плацебо на 490 мл (р<0,05), что свидетельствовало о значительном уменьшении гиперинфляции легких [9].
Влияние гликопиррония на клинические показатели ХОБЛ
Большинство больных ХОБЛ, независимо от тяжести заболевания, имеют сходные симптомы: кашель, отделение мокроты, затруднение дыхания вплоть до развития выраженной одышки. В исследованиях показано, что выраженные симптомы значительно ухудшают прогноз заболевания, уменьшая выживаемость [18]. Наиболее частым симптомом ХОБЛ является одышка. Уменьшение выраженности одышки позволяет улучшить самочувствие пациента и повлиять на прогноз заболевания.
Гликопиррония бромид значительно уменьшал выраженность одышки: транзиторный индекс одышки через 52 нед. терапии повысился по сравнению с плацебо на 1,04 балла (р<0,001) [7]. Минимальное клинически значимое улучшение транзиторного индекса одышки составляет 1 балл [14], т. е. уменьшение одышки на фоне терапии гликопирронием было не только статистически, но и клинически значимым. Кроме того, клинически значимого улучшения по показателям транзиторного индекса одышки при лечении гликопирронием достигали достоверно большее количество пациентов, чем в группе плацебо (p=0,001) [7]. При открытом сравнении гликопиррония с тиотропием оба препарата достоверно статистически значимо уменьшали одышку по отношению к плацебо через 12 нед. (р<0,01 в обеих группах) и через 26 нед. терапии (р<0,05 в обеих группах) [8], при слепом исследовании межгрупповых различий в отношении одышки не выявлено (р=0,385) [11]. Уровень симптомов через 12 нед. терапии при слепом сравнении с тиотропием был достоверно ниже в группе гликопиррония (различие в 0,3 балла; р=0,035) [11].
Лечение гликопирронием практически наполовину уменьшало потребность в КДБД по сравнению с плацебо в исследованиях GLOW1 (p=0,005) и GLOW2 (p<0,05), демонстрируя сопоставимые данные с тиотропием в исследованиях GLOW2 и GLOW5 [7, 8, 11].
Применение гликопиррония достоверно значимо улучшало качество жизни по сравнению с плацебо (p=0,004) [7]. Этот показатель оценивался на основании респираторного опросника госпиталя Святого Георгия. Минимальным клинически значимым различием для этого опросника считается изменение на 4 балла [14]. Число больных, у которых качество жизни улучшилось более чем на 4 балла при лечении гликопирронием, было достоверно выше, чем в группе плацебо (56,8 и 46,3% соответственно, р=0,006) [7]. В исследовании GLOW2 показано, что качество жизни достоверно улучшалось как в группе гликопиррония, так и в группе тиотропия по сравнению с группой плацебо, межгрупповые различия отсутствовали [8].
Влияние гликопиррония на физическую выносливость изучалось в исследовании GLOW3, дизайн которого был специально разработан для изучения этих показателей. Уже в первый день терапии гликопирроний повышал переносимость физической нагрузки на 43,1 с (10%) по сравнению с плацебо. Через 3 нед. терапии время переносимости физической нагрузки увеличилось по сравнению с плацебо на 88,9 с (21%). В этом же исследовании измеряли инспираторную емкость легких и остаточный объем на фоне терапии гликопирронием. В первый день терапии инспираторная емкость по сравнению с плацебо повысилась на 230 мл (р<0,001), а через 3 нед. – на 200 мл (р<0,001). Остаточный объем в первый день терапии уменьшился по сравнению с плацебо на 440 мл (р<0,05), через 3 нед. – на 500 мл (р<0,05) [9]. Увеличение инспираторной емкости легких и уменьшение остаточного объема означает уменьшение динамической гиперинфляции легких, вследствие чего у пациента с ХОБЛ увеличивается переносимость физической нагрузки.
Влияние гликопиррония на обострения ХОБЛ
Со временем при прогрессировании ХОБЛ обострения возникают чаще и отличаются более тяжелым течением [18]. Частые обострения – признак прогрессирования заболевания, что приводит к уменьшению выживаемости пациентов [19]. Профилактика обострений – одна из основных задач поддерживающей терапии ХОБЛ. Значительное снижение риска развития среднетяжелых и тяжелых обострений при лечении гликопирронием по сравнению с плацебо было продемонстрировано в исследованиях длительностью 26 и 52 нед. (снижение на 31% (р=0,023) и 34% (р=0,001) соответственно) [7, 8]. Гликопирроний значительно снижал процент госпитализаций в связи с обострением ХОБЛ в сравнении с плацебо (1,7 и 4,2% соответственно, OR 0,34; p=0,024) [7]. Данные по снижению риска развития обострений при лечении в группах гликопиррония и тиотропия не различались, оба препарата достоверно уменьшали (на 34% (p=0,001) и 39% (p=0,001) соответственно) по сравнению с плацебо риск развития среднетяжелых и тяжелых обострений [8]. Гликопирроний и тиотропий были сопоставимы как по влиянию на те обострения, которые требовали назначения системных кортикостероидов (гликопирроний по отношению к плацебо: OR 0,61, p=0,006; тиотропий по отношению к плацебо: OR 0,62, p=0,021), так и по влиянию на обострения, требовавшие назначения антибактериальных препаратов (гликопирроний по отношению к плацебо: OR 0,69, p=0,026; тиотропий по отношению к плацебо: OR 0,65, p=0,026) [8].
Безопасность гликопиррония
Гликопирроний продемонстрировал хорошую переносимость как в в рандомизированных клинических исследованиях, так и в исследованиях в реальной клинической практике. Частота нежелательных явлений в группе гликопиррония, тиотропия и плацебо была сопоставима. Нежелательные явления наблюдались в группе гликопиррония у 58,44% пациентов, в группе тиотропия – у 56,36%, в группе плацебо – у 63,63% пациентов [20]. Нежелательные явления, специфичные для антихолинергических препаратов, наблюдались при лечении гликопирронием менее чем в 2% случаев [16].
Серьезные нежелательные явления в группе гликопиррония выявлены с меньшей частотой, чем в группах тиотропия и плацебо, и составили 8,2, 15 и 8,6% соответственно. Из них серьезные нежелательные явления, связанные с сердечно-сосудистой системой, наблюдались при лечении гликопирронием, тиотропием и плацебо в 1,3, 0,7 и 1,6% случаях соответственно. Гликопирроний обладает высоким профилем кардиобезопасности, сопоставимым с тиотропием и плацебо. Одно и более нежелательных явлений, связанных с сердечно-сосудистой системой, наблюдались в группах гликопиррония, тиотропия и плацебо у 0,4, 1,1 и 0,2% пациентов соответственно. Нарушения мозгового кровообращения, инфаркт миокарда, внезапная смерть при приеме гликопиррония были зафиксированы у 0,1% пациентов и менее [16]. Совокупный анализ безопасности гликопиррония, включавший в себя 5 клинических исследований (GLOW1, GLOW2, SHINE, GLOW5 и GLOW7) и более 4 тыс. пациентов со среднетяжелым и тяжелым течением ХОБЛ, показал, что в группах гликопиррония, тиотропия и плацебо умерло 0,23, 0,46 и 0,54% больных соответственно [20]. В исследованиях GLOW3, GLOW5 и GLOW6 летальных исходов не было [9, 11, 12].
Ингаляционное устройство Бризхалер®
Гликопирроний выпускается в капсулах для ингаляций, содержимое которых вдыхается пациентом через ингаляционное устройство Бризхалер®, которое относится к порошковым капсульным ингаляторам с низким сопротивлением. Низкое сопротивление позволяет создать необходимую для ингаляции скорость потока у пациентов, независимо от возраста и степени тяжести обструктивных нарушений. Недавнее исследование показало, что даже пациенты с крайне тяжелой обструкцией, а также пациенты старших возрастных групп, при использовании Бризхалера, за счет его низкого сопротивления, способны создать достаточный инспираторный поток на вдохе [21]. Другим важным свойством Бризхалера являются его простота и наглядность, которые обеспечивают полный контроль ингаляции. Пациент слышит, как вращается капсула в Бризхалере, чувствует сладковатый привкус во время ингаляции и видит пустую капсулу в ингаляторе после ингаляции. Тройной контроль ингаляции (слуховой, вкусовой, визуальный) помогает пациенту и врачу убедиться в правильном выполнении ингаляции [22]. Данные по контролю ингаляции в разных ингаляционных устройствах представлены в таблице 3.
Именно простота и легкость в использовании ингалятора способствуют меньшему количеству ошибок при ингаляции и обеспечивают более высокую приверженность длительной базисной терапии. Недавно было проведено исследование в реальной клинической практике, которое показало, что более 50% пациентов допускали ошибки при пользовании ингалятором. В данном исследовании оценка правильности ингаляционного маневра изучалась у 2935 пациентов с ХОБЛ. Было показано, что при использовании Бризхалера меньше всего пациентов допускали критические ошибки (15,4%). При применении дозирующего аэрозольного ингалятора и Респимата критические ошибки допускали 43,8% и 46,9% больных соответственно (рис. 3). Критической ошибкой называется та ошибка при использовании ингалятора, которая влияет на доставленную дозу. В результате регулярных ошибок при ингаляции пациенты систематически не получают достаточную дозу препарата для поддерживающей терапии. Наличие, как минимум, одной критической ошибки при пользовании ингалятором (OR 1,86; p<0,0297) коррелировало с более высокой частотой тяжелых обострений за последние 3 мес. [23]. Таким образом, совершенно очевидно, что неправильное использование ингалятора способствует ухудшению прогноза заболевания. Обучение правильному использованию ингалятора и контроль техники ингаляции способствуют более эффективному лечению, снижению частоты обострений, что значительно улучшает течение заболевания и его прогноз.
Другим немаловажным фактором является количество лекарственного вещества, которое осаждается в легких. В современных дозирующих устройствах, которые появились в последнее время, легочная депозиция длительно действующих холинолитиков достаточно высока и составляет 30–40% (табл. 4). Депозиция гликопиррония через Бризхалер® составляет 39% [25], практически такая же депозиция (около 40%) у тиотропия, доставляемого через Респимат® [24].
Но пожалуй, самым важным в постоянной поддерживающей терапии ХОБЛ является приверженность терапии, т. к. пациент, не принимающий базисные препараты регулярно, не получает терапевтического эффекта, что ухудшает течение и прогноз болезни. Поэтому каждому пациенту необходимо подбирать оптимальный ингалятор, которым бы он успешно пользовался на протяжении длительного времени. При этом должны учитываться индивидуальные предпочтения пациента и простота использования ингалятора, т. к. это влияет на приверженность длительной ингаляционной терапии. Удовлетворенность от ингалятора и предпочтения пациентов изучались в недавно опубликованном исследовании, которое проводилось в Испании. Показатели удовлетворенности и предпочтения Бризхалеру и Респимату оценивались с помощью специального опросника (Patient Satisfaction and Preference Questionnaire – PASAPQ), состоявшего из 14 вопросов. Было показано, что общая удовлетворенность при использовании Бризхалера и Респимата была высокой и не различалась в группах пациентов, получавших тот или иной ингалятор. Средний балл по опроснику PASAPQ в группах пациентов, пользовавшихся Бризхалером и Респиматом, составлял 79,9 и 80,7 балла соответственно (различие 0,8 балла, р=0,67) [27].
В другом недавно проведенном исследовании REAL, в которое вошли 764 пациента из 9 стран (Германия, Нидерланды, Франция, Италия, США, Великобритания, Канада, Бразилия, Япония), выявлено, что применению Бризхалера сопутствовала самая высокая приверженность пациентов: среди 764 пациентов с ХОБЛ, приверженность при применении Бризхалера, Респимата, Эллипты и Дженуэйра составляла 90, 70, 65 и 58% соответственно [28]. Такая высокая приверженность, вероятно, объясняется комфортностью вдоха через ингалятор с низким сопротивлением, простотой и полным контролем ингаляции, удовлетворенностью и уверенностью пациента в том, что использована вся доза препарата.
Заключение
Согласно современным рекомендациям по лечению ХОБЛ всем пациентам с выраженными симптомами и/или частыми обострениями показаны длительно действующие антихолинергические препараты и длительно действующие β2-агонисты, которые могут назначаться в виде монотерапии или в комбинации друг с другом. Гликопиррония бромид (группа ДДАХП) одобрен к применению в Российской Федерации в сентябре 2013 г. под торговым названием Сибри® Бризхалер® в дозе 50 мкг 1 р./сут. Для изучения эффективности и безопасности гликопиррония бромида проведены 7 клинических исследований III фазы (программа клинических исследований GLOW), которая включала 3725 пациентов с ХОБЛ среднетяжелого и тяжелого течения.
Клинические исследования показали способность гликопиррония действовать в течении 24 ч, развивая эффект бронходилатации уже через 5 мин, что чрезвычайно важно для пациентов, т. к. позволяет принимать препарат 1 р./сут и ощущать быстрый бронхорасширяющий эффект с первого дня терапии.
Исследования подтвердили эффективность гликопиррония по сравнению с плацебо в улучшении легочной функции, при этом показатели ОФВ1 через 26 и 52 нед., в отличие от тиотропия, достигали не только статистической, но и клинической значимости. Уменьшение одышки, улучшение качества жизни и снижение потребности в применении КДБД было сопоставимо с действием тиотропия. Гликопирроний влиял на показатели легочной гиперинфляции (увеличивал емкость вдоха, уменьшал остаточный объем) и улучшал переносимость физической нагрузки по сравнению с плацебо. Кроме того, гликопирроний достоверно значимо снижал частоту обострений по сравнению с плацебо и был сопоставим в этом отношении с тиотропием.
Гликопирроний продемонстрировал профиль безопасности, сходный с плацебо и тиотропием, как в рандомизированных клинических исследованиях, так и в исследованиях в реальной клинической практике.
Ингаляционное устройство Бризхалер® отличается низким сопротивлением, что позволяет создать необходимую для ингаляции скорость потока, независимо от усилия пациента и степени тяжести обструктивных нарушений. Гликопирроний, ингалируемый через Бризхалер®, обладает высокой легочной депозицией, сопоставимой с депозицией тиотропия через Респимат®. Полный контроль ингаляции (звуковой, вкусовой и визуальный) позволяет пациенту и врачу быть уверенными, что препарат попал в бронхи. Техническая простота ингалятора избавляет пациента от ошибок, повышает его приверженность использованию Бризхалера, что обеспечивет терапевтический эффект.









![Рис. 2. Динамика показателей ОФВ1 после ингаляции гликопиррония и тиотропия по сравнению с плацебо [16] Рис. 2. Динамика показателей ОФВ1 после ингаляции гликопиррония и тиотропия по сравнению с плацебо [16]](https://www.rmj.ru/upload/medialibrary/7db/808-4.png)
![Таблица 3. Возможности контроля ингаляции в различных дозирующих ингаляционных устройствах [22] Таблица 3. Возможности контроля ингаляции в различных дозирующих ингаляционных устройствах [22]](https://www.rmj.ru/upload/medialibrary/90f/808-6.png)
![Рис. 3. Число пациентов с ХОБЛ, допускающих критические ошибки при использовании различных ингаляторов [23] Рис. 3. Число пациентов с ХОБЛ, допускающих критические ошибки при использовании различных ингаляторов [23]](https://www.rmj.ru/upload/medialibrary/5fd/808-5.png)
