Перегрузка железом
Также:
гемохроматоз
Версия: Клинические рекомендации РФ 2018-2020 (Россия)
Категории МКБ:
Нарушения обмена железа (E83.1)
Разделы медицины:
Гематология
Общая информация
Краткое описание
НАЦИОНАЛЬНОЕ ГЕМАТОЛОГИЧЕСКОЕ ОБЩЕСТВО
Рекомендации утверждены на IV Конгрессе гематологов России (апрель 2018г)
НАЦИОНАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ПЕРЕГРУЗКА ЖЕЛЕЗОМ: ДИАГНОСТИКА И ЛЕЧЕНИЕ
Определение
Перегрузка железом (МКБ 10:E83.1– Нарушения обмена железа) – состояние, характеризующееся избыточным накоплением данного микроэлемента в органах и тканях, что сопровождается:
— появлением свободных ионов железа в плазме крови, внеклеточном пространстве и внутри клеток;
— окислительными повреждениями белков и клеточных структур, ведущими к гибели клеток;
— дегенеративно-дистрофическими изменениями и фиброзной трансформацией вовлеченных в процесс органов и тканей;
— необратимыми нарушениями структуры и функций печени, сердца, поджелудочной железы и других органов эндокринной системы.
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 500 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация
В соответствии с основным механизмом развития перегрузки железом (или, синоним – гемохроматоз) выделяют первичные (наследственные) и вторичные (приобретенные) гемохроматозы [4,10].
Наследственный гемохроматоз (НГ) – полисистемное заболевание, в основе которого лежат генетически обусловленные нарушения метаболизма железа, приводящие к его избыточному накоплению в организме и токсическому повреждению органов и тканей [4,10].
В соответствии с установленным генетическим дефектом и характерной клинико-лабораторной картиной заболевания выделяют 4 типа наследственного гемохроматоза [3,4,]:
I тип – наследуется по аутосомно-рецессивному механизму, обусловлен мутациями гена HFE, расположенного на 6 хромосоме. Наиболее часто (у 87-90% больных) регистрируется мутация С282Y – замена цистеина на тирозин в 282-ой аминокислоте. Реже встречается мутация Н63D – замена цитидина на гуанин в 63-ей аминокислоте [4,10];
II тип – ювенильный гемохроматоз встречается редко, обусловлен мутациями гена, ответственного за синтез гепсидина [4,12];
III тип – генетическую основу составляют мутации гена, кодирующего синтез рецептора для трансферрина [4,12,13];
IV тип – генетическую основу составляют мутации гена SLC40A1, кодирующего синтез транспортного белка ферропортина [4,13].
Из 4 представленных типов НГ наиболее распространенным и изученным является тип I (HFE-ассоциированный или классический гемохроматоз).
Вторичная или приобретенная перегрузка железом развивается вследствие многократных трансфузий эритроцитарной массы и/или наличия неэффективного эритропоза, характерного для больных с некоторыми формами наследственных гемолитических анемий (β-талассемия, серповидно-клеточная анемия) и миелодиспластическими синдромами. Каждая трансфузия 250 мл эритроцитной массы, полученная из 420 мл донорской крови, содержит 200 мг железа, которое освобождается макрофагами селезенки и печени и рециркулирует в организме реципиента. Соответственно, после 20 гемотрансфузий содержание железа в организме реципиента увеличивается, по-меньшей мере, вдвое. Избыток железа, не использованный для нужд эритропоэза, доставляется трансферрином в гепатоциты для длительного хранения. Регулярные гемотрансфузии приводят к переполнению железом емкостей трансферрина и клеток печени и, как результат, появлению в плазме крови NTBI, накоплению железа в органах, не предназначенных для хранения запасов железа, в том числе в сердце, что ведет к развитию токсической кардиомиопатии. Последняя проявляется аритмиями, нарушением сократительной способности сердца и служит основной причиной смерти больных большой β-талассемией, с раннего детства получающих регулярные заместительные трансфузии эритроцитной массы. Другими клиническими последствиями посттрансфузионной перегрузки железом являются развитие фиброза/цирроза печени, сахарного диабета и других эндокринопатий [4,12,14].
Этиология и патогенез
Этиология и патогенез
Железо – необходимый микроэлемент, играющий ключевую роль в процессах метаболизма, роста и пролиферации клеток. Вместе с тем, избыточное содержание железа сопряжено с цитотоксическими эффектами, которые обусловлены способностью железа, как металла с переменной валентностью, запускать цепные свободнорадикальные реакции, приводящие к перекисному окислению липидов (ПОЛ) биологических мембран, токсическому повреждению белков и нуклеиновых кислот. Таким образом, как дефицит, так и перегрузка железом имеют катастрофические последствия для организма, поэтому содержание данного микроэлемента жестко регулируется [1,2,3,4,5].
В организме здорового человека содержится около 3 — 5 г железа, из которого большая часть — 2100 мг железа, входит в состав клеток крови и костного мозга. Практически все метаболически активное железо находится в связанном с белками состоянии; свободные ионы железа могут присутствовать в крайне низких концентрациях. В физиологических условиях ежедневно теряется не более 0,05% (< 2,5 мг) от общего количества железа. Эти потери включают железо, удаляющееся со слущивающимся эпителием кожи и желудочно-кишечного тракта, с потоотделением. Столько же (1-2 мг) железа ежедневно всасывается в кишечнике.
Для эритропоэза требуется ежедневно около 20-30 мг железа, тогда как ежедневное поступление пищевого железа из кишечника составляет всего 1-2 мг. Необходимые 20-30 мг железа ежедневно возвращаются в циркуляцию макрофагами селезенки и печени. Этот процесс носит название «рециркуляции железа» и имеет гораздо большее физиологическое значение, чем всасывание железа в кишечнике [1,2,3].
Процессы всасывания, рециркуляции и хранения запасов железа регулируются специальным гормоном – гепсидином, который продуцируется клетками печени. В физиологических условиях продукция гепсидина клетками печени регулируется уровнем железа в крови и степенью оксигенации ткани печени. При патологических условиях продукция гепсидина регулируется провоспалительными цитокинами, из которых главную роль играет интерлейкин-6 [3,6,7]. На экспериментальных моделях и добровольцах было показано, что внутривенное введение провоспалительных цитокинов (ТНФ, ИЛ-6) сопровождается повышением продукции гепсидина с последующим развитием гипоферремии и железодефицитного эритропоэза, а при длительном воздействии повреждающих факторов – развитием анемии, механизм которой идентичен таковому при анемии воспаления (или анемии хронических заболеваний) [1,3,8,9]. В организме человека отсутствуют физиологические механизмы выведения железа, в соответствии с этим нарушение механизмов регуляции гомеостаза железа, избыточное всасывание или парентеральное поступление железа быстро приводят к развитию перегрузки железом [1,6,].
Эпидемиология
Эпидемиология
Распространенность наследственного гемохроматоза (НГ) варьирует от 1 : 250 индивидуумов, проживающих в Северной Европе, до 1 : 3300 — среди черного населения США и стран Африки. При проведении генетического скрининга было установлено, что гомозиготная мутация гена HFE регистрируется у 1 из 500 обследованных, тогда как число клинически установленных случаев НГ составляет 1 : 5 000 [4,10,11]. Таким образом, значительное количество случаев заболевания не распознается или диагностируется поздно, на стадии необратимого поражения внутренних органов (цирроз печени, сахарный диабет, дилатационная кардиомиопатия).
Клиническая картина
Cимптомы, течение
Клинические признаки
Основные клинические проявления перегрузки железом включают [4,10,13]:
— немотивированная слабость, утомляемость, сонливость;
— гиперпигментация кожи;
— признаки поражения печени: немотивированное повышение и/или симптомы портальной гипертензии: асцит, гепатоспленомегалия, кровотечение из варикозно расширенных вен пищевода и желудка;
— симптомы поражения сердца: экстрасистолия, мерцательная аритмия и другие нарушения ритма, нарушение сократительной способности сердца, как проявление токсической кардиомиопатии;
— поражение суставов: упорные артралгии, наиболее часто вовлекаются пястно-фаланговые суставы, реже – коленные, тазобедренные, локтевые; постепенно развивается тугоподвижность суставов;
— развитие сахарного диабета и дисфункции половых желез.
Диагностика
Диагностика
При первичном обследовании больных с подозрением на гемохроматоз рекомендуется обращать внимание на наличие немотивированной слабости, утомляемости, болей в правом подреберье, артралгий, снижение либидо, импотенцию, гиперпигментацию кожи, нарушения ритма сердца, сахарный диабет.
Физикальное обследование
Рекомендуется проводить осмотр, включающий измерение роста и массы тела, оценку состояния кожных покровов и костно-суставной системы; выявление гепатоспленомегалии, признаков дисфункции сердца, легких, печени, органов эндокринной системы.
Лабораторная и инстументальная диагностика
Лабораторные критерии перегрузки железом включают:
— стойкое повышение содержания сывороточного ферритина (свыше 1000 мкг/л) в отсутствии очевидного воспалительного, деструктивного или опухолевого процесса;
— снижение содержания трансферрина в сыворотке крови и ОЖСС,
— повышение коэффициента НТЖ (> 60%)
— повышенная экскреция железа с мочой (спонтанная и индуцированная введением дефероксамина – «десфераловый тест»).
Морфологические критерии:
— повышенное количество сидеробластов в костном мозге,
— отложения гемосидерина в тканях (окраска по Перлсу),
— повышение содержания железа в ткани печени (≥ 3-7 мг/г сухого веса, при норме 0,17-1,8 мг/u)
Радиологические критерии:
— магнитно-резонансная томография печени и сердца по специальной программе Т2* позволяет выявить накопления железа на доклинической стадии.
Лечение
Лечение
Хелаторы – лекарственные препараты, обладающие способностью связывать и выводить из организма избыточное железо. Согласно современной концепции, больные получающие регулярные заместительные трансфузии эритроцитной массы нуждаются в проведении адекватной хелаторной терапии, целью которой служит элиминация потенциально токсичного железа внутри клеток и во внеклеточном пространстве (NTBI), снижение общих запасов железа в организме, что позволит предотвратить токсические эффекты свободного железа [15, 16, 17,18,19].
В Российской Федерации в настоящее время зарегистрирован 1 лекарственный препарат – хелатор железа: деферозирокс (Эксиджад). Деферазирокс является пероральным хелатором железа, период полувыведения которого составляет 8-16 часов, что позволяет принимать данный препарат 1 раз в день. Клинические исследования показали, что деферазирокс способен контролировать токсичный пул лабильного железа плазмы и удалять отложения железа из ткани печени и сердца.
Назначение хелаторной терапии деферазироксом показано в следующих клинических ситуациях:
1) наличие доказанной перегрузки железом у трансфузионно-зависимых больных:
— с наследственной патологией эритрона: талассемия, серповидно-клеточная болезнь и другие редкие формы наследственных гемолитических анемий;
— с миелодиспластическими синдромами (МДС) низкой степени риска (рефрактерная анемия, рефрактерная анемия с кольцевыми сидеробластами, 5q-синдром), с ожидаемой продолжительностью жизни более 1 года;
— апластической анемией;
— первичным миелофиброзом с благоприятным или промежуточным прогнозом;
2) наличие доказанной перегрузки железом у больных гемобластозами или МДС, ожидающих проведение трансплантации аллогенных гемопоэтических клеток.
Дозы и длительность хелаторной терапии
У больных с низкой трансфузионной нагрузкой (<2 единиц эритроцитной массы в месяц) назначение деферазирокса в дозе 20 мг/кг/сут является достаточным для снижения содержания железа в ткани печени. У больных со средней (2-4 единицы/месяц) и высокой (>4 единиц/месяц) трансфузионной нагрузкой эффективными дозами деферазирокса являются 30 мг/кг/сут и 40 мг/кг/сут, соответственно. Выбор начальной дозы деферазирокса определяется терапевтической целью: поддержание нейтрального баланса железа или достижение отрицательного баланса железа, т.е. обеспечение активного выведения железа из организма (рис.1). При снижении СФ до 800-1000 мкг/л рекомендуется снизить дозу препарата до 5-10 мг/кг/сут для сохранения нейтрального баланса железа. В случае снижения СФ <500 мкг/л целесообразно прервать хелаторную терапию, продолжить мониторирование СФ и при его повышении возобновить прием деферазирокса.
Необходимость в проведении хелаторной терапии у трансфузионно-зависимых больных сохраняется до тех пор, пока продолжается гемотрансфузионная терапия и/или пока перегрузка железом остается клинически значимой. Лечение, как правило, хорошо переносится; из побочных эффектов следует отметить желудочно-кишечные расстройства, преходящие кожные высыпания и небольшое повышение уровня сывороточного креатинина. В редких случаях, при назначении высоких доз деферазирокса наблюдается стойкое повышение креатинина, требующее коррекции дозы хелатора.
У больных, ожидающих аллогенную трансплантацию гемопоэтических клеток, хелаторная терапия проводится до момента трансплантации. В посттрансплантационном периоде назначение деферазирокса не рекомендуется, так как в сочетании с иммуносупрессивной терапией существенно возрастает риск токсического повреждения почек.
Рисунок 1. Схема коррекции дозы деферазирокса в зависимости от терапевтической цели (СФ – сывороточный ферритин; LIC – содержание железа в ткани печени)
Мониторинг показателей, отражающих степень перегрузки железом
Для контроля эффективности хелаторной терапии необходимо мониторировать показатели, отражающие степень перегрузки железом. Наиболее доступным является определение сывороточных показателей метаболизма железа — ферритина, ОЖСС, НТЖ.
Кратность определения этих показателей – ежемесячно в ходе подбора дозы хелатора, далее каждые 3-6 месяцев в зависимости от терапевтической цели.
Мониторинг содержания железа в печени и сердце проводится с помощью МРТ в режиме Т2* с частотой 1 раз в год у больных с умеренной и тяжелой перегрузкой железа.
По показаниям проводятся исследование костного мозга и биопсия печени с последующими морфологическими и гистохимическими исследованиями, а также количественным анализом содержания железа в ткани печени (при тяжелой перегрузке железом – ежегодно).
С целью контроля безопасности хелаторной терапии необходимо проводить следующие исследования:
- креатинин сыворотки – дважды до начала терапии деферазироксом и далее ежемесячно;
- содержание белка в моче (общий анализ мочи) – ежемесячно;
- активность АЛТ, АСТ – ежемесячно;
- контроль зрения и слуха – до начала хелаторной терапии и далее ежегодно;
- рост и масса тела – ежегодно у пациентов до 18 лет.
Хелаторная терапия у детей
Принципы хелаторной терапии у детей аналогичны таковым у взрослых. Начальная доза дефероксамина у детей составляет 20-30 мг/кг/сут. Учитывая влияние данного лекарственного препарата на рост ребенка, начало лечения возможно в возрасте старше 3 лет, при этом необходимо тщательно контролировать рост ребенка. В случае замедления темпов роста необходимо снизить дозу дефероксамина или перейти на деферазирокс, который может использоваться у детей старше 2 лет. Начальная доза деферазирокса у детей составляет 20 мг/кг/сут внутрь. При необходимости доза может быть постепенно (с шагом 5 мг/кг/сут) повышена до максимальной, составляющей 40 мг/кг/сут. Контроль эффективности и безопасности хелаторной терапии проводится в соответствии с теми же принципами, что и у взрослых.
Информация
Источники и литература
-
Клинические рекомендации Национального гематологического общества
- 1. Sussman H.H. Iron in cancer. Pathobiology. 1992, 60, p. 2-9.
2. Finch C.A., Huebers H.A. Iron metabolism. Clin. Physiol.Biochem. 1986, 4, p. 5-15.
3. Лукина Е.А., Деженкова А.В. Метаболизм железа в норме и при патологии // Клиническая онкогематология – 2015. – №4. – С.355-361
4. Adams PC. Hemochromatosis. Clin Liver Dis 8: 735-753, 2004.
5. Cabantchik Z. Y., Brener W, Zanninelili G. LPY-labile plasma iron in iron overload. Best Pract Res Clin Haematol 18: 277-287, 2005.
6. Denz H., Orth B., Huber P. at al. Immune activation and anemia of chronic disorders. Blood. 1993, 81, p. 1404-1409.
7. Ganz T. Hepcidin – a regulator of intestinal iron absorption and iron recycling by macrophages. Best Pract Res Clin Haematol 18: 171-182, 2005.
8. Ilickstein H, El R. B., Shvartsman M, Cabantchik Z. Y. Intracellular labile iron pools as direct targets of iron chelators: a fluorescence study of chelator action in living cells. Blood 106: 3242-3250, 2005.
9. Means R.T,, Krantz S.B. Progress in understanding the pathogenesis of anemia of chronic disease. Blood, 1992, 80, 1639-1644.
10. Kuntz E., Kuntz H-D. Haemochromatosis. In: “Hepatology — Principles and Practice”. 2002, Springer-Verlag Berlin, p.556-565.
11. Mims MP, Guan Y, Pospisilova D, et al. Identification of a human mutation of DMT 1 in a patient with microcytic anemia and iron overload. Blood 103: 1337-1342, 2005.
12. Ponka P. Tissue-specific regulation of iron metabolism and heme synthesis: distinct control mechanisms in erythroid cells. Blood 89: 1-25, 1997.
13. Porter J.B. Monitoring and treatment of iron overload: state of the art and new approaches. Sem.Hematol. 2005. v.42, 2, suppl. 1, p.14-18.
14. Roetto A, Camaschella C. New insights into iron homeostasis through the study of non-HFE hereditary haemochromatosis. Best Pract Res Clin Haematol 18: 235-250, 2005 15. Sarigianni M, Liakos A, ,Vlachaki E, Paschos P. et al. Accuracy of magnetic resonance imaging in diagnosis of liver iron overload: a systematic review and meta-analysis. Clin Gastroenterol Hepatol. 2015 Jan;13(1):55-63.e5. doi: 10.1016/j.cgh.2014.05.027. Epub 2014 Jun 30
16. Xia S, Zhang W, Huang L, Jiang H. Comparative efficacy and safety of deferoxamine, deferiprone and deferasirox on severe thalassemia: a meta-analysis of 16 randomized controlled trials. PLoS One. 2013 Dec 23;8(12):e82662. doi: 10.1371/journal.pone.0082662.
17. Maggio A, Filosa A, Vitrano A, et al. Iron chelation therapy in thalassemia major: a systematic review with meta-analyses of 1520 patients included on randomized clinical trials. Blood Cells Mol Dis. 2011 Oct 15;47(3):166-75. doi: 10.1016/j.bcmd.2011.07.002.
18. Taher A, Cappellini MD, Vichinsky E, et al. Efficacy and safety of deferasirox doses of >30 mg/kg per d in patients with transfusion-dependent anaemia and iron overload. Br J Haematol. 2009 Dec;147 (5):752-9. doi: 10.1111/j.1365-2141.2009.07908.x.
19. Bollig C1, Schell LK, Rücker G, et al. Deferasirox for managing iron overload in people with thalassaemia. Cochrane Database Syst Rev.2017, Aug.,15;8, CD007476 doi: 10.1002/14651858.CD007476.pub3.
- 1. Sussman H.H. Iron in cancer. Pathobiology. 1992, 60, p. 2-9.
Информация
Коллектив авторов под руководством академика В.Г. Савченко
Авторы и эксперты:
Лукина Е.А.1, д.м.н., профессор, зав. отделением орфанных заболеваний
Сметанина Н.С. 2, д.м.н. профессор, зам. Директора
Цветаева Н.В.1, к.м.н., ведущий научный сотрудник
Михайлова Е.А.1 д.м.н., профессор, ведущий научный сотрудник
Сысоева Е.П.1, к.м.н., старший научный сотрудник
1. ФГБУ «Национальный медицинский исследовательский центр гематологии» Минздрава России, Москва
2. ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Минздрава России, Москва
Рекомендации обсуждены на заседании Проблемной комиссии по гематологии (март 2018г).
Список сокращений
НГ — наследственный гемохроматоз
НТЖ – насыщение трансферрина железом
ОЖСС – общая железосвязывающая способность сыворотки
ПОЛ — перекисное окисление липидов
ТНФ — фактор некроза опухоли
ИЛ-6 – интерлейкин 6 Ген HFE — ген, кодирующий структуру белка наследственного гемохроматоза 1 типа ЭКГ – электрокардиограмма УЗИ – ультразвуковое исследование
АЧТВ – активированное частичное тромбопластиновое время
МРТ – магнитно-резонансная томография
КТ – компьютерная томография
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Гемохроматоз — это заболевание, при котором в организме накапливается слишком много железа, что может привести к повреждению органов и тканей.
Наиболее распространен I тип гемохроматоза, что обусловливает необходимость молекулярно-генетической диагностики. Он часто имеет семейную историю. Многие люди с наследственным гемохроматозом не знают, что он у них есть.
Чтобы оценить полученные результаты вы можете дополнить анализ Заключением врача-генетика.
Вы также можете сдать комплекс Лабораторная диагностика гемохроматоза, чтобы выявить перегрузку организма железом и оценить состояние печени.
Вам подойдет этот анализ, если у вас есть:
- повышенные показатели сывороточных железа и ферритина
- усталость, слабость
- непонятные боли в мышцах и суставах
- тяжесть в правом подреберье
- потеря сексуального интереса
- снижение веса и другие.
Метод исследования — ПЦР в режиме реального времени (Real-Time PCR)
Материал для исследования
— Венозная кровь с ЭДТА
Срок исполнения
Анализ будет готов в
течение 3 дней, исключая субботу, воскресенье и день забора.
Срок может быть увеличен на 1 день в случае необходимости.
Вы получите результаты на эл. почту сразу по готовности.
Как подготовиться
Накануне
За 24 часа до взятия крови:
- Ограничьте жирную и жареную пищу, не принимайте алкоголь.
Не менее 4х часов до сдачи крови не принимайте пищу, пейте только чистую негазированную воду.
В день сдачи
Перед забором крови
- 60 минут не курить,
- 15-30 минут находиться в спокойном состоянии.
Результат
Пример результата анализа.pdf
Расшифровка
Интерпретация результатов анализов носит информационный характер, не является диагнозом и не
заменяет консультации врача. Референсные значения могут отличаться от указанных в
зависимости от используемого оборудования, актуальные значения будут указаны на бланке
результатов.
Более 80% случаев гемохроматоза вызвано гомозиготной по гену C282Y мутацией или смешанной C282Y/H63D гетерозиготной мутацией.
Гемохроматоз — это заболевание, при котором в организме накапливается слишком много железа, что может привести к повреждению органов и тканей.
Наследственный гемохроматоз чаще всего вызывается некоторыми вариантами гена HFE на 6-й хромосоме и часто имеет семейную историю. Этот I тип гемохроматоза наследуется по аутосомно-рецессивному пути. Однако многие люди с наследственным гемохроматозом не знают, что он у них есть. У большинства людей с наследственным гемохроматозом никогда не развиваются симптомы или осложнения.
Ранние симптомы гемохроматоза, такие как чувство усталости или слабости, являются общими и могут привести к путанице с множеством других заболеваний.
Наследственный гемохроматоз I типа — не единственный вариант гемохроматоза. Другие типы включают:
Ювенильный гемохроматоз или II тип, обусловлен мутациями гена, ответственного за синтез белка метаболизма железа – гепсидина. Вызывает у подростков те же проблемы, что и наследственный гемохроматоз у взрослых. Но накопление железа начинается намного раньше, и симптомы обычно появляются в возрасте от 15 до 30 лет.
Неонатальный гемохроматоз. При этом тяжелом заболевании железо быстро накапливается в печени плода в утробе матери. Считается, что это аутоиммунное заболевание, при котором организм атакует сам себя.
Гемохроматоз III типа обусловлен мутацией гена, кодирующего синтез рецептора для трансферрина, а IV типа – мутацией гена SLC40A1, кодирующего синтез транспортного белка ферропортина.
Вторичный гемохроматоз. Эта форма заболевания не передается по наследству и ее часто называют перегрузкой железом. Людям с определенными видами анемии или заболеваниями печени часто может потребоваться многократное переливание крови. Это может привести к избыточному накоплению железа.
Гемохроматоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Гемохроматоз (перегрузка железом, пигментный цирроз, бронзовый диабет) – заболевание, связанное с накоплением в организме высоких, патологических уровней железа. Такое состояние приводит к нарушению функционирования органов и тканей организма. «Лишнее» железо накапливается в клетках, в результате чего клетки гибнут и замещаются фиброзной тканью.
В наибольшей степени от гемохроматоза страдают сердце, печень, поджелудочная железа, щитовидная железа, кожа, суставы.
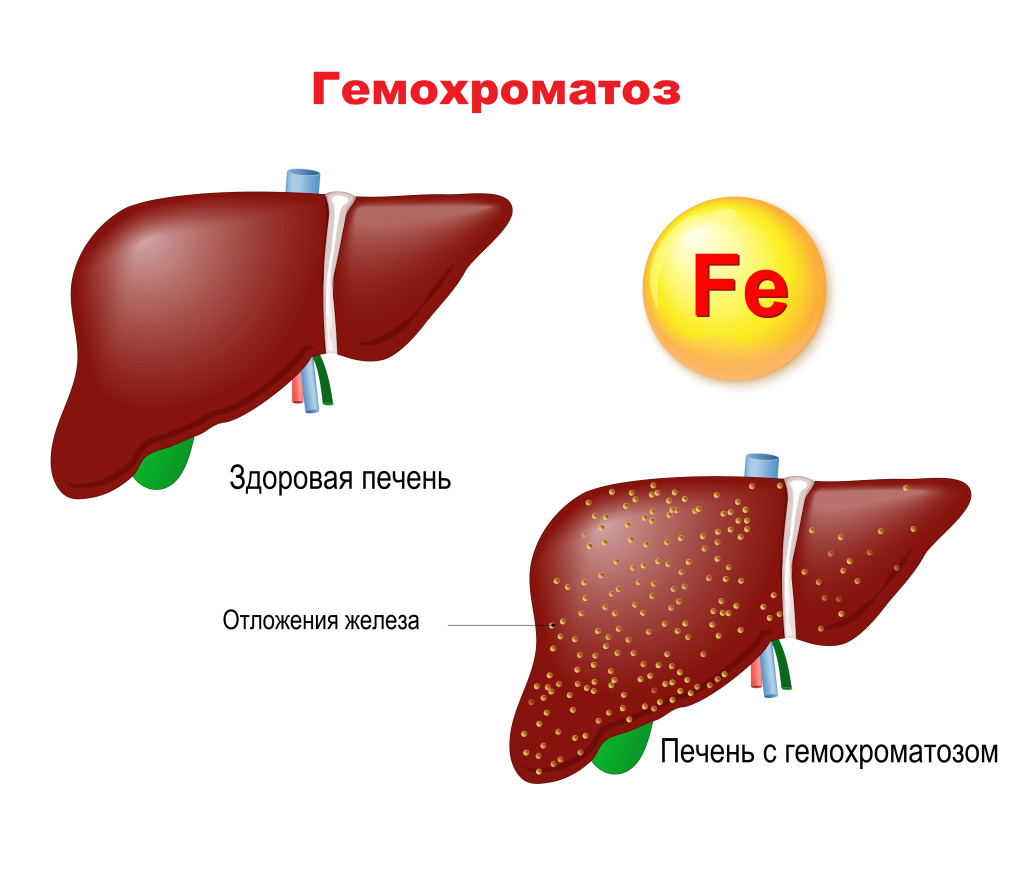
Причины появления гемохроматоза
Гемохроматоз может манифестировать в результате нескольких причин:
- врожденный гемохроматоз, наследственный;
- вторичный гемохроматоз:
- гемохроматоз, вызванный заболеваниями крови (железодефицитной анемией, талассемией, гемолитической анемией, апластической анемией и т.д.),
- гемохроматоз у пациентов, которым неоднократно на протяжении длительного времени переливали эритроцитарную массу,
- гемохроматоз, вызванный чрезмерным потреблением препаратов железа,
- гемохроматоз на фоне болезней печени,
- гемохроматоз на фоне нарушений метаболических процессов в организме.
Классификация заболевания
В соответствии с основным механизмом развития выделяют первичные (наследственные) и вторичные (приобретенные) гемохроматозы, развивающиеся в результате избыточного поступления железа в организм (при частых повторных гемотрансфузиях, неконтролируемом приеме препаратов железа, талассемии, некоторых видах анемии, кожной порфирии, алкогольном циррозе печени, хронических вирусных гепатитах В и С, злокачественных новообразованиях, низкобелковой диете).
Наследственный гемохроматоз – мультисистемное заболевание, в основе которого лежат генетически обусловленные нарушения обмена железа, приводящие к его избыточному накоплению в организме и токсическому повреждению органов и тканей.
В соответствии с установленным генетическим дефектом и характерной клинико-лабораторной картиной заболевания выделяют 4 типа наследственного гемохроматоза:
1-й тип – наследуется по аутосомно-рецессивному механизму, обусловлен мутациями гена HFE, расположенного на 6-й хромосоме;
2-й тип – ювенильный гемохроматоз (встречается редко) – мутации расположены в гене НАМР, ответственном за синтез гепсидина в печени;
3-й тип – генетическую основу составляют мутации гена, кодирующего синтез рецепторов трансферрина;
4-й тип – аутосомно-доминантный гемохроматоз – генетическую основу составляют мутации гена, кодирующего синтез транспортного белка ферропортина.
Гемохроматоз проходит 3 клинические стадии:
1-я стадия – без перегрузки железом;
2-я стадия – с перегрузкой железом, но без клинических симптомов;
3-я стадия – с развитием клинических проявлений.
Симптомы гемохроматоза
На начальной стадии на протяжении ряда лет преобладают жалобы на выраженную слабость, быструю утомляемость, снижение половой функции у мужчин. Может отмечаться боль в правом подреберье, сухость кожи.
Развернутая стадия заболевания характеризуется классической триадой: пигментацией кожи и слизистых оболочек (меланодермией), циррозом печени и диабетом.
Степень выраженности пигментации зависит от давности процесса. Бронзовый, дымчатый оттенок кожи более заметен на лице, шее, руках, на ранее пигментированных местах, в подмышечных впадинах, на половых органах.
У большинства пациентов железо в первую очередь откладывается в печени, поэтому ее увеличение наблюдается почти у всех больных.
Развиваются различные типы эндокринопатий: снижение функций гипофиза, эпифиза, надпочечников, щитовидной железы, половых желез. В результате поражения гипофиза при гемохроматозе страдает половая функция: у мужчин развивается атрофия яичек, импотенция, гинекомастия (избыточное развитие молочных желез); у женщин прекращаются менструации или нарушается менструальный цикл.
Очень часто на фоне гемохроматоза манифестирует сахарный диабет.
Отложение избыточного количества железа приводит к клиническим проявлениям поражения сердца: больные жалуются на нарушение ритма сердца, боль в грудине, постепенно развивается сердечная недостаточность, проявляющаяся одышкой и отеками ног.
Присоединяется поражение суставов: упорная боль в суставах (артралгия) кистей, реже – коленных, тазобедренных, локтевых. Постепенно развивается тугоподвижность суставов.
Диагностика гемохроматоза
Ранняя диагностика гемохроматоза позволяет повысить эффективность терапии и избежать осложнений. Поэтому врачу следует быть крайне внимательным при сборе анамнеза и осмотре пациента, а при малейшем подозрении на гемохроматоз назначить необходимые лабораторные обследования.
- Сывороточный ферритин – повышение этого показателя в отсутствии очевидного воспалительного, деструктивного или опухолевого процесса может свидетельствовать о гемохроматозе.
Ферритин (Ferritin)
Синонимы: Анализ крови на ферритин; Депонированное железо; Индикатор запасов железа. Serum ferritin.
Краткая характеристика определяемого вещества Ферритин
Ферритин &n…
Трансферрин (Сидерофилин, Transferrin)
Синонимы: Переносчик железа; Сидерофилин. Siderophilin, Transferrin; Tf.
Краткая характеристика определяемого вещества Транферрин
Транферрин – плазменный бел�…
Железо, моча (Iron, urine; Fe)
Жизненно важный элемент. Данное исследование входит в состав Профиля:
МЭ 4 Эссенциальные (жизненно необходимые) и токсичные микроэлементы в моче
См. также о�…
Наследственный гемохроматоз, I тип. HFE
Данное исследование предназначено для выявления наиболее частых мутаций в гене HFE, ответственном за развитие наследственного гемохроматоза 1 типа. Исследование …
Билирубин общий (Bilirubin total)
Синонимы: Общий билирубин крови; Общий билирубин сыворотки.
Totalbilirubin; TBIL.
Краткая характеристика определяемого вещества Билирубин общий
Билирубин – это пигм…
Глюкоза (в крови) (Glucose)
Материал для исследования
Сыворотка или плазма крови. Если нет возможности центрифугировать пробу через 30 минут после взятия для отделения сыворотки/плазм…
Глюкоза (суточная моча) (Glucose)
Показатель нарушений углеводного обмена.
Глюкоза относится к так называемым пороговым веществам, это означает, что она начинает выделяться с мочой тольк…
Лабораторная диагностика гемохроматоза дополняется инструментальными исследованиями:
- рентгенография пораженных суставов,
ЭКГ без расшифровки
ЭКГ представляет собой исследование, в основе которого — регистрация биопотенциалов сердца. Применяется для диагностики функциональной активности миокарда.
Эхокардиография
Исследование, позволяющее оценить функциональные и органические изменения сердца, его сократимость, а также состояние клапанного аппарата.
Гемохроматоз необходимо дифференцировать с патологиями крови (талассемией, сидеробластной анемией, поздней кожной порфирией), заболеваниями печени (алкогольным поражением печени, хроническим вирусным гепатитом, неалкогольным стеатогепатитом).
К каким врачам обращаться
Диагностикой и лечением гемохроматоза занимается врач-гематолог.
В некоторых случаях могут быть рекомендованы консультации
эндокринолога
,
кардиолога
, окулиста,
гастроэнтеролога
.
Лечение гемохроматоза
Основная цель терапии – удаление избытка железа из организма и недопущение развития осложнений. Больным с гемохроматозом назначают диету, предусматривающую ограничение пищевых продуктов с высоким содержанием железа (яблок, мяса, печени, гречневой крупы, шпината и пр.), легкоусвояемых углеводов. Запрещается прием мультивитаминных комплексов, аскорбиновой кислоты, а также БАД, содержащих железо. Для выведения избытков железа из организма прибегают к кровопусканиям под контролем показателей гемоглобина, гематокрита крови, ферритина. С этой же целью могут использоваться плазмаферез, гемосорбция, цитаферез.
Основная медикаментозная терапия гемохроматоза основана на внутримышечном или внутривенном введении хелаторов – лекарственных препаратов, обладающих способностью связывать и выводить из организма избыточное железо.
Одновременно проводится лечение сопутствующих патологий: цирроза печени, сердечной недостаточности, сахарного диабета, гипогонадизма.
Осложнения
На последней стадии гемохроматоза у пациентов развиваются портальная гипертензия, асцит, диабетическая кома, асептический перитонит, рак печени, печеночная недостаточность.
Профилактика гемохроматоза
При наследственном гемохроматозе профилактика сводится к проведению семейного скрининга.
Профилактика вторичного гемохроматоза может осуществляться за счет ограничения продуктов, содержащих значимые дозы железа, приема железосодержащих препаратов только по рекомендации врача, своевременного лечения болезней печени.
Источники:
- Клинические рекомендации «Перегрузка железом / гемохроматоз». Разраб.: Национальное гематологическое общество. – 2018.
- Соловьева А.В., Кодякова О.В., Никитина И.Н. и др. Клинический случай наследственного гемохроматоза// Казанский медицинский журнал. – 2018; 99 (6): 998–1003.
- Волошина Н.Б., Осипенко М.Ф., Литвинова Н.В., Волошин А.Н. Гемохроматоз – современное состояние проблемы // Терапевтический архив. – 2018. – № 3. – С. 107-111. doi.org/10.26442/terarkh2018903107-112
- Циммерман Я.С. Первичный (наследственный) гемохроматоз // Клиническая медицина. – 2017. – № 6. – С. 513-518.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы — 19 лет
Поделитесь этой статьей сейчас
Рекомендации
-
5900
26 Апреля
-
5935
26 Апреля
-
5921
26 Апреля
Похожие статьи
Гингивит
Гингивит: причины появления, симптомы, диагностика и способы лечения.
Жировая дистрофия
Жировая дистрофия: причины появления, симптомы, диагностика и способы лечения.
Бесплодие мужское
Бесплодие мужское: причины появления, симптомы, диагностика и способы лечения.
Цистит
Цистит – это воспаление слизистой оболочки мочевого пузыря, встречающееся, по данным медицинской статистики, у 35% лиц в возрасте до 45 лет. Чаще заболевание диагностируется у женщин, чем у мужчин, что объясняется анатомическими особенностями строения мочеполовой системы.
Наследственный гемохроматоз: определение болезни
Наследственный, или первичный, гемохроматоз (бронзовый диабет, пигментный цирроз печени) — редкое генетическое заболевание, при котором железа в организме становится слишком много и оно постепенно разрушает внутренние органы, кожу и суставы.
Заболевание встречается у 1 из 300–500 человек. Чтобы болезнь проявилась, человек должен унаследовать определённую генетическую мутацию от обоих родителей.
Гемохроматоз распространён среди населения Северной Европы, особенно у ирландцев, поэтому его называют кельтской болезнью.
Избыток железа в организме может проявляться по-разному: одни пациенты чувствуют постоянную усталость, боль в животе или суставах, другие замечают, что кожа приобрела бронзовый оттенок, появилась пигментация или возникли проблемы с сексуальным влечением.
Классический пациент с наследственным гемохроматозом — мужчина 40–60 лет с жалобами на повышенную утомляемость, снижение либидо, выпадение волос на теле, боль в суставах, пигментацию кожи.
У мужчин заболевание встречается в 2–3 раза чаще и проявляется в 40–60 лет, у женщин — после менопаузы
Диагноз ставят на основании повышенного уровня ферритина, железа, трансферрина, а также аномально высокой активности печёночных ферментов. Для подтверждения используют генетическое тестирование. Лечат заболевание с помощью препаратов, помогающих выводить железо из организма, и флеботомии — терапевтического кровопускания.
Код по МКБ
В Международной статистической классификации болезней и проблем, связанных со здоровьем, десятого пересмотра (МКБ-10) гемохроматоз обозначают кодом Е83.1 («Нарушения обмена железа», «Гемохроматоз»).
Причины болезни
Первичный гемохроматоз развивается из-за мутаций некоторых генов (преимущественно HFE, реже — HJV, HAMP, TFR2, SLC40A1), ответственных за усвоение железа и удаление его избытка из организма.
Ежедневно с пищей человек получает не только белки, жиры, углеводы и витамины, но и многие металлы, а также другие микроэлементы, которые обеспечивают жизненно важные функции. Железо участвует в кроветворении, кислородном обмене, влияет на состояние кожи, ногтей, волос.
Железо содержится в красном мясе, субпродуктах, яйцах, бобовых, злаках и орехах.
Метаболизм железа устроен так, что скорость его поступления и выведения регулируется в соответствии с потребностями организма. Этот процесс запрограммирован генетически, то есть заложен при рождении.
В норме обмен железа в организме контролирует белок гепсидин. Если железа поступает слишком много, гепсидин тормозит его всасывание в кишечнике и поступление в кровь. Эффективность работы белка определяется геном HFE.
Из-за мутаций в гене у некоторых людей гепсидин не работает совсем или работает с нарушениями. В результате железо накапливается во внутренних органах и разрушает их.
Гемохроматоз — это наследственное генетическое заболевание, которое передаётся по аутосомно-рецессивному типу. Это означает, что оба родителя выступают носителями генетической мутации (как правило, бессимптомными) и передают её ребёнку, у которого и проявляется патология.
Кроме первичного, или наследственного, встречается вторичный гемохроматоз. Он развивается из-за избыточного поступления железа в организм. Так бывает при продолжительном неконтролируемом приёме препаратов железа, частых переливаниях крови, некоторых видах анемии, хронических заболеваниях печени (вирусные гепатиты B и C, алкогольный цирроз), злокачественных новообразованиях.
Классификация
В зависимости от гена, в котором произошла мутация, выделяют 5 типов наследственного гемохроматоза.
Типы наследственного гемохроматоза:
- тип 1 — мутации в гене HFE;
- тип 2 — мутации в генах HJV и HAMP;
- тип 3 — мутации в гене TFR2;
- тип 4 — мутации в гене SLC40A1;
- тип 5 — мутации в гене церулоплазмина (CP).
Наследственный гемохроматоз 1-го типа
Классический наследственный гемохроматоз, также называемый HFE-связанным гемохроматозом. Более 80% случаев заболевания вызвано мутацией C282Y в гене гепсидина (HFE) или смешанной мутацией C282Y/H63D.
Такая форма болезни редко возникает у чернокожих людей и людей азиатского происхождения.
Наследственный гемохроматоз 2-го типа
Гемохроматоз 2-го типа вызывается мутациями в гене гемоювелина (HJV) или гепсидина (HFE). Чаще всего развивается в подростковом возрасте, поэтому его называют ювенильным.
Наследственный гемохроматоз 3-го типа
Вызван мутацией в гене рецептора трансферрина (TFR2), который контролирует насыщение транспортного белка трансферрина железом.
Наследственный гемохроматоз 4-го типа
Гемохроматоз 4-го типа также называют ферропортиновой болезнью, потому что он возникает из-за мутаций в гене ферропортина (SLC40A1). Встречается в основном у людей южноевропейского происхождения.
Наследственный гемохроматоз 5-го типа
Возникает из-за мутаций в гене церулоплазмина (CP), регулирующем выработку транспортного белка церулоплазмина, который участвует в метаболизме железа. Гемохроматоз этого типа также называют ацерулоплазминемией.
|
Тип |
Название болезни |
Мутировавший ген |
Симптомы |
|
1 |
Классический гемохроматоз |
HFE (гепсидин) |
Типичные: повышенная утомляемость, боль в животе и суставах, бронзовый оттенок кожи |
|
2A |
Ювенильный гемохроматоз |
HJV (гемоювелин) |
Появление типичных симптомов в возрасте до 30 лет |
|
2B |
Ювенильный гемохроматоз |
HFE (гепсидин) |
Появление типичных симптомов в возрасте до 30 лет |
|
3 |
Гемохроматоз |
TFR2 (рецептор трансферрина 2-го типа) |
Типичные: повышенная утомляемость, боль в животе и суставах, бронзовый оттенок кожи |
|
4 |
Ферропортиновая болезнь |
SLC40A1 (ферропортин) |
Типичные: повышенная утомляемость, боль в животе и суставах, бронзовый оттенок кожи |
|
5 |
Ацерулоплазминемия |
CP (церулоплазмин) |
Симптомы анемии: слабость, бледность кожи, дрожание рук, головная боль |
Развитие болезни
Из-за мутаций в гене HFE у некоторых людей белок гепсидин, который в норме регулирует обмен железа в организме, не работает совсем или работает с нарушениями. В результате при избытке железа белок не замедляет усвоение микроэлемента и он в большом количестве попадает в кровь, накапливается во внутренних органах (прежде всего в печени, поджелудочной железе, сердце и головном мозге, а также в коже и суставах), разрушая их.
Перегрузка железом при гемохроматозе, не связанном с HFE, развивается по тому же принципу: из-за сбоя в работе генов увеличивается всасывание металла из желудочно-кишечного тракта. В результате железо хронически накапливается в тканях.
В большинстве случаев повреждение тканей возникает из-за воздействия не самого железа, а свободных радикалов — агрессивных молекул, которые образуются в процессе окисления металла в организме.
Симптомы
На ранних стадиях болезни симптомы обычно отсутствуют. Со временем могут появиться неспецифические проявления: хроническая усталость и слабость.
В норме содержание железа в организме женщины составляет 2,5 г, мужчины — 3,5 г. Первые симптомы гемохроматоза могут возникнуть, только когда его уровень в крови становится чрезмерным (более 10 г).
Выраженные симптомы наследственного гемохроматоза обычно появляются у людей старше 40 лет и зависят от места накопления железа. Так, если микроэлемент откладывается в печени, то человек чувствует ноющую боль в правом подреберье. Она возникает из-за увеличения органа в размерах.
Распространённые симптомы наследственного гемохроматоза:
- боль и скованность в суставах,
- нарушения ритма сердца,
- пигментация или бронзовый оттенок кожи,
- импотенция и потеря сексуального влечения у мужчин,
- нарушения менструального цикла,
- частые переломы.
Кроме того, из-за токсического поражения органов железом могут возникнуть заболевания щитовидной железы (гипотиреоз) и патологии обмена веществ (сахарный диабет), онкологические заболевания (рак печени).
Осложнения
Осложнения болезни связаны с длительным накоплением железа в органах и тканях.
Цирроз печени — постепенное замещение нормальной ткани жёсткой фиброзной (соединительной). Может длительно развиваться бессимптомно, пока работа печени не нарушится настолько, что орган не сможет выполнять свои функции. В этом случае человек отмечает отёки, скопление жидкости в брюшной полости. Нарушается процесс свёртывания крови, из-за этого развиваются кровотечения или тромбозы.
Сахарный диабет формируется из-за отложения излишка железа в поджелудочной железе. Это мешает нормальной работе органа, ухудшает процесс обмена углеводов.
В результате поражения гипофиза при наследственном гемохроматозе страдает половая функция: у мужчин развивается атрофия яичек, импотенция, у женщин — нарушения менструального цикла, бесплодие.
Без лечения пациенты с наследственным гемохроматозом могут умереть из-за тяжёлой печёночной недостаточности, острой сердечной недостаточности, диабетической комы, сепсиса.
Диагностика
Из-за того что заболевание может длительно развиваться бессимптомно, патологию редко удаётся диагностировать на ранних стадиях, когда поражение органов минимально.
Поздние симптомы гемохроматоза неспецифичны, поэтому врач может предполагать что угодно: от отравления тяжёлыми металлами до гепатита С. Точный диагноз можно поставить только по результатам лабораторных анализов, молекулярно-генетического тестирования и инструментальных обследований.
Когда стоит обратиться к врачу
Если появились беспричинные боли в верхней части живота (особенно справа), общая слабость, желтушность и зуд кожи, следует как можно скорее записаться на консультацию к врачу-терапевту, гастроэнтерологу или гепатологу. Диагностикой и лечением детей с гемохроматозом занимается врач-педиатр.
Обратиться к специалисту стоит, если начали подрагивать руки, сбивается ритм сердца, возникают проблемы с сексуальным влечением. Как правило, с такими симптомами рекомендуется прийти на консультацию к врачу-терапевту.
Кроме того, у людей с гемохроматозом нарушается работа поджелудочной железы. В результате может развиться сахарный диабет. В этом случае человек будет чувствовать постоянную сильную жажду, слабость, частые позывы к мочеиспусканию. Такие симптомы — повод как можно скорее обратиться к врачу.
Осмотр
Во время осмотра врач выслушает жалобы, уточнит важные детали истории болезни и проведёт обследование кожи, слизистых оболочек, проверит рефлексы, силу мышц, чувствительность, состояние вестибулярного аппарата.
При наследственном гемохроматозе может обнаруживаться желтушность кожи и белков глаз, незначительное или умеренное увеличение печени и селезёнки.
Лабораторная диагностика
Чтобы оценить общее состояние здоровья, выявить нарушения со стороны системы крови, пациентам с подозрением на гемохроматоз назначают клинический анализ крови. У заболевших отмечается снижение концентрации лейкоцитов и тромбоцитов в крови, а также высокий уровень железосодержащего белка гемоглобина.
3.9.1. Вен. кровь (+230 ₽) 
Вен. кровь (+230 ₽) 1 день

Чтобы выявить избыток железа в организме, врач может назначить анализ крови на сывороточное железо, трансферрин, ферритин.
4.1. Вен. кровь (+230 ₽) 
Вен. кровь (+230 ₽) 1 день

4.6. Вен. кровь (+230 ₽) 
Вен. кровь (+230 ₽) Колич. 1 день

4.5. Вен. кровь (+230 ₽) 
Вен. кровь (+230 ₽) Колич. 1 день

На заболевание может указывать уровень железа в крови выше 27 мкмоль/л, насыщение трансферрина железом более 45%, концентрация ферритина в плазме 350–500 нг/мл.
Чтобы оценить работу внутренних органов и выявить нарушения со стороны печени и почек, может быть рекомендовано биохимическое исследование крови. Как правило, у заболевших повышена активность печёночных ферментов АСТ и АЛТ, высокий уровень общего билирубина в крови.
27.113. Вен. кровь (+230 ₽) 
Вен. кровь (+230 ₽) 1 день

Всем, у кого по результатам анализов крови выявлены отклонения от нормы значимых показателей, назначают подтверждающее молекулярно-генетическое исследование. Выявление одной из патогенных мутаций в генах HFE, HJV, TFR2, SLC40A1, CP и характерные симптомы у человека — основание для постановки диагноза «наследственный гемохроматоз».
GNP055 Взятие (2 вида, +590 ₽) 
Взятие (2 вида, +590 ₽) 5 дней

Инструментальная диагностика
Как правило, для постановки диагноза используют ультразвуковое исследование печени, жёлчного пузыря и его протоков, селезёнки. УЗИ позволяет выявить поражение органов (увеличение печени и селезёнки, фиброз печени, расширение воротной и селезёночной вены).
Рекомендовано также проведение фиброэластометрии — специального исследования печени для выявления цирроза и оценки динамики фиброза печени на фоне проводимой терапии.
Для диагностики патологий сердца проводят электрокардиографию и эхокардиографию.
Лечение
От наследственного гемохроматоза невозможно излечиться полностью, но разработана терапия, которая помогает пациентам жить привычной жизнью.
Консервативное лечение
Людям с наследственным гемохроматозом назначают лекарства, связывающие железо и выводящие его из организма.
Такое лечение помогает уменьшить симптомы болезни и предотвратить повреждение внутренних органов.
Флеботомия
Флеботомия, или так называемое терапевтическое кровопускание, в ходе которого из вены на руке или ноге забирают около 500 миллилитров крови. Процедуру проводят 1 или 2 раза в неделю в течение нескольких месяцев или года. Продолжительность лечения и частота процедур зависят от тяжести болезни.
Флеботомия — взятие крови из вены, которое длится чуть дольше, чем обычно (5–10 минут)
Лечение завершают, когда уровень железа возвращается к норме, при этом раз в несколько месяцев обычно назначают поддерживающую флеботомию, чтобы избежать перегрузки организма железом в будущем.
Диета при наследственном гемохроматозе
Важная составляющая лечения — диетотерапия. Всем пациентам с наследственным гемохроматозом рекомендуют изменить рацион — по возможности отказаться от продуктов, которые содержат много железа.
Продукты, богатые железом:
- красное мясо — баранина, говядина, телятина, свинина;
- субпродукты — печень, почки;
- жирные сорта рыбы — лосось, тунец;
- яйца;
- орехи;
- сухофрукты;
- цельнозерновые макароны и хлеб;
- бобовые;
- листовые овощи — шпинат, брокколи;
- тофу.
Кроме того, следует избегать добавок с витамином C (усиливает всасывание железа в кишечнике) и ограничить употребление алкоголя (повышает токсическое воздействие железа на печень).
Также людям с гемохроматозом следует отказаться от употребления сырых моллюсков вроде устриц, гребешков, креветок, морских ежей из-за риска заражения бактериями (Vibrio vulnificus), которые могут приводить к смертельно опасной форме сепсиса — септицемии.
Vibrio vulnificus может попасть в организм через открытую рану во время купания в прибрежных водах или при употреблении свежих моллюсков
Дело в том, что для роста и развития этой бактерии необходимо железо. Чтобы забрать себе как можно больше металла, она вырабатывает особые вещества — сидерофоры, которые связывают железо и переносят его внутрь клеток. Из-за того, что у людей с гемохроматозом, как правило, железа в крови изначально больше, Vibrio vulnificus растёт и размножается быстрее и чаще приводит к тяжёлой форме инфекции.
Прогноз и профилактика
Предотвратить заболевание нельзя, но можно выявить его на ранней стадии, когда поражение органов ещё не достигло критических значений.
Прогноз болезни благоприятный, но только при соблюдении диеты и пожизненном профилактическом лечении.
Если у кого-то из кровных родственников диагностировали наследственный гемохроматоз, рекомендуется сдать молекулярно-генетическое исследование, потому что патология может длительно протекать бессимптомно.
Источники
- Перегрузка железом / гемохроматоз : клинические рекомендации / Национальное гематологическое общество. 2020.
- Волошина Н. Б., Осипенко М. Ф., Литвинова Н. В., Волошин А. Н. Гемохроматоз — современное состояние проблемы // Терапевтический архив. 2018. № 3. С.—107—111. doi:10.26442/terarkh2018903107-112
1. наследственное, генетически обусловленное заболевание, проявляющееся нарушением обмена железа с накоплением его в тканях и органах
Все значения слова «гемохроматоз»
-
Кардиомиопатии – первичные изолированные поражения миокарда невоспалительного характера неизвестной этиологии (идиопатические), они не имеют связи с клапанными пороками или внутрисердечными шунтами, артериальной или лёгочной гипертензией, ишемической болезнью сердца или системными заболеваниями (как то: коллагенозы, амилоидоз, гемохроматоз и др.), причём в финальной стадии болезни развиваются тяжёлая застойная сердечная недостаточность и сложные нарушения сердечного ритма и проходимости.
- (все предложения)