флоризин
- флоризин
-
1) Chemistry: phlorhizin
2) Molecular biology: phlorizin
Универсальный русско-английский словарь.
.
2011.
Синонимы:
Смотреть что такое «флоризин» в других словарях:
-
флоризин — сущ., кол во синонимов: 2 • глюкозид (24) • флорризин (1) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
-
Семейство GH1 — гликозил гидролаз Обозначения в базах данных Pfam … Википедия
-
Семейство GH1 гликозид-гидролаз — Семейство GH1 гликозил гидролаз Обозначения в базах данных Pfam PF00232 InterPro IPR001360 PROSITE … Википедия
-
Семейство GH1 гликозидаз — Семейство GH1 гликозил гидролаз Обозначения в базах данных Pfam PF00232 InterPro IPR001360 PROSITE … Википедия
-
Семейство GH1 гликозилгидролаз — Семейство GH1 гликозил гидролаз Обозначения в базах данных Pfam PF00232 InterPro IPR001360 PROSITE … Википедия
-
Семейство GH1 гликозил-гидролаз — Обозначения в базах данных Pfam PF00232 InterPro IPR001360 PROSITE … Википедия
-
Семейство GH1 гликозидгидролаз — Семейство GH1 гликозил гидролаз Обозначения в базах данных Pfam PF00232 InterPro IPR001360 PROSITE … Википедия
-
Флоретин — Общие Систематическое наименование … Википедия
-
глюкозид — сущ., кол во синонимов: 24 • амигдалин (5) • арбутин (2) • гиталин (1) • … Словарь синонимов
-
флорризин — сущ., кол во синонимов: 1 • флоризин (2) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Силикат магния выпускается под названием магнезол, флоризил или трисиликат магния. Часто его употребляют в смеси с кремнеземом (от 1 1 до 2 1). [c.346]
Флоризил (силикат магния) — — 320 [c.173]
Флоризил — синтетический силикат магния. Считают, что он эффективен в аналитической работе по выделению азотистых соединений из дистиллятов сланцевой смолы. Флоризил, по-видимому, неэффективен для разделения различных типов углеводородов [25]. [c.266]
В основе адсорбционной хроматографии лежит разделение липидов в соответствии со степенью их полярности. Адсорбентом при тонкослойной хроматографии чаще всего служит силикагель. При колоночной хроматографии широкое применение получили три адсорбента силикагель, окись алюминия, флоризил (силикат магния). Прочность взаимодействия липида с адсорбентом определяется главным образом водородными и ионными связями, в меньшей степени — силами Ван-дер-Ваальса. [c.69]
Дисульфиды Флоризил Циклогексан—бензол (1 1), затем бензол и хлороформ 23 [c.156]
Разработан метод анализа с использованием минимальных количеств адсорбента и элюента [15]. Флоризил активируют при 650 °С, добавляют строго определенное количество воды в пределах 0,5—2,0%, которое специально подбирают в предварительных опытах для каждой партии.адсорбента. Если количество воды подобрано правильно, потери пестицидов не превышают 10% [15]. [c.239]
Уголь—флоризил—целит (1 2 2) [c.256]
ЖТХ Определение пестицидов—карбаматов в траве и фруктах Флоризил Метиленхлорид, насыщенный водой 63 [c.257]
ЖТХ Метаболиты фу-радана (группа карбаматов) в растениях Кремневая кислота, флоризил Диэтиловый эфир—н-гексан, хлороформ, этилацетат, метанол, ступенчатое элюирование 64 [c.257]
В табл. II.2 представлены некоторые свойства используемых в хроматографии растворителей, которые расположены в порядке возрастания бц. Значения Sq определены для AlgOs относительно пентана, адсорбционная энергия которого связана только с дисперсионными силами, пропорциональными величине и рассчитаны по формулам (11.37 и 11.38). Значения параметра для SiOg, флоризила (силиката магния) и MgO соответственно составляют 0,77, 0,52 и 0,58 значений 8q для AlgOg [c.76]
МАв [Со(БА)з] Флоризил Бензол—диэтиловый эфир (19 1) транс 88 [c.336]
Использование этих адсорбентов позволяет выделить из нефти при десорбции м-пентаном 71—61% углеводородов с низким содержанием серы (0,03—0,02%). При применении адсорбентов, не содержащих окислов алюминия, таких как флоризил, фуллерова земля и силикагель, четкость отделения сернистых соединений от углево- [c.116]
II Силикагель, алюмогель, кизельгур, силикат магния (флоризил) Смеси растворителей групп А и I) от 1 99 до 10 90 Целлюлоза, силикагель, кизельгур, гидроксил- апатит Вода, вода + аммиак, водные буферные растворы, водные растворители групп В и С (нижняя фаза) < меси 2—4-х растворителей групп В и В в широком диапазоне концентраций, насыщенные водой В распределительной хроматографии поверхность силикагеля инактивируется водой [c.148]
Для выделения органических суперэкотоксикантов из экарак-гов применяют различные сорбенты силикагель, кремниевую кислоту, оксид алюминия, флоризил(силикат магния), фосфат кальция, активный уголь, целлюлозу, полимерные смолы и др Классическим примером могут служить методы разделения ХОП и ПХБ с помощью флоризила [90,9 П и арохлора [92,93] Большое число работ посвящено вьщелению ХОС и ПАУ с применением колоночной хроматографии на силикагелях [36,94-96]. Установлено, что степень ра аделения ПХБ и ХОП зависит от пористости и удельной поверхности силикагелей, условий их активации и содержания воды Интересные результаты получены при использовании двух колонок, заполненных оксидами алюминия и кремния [97] (рис. 6 4) Для удаления остаточных количеств воды наряду с сорбентами в каждую колонку добавляют по 0,2 г безводного сульфата натрия [c.221]
При работе на лигроине процесс протекал следующим образом сырье со дна испарительной колонны насосом подавалось в трубчату ю печь. Печь де—Флориза по своей конструкции отличалась от обычных печей других систем тем, что по своей форме представляла цилиндрическую вертикальную шах1у, по внутренним стенкам которой были расположены радиант ные трубы. В верхней части печи — трубы конвекционной секции, над ней подогреватель воздуха и затем дымовая труба. [c.40]
Уже в 30—е гг. XX в. установки Бартона, Кросса, Льюиса, Тюб энд Тэнк, Холмс-Мэнли, де—Флориза, Нокса, Лимена, Холла и другие устарели и были вьггеснены другими методами, дававшими лучший бензин по более низкой цене (Виккерс, Винклер-Кох и др.). [c.41]
В этом методе в качестве неподвижных фаз наиболее широкое распространение получили оксид алюминия и силикагель. Реже применяют сищ-етический силикат магния (флоризил), оксид магния, пористые стекла, пористые полимеры и нсполярньЕЙ адсорбент — активированный уголь. С появлением ВЭЖХ силикагель [c.30]
Для эффективного разделения смесей большое значение имеет выбор сорбента. В ТСХ применяют следующие сорбенты силикагель, окись алюминия, кизельгур, гидроокись кальция, силикат магния, флоризит, целит, гипс, целлюлозу и др. При адсорбционном методе хроматографирования, если вещество обладает слабым сродством к сорбенту, используют активные слои и слабополярные растворители. Наоборот, если вещество сильно адсорбируется адсорбентом, то применяют слабоактивные сорбенты и сильнополярные растворители. [c.115]
Другие сорбенты. В качестве сорбентов дгожпо так ко использовать гидроокись кальция п силикагель — гипс (6 1) [50], силикат магния [51], флоризил (состав MgO 15,5% SIO2 84% NaaSOj 0,5% pH 8,5 [52], целит 545 [39], а также фосфат магния, фосфат кальция, гидроокись железа и уголь [27]. [c.17]
Бензил п-толуолсульфоксид и ге-толуолсульфинат Флоризил Хлороформ, этилацетат—бензол (1 9) 26 [c.156]
Предложена модификация метода, которая позволяет сократить время анализа за счет одновременного проведения экстракции и гидролиза с смесью метанола, хлороформа и едкого бария. Холин выделяют из гидролизата адсорбцией на колонке с флоризилом. При пропускании рейнеката аммония через колонку получают рейнекат холина, который проявляется в виде розовой полосы, после того как избыток реактива вымывают. При наличии хлорофилла колонку до пропускания рейнеката аммония промывают метилацетатом. Рейнекат холина с флоризила элюируют ацетоном и измеряют оптическую плотность раствора при 526 нм 13, 42]. [c.205]
Колоночную хроматографию используют главным образом для предварительной очистки материала и для выделения чистых веществ в препаративных целях. Из адсорбентов наиболее широко применяют окись алюминия, декалсо (De also), флоризил (Florisil), пермутит, карбонат цинка, кремневую кислоту, в некоторых случаях — окись магния. Витамины К, полученные синтетическим путем, были разделены на окиси алюминия, инактивированной разбавленной уксусной кислотой. Гомологи витамина К разделяли на метилированном сефадексе в системе хлороформ—метанол—н-гептан (1 1 2) [28]. [c.183]
При определении пестицидов в биологических материалах для их отделения от жиров, пигментов и других примесей наиболее щирокое применение находит твердо-жидкостная хроматография. В качестве сорбента обычно используют силикат магния флоризил (Florisil). Однако некоторые вещества, например, дильдрин и эндрин, сорбируются на флоризиле настолько прочно, что их не удается полностью элюировать даже высокополярными растворителями. В таких случаях проводят хроматографию на других сорбентах, например на силикагеле, ки-зельгуре, целите. Не рекомендуется применять окись алюминия, поскольку с этого сорбента полярные вещества элюируются неколичественно. [c.237]
В качестве сорбента для выделения хлорированных пестицидов наиболее широко используют флоризил [12—14]. В табл. 46.1 пpивeдeньJ данные по влиянию качества флоризила на эффективность извлечения хлорированных пестицидов. [c.239]
В меньшей степени флоризил используют в анализе фосфорорганических пестицидов Было исследовано извлечение 65 фосфорсодержащих пестицидов из флоризила в системах бензол, диэтиловый эфир—бензол (1 2), ацетон и метанол [16]. Большинство пестицидов извлекается элюирующими смесями или ацетоном, и только три пестицида элюируются бензолом. [c.239]
Паратион, паратион-метил, фенитротион и продукты их метаболизма Флоризил, инактивированный водой (5-8%) Бензол (180 мл) Ацетон (150 мл) Тионаты Окисленные продукты обмена и 5-изо-меры. Колонка 1,8X30 см. 8 г сорбента. Скорость подачи элюента 1,5 мл/мин 42 [c.249]
Разделение изомеров тр с(бензоилацетонато)хрома(1П) [88]. Густую суспензию 180 г флоризила в м-гексане вносят в колонку (2,8×84 см) и при включенном электрическом вибраторе удаляют растворитель. Затем в колонку вносят 0,5 г комплекса в минимальном объеме смеси бензол—к-гексан (1 1) и проводят элюирование в системе бензол—диэтиловый эфир (19 1) со скоростью подачи 2 мл/мин. После вымывания первой зоны (транс-изомер) скорость подачи увеличивают до 8 мл/мин и отбирают ч с-изомер. [c.335]
Соединения Фильтроль Силикагель Флоризил Окись магния Углекислый 1гальций Гидроокись кальция Гидрофосфат кальция [c.58]
Через оранжевый раствор 3 г 3-(Ы-пирролидил)-А2-холестена в 900 мл сухого бензола при комнатной температуре барботи-руют перхлорат фтора до исчезновения окраски ( 30 сек). После промывания реакционной смеси насыщенным водным раствором бикарбоната натрия и водой бензол отгоняют в вакууме, оставшиеся желтые кристаллы растворяют в 100 жл смеси бензола и петролейного эфира (1 1). Раствор фильтруют через 10 г флоризила, фильтрат упаривают в вакууме и остаток перекристаллизовывают из н-гексана. Получено 2,0 (выход 72%) 2а-фторхолестанона-3 с т. пл. 170—173 °С. [c.14]
Для тонкослойной хроматографии используется большой ассортимент пористых материалов, которые могут выполнять роль сорбентов (адсорбционная, ионообменная хроматография) или пористых твердых носителей для неподвижной жидкой фазы (распределительная хроматография). Основными видами пористых материалов, применяемыми в тонкослойной хроматографии, являются силикагель, окись алюминия, кизельгур, порошкообразная целлюлоза и целлюлозные ионообменники. В меньшей степени используются ионообменные смолы, полиамидные порошки, сефадексы, полиэтиленовый порошок, гидроксилаппатит, силикат магния, сульфат кальция, смеси гидроокиси кальция с силикагелем (6 1 и 4 1), флоризил (смесь силикагеля и магнезии). [c.285]
В делительную воронку переносят 500 мл пробы и энергично встряхивают в течение I ч с 10 мл 10%-ного раствора NaOH, 10 мл 10%-ного раствора Na-ЭДТА, 50 г Na l и 5 мл ССЦ, Добавляют I мл 25%-ного раствора серной кислоты, отделяют слой ССЦ центрифугированием, насыпают в него 0,5 г флоризила ( можно заменить окисью алюминия ) и фильтруют через тампон из ваты в маленький мерный цилиндр. Отобрав аликвот. [c.146]
Аналитическая химия промышленных сточных вод (1984) — [
c.34
,
c.303
]
Анализ воды (1955) — [
c.24
,
c.188
,
c.195
,
c.198
]
Методы анализа пестицидов (1967) — [
c.550
]
Газовая хроматография с программированием температуры (1968) — [
c.214
]
Флоризил
Cтраница 1
Флоризил не выпускается отечественной промышленностью, поэтому в СССР были предприняты поиски отечественных адсорбентов, применимых для очистки экстрактов при определении пестицидов.
[1]
Флоризил ( Florisil) нагревают в муфельной печи при 650 в течение 1 — 3 час. После часового выдерживания в термостате флоризил в закрытом сосуде может быть перенесен для хранения в эксикатор. Этот флоризил годен в течение 4 дней, по истечении срока он должен быть выдержан 12 час.
[2]
Флоризил активируют при 650 С, добавляют строго определенное количество воды в пределах 0 5 — 2 0 %, которое специально подбирают в предварительных опытах для каждой партии.
[3]
Флоризил, с частицами 100 — 200 меш, активированный изготовителем при 780 — 830 С.
[4]
Флоризил теряет свою активность примерно через 4 дня, для ее восстановления адсорбент нагревают при 130 С в течение ночи.
[5]
Адсорбент флоризил, 60 — 80 меш, температура активации 650 С.
[6]
На флоризиле с 8 % добавкой ( по весу) сернокислого кальция ( активирование при 160 в течение часа) в системе петролейный эфир — эфир ( 20: 80, объем / объем) 1 2 — и 1 3-диглицериды не разделяются, а холестерин движется быстрее последних. Жирные кислоты находятся близко к старту. Детектирование на подогретой до 160 пластинке проводят сначала 10 % спиртовым раствором фосфорномолибденовой кислоты, затем 50 % ( по объему) раствором серной кислоты. На гидро-ксилапатите с той же добавкой в системе ацетон — гептан 12: 88 по объему хорошо разделяются оба диглицерида и холестерин.
[7]
В меньшей степени флоризил используют в анализе фосфор-органических пестицидов. Большинство пестицидов извлекается элюирующими смесями или ацетоном, и только — три пестицида элюируются бензолом.
[8]
Поскольку адсорбционная способность флоризила несколько изменяется для разных его партий и поскольку в разных культурах содержатся разные мешающие вещества, проверку открываемого количества токсафена следует проводить для каждой серии анализов. При использовании метода А в сочетании с методом Б или В объем элюата, содержащего воски, определяют в 10 мл.
[9]
Два картриджа, содержащие флоризил и силикагель, соединяют последовательно.
[10]
Густую суспензию 180 г флоризила в м-гексане вносят в колонку ( 2 8X84 см) и при включенном электрическом вибраторе удаляют растворитель. Затем в колонку вносят 0 5 г комплекса в минимальном объеме смеси бензол — — гексан ( 1: 1) и проводят элюирование в системе бензол-диэтиловый эфир ( 19: 1) со скоростью подачи 2 мл / мин. После вымывания первой зоны ( гранс-изомер) скорость подачи увеличивают до 8 мл / мин и отбирают цыс-изомер.
[11]
Mills ( 1968), флоризил перед употреблением необходимо дополнительно активировать нагреванием при 130 — 135 С в течение ночи, после чего проверяется его способность к адсорбированию жира по пробе с лаурино-вой кислотой.
[12]
Раствор фильтруют через 10 г флоризила, фильтрат упаривают в вакууме и остаток перекристаллизовывают из н-гексана.
[13]
В колонку для ТФЭ засыпают 1г флоризила и кондиционируют ее ацетонитрилом.
[14]
Степень задерживания жира в колонке с флоризилом, позволяющая более полно отделить остатки жира от остатков пестицида, повышается путем применения описанного выше способа наполнения колонки.
[15]
Страницы:
1
2
3
4
Имена и идентификаторы
| наименование товара | Florisil (R), |
| Синонимы | ЧАСТИЦЫ КРЕМНИЯ MAGPREP®, Q-АГЕНТА СИЛИКАТА МАГНИЯ; Оксид магния (MgO), смесь. с кремнеземом; силикат магния; силикат с активированным магнием; адсорбент флоризила; флоризил (R); адсорбент флоризила (R), 60-100 MESH |
| Номер CAS Registry | 8014-97-9 |
| Молекулярная формула | MgO3Si |
| Молекулярная масса | 100.39 |
| EINECS | 215-681-1 |
| Другие номера реестра | |
| Имена IUPA, InChI, InChI Key, Canonical SMILES, И т.д.: | Имена IUPA, InChI, InChI Key, Canonical SMILES, И т.д. |
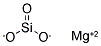 |
Химические и физические свойства
| S Фраза | 24/25 |
| WGK Германия | – |
Литература |
Патенты |
Транспортировка, хранение и использование |
| Применение | Нет информации |
Спектральные свойства |
Утвержденные производители |
|
| Хотите, чтобы вас указали в списке одобренных производителей (бесплатное обслуживание, но требуется одобрение)? | Пожалуйста, скачайте и заполните эта форма и отправить обратно [электронная почта защищена] |
Свяжитесь с нами для получения другой помощи |
|
| Свяжитесь с нами для получения других услуг, таких как передача технологий, синтетическая литература, поиск поставщиков, реклама и т. Д. | Нажмите здесь, чтобы связаться ChemWhat |
Назад
Флорисил Florisil 100-200 mesh 250гр. cas 1343-88-0 Есть на складе!!!
Артикул: нет
- Описание
- Отзывы
Твердозернистый силикагель с оксидом магния, состав: MgO — 15,5 ±0,5 %, SiO2 — 84,0 ±0,5 %, Na2SO4 ≤ 1,0 %.
Типичные применения: предочистка остатков пестицидов, разделение хлорированных пестицидов, изолирование стероидов, половых гормонов, антибиотиков, липидов и т. д.
Для хроматографии 30-60 mesh
Для хроматографии 60-100 mesh (150-250мкм.)
Для хроматографии 100-200 mesh
Также Вы можете войти через:
Я согласен(на) на обработку моих персональных данных. Подробнее
Дезинфекции всегда должна предшествовать стадия очистки поверхности. Пищевые загрязнения, оставшиеся на плохо очищенной поверхности, являются источниками питания и очагами роста микроорганизмов. Хорошее санитарно-гигиеническое состояние на пищевом предприятии достигается комбинированной программой тщательной очистки всех поверхностей и оборудования с последующей дезинфекцией. Известно, что при тщательной очистке с поверхности удаляется до 90% микроорганизмов. На недомытой поверхности остатки загрязнений не только защищают микроорганизмы от санитарной обработки, но и снижают эффективность дезинфицирующего средства за счет эффекта разбавления или химической реакции органического вещества с дезинфектантом.
Химические соединения, предназначенные для использования в пищевой промышленности в качестве дезинфектантов, отличаются химической структурой, активностью против различного вида микроорганизмов и условиями, при которых они проявляют максимальную активность. В общем, случае справедлива закономерность – чем выше концентрация дезинфицирующего средства, тем быстрее и эффективнее его действие. Чтобы выбрать эффективное дезинфицирующее средство, нужно экспериментальным или теоретическим путем определить потенциальные патогенные микроорганизмы и убедиться в том, что, выбранный дезинфектант активен в отношении этих микроорганизмов. Поскольку химические дезинфектанты не обладают высокой проникающей способностью, микроорганизмы в трещинах, царапинах и других неровностях поверхности, внутри минеральных загрязнений могут быть не полностью уничтожены после обработки. Чтобы действие химических дезинфектантов было эффективно, поверхность перед обработкой должна быть тщательно очищена.
Эффективность обработки зависит от ряда физико-химических факторов:
- время экспозиции. Исследования показали, что гибель популяции микроорганизмов носит логарифмический характер: 90% микроорганизмов гибнет в определенный интервал времени, 90% оставшихся организмов гибнет в следующий интервал времени, при этом остается лишь 1% от первоначального количества микроорганизмов. Время экспозиции зависит от эффективности воздействия дезинфицирующего средства на данный вид микроорганизмов, способности к образованию спор и других физико-химических факторов.
- температура. С увеличением температуры возрастают скорости роста микроорганизмов и их гибели вследствие действия химических дезинфицирующих средств. Увеличение температуры приводит к снижению поверхностного натяжения, вязкости и изменению ряда других параметров, которые способствуют гибели микроорганизмов.
- концентрация. С увеличением концентрации дезинфицирующего средства возрастает скорость гибели микроорганизмов.
- показатель pH . Активность антимикробных соединений, как правило, зависит от показателя pH среды. Например, хлор и йод содержащие дезинфицирующие средства теряют свою активность с увеличением показателя pH среды.
- жесткость воды. С увеличением концентрации солей жесткости воды снижается биологическая активность дезинфицирующих средств, в результате их взаимодействия с солями жесткости воды. Например, четвертичные аммониевые соединения не совместимы с солями кальция и магния. При жесткости воды выше 200 ppm дезинфицировать поверхность четвертичными аммониевыми соединениями без добавления комплексообразователей, смягчающих воду, бесполезно.
- чистота поверхности и оборудования. Многие дезинфицирующие вещества – гипохлорит, йодофоры и многие другие химические дезинфектанты взаимодействуют с органическими соединениями, оставшимися на плохо очищенной поверхности, и теряют свою биологическую активность. Характеристики идеального дезинфектанта.
Идеальный дезинфектант должен обладать следующими свойствами
- высокой биологической активностью против вегетативных бактерий, грибов, дрожжей, обеспечивающей быструю гибель микроорганизмов;
- устойчивостью к окружающей среде (быть эффективным в жесткой воде, в присутствии остатков органических соединений, остатков моющих средств);
- отсутствием токсичности и кожно-раздражающего действия;
- отсутствием запаха;
- стабильностью в концентрированном виде и виде рабочего раствора;
- легкостью в использовании;
- доступностью;
- доступной ценой;
- легкостью идентификации во время использования.
К сожалению, идеальное дезинфицирующее средство, удовлетворяющее одновременно всем выше перечисленным параметрам пока не создано. На практике следует выбирать дезинфектант с высокой биологической активностью против микроорганизмов, которые есть или теоретически могут появиться на предприятии. От правильного выбора дезинфицирующего средства и соблюдения санитарно-гигиенических правил обработки поверхностей и оборудования будет зависеть безопасность произведенных продуктов питания.
Классификация химических дезинфицирующих веществ.
Дезинфицирующие средства классифицируют по их действию на различные формы микроорганизмов: бактерициды уничтожают вегетативные микроорганизмы, спороциды уничтожают споры, фунгициды уничтожают грибы, вируциды уничтожают вирусы. Химические антисептики используются для дезинфекции кожи. Бактериостатические вещества препятствуют размножению бактерий, фактически их не уничтожая.
Химические соединения воздействуют на клетку несколькими способами. Один из них — коагуляция протеина. В обычном состоянии протеин диспергирован внутри клетки. Дезинфицирующее соединение взаимодействует с протеином, вызывая его коагуляцию и выпадение в осадок. Клетка перестает функционировать в нормальном режиме и погибает. Еще один способ воздействия дезинфицирующего вещества на микроорганизмы – разрушение мембраны клетки. Мембрана клетки работает как избирательный барьер, одни растворы она пропускает внутрь клетки, другие растворы не могут преодолеть этот барьер. Вещества, которые сорбируются на клеточной мембране, могут заметно изменить ее физико-химические характеристики, препятствуя нормальному функционированию. Это может привести к ингибированию активности или к гибели клетки.
Химический антагонизм. Ферменты выполняют свою каталитическую функцию благодаря их сродству с некоторыми химическими соединениями, которые называют природными субстратами. Природные субстраты в стандартном режиме находятся внутри клетки. Если природные субстраты в заметном количестве заменяются дезинфектантом, фермент будет связан с химическим веществом, а не субстратом. В случае образования достаточно устойчивой связи фермент — химический дезинфектант клетка теряет способность к размножению.
Обычно химические дезинфицирующие вещества классифицируют по типу биологически-активного вещества, входящего в его состав.
Хлор-содержащие дезинфицирующие средства.
Жидкий хлор, гипохлорит, хлорамин, диоксид хлора являются дезинфицирующими агентами. Они различаются по своей антимикробной активности. Хлор в газообразном состоянии (Cl2) вводят в воду и получают антимикробный агент — хлорноватистую кислоту (НОСl). НОСl диссоциирует в воде с образованием иона водорода Н+ и иона гипохлорита (OCl— ).
Жидким хлором называют раствор гипохлорита натрия в воде (NaOCl), это наиболее распространенная форма дезинфицирующего средства на основе хлора. Следует отметить, что хлорноватистая кислота в 80 раз активнее в качестве дезинфицирующего агента, чем гипохлорит ион. Считается, что механизм антимикробного действия хлорсодержащих соединений заключается в окислении аминокислот мембраны клетки, разрушении мембраны, прерывании синтеза протеина, ингибировании поглощения кислорода клетки и т.д. Некоторые соединения хлорамина более активны против ряда микроорганизмов, чем гипохлориты. Например, дихлороизоцианурат натрия более активен, чем гипохлорит натрия против таких бактерий, как E.coli, S.aureus и некоторых других.
В последние годы возрос интерес к дезинфицирующим средствам на основе диоксида хлора (ClO2). Диоксид хлора в 2.5 раза активнее, чем гипохлорит натрия в качестве окислителя. Диоксид хлора наиболее активен при рН=8.5.
Один из способов получения диоксида хлора можно представить следующим образом:
5NaClO2 + 4HCl → 4ClO2 + 5NaCl + 2H2O
NaOCl + HCl → NaCl + HOCl
HOCl + 2NaClO2 → ClO2 + 2NaCl + H2O
Используя эти химические реакции, можно непосредственно в пенной пушке или пеногенераторе получать пену, содержащую 5 ppm диоксида хлора. Диоксид хлора активен против широкого спектра микроорганизмов, в том числе спорообразующие бактерии и вирусы. Его действие на микроорганизмы заключается в ингибировании воспроизведения микроорганизмов, поскольку диоксид хлора является сильным окислителем.
Когда хлорсодержащие соединения используют для обработки поверхностей, уничтожаются клетки вегетативных и спорообразующих бактерий. Вегетативные клетки уничтожить легче, чем споры Clostridium, которые в свою очередь легче уничтожить, чем споры Bacillius. Хлорсодержащие соединения в концентрации 50 ppm обладают слабой активностью в отношении Listeria monocytogenes, концентрации выше 50 ppm хлорсодержащие соединения эффективны в отношении этого патогенного микроорганизма. В целом эффективность хлорсодержащих соединений возрастает с увеличением концентрации и температуры раствора и понижением значения pH. Следует отметить, что с увеличением температуры увеличивается и скорость коррозии металлов, если обрабатывается металлическая поверхность.
К достоинствам хлорсодержащих соединений следует отнести:
- эффективность в отношении различных бактерий, грибков и вирусов;
- доступность в жидкой и гранулированной форме;
- соли жесткости воды оказывают слабое влияние на активность;
- при использовании хлорсодержащих соединений не происходит образования токсичных побочных продуктов;
Хлорсодержащие соединения обладают меньшей коррозионной способностью, чем жидкий хлор.
К недостаткам хлорсодержащих соединений следует отнести:
- нестабильность и потеря активности с увеличением температуры и при взаимодействии с органическими веществами;
- снижение биологической активности с увеличением показателя pH среды.
- коррозия нержавеющей стали и других металлов, что допускает лишь кратковременный контакт с поверхностями и оборудованием из металлов;
- теряют активность при хранении на свету и использовании при температурах выше 60ºС
- в области низких значений pH (pH <4.0) может происходить образование токсичного газа Cl2, обладающего сильным коррозионным действием;
- при высоких концентрациях в жидких формах могут быть взрывоопасными.
Йод содержащие соединения.
Соединения йода используются для дезинфекции поверхностей и оборудования, а также в качестве кожных антисептиков. Йодофоры используют также как соединения хлора в водоподготовке. Оказалось, что двухатомный йод J2 является самым активным антимикробным агентом из йодсодержащих соединений. Его активность проявляется в том, что он разрушает связи, удерживающие протеины в клетке вместе и ингибирует синтез протеинов. Свободный элементарный йод и йодноватистая кислота проявляют высокую активность в уничтожении микроорганизмов. В качестве дезинфицирующих агентов используют спиртосодержащие соединения йода и соединения на водной основе, эти растворы также используют в качестве кожных антисептиков. Активными в отношении микроорганизмов формами являются J2 и иодноватистая кислота НОJ.
Йодофорами называют комплексы элементарного йода J с неионогенными ПАВ, например нонилфенолэтиленоксидом, или комплекс йода с полимером – поливинилпирролидоном в водном растворе. Йодофоры чаще других йод содержащих соединений используются в качестве дезинфицирующих агентов. Поскольку активность в отношении микроорганизмов увеличивается с понижением значения pH, йодофоры комбинируют с фосфорной кислотой. Сочетание йодофоров с поверхностно-активными веществами и кислотами придает им моющие свойства. Такие средства обладают одновременно моющими и дезинфицирующими свойствами, они обладают лучшей растворимостью в водных растворах, чем суспензии или водные растворы йода. Они не обладают запахом и кожно-раздражающим действием.
Поведение комплекса ПАВ-йод можно объяснить химическим равновесием:
R + J2 ↔ RJ + HJ, R — неионогенное ПАВ
Количество доступного свободного йода определяет биологическую активность йодофора. Спорообразующие бактерии более устойчивы к действию йодофоров, чем вегетативные, и времена экспозиции, приведенные в таблице 4.1, в 10 -1000 раз больше, чем времена экспозиции, необходимые для аналогичного воздействия на вегетативные клетки. Активность йод содержащих веществ по своему действию на вегетативные клетки сравнима с хлор содержащими дезинфектантами, однако действие йодофоров на спорообазующие бактерии слабее. Йод содержащие дезинфицирующие агенты более устойчивы к воздействию органических веществ, чем хлор содержащие. Йодофоры обычно используют в концентрациях 12.5 – 25 ppm. Йодофоры более активны против Tubercule bacillus и других вирусов, чем остальные дезинфицирующие агенты. Йод содержащие соединения проявляют максимальную активность в области значений pH 2.5 – 3.5. Йодофоры в виде концентрированных и стабилизированных растворов имеют длительные сроки хранения. В разбавленных растворах йод имеет тенденцию к испарению, особенно активно этот процесс протекает при температуре выше 50ºС.
Таблица 1 Инактивация спорообразующих бактерий. Тесты проведены в дистиллированной воде при Т=15-20ºС.
|
Микроорганизм |
Показатель рН |
Концентрация, ppm |
Время снижения числа микроорганизмов на 90%, мин. |
|
Bacillus cereus |
6.5 |
50 |
10 |
|
6.5 |
25 |
30 |
|
|
2.3 |
25 |
30 |
|
|
Bacillus subtilis |
— |
25 |
5 |
|
Clostridium botulinum A |
2.8 |
100 |
6 |
Материалы из пластмасс и резины способны адсорбировать соединения йода, что может привести к появлению пятен. В желтый цвет соединения йода окрашивают и органические загрязнения, этот эффект можно использовать для контроля остатков пищевых загрязнений на поверхностях.
Растворы йодофоров имеют кислый характер, поэтому они эффективны в жесткой воде, не способствуя при этом удалению минеральных отложений. Многие органические вещества, особенно молоко и молочные продукты инактивируют дезинфектанты на основе соединений йода.
К недостаткам дезинфицирующих агентов на основе соединений йода следует отнести невысокую активность против спорообразующих бактерий и бактериофагов, а также слабую биологическую активность при низких температурах. При температурах выше 50ºС.
Четвертичные аммониевые соединения.
Четвертичные аммониевые соединения часто используют для обработки полов, стен, мебели и оборудования. Эти соединения являются поверхностно-активными веществами и обладают хорошей смачивающей способностью. Невысокая моющая способность четвертичных аммониевых соединений при великолепной антимикробной активности предопределило их использование в качестве дезинфицирующих средств. Например, четвертичные аммониевые соединения обладают высокой активностью против L.monocytogenes и плесневых грибов.
В четвертичных аммониевых соединениях азот, соединенный с четырьмя органическими радикалами имеет положительный заряд:
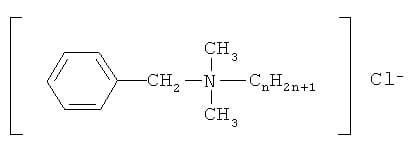
Механизм воздействия четвертичных аммониевых соединений на микроорганизмы отличается от соединений хлора и йода. Дезинфицирующие агенты на основе четвертичных аммониевых соединений образуют бактериостатическую пленку на поверхности. Эти соединения селективно убивают патогенные микроорганизмы. Они не убивают спорообразующие бактерии, однако ингибируют их рост. Четвертичные аммониевые соединения обладают большей стабильностью в присутствии органических соединений по сравнению с хлор и йод содержащими дезинфектантами, однако присутствие органических веществ может привести к снижению их активности. Как правило, в состав дезинфицирующих веществ на основе четвертичных аммониевых солей входят диметилбезиламмонийхлорид, диметилэтилбензиламмонийхлорид, оба соединения не теряют активности в воде с содержанием солей жесткости от 500 до 1000 ppm, даже без добавления комплексообразующих агентов. В концентрациях, в которых четвертичные аммониевые соли используются для дезинфекции оборудования и поверхностей они не являются токсичными, не обладают кожно-раздражающим действием, не вызывают коррозию металлов, что является большим преимуществом по сравнению с хлор — содержащими соединениями. Следует иметь в виду, что четвертичные аммониевые соединения инактивируются анионными ПАВ, поэтому их можно комбинировать или использовать совместно только с определенными классами ПАВ – катионными и амфотерными.
К преимуществам дезинфектантов на основе четвертичных аммониевых солей следует отнести – бесцветность и отсутствие запаха, стабильность в присутствии органических веществ, отсутствие коррозии металлов, стабильность в широком интервале температур, отсутствие кожно-раздражающего действия, эффективность при высоких значениях pH, высокая активность в отношении плесневых грибов, отсутствие токсичности.
К недостаткам четвертичных аммониевых оснований следует отнести потерю активности в присутствии анионных ПАВ, пленкообразование на пищевом оборудовании и поверхностях, а также слабую активность в отношении грам-отрицательных бактерий за исключением Salmonella и E.coli. Активность в отношении грам-отрицательных бактерий усиливают, комбинируя четвертичные аммониевые соли с другими дезинфицирующими агентами.
Учитывая выше приведенные сведения, компания НПФ Химитек разработала и выпускает дезинфицирующее средство ХИМИТЕК УНИВЕРСАЛ-ДЕЗ. В качестве действующего вещества продукт содержит в составе четвертичное аммонийное соединение (ЧАС) нового поколения – дидецилдиметиламмоний хлорида, который внесён в Реестр Биоцидной продукции по Регламенту №(EU) 528/2012.
Рабочие растворы средства обладают стабильностью в жёсткой воде, а также не теряет активности при наличии на поверхности органических загрязнений и остаточных количеств ПАВ. На практике это означает: если предварительная очистка поверхности проведена не очень тщательно, эффективность дезинфектанта не снижается. Рабочие растворы средство обладают активностью против грамположительных и грамотрицательных бактерий, дрожжеподобных грибов и дрожжей — специфической микрофлоры предприятий пищевой промышленности и общественного питания. Средство не проявляет коррозионную активность, т.е. не повреждает объекты и поверхности из любых материалов. Обладают широкой областью применения: можно обеззараживать всё — от яичной скорлупы до мусоровозов. Обладает моющей способностью и высокой стабильность растворов при хранении.
Дезинфектанты на основе кислот
Дезинфицирующие вещества на основе кислот считаются токсикологически безопасными и биологически активными. Их используют в ополаскивающих и дезинфицирующих составах. Чаще всего используют органические кислоты, такие как уксусная, надуксусная, молочная, пропионовая и муравьиная. Присутствие кислот в ополаскивающих составах позволяет нейтрализовать и удалить остатки щелочных моющих и дезинфицирующих веществ. Действие кислотосодержащих дезинфицирующих веществ основано на взаимодействии и разрушении мембраны клетки. Появление технологий автоматической мойки, в которых последнюю стадию ополаскивания желательно комбинировать с дезинфекцией, вызвало появление большого количества дезинфицирующих продуктов на основе кислот. Эти продукты, как правило, используют в заключительной стадии обработки оборудования – ополаскивания и дезинфекции, после чего оборудование оставляют на ночь с минимальным риском микробного обсеменения. Требования к таким продуктам – отсутствие коррозионной способности по отношению к металлам.
На активность дезинфицирующих веществ на основе кислот может повлиять изменение pH среды, pH <3 — наиболее благоприятная среда для таких продуктов. В отличие от йодофоров соли жесткости воды не оказывают заметного влияния активность кислотосодержащих дезинфицирующих веществ. Кислотосодержащие вещества относятся к быстро действующим, они проявляют активность не только в отношении бактерий, но и дрожжей и вирусов. Дезинфектанты на основе кислот обладают хорошими смачивающими свойствами, не оставляют пятен, не вызывают коррозию оборудования. Жесткая вода и присутствие органических веществ практически не оказывают влияния на эффективность продуктов. Дезинфицирующие вещества наносят на поверхность различными способами – распылением, с помощью пеногенератора, с помощью уборочного инвентаря – салфеток и губок, а также используют в CIP- мойках. Поскольку кислотосодержащие дезинфицирующие вещества теряют активность в щелочной области pH, следует тщательно смывать щелочные моющие и дезинфицирующие средства перед обработкой кислотосодержащими дезинфицирующими веществами. В состав кислотосодержащих средств входят анионные ПАВ, кислоты – фосфорная кислота или органические кислоты, перекись водорода. Дезинфицирующий продукт выбирают в зависимости от способа применения (ручная уборка, уборка с использованием пеногенератора, CIP- мойка и т.д.), вида поверхности и устойчивости поверхности к действию продукта.
В последние годы очень сильно вырос интерес к дезинфицирующим веществам на основе надуксусной кислоты. Дезинфицирующие средства на надуксусной (перуксусной) кислоте, обладают высокой эффективностью, широким спектром действия. В зависимости от задачи надуксусную кислоту используют в интервале концентрации от 30 до 250 ppm. Надуксусная кислота практически безопасна для человека: в концентрациях до 80 ppm может присутствовать на овощах и фруктах, а в концентрациях до 250 ppm – на обработанных поверхностях. Дезинфицирующие средства на основе надуксусной кислоты не требуют смывания (если не содержат моющих компонентов или других веществ, которые сами по себе должны смываться с поверхностей или пищевого оборудования). Использование таких средств позволяет сэкономить время, снизить расход воды, и таким образом, сократить финансовые затраты на дезинфекцию.
Надуксусная кислота нашла широкое применение в различных областях. Ее используют для дезинфекции оборудования и предварительно очищенных твёрдых поверхностей в производстве молочных продуктов, вина, напитков, оборудования птицеферм и животноводческих хозяйств. Поскольку надуксусная кислота активна против дрожжей Candida, Saccharomyces, Hansenula и плесневых грибов – Penicillium, Aspergillus, Mucor Geotrichum, она нашла широкое применение в производстве пива и безалкогольных напитков. Именно надуксусная кислота используется для дезинфекции алюминиевой тары – банок для пива и безалкогольных напитков и для консервированных продуктов.. Увеличившийся интерес к использованию надуксусной кислоты в пищевой промышленности связан с ее высокой активностью в отношении таких патогенных микроорганизмов, как Listeria, Salmonella,
а также способностью уничтожать биопленки. Надуксуная кислота нашла широкое применение для ограничения роста бактерий, грибов и слизи в системах охлаждения воды, парообразования, системах обратного осмоса и фильтрации. Кроме того, ее используют для удаления минеральных отложений, запахов, биопленок с оборудования и поверхностей. К положительным свойствам надуксусной кислоты следует также отнести свойства отбеливателя.
Действие надуксусной кислоты основано на окислении внешней клеточной мембраны вегетативных бактериальных клеток, эндоспор, дрожжей и плесневых грибов. Чем сильнее окислитель, тем быстрее погибает патогенный микроорганизм. Надуксусная кислота является очень эффективным окислителем. По своей окислительной способности надуксусная кислота уступает только озону и намного превосходит хлорсодержащие соединения (Таблица 2).
Таблица 2. Окислительная способность некоторых дезинфектантов.
|
Дезинфицирующее вещество |
Окислительная .способность, эВ |
|
Озон |
2.07 |
|
Надуксуная кислота |
1.81 |
|
Диоксид хлора |
1.51 |
|
Гипохлорит натрия |
1.36 |
Дезинфицирующие средства на основе надуксусной кислоты не оказывают значительного воздействия на окружающую среду. Средства имеют короткий период полураспада на уксусную кислоту и кислород и обычно не требуют нейтрализации перед выбросом в сточные воды. Результаты токсикологических исследований показали, что надуксусная кислота обладает гораздо меньшей токсичностью для живых организмов морской и пресной воды, чем другие средства дезинфекции. При попадании на почву надуксусная кислота разлагается в течение нескольких минут, не оказывая влияния на качество почвы.
Хранение продуктов на основе надуксусной кислоты осуществляют с соблюдением несложных правил – в отсутствии прямого попадания солнечных лучей и при температуре, не превышающей 20°С.
Одним из немногих ограничений для использования этого дезинфектанта является характерный запах уксуса. Но поскольку надуксусная кислота эффективно воздействует на патогенные микроорганизмы даже в очень низких концентрациях, рабочие растворы обладают очень слабым запахом.
Надуксусную кислоту (НУК) в качестве действующего вещества содержат дезинфицирующие средства ХИМИТЕКПОЛИДЕЗ®-СУПЕР и ХИМИТЕК ПОЛИДЕЗ®-DRY. Оба высокоэффективны при низких концентрациях, работают в воде любой степени жёсткости, обладают отбеливающими свойствами, применяются в различных областях. ХИМИТЕК ПОЛИДЕЗ®-СУПЕР жидкий концентрированный продукт, широко используется на предприятиях пищевой и перерабатывающей промышленности после мойки для дезинфекции всех кислотостойких поверхностей. Средство эффективно в малых концентрациях – от 0,2%, не требует ротации. Средство разрешено для дезинфекции не только поверхностей, но и продуктов питания: овощного сырьё, зелени, скорлупы яиц и тушек птиц.
ХИМИТЕК ПОЛИДЕЗ®-DRY отличается от средства ХИМИТЕК ПОЛИДЕЗ®-СУПЕР тем, что выпускается в форме порошка, при растворении которого в воде происходит реакция образования НУК, при этом раствор обладает нейтральным рН (7,0-8,5) и не имеет резкого химического запаха. Он не оказывает коррозионного воздействия на металлические поверхности. Средство не имеет побочных эффектов в форме фиксации белковых загрязнений и развития резистентности у микроорганизмов. Безопасно и экологично. Дополнительным свойством этого дезинфектанта является хорошая моющая способность за счет содержащихся в составе ПАВ, что позволяет добиться высокой степени чистоты обрабатываемых поверхностей.
Перекись водорода.
Перекись водорода используется в пищевой промышленности в различных концентрациях от 3% и до 90% применяется в пищевой промышленности. Перекисью водорода обрабатывают поверхность упаковки для фруктов. В концентрации 6% перекись водорода проявляет бактерицидные свойства. В общем можно сказать, что перекись водорода более активна в отношении грам — положительных бактерий, чем грам — отрицательных. Уничтожение спор спорообразующих бактерий происходит при обработке поверхности перекись водорода в концентрации от 10 до 30%. Этот антимикробный агент может использоваться на любом оборудовании и поверхностях. В случае использования концентрированных растворов пероксида и опасения возможности коррозии оборудования следует использовать антикоррозионные добавки. Было показано, что перекись водорода убивает Listeria monocytogenes на латексных перчатках. Перекись водорода используют для обработки различных поверхностей из полимерных материалов, смол и каучуков.
Перекись водорода часто используют в комбинации с другими дезинфицирующими веществами, например, надуксусной кислотой или четвертичными аммониевыми соединениями.
Средство ПОЛИДЕЗ® производства НПФ Химитек в качестве действующего вещества содержит перекись водорода и четвертичные аммонийные соединения. Средство активно в отношении грамотрицательных и грамположительных бактерий (включая бактерии туберкулёза), вирусов, грибов рода Кандида и Трихофитон. Продукт имеет нейтральный pH (5,8–7,0), не вызывает коррозию металлов, не имеет резкого запаха. Рабочие растворы стабильны в широком температурном диапазоне, режим разведения и применения – от 20 до 50°C, работает в воде любой степени жёсткости.
Дезинфектанты на основе спиртов.
В целя дезинфекции наиболее часто используют три спирта- этиловый, изопропиловый и n-пропиловый, последний, в основном, используется в Европе. Дезинфицирующие агенты на основе спиртов проявляют максимальную эффективность в интервале концентраций 60-70%. Концентрации дезинфицирующего агента, необходимые для инактивации патогенных микроорганизмов выше, чем концентрации хлор- содержащих, четвертичных аммониевых солей и кислотосодержащих дезинфицирующих агентов. Спорообразующие микроорганизмы в достаточной степени устойчивы к действию спиртов, однако обработка спиртосодержащими растворами при концентрации спирта 70% и 65ºС инактивирует споры, например споры Bacillus subtilis. Обработка спиртосодержащими дезинфектантами дороже, чем продуктами других химических классов, поэтому их не используют для полной обработки поверхностей или оборудования. В основном, такими составами обрабатывают небольшие малодоступные участки оборудования и поверхностей. Кроме того, составы на основе спиртов используют для дезинфекции рук персонала.
Для проведения экспресс-дезинфекции небольших по площади, а также труднодоступных поверхностей компания НПФ Химитек разработала и выпускает дезинфицирующее средство ХИМИТЕК ПОЛИДЕЗ-ЭКСПРЕСС. В качестве действующего вещества продукт содержит изопропиловый и пропиловый спирты, обладает антимикробной активностью в отношении грамотрицательных и грамположительных бактерий, дрожжеподобных грибов и дрожжей. Помимо всего продукт готов к использованию, имеет удобную упаковку и не требует смывания. Обладает стабильностью микробиологической активности при хранении, низкой токсичностью.
Дезинфектанты на основе альдегидов.
Наиболее известными дезинфицирующими агентами этого класса являются глютаровый альдегид и формальдегид. Альдегиды активны в отношении бактерий, вирусов, плесневых грибов и спор. Однако этот класс соединений очень быстро инактивируется протеинами, поэтому для достижения необходимого эффекта дезинфекции поверхность должна быть предварительно тщательно очищена. Известно, что глютаровый альдегид вызывает сильную денатурацию белка и потому, в случае некачественной очистки, фиксирует загрязнения на обрабатываемой поверхности.
Действие альдегидов основано на их взаимодействии с внешними слоями клетки, в результате чего клетка метаболизирует, и происходит ингибирование ее активности. Щелочная среда наиболее благоприятна для взаимодействия альдегидов с внешними слоями клетки. Для обработки используют растворы различных концентраций — 0.8-1.6% для ингибирования E.coli. Для ингибирования спорообразующих бактерий концентрацию альдегидов в растворе увеличивают до 2%.
При работе с дезинфицирующими агентами на основе альдегидов персонал должен быть хорошо обучен, нарушение правил работы с такими продуктами может нанести ущерб здоровью работников, поскольку обладает альдегиды обладают ярко выраженным раздражающим, наркологическим, сенсибилизирующим и токсическим эффектом.
Бисфенолы.
Бисфенолы – это соединения дифенил метана, дифенил эфира, дифенил сульфида, содержащие галогены и гидроксильные группы. Они проявляют активность в отношении бактерий, грибов и водорослей. Триклозан и гексахлоропрен – представители этого класса соединений, которые наиболее часто используются в качестве дезинфектантов и антисептиков. Триклозан — 5-хлоро-2-(2,4-дихлорфеноси)фенол входит в состав антибактериального мыла, очищающих гелей для рук и зубных паст, поскольку проявляет высокую активность в отношении стафилокков. Триклозан может содержать высоко токсичные для человека соединения диоксин и дибензофуран, поэтому перед использованием этого дезинфицирующего агента на пищевом средстве следует внимательно ознакомиться со способом производства этого соединения и содержанием примесей, которые должны присутствовать в паспорте безопасности.
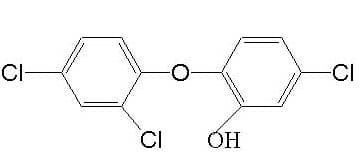
Механизм действия триклозана на бактериальную клетку считается до конца не установленным. Предполагается, что триклозан блокирует биосинтез липидов путем специфического ингибирования фермента еноил-ацил-преносящий белок-редуктазы.
Действие триклозана, как и диоксинов и фенолов — подавление развития микроорганизмов. Но в свою очередь они могут вызывать у них мутации. Помимо этого, у них у всех сильно выражено раздражающее действие на кожу.
Бигуанидины.
Группа бигуанидинов представлена хлоргексидином, алексидином и полимерными бигуанидинами. Хлоргексидин один из наиболее используемых антисептиков для обработки рук, в концентрации 0.0001 мг/л он является бактериостатиком. В концентрации 0.002 мг/л – бактерицидом с широким спектром действия. Активность хлоргексидина зависит от pH среды, в щелочной среде она выше, чем в кислой среде. Его активность заметно снижается в присутствии органических веществ. При концентрации выше 0.005 мг/л и температуре 70º С хлоргексидин проявляет активность в отношении спорообразующих бактерий, хотя действует, в основном, как бактериостатик. Полимерные бигуанидины нашли применение в пищевой промышленности, в медицине, в санитарной обработке бассейнов.
Таблица 3.Основные дезинфицирующие вещества.
|
Дезинфицирующие агенства |
Применение |
Активность в отношении бактерий |
Активность в отношении спор |
Комментарии |
|
Галоген-содержащие |
50-250 мг/л |
> 10 мг/л |
> 50 мг/л |
Хлор содержащие соединение дешевле, чем йодофоры, но обладают коррозионным действием |
|
Четвертичные аммониевые соединения |
150-250 мг/л |
>100 мг/л |
— |
Обладают пролонгированным действием (~ 1 день), нейтральны, не агрессивны |
|
Перекись водорода |
3-90% |
>6% |
10-30% |
Более эффективна в сочетании с надуксусной кислотой |
|
Надуксусная кислота |
30-250 ppm |
30 ppm |
> 100 ppm |
Широкий спектр активности, присутствие органических веществ практически не снижает активности |
|
Спирты (этанол) |
20-70% |
>22% |
60-70% |
Имеют промышленное применение |
|
Альдегиды |
0.8-16 мг/л |
< 10 мг/л |
20 мг/л |
Имеют ограниченное промышленное применение в пищевой промышленности |
|
Бисфенолы |
2-20 мг/л |
> 10 мг/л |
— |
|
|
Бигуанидины |
> 150 мг/л |
1-60 мг/л |
— |
Используют в рецептурах кожного антисептика |
Стратегия оптимизации процессов очистки и дезинфекции.
Устойчивость патогенных микроорганизмов к действию моющих и дезинфицирующих веществ пока еще не стала глобальной проблемой пищевой промышленности. Однако работники пищевой промышленности должны осознавать возможность появления устойчивых штаммов патогенных микроорганизмов в случае неправомерного использования моющих и дезинфицирующих средств. Исследования показали, что даже кратковременное воздействие дезинфицирующими веществами на Listeria Monocytogenes в концентрациях, недостаточных для гибели патогенных микроорганизмов вызывают их мутацию, при этом могут сформироваться патогенные микроорганизмы, устойчивые к действию дезинфицирующих веществ. При использовании моющих и дезинфицирующих веществ следует принимать во внимание следующие факторы:
- выбор дезинфектанта, активного против данного вида патогенных микроорганизмов,
- соблюдение условий применения, рекомендованных производителем (температура, pH среды),
- присутствие веществ, способных к инактивации моющих или дезинфицирующих веществ,
- мониторинг чистоты поверхности и микробного фона до и после применения моющих и дезинфицирующих средств.
Как уже отмечалось, важным обстоятельством является правильный выбор дезинфицирующего агента, обладающего необходимым спектром активности против конкретного вида микроорганизмов. Например, не имеет смысла использовать дезинфицирующий агент на основе спиртов против спорообразующих бактерий вследствие низкой эффективности и возможности мутации некоторых микроорганизмов. Использование дезинфицирующих агентов, выделяющих активный хлор, будет ограничено их способностью к коррозии металлов и их способностью разрушать материалы на полимерной основе.
Соблюдение условий применения, обеспечивающих максимальный эффект снижения числа микроорганизмов, является важным обстоятельством как с точки зрения безопасности пищевого производства, так и с точки зрения сохранения сокращения финансовых затрат на уборку и дезинфекцию. К основным факторам, влияющим на процессы мойки и дезинфекции, относят концентрацию моющих или дезинфицирующих веществ, механическую работу, время и температуру. При применении дезинфицирующих средств следует руководствоваться рекомендациями производителя. Использование более концентрированных растворов, чем это необходимо, может привести к образованию нерастворимых соединений и активизации коррозионных процессов. Обработка поверхностей и оборудования при температурах более высоких, чем рекомендовано в инструкции производителя может привести к химическому разложению активного вещества, выпадению солей жесткости воды, полимеризации протеинов и жиров, что негативно скажется на качестве дезинфекции. Еще одним важным фактором в процессе дезинфекции является время контакта дезинфицирующего вещества, чем выше время контакта, тем выше число инактивированных микроорганизмов.
Существует много математических моделей, описывающих процесс инактивации микроорганизмов. При использовании этих моделей возникают трудности, поскольку они включают в себя параметры, которые сложно определить экспериментальным путем. Одна из моделей, которая используется чаще других, является линейно-логарифмическая модель Чика-Ватсона:
Log(N1/N0) = — ĸCnt ,
N1 — выжившее число микроорганизмов,
N0 –первоначальное число микроорганизмов,
ĸ — константа скорости дезинфекции,
C –концентрация дезинфектанта,
n – коэффициент разбавления,
t – время контакта.
Коэффициент разбавления n зависит от вида дезинфицирующего агента. Например, для четвертичных аммониевых солей n=1. Это означает, что при снижении концентрации n в два раза следует в два раза увеличить время экспозиции. Для этанола n=10, это означает, что при снижении концентрации этанола в два раза эффективность обработки снижается в 2¹º, т.е. в 1024 раза.
Очевидно, что механическая работа вносит важный вклад в качество дезинфекционной обработки. Чем больше затрачено механических усилий, тем меньше количество микроорганизмов остается на поверхности после очистки. Конечный результат зависит от правильности выбора дезинфектанта и технологий мойки и дезинфекции. При выборе моющих и дезинфицирующих средств и определении порядка выполнения технологических операций следует выбирать такое сочетание моющих и дезинфицирующих средств, чтобы не происходило инактивации дезинфицирующего вещества.
Таблица 5. Характеристики стандартных дезинфицирующих веществ
|
Характеристики |
Йодофоры |
Хлорсодержа- щие соединения |
Кислотосодер- жащие соединения |
Четвертичные аммониевые соли |
|
Антимикробная активность |
Вегетативные клетки |
Хорошая |
Хорошая |
Хорошая, имеется некоторая селективность |
|
Воздействие на дрожжи |
Хорошая |
Хорошая |
Хорошая |
Хорошая |
|
Воздействие на плесневые грибы |
Хорошая |
Хорошая |
Хорошая |
Хорошая |
|
Стабильность |
||||
|
при хранении |
Зависит от температуры |
Низкая |
Великолепная |
Великолепная |
|
при использовании |
Зависит от температуры |
Зависит от температуры |
Великолепная |
Великолепная |
|
Быстрота воздействия |
Быстрое |
Быстрое |
Быстрое |
Быстрое |
|
Проницаемость |
Хорошая |
Слабая |
Хорошая |
Великолепная |
|
Пленкообразование |
Нет или слабое |
— |
— |
+ |
|
Влияние органических веществ |
Среднее |
Сильное |
Незначительное |
Незначительное |
|
Легкость измерения |
Великолепная |
Великолепная |
Великолепная |
Великолепная |
Если после прочтения статьи у вас позникли вопросы — звоните по телефону вверху страницы! Или пишите на service@chemitech.ru Ответим на ваши вопросы по применению!



