Аквапенем
Порошок д/пригот. р-ра д/инф. 500 мг+500 мг: фл. 1 шт.
рег. №: ЛП-002698
от 07.11.14
Дата перерегистрации: 10.01.20
Бактопенем
Порошок д/пригот. р-ра д/инфузий 250 мг+250 мг: фл. 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006237
от 05.06.20
Порошок д/пригот. р-ра д/инфузий 500 мг+500 мг: фл. 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006237
от 05.06.20
Бианем-АФ
Порошок д/пригот. р-ра д/инф. 300 мг: фл. 1 шт.
рег. №: ЛП-007122
от 24.06.21
Порошок д/пригот. р-ра д/инф. 600 мг: фл. 1 шт.
рег. №: ЛП-007122
от 24.06.21
Биапенем-Джиэфси®
Порошок д/пригот.р-ра д/инфузий 300 мг
рег. №: ЛП-(001558)-(РГ-RU )
от 16.12.22
Порошок д/пригот.р-ра д/инфузий 600 мг
рег. №: ЛП-(001558)-(РГ-RU )
от 16.12.22
Велпенем®
Порошок д/пригот. р-ра д/в/в введения 1000 мг: фл. 1, 5 или 10 шт.
рег. №: ЛП-004172
от 03.03.17
Произведено и упаковано:
СИНТЕЗ
(Россия)
Велпенем®
Порошок д/пригот. р-ра д/в/в введения 500 мг : фл. 1, 5 или 10 шт.
рег. №: ЛП-004172
от 03.03.17
Произведено и упаковано:
СИНТЕЗ
(Россия)
Гримипенем®

Порошок д/пригот. р-ра д/инф. 500 мг+500 мг: фл. 1 шт.
рег. №: ЛСР-008834/08
от 06.11.08
Дата перерегистрации: 07.02.18
Дженем
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1, 3, 5, 6, 10, 30, 50 или 100 шт.
рег. №: ЛП-001177
от 11.11.11
Дата перерегистрации: 14.11.16
Порошок д/пригот. р-ра д/в/в введения 1000 мг: фл. 1, 3, 5, 6, 10, 30, 50 или 100 шт.
рег. №: ЛП-001177
от 11.11.11
Дата перерегистрации: 14.11.16
Доренем
Порошок д/пригот. р-ра д/инф. 500 мг: фл. 1 или 5 шт.
рег. №: ЛП-006951
от 19.04.21
Дорипенем
Порошок д/пригот. концентрата д/пригот. р-ра д/инф. 500 мг: фл. 1, 5 или 10 шт.
рег. №: ЛП-007143
от 30.06.21
Дорипенем
Порошок д/пригот. р-ра д/инф. 250 мг: фл.
рег. №: ЛП-005931
от 22.11.19
Порошок д/пригот. р-ра д/инф. 500 мг: фл.
рег. №: ЛП-005931
от 22.11.19
Дорипенем
Порошок д/пригот. р-ра д/инф. 250 мг: фл. 1 шт.
рег. №: ЛП-007920
от 28.02.22
Порошок д/пригот. р-ра д/инф. 500 мг: фл. 1 шт.
рег. №: ЛП-007920
от 28.02.22
Дорипенем
Порошок д/пригот. р-ра д/инф. 250 мг: фл. 1, 5 или 10 шт.
рег. №: ЛП-008503
от 29.08.22
Порошок д/пригот. р-ра д/инф. 500 мг: фл. 1, 5 или 10 шт.
рег. №: ЛП-008503
от 29.08.22
Дорипенем
Порошок д/пригот. р-ра д/инф. 250 мг: фл. 1, 5 или 10 шт.
рег. №: ЛП-007551
от 28.10.21
Дорипенем
Порошок д/пригот. р-ра д/инф. 500 мг: фл. 1 шт.
рег. №: ЛП-008206
от 30.05.22
Дорипенем
Порошок д/пригот. р-ра д/инф. 500 мг: фл. 1, 5 или 10 шт.
рег. №: ЛП-004833
от 04.05.18
Дата перерегистрации: 26.10.21
Дорипенем
Порошок д/пригот.р-ра д/инфузий 250 мг
рег. №: ЛП-008122
от 04.05.22
Порошок д/пригот.р-ра д/инфузий 500 мг
рег. №: ЛП-008122
от 04.05.22
Дорипенем Дж
Порошок д/пригот.р-ра д/инфузий 250 мг
рег. №: ЛП-008165
от 16.05.22
Порошок д/пригот.р-ра д/инфузий 500 мг
рег. №: ЛП-008165
от 16.05.22
Дорипенем МД
Порошок д/пригот. р-ра д/инф. 250 мг: фл. 1 шт.
рег. №: ЛП-007954
от 14.03.22
Дата перерегистрации: 16.08.22
Порошок д/пригот. р-ра д/инф. 500 мг: фл. 1 шт.
рег. №: ЛП-007954
от 14.03.22
Дата перерегистрации: 16.08.22
Дорипенем Эльфа
Порошок д/пригот. р-ра д/инф. 500 мг: фл. 1 шт.
рег. №: ЛП-006109
от 20.02.20
Дорипенем-Бинергия
Порошок д/пригот.р-ра д/инфузий 250 мг
рег. №: ЛП-008214
от 30.05.22
Порошок д/пригот.р-ра д/инфузий 500 мг
рег. №: ЛП-008214
от 30.05.22
Имипенем и Циластатин джодас
Порошок д/пригот. р-ра д/в/в введения 500 мг+500 мг: фл. 1, 5 или 10 шт.
рег. №: ЛСР-010475/08
от 24.12.08
Имипенем и Циластатин спенсер
Порошок д/пригот. р-ра д/в/в введения 500 мг+500 мг: фл. 1 шт.
рег. №: ЛСР-001340/07
от 29.06.07
Имипенем+Циластатин
Порошок д/пригот. р-ра д/инфузий 250 мг+250 мг: фл. 1 или 10 шт.
рег. №: ЛП-005318
от 25.01.19
Имипенем+Циластатин
Порошок д/пригот. р-ра д/инфузий 500 мг + 500 мг: фл. 1000 мг 1, 10 или 50 шт.
рег. №: ЛП-008518
от 31.08.22
Имипенем+Циластатин
Порошок д/пригот. р-ра д/инфузий 500 мг+500 мг: фл. 1 или 10 шт.
рег. №: ЛП-002466
от 19.05.14
Имипенем+Циластатин
Порошок д/пригот. р-ра д/инфузий 500 мг+500 мг: фл. 1 шт.
рег. №: ЛП-008128
от 05.05.22
Имипенем+Циластатин
Порошок д/пригот. р-ра д/инфузий 500 мг+500 мг: фл. 1 шт.
рег. №: ЛП-003845
от 20.09.16
Дата перерегистрации: 02.10.17
Имипенем+Циластатин

Порошок д/пригот. р-ра д/инфузий 500 мг+500 мг: фл. 1, 5, 10 или 25 шт.; бутылки 1 или 35 шт.
рег. №: ЛП-005254
от 20.12.18
Имипенем+Циластатин
Порошок д/пригот.р-ра д/инфузий 500 мг+500 мг
рег. №: ЛП-008723
от 13.01.23
Имипенем+Циластатин-Виал
Порошок д/пригот. р-ра д/инфузий 500 мг+500 мг: фл. 1 или10 шт.
рег. №: ЛП-003066
от 01.07.15
Имипенем+Циластатин-Джиэфси
Порошок д/пригот.р-ра д/инфузий 250 мг+250 мг: фл. 1, 5, 10 или 50 шт.
рег. №: ЛП-008021
от 06.04.22
Порошок д/пригот.р-ра д/инфузий 500 мг+500 мг: фл. 1, 5, 10 или 50 шт.
рег. №: ЛП-008021
от 06.04.22
Имицинем-ТФ
Порошок д/пригот.р-ра д/инфузий 500 мг+500 мг
рег. №: ЛП-008373
от 20.07.22
Мепенем
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 шт.
рег. №: ЛП-002354
от 28.01.14
Дата перерегистрации: 12.03.19
Мепенем
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 шт.
рег. №: ЛП-006008
от 24.12.19
Мерексид
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 шт.
рег. №: ЛСР-008460/10
от 19.08.10
Дата перерегистрации: 25.04.19
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 шт.
рег. №: ЛСР-008460/10
от 19.08.10
Дата перерегистрации: 25.04.19
Меронем®
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 10 шт.
рег. №: П N013294/01
от 04.02.10
Дата перерегистрации: 27.11.17
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 10 шт.
рег. №: П N013294/01
от 04.02.10
Дата перерегистрации: 27.11.17
Меропенабол®
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 шт.
рег. №: ЛСР-002218/07
от 15.08.07
Дата перерегистрации: 12.02.18
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 шт.
рег. №: ЛСР-002218/07
от 15.08.07
Дата перерегистрации: 12.02.18
Меропенем
Порошок д/пригот. р-ра д/в/в введения 0.5 г: фл.
рег. №: ЛП-004174
от 03.03.17
Меропенем
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 или 10 шт.
рег. №: ЛСР-002913/10
от 07.04.10
Меропенем
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 шт.
рег. №: ЛСР-007540/09
от 28.09.09
Меропенем
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 шт.
рег. №: ЛСР-007395/10
от 30.07.10
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 шт.
рег. №: ЛСР-007395/10
от 30.07.10
Меропенем
Порошок д/пригот. р-ра д/в/в введения 1000 мг: фл. 1 шт.
рег. №: ЛП-005948
от 02.12.19
Меропенем
Порошок д/пригот. р-ра д/в/в введения 1г : фл.
рег. №: ЛП-004174
от 03.03.17
Меропенем
Порошок д/пригот. р-ра д/в/в введения 500 мг : фл.
рег. №: ЛП-003989
от 01.12.16
Порошок д/пригот. р-ра д/в/в введения 1000 мг : фл.
рег. №: ЛП-003989
от 01.12.16
Меропенем
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл.
рег. №: ЛП-005073
от 26.09.18
Порошок д/пригот. р-ра д/в/в введения 1000 мг : фл.
рег. №: ЛП-005073
от 26.09.18
Меропенем
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 или 10 шт.
рег. №: ЛП-(000766)-(РГ-RU )
от 05.05.22
Предыдущий рег. №: ЛП-005940
Порошок д/пригот. р-ра д/в/в введения 1000 мг: фл. 1 или 10 шт.
рег. №: ЛП-(000766)-(РГ-RU )
от 05.05.22
Предыдущий рег. №: ЛП-005940
Меропенем
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 шт.
рег. №: ЛСР-007540/09
от 28.09.09
Меропенем
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 шт.
рег. №: ЛП-005948
от 02.12.19
Меропенем
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1, 10 или 50 шт.
рег. №: ЛП-000189
от 25.01.11
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1, 10 или 50 шт.
рег. №: ЛП-000189
от 25.01.11
Меропенем
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1, 5 или 10 шт.
рег. №: ЛП-005987
от 16.12.19
Порошок д/пригот. р-ра д/в/в введения 1000 мг: фл. 1, 5 или 10 шт.
рег. №: ЛП-005987
от 16.12.19
Меропенем
Порошок д/пригот.р-ра д/в/в введения 500 мг
рег. №: ЛП-008366
от 22.07.22
Порошок д/пригот.р-ра д/в/в введения 1000 мг
рег. №: ЛП-008366
от 22.07.22
Меропенем
Порошок д/пригот.р-ра д/в/м введения 500 мг: фл. 1 шт.
рег. №: ЛП-007973
от 21.03.22
Меропенем Джодас
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1, 5, 10, 25, 48 или 100 шт.
рег. №: ЛСР-010476/08
от 24.12.08
Меропенем Джодас
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1, 5, 10, 25,48 или 100 шт.
рег. №: ЛСР-010476/08
от 24.12.08
Меропенем МД
Порошок для приготовления раствора для внутривенного введения 1 г
рег. №: ЛП-008624
от 19.10.22
Меропенем Спенсер
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 шт.
рег. №: ЛСР-001342/07
от 29.06.07
Меропенем Спенсер
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 шт.
рег. №: ЛСР-001342/07
от 29.06.07
Меропенем Спенсер
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 шт.
рег. №: ЛСР-001342/07
от 29.06.07
Меропенем-Веро
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1, 10, 25 или 35 шт.
рег. №: ЛСР-002592/09
от 02.04.09
Меропенем-Веро
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1, 10, 25 или 35 шт.
рег. №: ЛСР-002592/09
от 02.04.09
Меропенем-Виал
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 или 600 шт. (упаковано Озон)
рег. №: ЛСР-001145/10
от 18.02.10
Упаковано:
ОЗОН
(Россия)
Меропенем-Виал
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 шт.
рег. №: ЛСР-001145/10
от 18.02.10
Меропенем-Виал
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 или 600 шт. (упаковано Озон)
рег. №: ЛСР-001145/10
от 18.02.10
Упаковано:
ОЗОН
(Россия)
Меропенем-Виал
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 шт.
рег. №: ЛСР-001145/10
от 18.02.10
Меропенем-ДЕКО
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 5 или 10 шт.
рег. №: ЛП-001718
от 02.07.12
Дата перерегистрации: 24.12.18
Меропенем-ДЕКО
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 5 или 10 шт.
рег. №: ЛП-005374
от 27.02.19
Меропенем-Джиэфси®
Порошок д/пригот.р-ра д/в/в введения 500 мг
рег. №: ЛП-008064
от 20.04.22
Порошок д/пригот.р-ра д/в/в введения 1000 мг
рег. №: ЛП-008064
от 20.04.22
Меропенем-ЛЕКСВМ®
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 или 10 шт.
рег. №: ЛП-000023
от 03.11.10
Дата перерегистрации: 08.04.20
Меропенем-Плетхико
Порошок д/пригот. р-ра д/в/в введения 1000 мг: фл. 1 шт.
рег. №: ЛП-001202
от 11.11.11
Меропенем-Плетхико
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 шт.
рег. №: ЛП-001202
от 11.11.11
Меропенем-ТФ
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 или 5 шт.
рег. №: ЛП-006523
от 20.10.20
Порошок д/пригот. р-ра д/в/в введения 1000 мг: фл. 1 или 5 шт.
рег. №: ЛП-006523
от 20.10.20
Меропенем-Элеас
Порошок д/пригот. р-ра д/в/в введения 1000 мг: фл. 1 шт.
рег. №: ЛП-007838
от 31.01.22
Пропинем
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 шт.
рег. №: ЛП-000524
от 01.03.11
Сайронем
Порошок д/пригот. р-ра д/в/в введения 0.5 г: фл. 1 или 10 шт.
рег. №: ЛСР-004345/09
от 01.06.09
Дата перерегистрации: 11.06.20
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 или 10 шт.
рег. №: ЛСР-004345/09
от 01.06.09
Дата перерегистрации: 11.06.20
Саноцеф®
Порошок д/пригот. р-ра д/инф. 500 мг: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006043
от 17.01.20
ТиелВел®
Порошок д/пригот. р-ра д/инфузий 250 мг+250 мг: фл. 1, 5 или 10 шт.
рег. №: ЛП-007497
от 15.10.21
ТиелВел®
Порошок д/пригот. р-ра д/инфузий 500 мг+500 мг: фл. 1, 5 или 10 шт.
рег. №: ЛП-(000236)-(РГ-RU )
от 19.05.21
Предыдущий рег. №: ЛП-003812
Тиепенем®
Порошок д/пригот. р-ра д/инфузий 500 мг+500 мг: фл. 1 или 10 шт.
рег. №: ЛП-002930
от 30.03.15
ФармАмеропен
Порошок д/пригот. р-ра д/в/в введения 0.5 г: 1, 5, 10, 15, 25 или 50 шт.
рег. №: ЛП-005985
от 16.12.19
Порошок д/пригот. р-ра д/в/в введения 1 г: 1, 5, 10, 15, 25 или 50 шт.
рег. №: ЛП-005985
от 16.12.19
Цилапенем
Порошок д/пригот. р-ра д/инфузий 0.25 г+0.25 г: фл.
рег. №: ЛП-006940
от 15.04.21
Цилапенем
Порошок д/пригот. р-ра д/инфузий 250 мг+250 мг: бут. 1 или 12 шт.
рег. №: ЛП-001141
от 09.11.11
Цилапенем
Порошок д/пригот. р-ра д/инфузий 500 мг+500 мг: бут. 1 или 12 шт.
рег. №: ЛП-001141
от 09.11.11
Циласпен
Порошок д/пригот. р-ра д/инф. 500 мг+500 мг: фл. 1 шт.
рег. №: ЛСР-004732/10
от 26.05.10
Азаран
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 50 шт.
рег. №: П N015049/01
от 31.10.08
Дата перерегистрации: 18.09.17
Порошок д/пригот. р-ра д/инъекц. 250 мг: фл. 1, 10 или 50 шт.
рег. №: П N015049/01-2003
от 23.06.03
Азарексон
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006110
от 20.02.20
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006110
от 20.02.20
Порошок д/пригот. р-ра д/в/в и в/м введения 1000 мг: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006110
от 20.02.20
Азнам Дж
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1, 10, 25, 48 или 100 шт.
рег. №: ЛСР-002492/10
от 26.03.10
Дата перерегистрации: 05.02.16
Азнам Дж
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10, 25, 48 или 100 шт.
рег. №: ЛСР-002492/10
от 26.03.10
Дата перерегистрации: 05.02.16
Азтреабол
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл.
рег. №: ЛСР-000123/09
от 14.01.09
Азтреабол
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл.
рег. №: ЛСР-000123/09
от 14.01.09
Азтреонам Эльфа
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 шт.
рег. №: ЛП-006997
от 12.05.21
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛП-006997
от 12.05.21
Азтреонам-Деко
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 шт.
рег. №: ЛП-005790
от 11.09.19
Азтреонам-Деко
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛП-005790
от 11.09.19
Аксетин
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г: фл. 1 или 100 шт.
рег. №: ЛС-000023
от 12.04.10
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1 или 100 шт.
рег. №: П N012836/01
от 16.04.12
Аксоне
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛС-002684
от 05.03.12
Аксосеф
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. в комплекте с растворителем
рег. №: ЛП-001214
от 15.11.11
Аксосеф
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. в комплекте с растворителем
рег. №: ЛП-001214
от 15.11.11
Аксосеф
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. в комплекте с растворителем
рег. №: ЛП-001214
от 15.11.11
Аксосеф
Таб., покр. пленочной оболочкой, 250 мг: 20 шт.
рег. №: ЛП-001198
от 11.11.11
Аксосеф
Таб., покр. пленочной оболочкой, 500 мг: 20 шт.
рег. №: ЛП-001198
от 11.11.11
Амбицеф
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-005913
от 18.11.19
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-005913
от 18.11.19
Анаэроцеф®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N003297/01
от 02.03.09
Дата перерегистрации: 07.02.18
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N003297/01
от 02.03.09
Дата перерегистрации: 07.02.18
Антибиоксим
Порошок д/пригот. р-ра д/в/в введения 1.5 г: фл. 1 шт.
рег. №: ЛСР-005423/10
от 10.06.10
Бакперазон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл. 1 шт.
рег. №: ЛСР-009612/09
от 30.11.09
Бакперазон
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг+250 мг: фл. 1 шт.
рег. №: ЛСР-009612/09
от 30.11.09
Бакперазон
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг+500 мг: фл. 1 шт.
рег. №: ЛСР-009612/09
от 30.11.09
Бакцефорт
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г+0.5 г: фл. 1 или 10 шт.; фл. 1 или 5 шт. в компл. с растворителем
рег. №: ЛП-004449
от 11.09.17
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл. 1 или 10 шт.; фл. 1 или 5 шт. в компл. с растворителем
рег. №: ЛП-004449
от 11.09.17
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г+1.5 г: фл. 1 или 10 шт.; фл. 1 или 5 шт. в компл. с растворителем
рег. №: ЛП-004449
от 11.09.17
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г+2 г: фл. 1 или 10 шт.; фл. 1 или 5 шт. в компл. с растворителем
рег. №: ЛП-004449
от 11.09.17
Бестум
Порошок д/пригот. р-ра д/инъекц. 1 г: фл. 1 шт.
рег. №: П N015905/01
от 06.10.09
Бестум
Порошок д/пригот. р-ра д/инъекц. 250 мг: фл. 1 шт.
рег. №: П N015905/01
от 06.10.09
Бестум
Порошок д/пригот. р-ра д/инъекц. 500 мг: фл. 1 шт.
рег. №: П N015905/01
от 06.10.09
Бетаспорина
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 50 шт.
рег. №: ЛСР-007701/09
от 01.10.09
Броадсеф-С
Порошок д/пригот. р-ра д/в/в и в/м введения1 г+0.5 г: фл. 1 шт.
рег. №: ЛП-002913
от 16.03.15
Велоцесим
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-008644
от 31.10.22
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл.1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-008644
от 31.10.22
Порошок д/пригот. р-ра д/в/в и в/м введения 1500 мг: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-008644
от 31.10.22
Винцепим
Порошок д/пригот. р-ра д/в/м введения 0.5 г: фл. 1 или 10 шт.
рег. №: ЛСР-005870/09
от 20.07.09
Дата перерегистрации: 26.05.21
Порошок д/пригот. р-ра д/в/м введения 1 г: фл. 1 или 10 шт.
рег. №: ЛСР-005870/09
от 20.07.09
Дата перерегистрации: 26.05.21
Вицеф®
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000653/01
от 20.12.07
Дата перерегистрации: 12.08.19
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000653/01
от 20.12.07
Дата перерегистрации: 12.08.19
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000653/01
от 20.12.07
Дата перерегистрации: 12.08.19
Децефим
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006401
от 12.08.20
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006401
от 12.08.20
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006401
от 12.08.20
Доксеф
Таб., покр. пленочной оболочкой, 100 мг: 10 или 20 шт.
рег. №: ЛП-004285
от 10.05.17
Доксеф
Таб., покр. пленочной оболочкой, 200 мг: 10 или 20 шт.
рег. №: ЛП-004285
от 10.05.17
Завицефта
Порошок д/пригот. концентрата д/пригот. р-ра д/инф. 2000 мг+ 500 мг: фл. 10 шт.
рег. №: ЛП-004289
от 15.05.17
Зербакса®
Порошок д/пригот. конц. д/пригот. р-ра д/инф. 1000 мг+500 мг: фл. 10 шт.
рег. №: ЛП-(000903)-(РГ-RU )
от 16.06.22
Предыдущий рег. №: ЛП-005085
Фасовка, упаковка и выпускающий контроль качества:
STERI-PHARMA LLC
(США)
Упаковка и выпускающий контроль качества:
FAREVA Mirabel
(Франция)
Зинацеф
Порошок д/пригот. р-ра д/инъекц. 1.5 г: фл. 1 шт.
рег. №: П N015538/01
от 15.05.09
Порошок д/пригот. р-ра д/инъекц. 250 мг: фл. 1 шт.
рег. №: П N015538/01
от 15.05.09
Порошок д/пригот. р-ра д/инъекц. 750 мг: фл. 1 шт.
рег. №: П N015538/01
от 15.05.09
Зиннат®
Гранулы д/пригот. сусп. д/приема внутрь 125 мг/5 мл: фл. 1 шт. в компл. с дозир. ложкой и мерн. стаканом
рег. №: П N008779
от 28.06.10
Дата перерегистрации: 10.11.17
Зиннат®
Таб., покр. пленочной оболочкой, 125 мг: 10 шт.
рег. №: П N015531/01
от 06.03.09
Дата перерегистрации: 12.02.14
Таб., покр. пленочной оболочкой, 250 мг: 10 шт.
рег. №: П N015531/01
от 06.03.09
Дата перерегистрации: 12.02.14
Зинфоро®
Порошок д/пригот. концентрата д/пригот. р-ра д/инфузий 600 мг: фл. 1 или 10 шт.
рег. №: ЛП-001912
от 20.11.12
Золин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 20 или 50 шт.
рег. №: П N012534/01
от 04.03.10
Золин
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1, 5, 20 или 50 шт.
рег. №: П N012534/01
от 04.03.10
Золин
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5, 20 или 50 шт.
рег. №: П N012534/01
от 04.03.10
Иксим Люпин
Порошок д/пригот. сусп. д/приема внутрь 100 мг/5 мл: фл. 25 г
рег. №: ЛСР-005238/09
от 30.06.09
Интразолин
Порошок д/пригот. р-ра д/инъекций 1 г: фл. 10 мл 1 шт.
рег. №: П N013048/01-2001
от 26.11.08
Интрасеф
Порошок д/пригот. р-ра д/в/в введения 1 г в компл. с растворителем: фл. 1 или 100 шт.
рег. №: П N014008/01
от 10.06.08
Интрасеф
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 или 100 шт.
рег. №: П N014008/01
от 10.06.08
Интрасеф
Порошок д/пригот. р-ра д/в/в введения 500 мг в компл. с растворителем: фл. 100 шт.
рег. №: П N014008/01
от 10.06.08
Интрасеф
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 или 100 шт.
рег. №: П N014008/01
от 10.06.08
Интрасеф
Порошок д/пригот. р-ра д/в/м введения 1 г в компл. с растворителем: фл. 1 или 100 шт.
рег. №: П N014008/02
от 17.06.08
Интрасеф
Порошок д/пригот. р-ра д/в/м введения 1 г: фл. 1 или 100 шт.
рег. №: П N014008/02
от 17.06.08
Интрасеф
Порошок д/пригот. р-ра д/в/м введения 500 мг в компл. с растворителем: фл. 100 шт.
рег. №: П N014008/02
от 17.06.08
Интрасеф
Порошок д/пригот. р-ра д/в/м введения 500 мг: фл. 1 или 100 шт.
рег. №: П N014008/02
от 17.06.08
Интратаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 100 шт.
рег. №: П N013197/01
от 01.08.08
Ифицеф®
Порошок д/пригот. р-ра д/в/в или в/м введения 1 г: фл. 1 шт.
рег. №: П N011722/01
от 30.08.11
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт.
рег. №: П N011722/01
от 30.08.11
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: П N011722/01
от 30.08.11
Кефотекс
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N016209/01
от 26.02.10
Кефотекс
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт.
рег. №: П N016209/01
от 26.02.10
Кефотекс
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: П N016209/01
от 26.02.10
Кефсепим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛП-001266
от 24.11.11
Дата перерегистрации: 22.05.19
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: ЛП-001266
от 24.11.11
Дата перерегистрации: 22.05.19
Кларуктам
Порошок д/пригот. р-ра д/в/в и в/м введения 1000 мг+ 500 мг: фл. 1 или 5 шт. в комплекте с растворителем или без него
рег. №: ЛП-004552
от 20.11.17
Дата перерегистрации: 07.12.15
Клафобрин
Порошок д/пригот. р-ра д/инъекц. 1 г: фл. 1, 5 или 50 шт.
рег. №: Р N000677/01-2001
от 31.07.08
Клафобрин
Порошок д/пригот. р-ра д/инъекц. 500 мг: фл. 1 шт.
рег. №: Р N000677/01-2001
от 31.07.08
Клафоран®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N008945
от 05.09.11
Лендацин®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10 или 50 шт.
рег. №: П N008670
от 13.08.10
Произведено:
SANDOZ
(Австрия)
Лендацин®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10 или 50 шт.
рег. №: П N008670
от 13.08.10
Лендацин®
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1, 5 или 10 шт.
рег. №: П N008670
от 13.08.10
Произведено:
SANDOZ
(Австрия)
Лендацин®
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1, 5 или 10 шт.
рег. №: П N008670
от 13.08.10
Лендацин®
Порошок д/пригот. р-ра д/инф. 2 г: фл. 1, 5 или 10 шт.
рег. №: П N008670
от 13.08.10
Произведено:
SANDOZ
(Австрия)
Лендацин®
Порошок д/пригот. р-ра д/инф. 2 г: фл. 1, 5 или 10 шт.
рег. №: П N008670
от 13.08.10
Лизолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N016309/01
от 20.05.05
Дата перерегистрации: 08.07.15
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: П N016309/01
от 20.05.05
Дата перерегистрации: 08.07.15
Произведено и расфасовано:
LYKA LABS
(Индия)
Лифаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N012292/01
от 05.10.09
Лифоран
Порошок д/пригот. р-ра д/инъекц. 1 г: фл. 1 шт.
рег. №: П N013793/01-2002
от 08.06.09
Порошок д/пригот. р-ра д/инъекц. 250 мг: фл. 1 шт.
рег. №: П N013793/01-2002
от 08.06.09
Порошок д/пригот. р-ра д/инъекц. 500 мг: фл. 1 шт.
рег. №: П N013793/01-2002
от 08.06.09
Максиктам®-АФ
Порошок д/пригот. р-ра д/в/в и в/м введения 1000 мг+1000 мг: фл. 1 шт.
рег. №: ЛП-005253
от 20.12.18
Дата перерегистрации: 19.03.20
Максицеф®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N003298/01
от 02.03.09
Дата перерегистрации: 15.01.18
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N003298/01
от 02.03.09
Дата перерегистрации: 15.01.18
Медаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 100 шт.
рег. №: П N015208/01-2003
от 15.08.08
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1,10 или 100 шт.
рег. №: П N015208/01-2003
от 15.08.08
Медоцеф
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N011311/01
от 12.04.10
Медоцеф
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 шт.
рег. №: П N011311/01
от 12.04.10
Мовигип
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 10 шт.
рег. №: ЛСР-002217/07
от 15.08.07
Мовигип
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 или 10 шт.
рег. №: ЛСР-002217/07
от 15.08.07
Мовигип
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 10 шт.
рег. №: ЛСР-002217/07
от 15.08.07
Мовизар
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 10 шт.
рег. №: ЛСР-001565/08
от 14.03.08
Мовизар
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 или 10 шт.
рег. №: ЛСР-001565/08
от 14.03.08
Мовизар
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 или 10 шт.
рег. №: ЛСР-001565/08
от 14.03.08
Мовопериз
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 10 шт.
рег. №: ЛСР-002223/07
от 15.08.07
Нацеф®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000882/01
от 17.04.07
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000882/01
от 17.04.07
Дата перерегистрации: 29.08.19
Операз
Порошок д/пригот. р-ра д/инъекц. 1 г: фл. 1 или 100 шт.
рег. №: П N015385/01
от 11.01.09
Орзид
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N014421/01
от 28.03.14
Орзид
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт.
рег. №: П N014421/01
от 22.03.14
Орзид
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: П N014421/01
от 28.03.14
Оритакс
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10, 25 или 100 шт.
рег. №: ЛСР-001139/10
от 18.02.10
Оритакс
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 10, 25 или 100 шт.
рег. №: ЛСР-001139/10
от 18.02.10
Оритаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N011830/01
от 19.09.11
Оритаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт.
рег. №: П N011830/01
от 19.09.11
Оритаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: П N011830/01
от 19.09.11
Орпин®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-009318/08
от 25.11.08
Дата перерегистрации: 27.03.18
Офрамакс
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт. в компл. с растворителем
рег. №: П N012523/01
от 15.07.11
Офрамакс
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт. в компл. с растворителем
рег. №: П N012523/01
от 15.07.11
Панцеф®
Гранулы д/пригот. сусп. д/приема внутрь 100 мг/5 мл: фл. 32 г или 53 г в компл. с дозир. шприцем и мерн. колпачком
рег. №: ЛП-(000250)-(РГ-RU )
от 26.05.21
Предыдущий рег. №: ЛСР-009444/09
Панцеф®
Таб., покр. пленочной оболочкой, 400 мг: 6, 7 или 10 шт.
рег. №: ЛП-(000246)-(РГ-RU )
от 25.05.21
Предыдущий рег. №: ЛСР-001308/09
Протозидим
Порошок д/пригот. р-ра д/в/в и в/м введения 0.25 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006039
от 15.01.20
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006039
от 15.01.20
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006039
от 15.01.20
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006039
от 15.01.20
Роцефин®
Порошок д/пригот. р-ра д/в/в введения 1 г: фл. 1 шт. в компл. с растворителем
рег. №: П N013244/02
от 27.08.10
Дата перерегистрации: 06.12.17
Порошок д/пригот. р-ра д/в/м введения 1 г: фл. 1 шт. в компл. с растворителем
рег. №: П N013244/01
от 31.08.10
Дата перерегистрации: 09.11.17
Порошок д/пригот. р-ра д/в/м введения 250 мг: фл. 5 шт. в компл. с растворителем
рег. №: П N013244/01
от 31.08.10
Дата перерегистрации: 09.11.17
Порошок д/пригот. р-ра д/в/в введения 250 мг: фл. 5 шт. в компл. с растворителем
рег. №: П N013244/02
от 27.08.10
Дата перерегистрации: 06.12.17
Порошок д/пригот. р-ра д/в/м введения 500 мг: фл. 1 шт. в компл. с растворителем
рег. №: П N013244/01
от 31.08.10
Дата перерегистрации: 09.11.17
Порошок д/пригот. р-ра д/в/в введения 500 мг: фл. 1 шт. в компл. с растворителем
рег. №: П N013244/02
от 27.08.10
Дата перерегистрации: 06.12.17
Руцектам®
Порошок д/пригот. р-ра д/в/в и в/м введения1000 мг+500 мг: фл.
рег. №: ЛП-007285
от 12.08.21
Руцеф
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г: фл. 1 или 10 шт.
рег. №: ЛП-004677
от 02.02.18
Дата перерегистрации: 25.11.21
Руцеф
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 или 10 шт.
рег. №: ЛСР-002529/07
от 31.08.07
Дата перерегистрации: 01.12.21
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1 или 10 шт.
рег. №: ЛСР-002529/07
от 31.08.07
Дата перерегистрации: 01.12.21
Руцеф
Порошок д/пригот. р-ра д/в/м введения 250 мг: фл. 1, 10 или 50 шт.
рег. №: ЛСР-002181/07
от 15.08.07
Дата перерегистрации: 16.12.21
Порошок д/пригот. р-ра д/в/м введения 750 мг: фл. 1, 10 или 50 шт.
рег. №: ЛСР-002181/07
от 15.08.07
Дата перерегистрации: 16.12.21
Сефпотек®
Таб., покр. пленочной оболочкой, 200 мг: 10, 14 или 20 шт.
рег. №: ЛП-001006
от 18.10.11
Дата перерегистрации: 18.08.17
Спектрацеф
Таб., покр. пленочной оболочкой, 200 мг: 14 или 20 шт.
рег. №: ЛП-001420
от 12.01.12
Дата перерегистрации: 10.12.20
Таб., покр. пленочной оболочкой, 400 мг: 10 шт.
рег. №: ЛП-001420
от 12.01.12
Дата перерегистрации: 10.12.20
Вторичная упаковка и выпускающий контроль качества:
ОРТАТ
(Россия)
Стафотаксим
Порошок д/пригот. р-ра д/инъекций 0.25 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006587
от 23.11.20
Порошок д/пригот. р-ра д/инъекций 0.5 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006587
от 23.11.20
Порошок д/пригот. р-ра д/инъекций 1 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006587
от 23.11.20
Порошок д/пригот. р-ра д/инъекций 2 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006587
от 23.11.20
Стерицеф
Порошок д/пригот. р-ра д/инъекц. 1 г: фл. 1 шт.
рег. №: П N014470/01
от 03.02.14
Стерицеф
Порошок д/пригот. р-ра д/инъекц. 250 мг: фл. 1 шт.
рег. №: П N014470/01
от 03.02.14
Стерицеф
Порошок д/пригот. р-ра д/инъекц. 500 мг: фл. 1 шт.
рег. №: П N014470/01
от 03.02.14
Сульзонцеф®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл. 1, 5, 10 или 50 шт.
рег. №: ЛСР-003512/09
от 13.05.09
Сульзонцеф®
Порошок д/пригот. р-ра д/в/в и в/м введения 1500 мг+1500 мг: фл. 1 или 10 шт.
рег. №: ЛП-(000929)-(РГ-RU )
от 24.06.22
Предыдущий рег. №: ЛП-006420
Сульзонцеф®
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг+250 мг: фл. 1 шт. в компл. с растворителем или без него, или 10 шт.
рег. №: ЛП-(000788)-(РГ-RU )
от 16.05.22
Предыдущий рег. №: ЛП-006542
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг+500 мг: фл. 1 шт. в компл. с растворителем или без него, или 10 шт.
рег. №: ЛП-(000788)-(РГ-RU )
от 16.05.22
Предыдущий рег. №: ЛП-006542
Сульмаграф
Порошок д/пригот. р-ра д/в/в и в/м введения 0.25 г+0.25 г: фл. 1 или 10 шт.
рег. №: ЛП-000972
от 18.10.11
Дата перерегистрации: 14.12.17
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г+0.5 г: фл. 1 или 10 шт.
рег. №: ЛП-000972
от 18.10.11
Дата перерегистрации: 14.12.17
Порошок д/пригот. р-ра д/в/в и в/м введения 0.75 г+0.75 г: фл. 1 или 10 шт.
рег. №: ЛП-000972
от 18.10.11
Дата перерегистрации: 14.12.17
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г+1.5 г: фл. 1 или 10 шт.
рег. №: ЛП-000972
от 18.10.11
Дата перерегистрации: 14.12.17
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г+2 г: фл. 1 или 10 шт.
рег. №: ЛП-000972
от 18.10.11
Дата перерегистрации: 14.12.17
Сульмаграф
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл. 1 или 10 шт.
рег. №: ЛС-001042
от 14.05.10
Дата перерегистрации: 06.03.19
Сульперацеф®

Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N003060/01
от 15.01.09
Дата перерегистрации: 15.01.18
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг+250 мг: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N003060/01
от 15.01.09
Дата перерегистрации: 15.01.18
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг+500 мг: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N003060/01
от 15.01.09
Дата перерегистрации: 15.01.18
Сультриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения1 г+0.5 г: фл. 1 или 10 шт.
рег. №: ЛП-(000751)-(РГ-RU )
от 04.05.22
Предыдущий рег. №: ЛП-005811
Сульцеф
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл. 1 или 100 шт.
рег. №: ЛС-001677
от 24.01.13
Супракс®
Гранулы д/пригот. сусп. д/приема внутрь 100 мг/5 мл: фл. 30.3-35.0 г в компл. с дозир. ложкой
рег. №: П N013023/02
от 09.06.09
Дата перерегистрации: 01.11.16
Произведено и упаковано:
ACS DOBFAR
(Италия)
Супракс®
Гранулы д/пригот. сусп. д/приема внутрь 100 мг/5 мл: фл. 30.3-35.0 г в компл. с дозир. шприцем
рег. №: П N013023/02
от 09.06.09
Дата перерегистрации: 01.11.16
Или упаковка и выпускающий контроль качества:
FACTA FARMACEUTICI
(Италия)
Супракс®
Капс. 400 мг: 6 шт.
рег. №: П N013023/01
от 09.06.09
Дата перерегистрации: 31.05.13
Супракс® Солютаб®
Таб. диспергируемые 400 мг: 1, 5, 7 или 10 шт.
рег. №: ЛСР-005995/10
от 25.06.10
Дата перерегистрации: 02.09.14
Такс-О-Бид
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N012988/01
от 23.07.09
Талцеф
Порошок д/пригот. р-ра д/инъекц. 1 г: фл. 1 шт.
рег. №: П N013805/01-2002
от 29.08.08
Порошок д/пригот. р-ра д/инъекц. 250 мг: фл. 1 шт.
рег. №: П N013805/01-2002
от 29.08.08
Порошок д/пригот. р-ра д/инъекц. 500 мг: фл. 1 шт.
рег. №: П N013805/01-2002
от 29.08.08
Тизим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N014900/01
от 30.06.09
Тизим
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт.
рег. №: П N014900/01
от 30.06.09
Тизим
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: П N014900/01
от 30.06.09
Тороцеф®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 50 шт.
рег. №: П N012503/01
от 03.02.12
Тороцеф®
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт.
рег. №: П N012503/01
от 03.02.12
Триаксон
Порошок д/пригот. инъекцион. р-ра 1 г: фл. 1, 5, 20 или 50 шт.
рег. №: П N012572/01-2001
от 01.07.08
Триаксон
Порошок д/пригот. инъекцион. р-ра 250 мг: фл. 1, 5, 20 или 50 шт.
рег. №: П N012572/01-2001
от 01.07.08
Триаксон
Порошок д/пригот. инъекцион. р-ра 500 мг: фл. 1, 5, 20 или 50 шт.
рег. №: П N012572/01-2001
от 01.07.08
Фортазим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N011799/01
от 21.12.11
Фортазим
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 шт.
рег. №: ЛСР-004892/09
от 19.06.09
Фортум
Порошок д/пригот. р-ра д/инъекц. 1 г: фл. 1 шт.
рег. №: П N015707/01
от 25.05.09
Порошок д/пригот. р-ра д/инъекц. 2 г: фл. 1 шт.
рег. №: П N015707/01
от 25.05.09
Порошок д/пригот. р-ра д/инъекц. 250 мг: фл. 1 шт.
рег. №: П N015707/01
от 25.05.09
Порошок д/пригот. р-ра д/инъекц. 500 мг: фл. 1 шт.
рег. №: П N015707/01
от 25.05.09
Хизон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 10 шт.
рег. №: ЛСР-001363/08
от 29.02.08
Цебактофан
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 0.25 г+0.25 г: фл. 1, 5, 10, 15, 25 шт.
рег. №: ЛП-006442
от 04.09.20
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 0.5 г+0.5 г: фл. 1, 5, 10, 15, 25 шт.
рег. №: ЛП-006442
от 04.09.20
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 0.75 г+0.75 г: фл. 1, 5, 10, 15, 25 шт.
рег. №: ЛП-006442
от 04.09.20
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 1 г+1 г: фл. 1, 5, 10, 15, 25 шт.
рег. №: ЛП-006442
от 04.09.20
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 1.5 г+1.5 г: фл. 1, 5, 10, 15, 25 шт.
рег. №: ЛП-006442
от 04.09.20
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 2 г+2 г: фл. 1, 5, 10, 15, 25 шт.
рег. №: ЛП-006442
от 04.09.20
Цебанекс
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 1 г+1 г: фл. 1 или 50 шт.
рег. №: ЛП-000725
от 29.09.11
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 500 мг+500 мг: фл. 1 или 50 шт.
рег. №: ЛСР-005034/07
от 21.12.07
Цезолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N016211/01
от 05.05.10
Цезолин
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: П N016211/01
от 05.05.10
Цемидексор®
Таб., покр. пленочной оболочкой, 100 мг: 6, 12 или 24 шт.
рег. №: ЛП-000814
от 06.10.11
Дата перерегистрации: 16.03.17
Цеперон ДЖ
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10, 25, 48 или 100 шт.
рег. №: ЛСР-006701/10
от 15.07.10
Цеперон ДЖ
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1, 10, 25, 48 или 100 шт.
рег. №: ЛСР-006701/10
от 15.07.10
Цепим®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 50 шт.
рег. №: ЛСР-009403/09
от 23.11.09
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 10 или 50 шт.
рег. №: ЛСР-009403/09
от 23.11.09
Произведено:
СИНТЕЗ
(Россия)
Церафазон
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-(000825)-(РГ-RU )
от 27.05.22
Предыдущий рег. №: ЛП-006095
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-(000825)-(РГ-RU )
от 27.05.22
Предыдущий рег. №: ЛП-006095
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-(000825)-(РГ-RU )
от 27.05.22
Предыдущий рег. №: ЛП-006095
Цетакс
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 20 или 50 шт.
рег. №: П N012571/01
от 05.10.09
Цетакс
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1, 5, 20 или 50 шт.
рег. №: П N012571/01
от 05.10.09
Цетакс
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5, 20 или 50 шт.
рег. №: П N012571/01
от 05.10.09
Цетил Люпин
Таб., покр. оболочкой, 250 мг: 40 или 100 шт.
рег. №: ЛСР-001905/10
от 12.03.10
Цетил Люпин
Таб., покр. оболочкой, 500 мг: 40 или 100 шт.
рег. №: ЛСР-001905/10
от 12.03.10
Цефабол®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N001155/01
от 21.04.08
Дата перерегистрации: 15.01.18
Порошок д/пригот. р-ра д/инъекц. 500 мг: фл. 1 шт.
рег. №: Р N001155/01-2002
от 21.04.08
Цефазолин
Порошок д/пригот. инъекц. р-ра 1 г: фл. 1 шт.
рег. №: ЛСР-002485/07
от 28.08.07
Цефазолин
Порошок д/пригот. инъекц. р-ра 1 г: фл. 1 шт.
рег. №: ЛСР-002485/07
от 28.08.07
Цефазолин
Порошок д/пригот. инъекц. р-ра 1 г: фл. 1 шт.
рег. №: П N012330/01
от 19.02.10
Цефазолин
Порошок д/пригот. инъекц. р-ра 250 мг: фл. 1 шт.
рег. №: П N012330/01
от 19.02.10
Цефазолин
Порошок д/пригот. инъекц. р-ра 500 мг: фл. 1 шт.
рег. №: П N012330/01
от 19.02.10
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. по 10 мл 1 шт., в комплекте с растворителем 2 мл или 5 мл 1 шт.
рег. №: ЛП-003093
от 14.07.15
Дата перерегистрации: 02.11.21
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 10 шт.
рег. №: ЛП-003947
от 08.11.16
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 40 шт.
рег. №: П N010948/01
от 27.07.10
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 5 шт.
рег. №: ЛС-000084
от 16.02.10
Дата перерегистрации: 14.10.19
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N015271/01
от 15.12.08
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт.
рег. №: П N015271/01
от 15.12.08
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: П N015271/01
от 15.12.08
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 2, 5 10 или 50 шт.
рег. №: ЛСР-009187/08
от 20.11.08
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5 или 50 шт.
рег. №: ЛС-002273
от 29.11.11
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. по 10 мл 1 шт., в комплекте с растворителем 5 мл 1 шт.
рег. №: ЛП-003093
от 14.07.15
Дата перерегистрации: 02.11.21
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1000 мг: фл. 1 шт.
рег. №: ЛП-003038
от 18.06.15
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 или 40 шт.
рег. №: П N010948/01
от 27.07.10
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 50 шт.
рег. №: ЛС-000926
от 27.02.12
Дата перерегистрации: 17.05.19
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 или 50 шт.
рег. №: ЛС-000926
от 27.02.12
Дата перерегистрации: 17.05.19
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: ЛП-003038
от 18.06.15
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛП-008201
от 24.05.22
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: ЛП-008201
от 24.05.22
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5 или 50 шт.
рег. №: ЛС-002273
от 29.11.11
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5, 10 или 50 шт.
рег. №: ЛС-001403
от 17.04.13
Цефазолин
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5, 30 или 50 шт.
рег. №: ЛС-000084
от 16.02.10
Дата перерегистрации: 14.10.19
Цефазолин
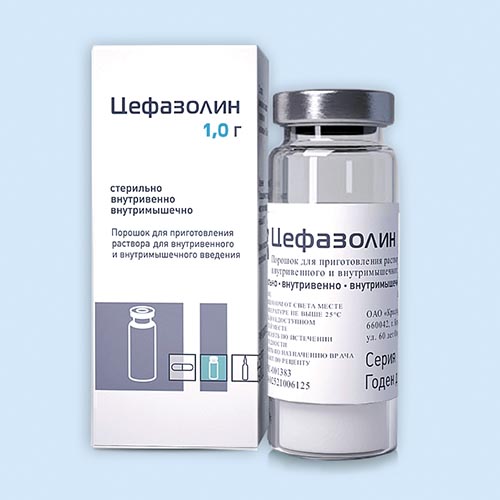
Порошок д/пригот. р-ра д/в/м введения 1 г: фл. по 9, 10 или 15 мл, 1, 10 или 50 шт.
рег. №: Р N003079/01
от 21.11.08
Цефазолин
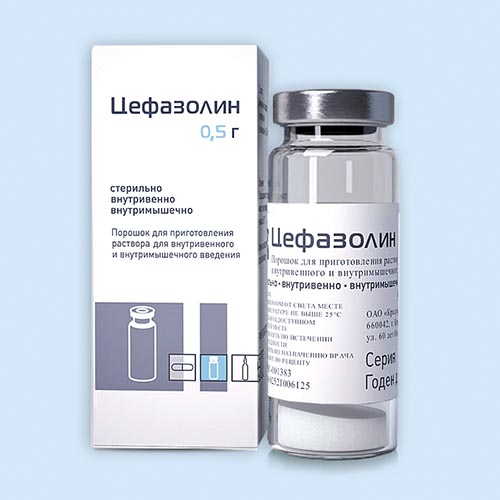
Порошок д/пригот. р-ра д/в/м введения 500 мг: фл. 9, 10 или 15 мл, 1, 10 или 50 шт.
рег. №: Р N003079/01
от 21.11.08
Цефазолин Эльфа®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-001364/08
от 29.02.08
Дата перерегистрации: 17.02.22
Цефазолин-АКОС
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 50 шт.
рег. №: Р N002895/01
от 10.12.12
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 10 или 50 шт.
рег. №: Р N002895/01
от 10.12.12
Цефазолин-Ферейн
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10, 50, 100, 108, 115, 150, 200, 250, 350, 500, 888 или 1000 шт.
рег. №: Р N000982/02
от 13.10.08
Цефазолин-Ферейн
Порошок д/пригот. р-ра д/в/м введения 1 г: фл. 1, 5, 10, 50, 100, 108, 115, 150, 200, 250, 350, 500, 888 или 1000 шт.
рег. №: Р N000982/01
от 13.10.08
Цефазолина натриевая соль
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 50 шт.
рег. №: ЛС-001383
от 31.01.11
Цефазолина натриевая соль
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 10 или 50 шт.
рег. №: ЛС-001383
от 31.01.11
Цефаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N014935/01
от 27.10.11
Цефактив
Порошок для приготовления раствора для в/в и в/м введения 0.25 г: фл. 1, 5 или 10 шт. в компл. с растворителем
рег. №: ЛП-004873
от 30.05.18
Цефактив
Порошок для приготовления раствора для в/в и в/м введения 0.5 г: фл. 1, 5 или 10 шт. в компл. с растворителем
рег. №: ЛП-004873
от 30.05.18
Цефактив
Порошок для приготовления раствора для в/в и в/м введения 1 г: фл. 1, 5 или 10 шт. в компл. с растворителем
рег. №: ЛП-004873
от 30.05.18
Цефалексин
Капс. 250 мг: 10, 20 или 30 шт.
рег. №: ЛС-002617
от 30.12.11
Цефалексин
Капс. 250 мг: 30 или 1500 шт.
рег. №: ЛС-000864
от 27.07.10
Цефалексин
Гранулы д/пригот. сусп. д/приема внутрь 250 мг/5 мл: фл. 100 мл
рег. №: П N011645/02
от 02.09.11
Капс. 250 мг: 16 шт.
рег. №: П N011645/01
от 20.04.11
Капс. 500 мг: 16 шт.
рег. №: П N011645/01
от 20.04.11
Цефалексин
Таб., покр. оболочкой, 250 мг: 10 или 20 шт.
рег. №: Р N003669/01
от 31.08.09
Цефалотин Дж
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 шт.
рег. №: ЛП-005694
от 06.08.19
Цефалотин Дж
Порошок д/пригот. р-ра д/в/в и в/м введения: 1 г фл. 1 шт.
рег. №: ЛП-005694
от 06.08.19
Цефалотин Дж
Порошок д/пригот. р-ра д/в/в и в/м введения: 2 г фл. 1 шт.
рег. №: ЛП-005694
от 06.08.19
Цефамабол®
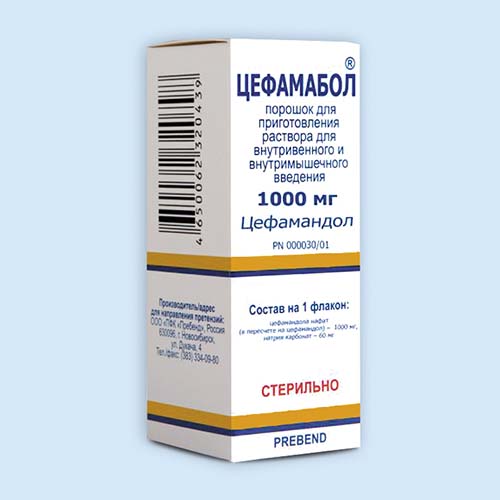
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000030/01
от 04.08.06
Порошок д/пригот. р-ра д/в/в и в/м введения 1000 мг: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000030/01
от 18.05.12
Дата перерегистрации: 07.02.18
Цефанорм
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5 или 10 шт.
рег. №: ЛСР-007627/09
от 29.09.09
Цефанорм
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5 или 10 шт.
рег. №: ЛСР-007627/09
от 29.09.09
Цефантрал
Порошок д/пригот. р-ра д/инъекц. 1 г: фл. 1 шт.
рег. №: П N014934/01
от 17.10.07
Цефантрал
Порошок д/пригот. р-ра д/инъекц. 250 мг: фл. 1 шт.
рег. №: П N014934/01
от 17.10.07
Цефантрал
Порошок д/пригот. р-ра д/инъекц. 500 мг: фл. 1 шт.
рег. №: П N014934/01
от 17.10.07
Цефатрин
Порошок д/пригот. р-ра д/инъекц. 1 г: фл. 1 шт.
рег. №: П N015109/01
от 01.09.08
Цефатрин
Порошок д/пригот. р-ра д/инъекц. 250 мг: фл. 1 шт.
рег. №: П N015109/01
от 01.09.08
Цефатрин
Порошок д/пригот. р-ра д/инъекц. 500 мг: фл. 1 шт.
рег. №: П N015109/01
от 01.09.08
Цефбактам®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл. 1 шт.
рег. №: ЛП-001495
от 10.02.12
Дата перерегистрации: 22.02.17
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг+250 мг: фл. 1 шт.
рег. №: ЛП-001495
от 10.02.12
Дата перерегистрации: 22.02.17
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг+500 мг: фл. 1 шт.
рег. №: ЛП-001495
от 10.02.12
Дата перерегистрации: 22.02.17
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: 1 шт.
рег. №: ЛП-008243
от 10.06.22
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: 1 шт.
рег. №: ЛП-008243
от 10.06.22
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: 1 шт.
рег. №: ЛП-008243
от 10.06.22
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: 1, 5 или 10 шт.
рег. №: ЛП-005926
от 20.11.19
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: 1, 5 или 10 шт.
рег. №: ЛП-005926
от 20.11.19
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: 1, 5 или 10 шт.
рег. №: ЛП-005926
от 20.11.19
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 шт.
рег. №: ЛСР-010038/09
от 23.04.13
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 10 шт.
рег. №: ЛП-004131
от 08.02.17
Дата перерегистрации: 26.03.18
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 50 шт.
рег. №: ЛП-001406
от 30.12.11
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-004483/07
от 06.12.07
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-010038/09
от 23.04.13
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-004400/10
от 18.05.10
Цефепим

Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 50 шт.
рег. №: ЛСР-005610/09
от 13.07.09
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 14, 24 или 50 шт.
рег. №: ЛС-002441
от 29.12.11
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5 или 30 шт.
рег. №: ЛСР-010516/09
от 24.12.09
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 шт.
рег. №: ЛСР-010038/09
от 09.12.09
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1, 10 или 50 шт.
рег. №: ЛП-004582
от 12.12.17
Цефепим
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 10, 14, 24 или 50 шт.
рег. №: ЛС-002441
от 29.12.11
Цефепим

Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1,10 или 50 шт.
рег. №: ЛСР-005610/09
от 13.07.09
Цефепим-Виал
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-006747/08
от 18.08.08
Цефепим-Виал
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 600 или 1000 шт. (упаковано Озон ООО)
рег. №: ЛСР-006747/08
от 18.08.08
Упаковано:
ОЗОН
(Россия)
Цефепим-Джодас
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10, 20, 35, 48, 50 или 100 шт.
рег. №: ЛС-002554
от 22.12.11
Цефзид
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N014541/01
от 11.01.09
Цефзоксим Дж
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл.
рег. №: ЛСР-006699/10
от 15.06.10
Цефиксим
Капс. 400 мг: 6, 10, 12 или 20 шт.
рег. №: ЛП-006958
от 19.04.21
Цефиксим Экспресс
Таб. диспергируемые 400 мг: 7 или 21 шт.
рег. №: ЛП-005838
от 02.10.19
Цефинвик
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1, 5 или 10 шт.
рег. №: ЛС-000253
от 12.01.10
Дата перерегистрации: 30.07.21
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5 или 10 шт.
рег. №: ЛС-000253
от 12.01.10
Дата перерегистрации: 30.07.21
Цефинвик
Порошок д/пригот.р-ра д/в/в введения 2 г: фл. 1 или 10 шт., фл. 1 или 5 шт. в компл. с растворителем
рег. №: ЛП-002920
от 20.03.15
Дата перерегистрации: 06.04.22
Цефограм
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 50 шт.
рег. №: П N014422/01
от 18.11.08
Цефограм
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 или 50 шт.
рег. №: П N014422/01
от 18.11.08
Цефограм
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 или 50 шт.
рег. №: П N014422/01
от 18.11.08
Цефокситин
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл.
рег. №: ЛП-005082
от 27.09.18
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл.
рег. №: ЛП-005082
от 27.09.18
Цефомакс
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 шт.
рег. №: ЛП-000961
от 18.10.11
Цефомакс
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛП-000961
от 18.10.11
Цефомакс
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 шт.
рег. №: ЛП-000961
от 18.10.11
Цефоперабол®

Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000581/01
от 28.03.12
Дата перерегистрации: 12.02.18
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000581/01
от 28.03.12
Дата перерегистрации: 12.02.18
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 или 5 шт. в комп. с растворителем или без него
рег. №: Р N000581/01
от 28.03.12
Дата перерегистрации: 12.02.18
Цефоперазон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 50 шт.
рег. №: ЛП-001608
от 23.03.12
Цефоперазон
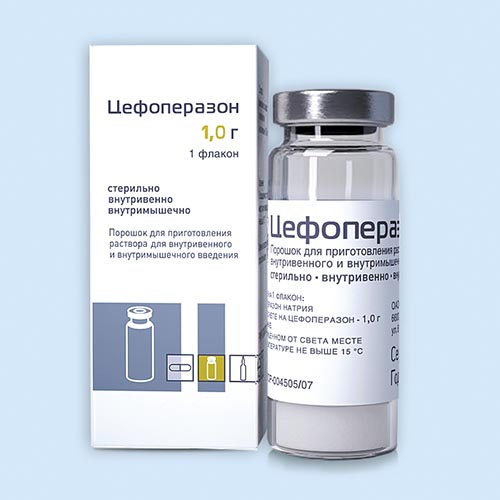
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 50 шт.
рег. №: ЛСР-004505/07
от 06.12.07
Цефоперазон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10, 25 или 50 шт.
рег. №: ЛС-002116
от 18.10.11
Цефоперазон
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1, 10, 25 или 50 шт.
рег. №: ЛС-002116
от 18.10.11
Цефоперазон
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: ЛСР-004505/07
от 06.12.07
Цефоперазон
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 10, 25 или 50 шт.
рег. №: ЛС-002116
от 18.10.11
Цефоперазон и Сульбактам
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл.
рег. №: ЛП-005292
от 14.01.19
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г+1.5 г: фл.
рег. №: ЛП-005292
от 14.01.19
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г+2 г: фл.
рег. №: ЛП-005292
от 14.01.19
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг+250 мг: фл.
рег. №: ЛП-005292
от 14.01.19
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг+500 мг: фл.
рег. №: ЛП-005292
от 14.01.19
Цефоперазон и Сульбактам Джодас
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г+1.5 г: фл.
рег. №: ЛП-006466
от 16.09.20
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г+2 г: фл.
рег. №: ЛП-006466
от 16.09.20
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг+250 мг: фл.
рег. №: ЛП-006466
от 16.09.20
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг+500 мг: фл.
рег. №: ЛП-006466
от 16.09.20
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг+750 мг: фл.
рег. №: ЛП-006466
от 16.09.20
Цефоперазон и Сульбактам джодас
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 1 г+1 г: фл. 1 шт.
рег. №: ЛСР-000391/09
от 26.01.09
Цефоперазон и Сульбактам спенсер
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 1 г+1 г: фл. 1 шт.
рег. №: ЛСР-001341/07
от 29.06.07
Цефоперазон-Аджио
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-004328/10
от 17.05.10
Цефоперазон-АКОС
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 или 10 шт.
рег. №: ЛС-001874
от 30.08.11
Дата перерегистрации: 12.01.21
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 10 шт.
рег. №: ЛС-001874
от 30.08.11
Дата перерегистрации: 12.01.21
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 или 10 шт.
рег. №: ЛС-001874
от 30.08.11
Дата перерегистрации: 12.01.21
Цефоперазон-Виал
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-002589/09
от 02.04.09
Цефоперазон+Сульбактам
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл. 1 шт.
рег. №: ЛП-005095
от 09.10.18
Цефоперазон+Сульбактам
Порошок д/пригот. р-ра д/в/в и в/м введения 1000 мг+1000 мг: фл. 1, 5 или 10 шт. в компл. с растворителем или без него.
рег. №: ЛП-005771
от 04.09.19
Цефоперазон+Сульбактам
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг+250 мг: фл. 1 или 10 шт.
рег. №: ЛП-007626
от 23.11.21
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг+500 мг: фл. 1 или 10 шт.
рег. №: ЛП-007626
от 23.11.21
Порошок д/пригот. р-ра д/в/в и в/м введения 1000 мг+1000 мг: фл. 1 или 10 шт.
рег. №: ЛП-007626
от 23.11.21
Цефоперазон+Сульбактам
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг+250 мг: фл. 1, 5 или 10 шт. в компл. с растворителем или без него.
рег. №: ЛП-005771
от 04.09.19
Цефоперазон+Сульбактам
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг+250 мг: фл. 1, 5 или 10 шт. в компл. с растворителем или без него.
рег. №: ЛП-008137
от 06.05.22
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг+500 мг: фл. 1, 5 или 10 шт. в компл. с растворителем или без него.
рег. №: ЛП-008137
от 06.05.22
Порошок д/пригот. р-ра д/в/в и в/м введения 1000 мг+1000 мг: фл. 1, 5 или 10 шт. в компл. с растворителем или без него.
рег. №: ЛП-008137
от 06.05.22
Порошок д/пригот. р-ра д/в/в и в/м введения 1500 мг+1500 мг: фл. 1, 5 или 10 шт. в компл. с растворителем или без него.
рег. №: ЛП-008137
от 06.05.22
Порошок д/пригот. р-ра д/в/в и в/м введения 2000 мг+2000 мг: фл. 1, 5 или 10 шт. в компл. с растворителем или без него.
рег. №: ЛП-008137
от 06.05.22
Цефоперазон+Сульбактам

Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг+500 мг: фл. 1, 5 или 10 шт. в компл. с растворителем или без него.
рег. №: ЛП-005771
от 04.09.19
Цефоперазон+Сульбактам
Порошок д/пригот.р-ра д/в/в и в/м введения 1 г+1 г
рег. №: ЛП-008363
от 18.07.22
Цефоперазон+Сульбактам-ДЖИЭФСИ®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл. 1 шт.
рег. №: ЛП-008119
от 04.05.22
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г+1.5 г: фл. 1 шт.
рег. №: ЛП-008119
от 04.05.22
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г+2 г: фл. 1 шт.
рег. №: ЛП-008119
от 04.05.22
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг+250 мг: фл. 1 шт.
рег. №: ЛП-008119
от 04.05.22
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг+500 мг: фл. 1 шт.
рег. №: ЛП-008119
от 04.05.22
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг+750 мг: фл. 1 шт.
рег. №: ЛП-008119
от 04.05.22
Цефосульбакт
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г + 0.5 г: фл. 1, 5, 10, 15, 25, 50 или 100 шт.
рег. №: ЛП-006372
от 27.07.20
Цефотаксим
Порошок д/пригот. инъекц. р-ра 1 г: фл. 1 шт.
рег. №: П N012538/01
от 19.02.10
Цефотаксим
Порошок д/пригот. инъекц. р-ра 250 мг: фл. 1 шт.
рег. №: П N012538/01
от 19.02.10
Цефотаксим
Порошок д/пригот. инъекц. р-ра 500 мг: фл. 1 шт.
рег. №: П N012538/01
от 19.02.10
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 или 10 шт.
рег. №: ЛП-(000988)-(РГ-RU )
от 06.07.22
Предыдущий рег. №: Р N002102/02
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 10 шт.
рег. №: ЛП-(000988)-(РГ-RU )
от 06.07.22
Предыдущий рег. №: Р N002102/02
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 или 10 шт.
рег. №: ЛП-(000988)-(РГ-RU )
от 06.07.22
Предыдущий рег. №: Р N002102/02
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 40 шт.
рег. №: ЛСР-006468/09
от 13.08.09
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 50 шт.
рег. №: ЛС-001225
от 30.01.12
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N011901/01
от 09.07.07
Дата перерегистрации: 05.11.14
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛП-000261
от 16.02.11
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-000004
от 02.03.07
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 270 шт.
рег. №: ЛП-001790
от 06.08.12
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 50 шт. в комплекте с растворителем или без
рег. №: Р N002159/01
от 21.02.13
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5 или 50 шт.
рег. №: П N012823/01
от 07.08.08
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10 или 50 шт.
рег. №: ЛС-002118
от 27.12.11
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10, 25 или 50 шт. в компл. с растворителем
рег. №: ЛС-002117
от 06.12.11
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 10 или 50 шт.
рег. №: ЛСР-001973/07
от 07.08.07
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 5 или 30 шт.
рег. №: ЛСР-008487/08
от 24.10.08
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 5 шт. в компл. с растворителем
рег. №: ЛС-002118
от 27.12.11
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 или 40 шт.
рег. №: ЛСР-006468/09
от 13.08.09
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 10 или 270 шт.
рег. №: ЛП-001790
от 06.08.12
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 10 или 50 шт. в комплекте с растворителем или без
рег. №: Р N002159/01
от 21.02.13
Цефотаксим
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5, 10, 25 или 50 шт. в компл. с растворителем
рег. №: ЛС-002117
от 06.12.11
Цефотаксим
Порошок д/пригот. р-ра д/в/м введения 1 г: фл. 1, 10 или 50 шт.
рег. №: Р N002159/02
от 15.06.09
Цефотаксим
Порошок д/пригот. р-ра д/в/м введения 500 мг: фл. 1 шт.
рег. №: Р N002159/02
от 15.06.09
Цефотаксим
Порошок д/пригот. р-ра д/инъекц. 1 г: фл. 1 шт.
рег. №: П N015272/01
от 15.12.08
Порошок д/пригот. р-ра д/инъекц. 500 мг: фл. 1 шт.
рег. №: П N015272/01
от 15.12.08
Цефотаксим
Лиофилизат д/пригот. р-ра д/инфузий 1 г
рег. №: ЛП-008081
от 22.04.22
Порошок д/пригот.р-ра д/в/в и в/м введения 0.5 г
рег. №: ЛП-008081
от 22.04.22
Цефотаксим ДС
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-005800/08
от 22.07.08
Цефотаксим Эльфа
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-000048
от 26.04.07
Цефотаксим-Виал
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-000024
от 07.11.07
Цефотаксим-Виал
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт. (упаковано Озон ООО)
рег. №: ЛСР-000024
от 07.11.07
Упаковано:
ОЗОН
(Россия)
Цефотаксим-ЛЕКСВМ
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1, 10 или 50 шт.
рег. №: ЛП-001545
от 28.02.12
Цефотаксим-ЛЕКСВМ
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 50 шт.
рег. №: ЛП-001545
от 28.02.12
Цефотаксим+Сульбактам
Порошок д/пригот.р-ра д/в/в и в/м введения 1000 мг+500 мг
рег. №: ЛП-(000909)-(РГ-RU )
от 20.06.22
Цефпар
Порошок д/пригот. р-ра д/в/м и в/в введения 1 г: фл. 1 или 50 шт.
рег. №: ЛСР-004597/09
от 09.06.09
Порошок д/пригот. р-ра д/в/м и в/в введения 2 г: фл. 1 или 50 шт.
рег. №: ЛСР-004597/09
от 09.06.09
Порошок д/пригот. р-ра д/в/м и в/в введения 500 мг: фл. 1 или 50 шт.
рег. №: ЛСР-004597/09
от 09.06.09
Цефпар СВ
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г+1 г: фл. 1 шт.
рег. №: ЛСР-003639/10
от 30.04.10
Порошок д/пригот. р-ра д/в/в и в/м инъекц. 500 мг+500 мг: фл. 1 или 50 шт.
рег. №: ЛСР-003639/10
от 30.04.10
Цефроксим Дж
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г: фл. 1, 10, 48 или 100 шт.
рег. №: ЛСР-007152/10
от 26.07.10
Цефроксим Дж
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1, 10, 48 или 100 шт.
рег. №: ЛСР-007152/10
от 26.07.10
Цефтазидим
Порошок д/пригот. инъекц. р-ра 1 г: фл. 1 шт.
рег. №: П N012009/01
от 19.02.10
Порошок д/пригот. инъекц. р-ра 2 г: фл. 1 шт.
рег. №: П N012009/01
от 19.02.10
Порошок д/пригот. инъекц. р-ра 250 мг: фл. 1 шт.
рег. №: П N012009/01
от 19.02.10
Порошок д/пригот. инъекц. р-ра 500 мг: фл. 1 шт.
рег. №: П N012009/01
от 19.02.10
Цефтазидим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 25 шт.
рег. №: ЛП-003350
от 03.12.15
Цефтазидим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-000005
от 02.03.07
Цефтазидим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N014387/01
от 17.03.09
Цефтазидим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 50 шт.
рег. №: ЛСР-003633/10
от 30.04.10
Цефтазидим
Порошок д/пригот. р-ра д/в/в и в/м введения 1000 мг: фл. 1 шт.
рег. №: ЛП-001425
от 12.01.12
Цефтазидим
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 шт.
рег. №: ЛСР-000005
от 02.03.07
Цефтазидим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-000005
от 02.03.07
Дата перерегистрации: 14.06.18
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 шт.
рег. №: ЛСР-000005
от 02.03.07
Дата перерегистрации: 14.06.18
Цефтазидим
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: П N014387/01
от 17.03.09
Цефтазидим-АКОС
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 или 10 шт. в компл. с растворителем или без него
рег. №: ЛП-(000560)-(РГ-RU )
от 09.02.22
Предыдущий рег. №: Р N002274/01
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 10 шт. в компл. с растворителем или без него
рег. №: ЛП-(000560)-(РГ-RU )
от 09.02.22
Предыдущий рег. №: Р N002274/01
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1 или 10 шт. в компл. с растворителем или без него
рег. №: ЛП-(000560)-(РГ-RU )
от 09.02.22
Предыдущий рег. №: Р N002274/01
Цефтазидим-Виал
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 10 шт.
рег. №: ЛП-002753
от 11.12.14
Цефтазидим-Джодас
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10, 20, 25, 48, 50 или 100 шт.
рег. №: ЛС-002537
от 22.12.11
Цефтидин
Порошок д/пригот. р-ра д/в/м и в/в введения 1 г: фл. 1, 1000 или 2000 шт.
рег. №: П N012310/01
от 24.03.10
Цефтриабол®
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N001156/01
от 22.04.08
Дата перерегистрации: 15.01.18
Порошок д/пригот. р-ра д/инф. 2 г: фл. 1 шт.
рег. №: ЛСР-008018/10
от 11.08.10
Дата перерегистрации: 09.10.18
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 или 10 шт.
рег. №: ЛП-004146
от 14.02.17
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: фл. 1 или 25 шт.
рег. №: ЛП-002002
от 18.02.13
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 мг: фл. 1 шт.
рег. №: ЛП-000937
от 18.10.11
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 10 шт.
рег. №: ЛП-004146
от 14.02.17
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 25 шт.
рег. №: ЛП-002002
от 18.02.13
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 50 шт.
рег. №: П N012822/01
от 23.06.08
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛС-001871
от 26.09.11
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛС-001871
от 26.09.11
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛП-000937
от 18.10.11
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N013445/01
от 31.07.08
Дата перерегистрации: 31.05.17
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-003634/10
от 30.04.10
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N015852/01
от 18.11.09
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-005252/08
от 04.07.08
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛП-000538
от 12.05.11
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-000006
от 02.03.07
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-002294
от 17.08.07
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт. в компл. с растворителем
рег. №: Р N001456/01
от 23.07.08
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 50 шт.
рег. №: Р N000846/02
от 12.10.11
Дата перерегистрации: 21.06.18
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10, 25 или 50 шт.
рег. №: ЛС-002533
от 09.08.11
Цефтриаксон

Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10 или 50 шт.
рег. №: Р N001456/01
от 23.07.08
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 10 или 50 шт., фл. 1 шт. в компл. с растворителем
рег. №: Р N000750/01
от 26.10.07
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 5, 30 или 50 шт.
рег. №: ЛС-000140
от 23.12.09
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: фл. 1, 5, 10 или 50 шт., фл. 1 шт. в компл. с растворителем
рег. №: Р N000750/01
от 27.10.07
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт.
рег. №: ЛСР-003634/10
от 30.04.10
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт.
рег. №: П N015852/01
от 18.11.09
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1, 5, или 10 шт., в компл. с растворителем или без него
рег. №: ЛП-007499
от 15.10.21
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5, или 10 шт., в компл. с растворителем или без него
рег. №: ЛП-007499
от 15.10.21
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: ЛСР-005252/08
от 04.07.08
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 шт.
рег. №: ЛСР-002294
от 17.08.07
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 10, 25 или 50 шт.
рег. №: ЛС-002533
от 09.08.11
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5, 10 или 50 шт., фл. 1 шт. в компл. с растворителем
рег. №: Р N000750/01
от 26.10.07
Цефтриаксон
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 5, 30 или 50 шт.
рег. №: ЛС-000140
от 23.12.09
Цефтриаксон
Порошок д/пригот. р-ра д/инф. 2 г: фл. 1 шт.
рег. №: ЛП-005010
от 28.08.18
Цефтриаксон

Порошок д/пригот. р-ра д/инфузий 2 г: фл. 1 или 10 шт.
рег. №: ЛП-002661
от 16.10.14
Цефтриаксон Дансон
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 или 10 шт.
рег. №: ЛСР-008335/10
от 18.08.10
Дата перерегистрации: 15.09.21
Цефтриаксон ДС
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-004519/08
от 10.06.08
Дата перерегистрации: 08.04.20
Цефтриаксон Каби
Порошок д/пригот. р-ра д/в/в и в/м введения 1000 мг: фл. 1 или 10 шт.
рег. №: ЛП-000047
от 22.11.10
Дата перерегистрации: 26.02.16
Цефтриаксон Протекх
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: П N014003/01
от 19.09.08
Цефтриаксон Эльфа
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛС-002191
от 12.03.12
Цефтриаксон-Акос
Порошок для приготовления раствора для внутривенного и внутримышечного введения 0.5 г
рег. №: ЛП-(001419)-(РГ-RU )
от 15.11.22
Порошок для приготовления раствора для внутривенного и внутримышечного введения 1 г
рег. №: ЛП-(001419)-(РГ-RU )
от 15.11.22
Порошок для приготовления раствора для внутривенного и внутримышечного введения 2 г
рег. №: ЛП-(001419)-(РГ-RU )
от 15.11.22
Цефтриаксон-Виал
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт.
рег. №: ЛСР-000023
от 06.11.07
Цефтриаксон-Виал
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 шт. (упаковано Озон ООО)
рег. №: ЛСР-000023
от 06.11.07
Цефтриаксон-Джодас
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10, 20, 25, 48, 50 или 100 шт.
рег. №: ЛС-002538
от 25.12.11
Цефтриаксон-КМП
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1, 10 или 40 шт.
рег. №: П N012643/01
от 15.02.08
Цефтриаксон-КМП
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1, 10 или 40 шт.
рег. №: П N012643/01
от 15.02.08
Цефтриаксон-ЛЕКСВМ
Порошок д/пригот. р-ра д/в/в и в/м введен. 0.5 г: фл. 1, 10 или 50 шт.
рег. №: ЛП-001551
от 01.03.12
Цефтриаксон-ЛЕКСВМ
Порошок д/пригот. р-ра д/в/в и в/м введен. 1 г: фл. 1, 10 или 50 шт.
рег. №: ЛП-001551
от 01.03.12
Цефтриаксон-ЛЕКСВМ
Порошок д/пригот. р-ра д/в/в и в/м введен. 1 г: фл. 1, 10 или 50 шт.
рег. №: ЛП-001551
от 01.03.12
Цефтриаксон+Сульбактам
Порошок д/пригот. р-ра д/в/в и в/м введения1000 мг+500 мг: фл.
рег. №: ЛП-007926
от 02.03.22
Цефтриаксон+Сульбактам
Порошок для приготовления раствора для внутривенного и внутримышечного введения 1 г+0.5 г
рег. №: ЛП-008564
от 16.09.22
Цефурабол®
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000129/01
от 01.02.12
Дата перерегистрации: 12.02.18
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1 или 5 шт. в компл. с растворителем или без него
рег. №: Р N000129/01
от 01.02.12
Дата перерегистрации: 12.02.18
Цефурозин®
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1 шт.
рег. №: П N014926/01
от 27.01.09
Цефуроксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г: фл. 1 шт.
рег. №: ЛСР-000003
от 02.03.07
Дата перерегистрации: 14.06.18
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1 шт.
рег. №: ЛСР-000003
от 02.03.07
Дата перерегистрации: 14.06.18
Цефуроксим
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г: фл. 1, 10, 14, 25 или 50 шт.
рег. №: ЛСР-009307/08
от 24.11.08
Цефуроксим
Порошок д/пригот. р-ра д/в/в и в/м введения 250 мг: фл. 1 шт.
рег. №: ЛП-007389
от 13.09.21
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1 шт.
рег. №: ЛП-007389
от 13.09.21
Порошок д/пригот. р-ра д/в/в и в/м введения 1500 мг: фл. 1 шт.
рег. №: ЛП-007389
от 13.09.21
Цефуроксим
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1 или 50 шт.
рег. №: ЛСР-000002/10
от 11.01.10
Цефуроксим
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1, 10, 14, 25 или 50 шт.
рег. №: ЛСР-009307/08
от 24.11.08
Цефуроксим Каби
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1 или 10 шт.
рег. №: ЛП-000038
от 15.11.10
Дата перерегистрации: 18.02.16
Цефуротек
Таб., покр. пленочной оболочкой, 250 мг: 7, 14 или 21 шт.
рег. №: ЛП-000768
от 29.09.11
Цефуротек
Таб., покр. пленочной оболочкой, 500 мг: 7, 14 или 21 шт.
рег. №: ЛП-000768
от 29.09.11
Цефурус®
Порошок д/пригот. р-ра д/в/в и в/м введения 1.5 г: фл. 1 или 50 шт.
рег. №: ЛС-001160
от 30.06.11
Порошок д/пригот. р-ра д/в/в и в/м введения 750 мг: фл. 1 или 50 шт.
рег. №: ЛС-001160
от 30.06.11
Эфипим
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: фл. 1 и 50 шт.
рег. №: ЛСР-002814/09
от 08.04.09
Эфипим
Порошок д/пригот. р-ра д/в/в и в/м введения 500 мг: фл. 1 и 50 шт.
рег. №: ЛСР-008605/09
от 28.10.09
Эртапенем Дж — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005483
Торговое наименование:
ЭРТАПЕНЕМ Дж
Международное непатентованное или группировочное наименование:
Эртапенем.
Лекарственная форма:
лиофилизат для приготовления раствора для внутривенного и внутримышечного введения
Состав:
Каждый флакон содержит:
Действующее вещество: эртапенем натрия 1046,0 мг (в пересчете на эртапенем 1000 мг);
Вспомогательные вещества: натрия гидрокарбонат 203,00 мг, натрия гидроксид q.s. до pH 6,5-8,5.
Описание:
белый или желтовато-белый лиофилизированный порошок или пористая масса.
Восстановленный раствор должен быть прозрачным, бесцветным или светло-желтым.
Фармакотерапевтическая группа:
антибиотик-карбапенем.
Код ATX:
J01DH03.
Фармакологическое действие
Фармакодинамика/ Микробиология
Эртапенем – 1-β метилкарбапенем, бета-лактамный антибиотик длительного действия для парентерального введения, обладающий активностью в отношении широкого спектра грамположительных и грамотрицательных аэробных и анаэробных бактерий.
Бактерицидная активность эртапенема обусловлена ингибированием синтеза клеточной стенки и опосредована его связыванием с пенициллин-связывающими белками (ПСБ). У Escherichia coli он проявляет сильное сродство к ПСБ la, lb, 2, 3, 4 и 5, причем предпочтительно – к ПСБ 2 и 3. Эртапенем обладает значительной устойчивостью к гидролизу бета-лактамазами большинства классов, включая пенициллиназы, цефалоспориназы и бета-лактамазы расширенного спектра, но не металло-бета-лактамазы. Эртапенем эффективен против большинства штаммов следующих микроорганизмов in vitro и вызываемых ими инфекций в клинических ситуациях (см. раздел «Показания к применению»):
Аэробные и факультативные анаэробные грамположительные микроорганизмы:
Staphylococcus aureus (включая штаммы, продуцирующие пенициллиназу, метициллин-резистентные стафилококки устойчивые к эртапенему)
Streptococcus agalactiae
Streptococcus pneumoniae
Streptococcus pyogenes
К эртапенему устойчивы многие штаммы Enterococcus faecalis и большинство штаммов Enterococcus faecium.
Аэробные и факультативные анаэробные грамотрицательные микроорганизмы:
Escherichia coli
Haemophilus influenzae (включая штаммы, продуцирующие бета-лактамазу)
Klebsiella pneumoniae
Moraxella catarrhalis
Proteus mirabilis
Анаэробные микроорганизмы:
Bacteroides fragilis и другие виды группы В. fragilis
Микроорганизмы рода Clostridium (кроме С. difficile)
Микроорганизмы рода Eubacterium
Микроорганизмы рода Peptostreptococcus
Porphyromonas asaccharolytica
Микроорганизмы рода Prevotella
Нижеприведенные данные о величинах минимальных подавляющих концентраций (МПК) получены в исследованиях in vitro, однако их клиническая значимость неизвестна.
Эртапенем при МПК ≤1мкг/мл активен против большинства (≥90%) штаммов микроорганизмов рода Streptococcus, включая Streptococcus pneumoniae; при концентрации ≤0,5 мкг/мл – против большинства (≥90%) штаммов микроорганизмов рода Haemophilus; при концентрации ≤2 мкг/мл – против большинства (≥90%) штаммов других аэробных и факультативных анаэробных микроорганизмов; при концентрации ≤4 мкг/мл – против большинства (≥90%) штаммов анаэробных микроорганизмов из приведенного ниже списка. Однако безопасность и эффективность эртапенема при лечении инфекций, вызванных данными микроорганизмами, в клинической практике не была подтверждена в качественных и хорошо контролируемых клинических исследованиях.
Аэробные и факультативные анаэробные грамположительные микроорганизмы:
Микроорганизмы рода Staphylococcus, коагулазонегативные, чувствительные к метициллину (метициллин-резистентные стафилококки устойчивы к эртапенему)
Streptococcus pneumoniae, пенициллин-резистентные Streptococci viridans
К эртапенем устойчивы многие штаммы Enterococcus faecalis и большинство штаммов Enterococcus faecium.
Аэробные и факультативные анаэробные грамотрицательные микроорганизмы:
Citrobacter freundii
Enterobacter aerogenes
Enterobacter cloacae
Escherichia coli, продуцирующая бета-лактамазы расширенного спектра действия (ESBLs)
Haemophilus parainfluenzae
Klebsiella oxytoca
Klebsiella pneumoniae, продуцирующие ESBLs
Morganella morganii
Proteus vulgaris
Serratia marcescens
Многие штаммы перечисленных выше микроорганизмов, обладающих мультирезистентностью к другим антибиотикам, например, пенициллинам, цефалоспоринам (в том числе III поколения) и аминогликозидам, чувствительны к эртапенему.
Анаэробные микроорганизмы:
Микроорганизмы рода Fusobacterium
Определяемые значения МПК должны быть интерпретированы в соответствии с критериями, указанными в Таблице 1.
Таблица 1.
| Критерии чувствительности для эртапенема | Метод разведения (МПК в мкг/мл) |
Дискодиффузионный метод (Диаметр зоны в мм) |
||||
| Микроорганизмы | ||||||
| Чувствит. | Умер. | Резист. | Чувствит. | Умер. | Резист. | |
| Аэробы и факультативные анаэробы, кроме Streptococcus spp. и Haemophilus spp. | ≤2 | 4 | ≥8 | ≥19 | 16-18 | ≤15 |
| Streptococcus pneumoniae (только пенициллин-чувствительные, non-meningitis штаммы)b | ≤1c | 2 | ≥4 | – | – | – |
| Streptococcus spp. (только бета-гемолитические)a,d | ≤1c | – | – | – | – | – |
| Haemophilus spp.aUP> | ≤0,5e | – | – | ≥19f | – | – |
| Анаэробы | ≤4g | 8 | ≥16 | – | – | – |
a Отсутствие в настоящее время данных о резистентных штаммах не дает возможности определить любую категорию иначе как «чувствительную». Если по данным исследования МПК штаммы охарактеризованы не как чувствительные, они должны быть отправлены в лабораторию для дальнейшего исследования.
bStreptococcus pneumoniae, чувствительные к пенициллину (диаметр зоны 1 мкг оксациллинового диска ≥20 мм), могут считаться чувствительными к эртапенему. Изоляты с диаметром зоны 1 мкг оксациллинового диска ≤19 мм должны тестироваться на чувствительность к эртапенему методом определения МПК.
c Изоляты Streptococcus pneumoniae, чувствительные к пенициллину (МПК ≤0,06 мкг/мл), и Streptococcus spp. (кроме S. pneumoniae), чувствительные к пенициллину (МПК ≤0,12 мкг/мл), могут считаться чувствительными к эртапенему. Тестирование изолятов с промежуточной чувствительностью к пенициллину или пенициллин-резистентных изолятов на чувствительность к эртапенему не рекомендуется, поскольку надежные критерии интерпретации для эртапенема отсутствуют.
d Бета-гемолитические Streptococcus spp., чувствительные к пенициллину (диаметр зоны 10 ЕД пенициллинового диска ≥24 мм) могут считаться чувствительными к эртапенему. Изоляты с диаметром зоны 10 ЕД пенициллинового диска <24 мм должны тестироваться на чувствительность к эртапенему методом определения МПК. Критерии интерпретации пенициллинового дискодиффузионного метода не применимы для стрептококков группы viridans, которые не следует тестировать в отношении эртапенема.
e Эти стандарты интерпретации применимы к процедуре микродилюции бульона с использованием среды Haemophilus Test Medium (НТМ), инокулированной суспензией чистой колонии с инкубацией на воздухе при температуре 35°С в течение 20-24 часов.
f Эти диаметры зон применимы к тестам с использованием дискодиффузионного метода на НТМ агаре, инокулированном суспензией чистых колоний с инкубацией в 5% С02 при 35° С в течение 16-18 часов.
g Эти стандарты интерпретации применимы только к дилюции агара с использованием агара Brucella с добавлением гемина, витамина К1 и 5% дефибринированной или гемолизированной крови барана, инокулированного суспензией чистой колонии, или 6-24 часовой свежей культуре в обогащенной тиогликолатом среде при инкубации в анаэробном контейнере или камере при 35-37° С в течение 42-48 часов.
Фармакокинетика
Всасывание
Эртапенем, растворенный в 1% растворе лидокаина (без эпинефрина), хорошо абсорбируется после внутримышечного (в/м) введения в рекомендованной дозе 1 г.
Биодоступность составляет приблизительно 92%. После в/м введения 1 г в день максимальная концентрация в плазме (Сmax) достигается приблизительно через 2 часа (Тmax).
Распределение
Эртапенем в значительной степени связывается с белками плазмы крови человека (связь эртапенема с белками уменьшается по мере повышения его концентрации в плазме крови примерно с 95% при концентрации в плазме <100 мкг/мл до 85% при концентрации в плазме крови около 300 мкг/мл).
Средние концентрации (мкг/мл) в плазме крови эртапенема после однократной 30-минутной внутривенной (в/в) инфузии дозы 1 г или 2 г и в/м введения разовой дозы 1 г здоровым добровольцам представлены в Таблице 2.
Таблица 2.
| Концентрация эртапенема в плазме у взрослых после введения разовой дозы | |||||||||
| Доза – Способ введения | Средние концентрации в плазме (мкг/мл) | ||||||||
| 0,5 ч | 1 ч | 2 ч | 4 ч | 6 ч | 8 ч | 12 ч | 18 ч | 24 ч | |
| 1 г – в/в* | 155 | 115 | 83 | 48 | 31 | 20 | 9 | 3 | 1 |
| 1 г – в/м | 33 | 53 | 67 | 57 | 40 | 27 | 13 | 4 | 2 |
| 2 г – в/в* | 283 | 202 | 145 | 86 | 58 | 36 | 16 | 5 | 2 |
| * в/в инфузия проводилась при постоянной скорости в течение 30 минут. |
Площадь под фармакокинетической кривой «концентрация-время» эртапенема в плазме крови (AUC) у взрослых пациентов увеличивается почти прямо пропорционально дозе в диапазоне доз от 0,5 г до 2 г.
Кумуляции эртапенема у взрослых пациентов после многократного в/в введения в диапазоне доз от 0,5 г до 2 г в день или в/м введения по 1 г в день не наблюдается.
Средние концентрации (мкг/мл) в плазме эртапенема у детей представлены в Таблице 3.
Таблица 3.
| Концентрация эртапенема в плазме у детей после внутривенного введения разовой дозы* | ||||||||
| Возраст/доза | Средние концентрации в плазме (мкг/мл) | |||||||
| 0,5 ч | 1 ч | 2 ч | 4 ч | 6 ч | 8 ч | 12 ч | 24 ч | |
| 3-23 месяца (15 мг/кг)** (20 мг/кг)** (40 мг/кг)*** |
103,8 126,8 199,1 |
57,3 87,6 144,1 |
43,6 58,7 95,7 |
23,7 28,4 58,0 |
13,5 – – |
8,2 12,0 20,2 |
2,5 3,4 7,7 |
– 0,4 0,6 |
| 2-12 лет (15 мг/кг)** (20 мг/кг)** (40 мг/кг)*** |
113,2 147,6 241,7 |
63,9 97,6 152,7 |
42,1 63,2 96,3 |
21,9 34,5 55,6 |
12,8 – – |
7,6 12,3 18,8 |
3,0 4,9 7,2 |
– 0,5 0,6 |
| 13-17 лет (20 мг/кг) ** (1 г) (40 мг/кг) *** |
170,4 155,9 255,0 |
98,3 110,9 188,7 |
67,8 74,8 127,9 |
40,4 – 76,2 |
– 24,0 – |
16,0 – 31,0 |
7,0 6,2 15,3 |
1,1 – 2,1 |
| * – в/в инфузия проводилась при постоянной скорости в течение 30 минут. ** – до максимальной дозы 1 г/сутки *** – до максимальной дозы 2 г/сутки |
Объем распределения эртапенема у взрослых пациентов – около 8 литров (0,11 л/кг), у детей в возрасте от 3 месяцев до 13 лет – 0,2 л/кг и около 0,16 л/кг у детей в возрасте 13-17 лет.
Концентрация эртапенема в грудном молоке у пяти кормящих женщин, определяемая ежедневно в случайных временных точках последовательно в течение 5 дней после последнего в/в введения дозы 1 г, составляла в последний день лечения (через 5-14 дней после родов) <0,38 мкг/мл. К 5-му дню после прекращения лечения концентрация эртапенема у 4 женщин была ниже предела обнаружения, а у 1 женщины обнаруживались следовые количества (<0,13 мкг/мл).
Эртапенем не подавляет транспорт дигоксина и винбластина, опосредованный Р-гликопротеином, и сам не является субстратом этого транспорта (см. раздел «Взаимодействие с другими лекарственными средствами»).
Метаболизм
После в/в инфузии 1 г эртапенема с изотопной меткой источником радиоактивности в плазме является в основном (94%) эртапенем. Основной метаболит эртапенема представляет собой производное с незамкнутым кольцом, образующееся при гидролизе бета-лактамного кольца.
Исследования in vitro микросом печени человека показывают, что эртапенем не ингибирует метаболизм, опосредованный шестью основными изоферментами цитохрома Р450 (CYP) – 1А2, 2С9, 2С19, 2D6, 2Е1 и ЗА4 (см. раздел «Взаимодействие с другими лекарственными средствами»).
Выведение
Эртапенем выводится главным образом почками. Среднее время полувыведения в плазме крови у здоровых молодых добровольцев и детей в возрасте 13-17 лет составляет около 4 часов, у детей от 3 месяцев до 13 лет – около 2,5 часов. После в/в введения 1 г эртапенема с изотопной меткой здоровым молодым добровольцам около 80% препарата выводится почками, а 10% – через кишечник. Из 80% эртапенема, определяемого в моче, около 38% выделяется в виде неизмененного препарата, а около 37% – в виде метаболита с незамкнутым β-лактамным кольцом.
У здоровых молодых добровольцев, получивших в/в дозу 1 г, средняя концентрация эртапенема в моче в течение 0-2 часов после введения этой дозы превышает 984 мкг/мл, а в течение 12-24 после введения этой дозы превышает 52 мкг/мл.
Особенности фармакокинетики у отдельных групп пациентов
Пол. Концентрация эртапенема в плазме у мужчин и женщин сопоставима.
Пожилые пациенты. Концентрация эртапенема в плазме после в/в введения дозы 1 г и 2 г у пожилых пациентов (≥65 лет) немного выше (приблизительно на 39% и 22%, соответственно), чем у более молодых (<65 лет). Коррекции дозы для пожилых пациентов не требуется.
Дети. После внутривенного введения препарата в дозе 1 г/сутки концентрация эртапенема в плазме крови у детей 13-17 лет и взрослых пациентов сопоставима.
После назначения препарата в дозе 20 мг/кг (до максимальной дозы 1 г) значения фармакокинетических параметров у пациентов в возрасте 13-17 лет в целом были сравнимы с таковыми у здоровых молодых добровольцев. Трое из шести пациентов 13-17 лет получали дозу менее 1 г. Для оценки фармакокинетических критериев у всех пациентов данной группы полученные показатели были рассчитаны с учетом того, что все пациенты получали дозу препарата 1 г, с допущением линейной зависимости.
Результаты сравнения показывают, что фармакокинетический профиль у пациентов 13-17 лет, получавших эртапенем в дозе 1 г/сутки, был сопоставим с таковым у взрослых пациентов. Соотношения (пациенты 13-17 лет / взрослые пациенты) для значений AUC, концентрации в конце введения инфузии и концентрации в середине интервала дозирования составили 0,99, 1,20 и 0,84, соответственно.
Концентрации в плазме крови в середине интервала дозирования после однократного в/в введения эртапенема в дозе 15 мг/кг у пациентов в возрасте от 3 месяцев до 13 лет сравнимы с данными концентрациями в середине интервала дозирования после в/в введения препарата в дозе 1 г/сутки у взрослых. Клиренс эртапенема из плазмы крови (мл/мин/кг) у пациентов в возрасте от 3 месяцев до 13 лет был приблизительно в 2 раза больше в сравнении с таковым у взрослых пациентов. При введении дозы 15 мг/кг значения AUC у пациентов в возрасте от 3 месяцев до 13 лет были сравнимы с данными значениями у молодых здоровых добровольцев, принимавших эртапенем внутривенно в дозе 1 г.
Пациенты с печеночной недостаточностью. Фармакокинетика эртапенема у пациентов с печеночной недостаточностью не изучалась. В связи с небольшой интенсивностью метаболизма препарата в печени можно ожидать, что нарушение ее функции не должно влиять на фармакокинетику эртапенема. Коррекции режима дозирования у пациентов с печеночной недостаточностью не требуется.
Пациенты с почечной недостаточностью. После однократного в/в введения 1 г эртапенема AUC у пациентов с почечной недостаточностью легкой степени (клиренс креатинина С1cr 60-90 мл/мин/1,73 м²) не отличается от таковой у здоровых добровольцев (в возрасте от 25 до 82 лет).
У пациентов с умеренной почечной недостаточностью (С1cr 31-59 мл/мин/1,73 м²) AUC увеличена приблизительно в 1.5 раза по сравнению со здоровыми добровольцами.
У пациентов с тяжелой почечной недостаточностью (С1cr 5-30 мл/мин/1,73 м²) AUC увеличена приблизительно в 2,6 раза по сравнению со здоровыми добровольцами.
У пациентов с терминальной стадией почечной недостаточности (С1cr <10 мл/мин/1,73 м²) AUC увеличена приблизительно в 2,9 раза по сравнению со здоровыми добровольцами. После однократного в/в введения разовой дозы 1 г эртапенема непосредственно перед сеансом гемодиализа около 30% введенной дозы определяется в диализате.
Данные о применении препарата у детей с почечной недостаточностью отсутствуют.
Пациентам с тяжелой и терминальной почечной недостаточностью рекомендуется проводить коррекцию режима дозирования (см. раздел «Способ применения и дозы»).
Показания к применению
Эртапенем показан для лечения пациентов с тяжелыми и средней тяжести инфекциями, вызванными чувствительными штаммами микроорганизмов, в том числе для стартовой эмпирической антибактериальной терапии до определения бактериальных возбудителей, при нижеперечисленных инфекциях:
- Интраабдоминальные инфекции;
- Инфекции кожи и подкожной клетчатки, включая инфекции нижних конечностей при сахарном диабете («диабетическая» стопа);
- Внебольничная пневмония;
- Инфекции мочевыделительной системы, включая пиелонефрит;
- Острые инфекции органов малого таза, включая послеродовой эндомиометрит, септический аборт и пост-хирургические гинекологические инфекции;
- Бактериальная септицемия.
Противопоказания
- Повышенная чувствительность к эртапенему или другим компонентам препарата, к другим препаратам класса карбапенемов, повышенная чувствительность (например, анафилактические реакции, тяжелые кожные реакции) на любой другой антибиотик бета-лактамной группы (например, пенициллины или цефалоспорины).
- Эртапенем Дж не рекомендован для применения у детей в возрасте младше 3 месяцев в связи с недостаточной изученностью эффективности и безопасности.
При использовании в качестве растворителя лидокаина внутримышечное введение препарата Эртапенем Дж противопоказано пациентам с известной гиперчувствительностью к амидным анестетикам местного действия, пациентам с тяжелой артериальной гипотензией или нарушением внутрисердечной проводимости (см. инструкцию по медицинскому применению лидокаина).
Применение при беременности и в период грудного вскармливания
Достаточного клинического опыта по применению препарата у беременных женщин не имеется. Эртапенем Дж следует применять во время беременности, только если возможная польза для матери оправдывает потенциальный риск для плода.
Эртапенем выделяется с грудным молоком (см. раздел «Фармакокинетика. Распределение»). Ввиду возможного неблагоприятного воздействия препарата на ребенка, в период лактации грудное вскармливание следует прекратить на период применения препарата.
Способ применения и дозы
Обычная суточная доза эртапенема для пациентов в возрасте 13 лет и старше составляет 1 г, кратность введения – 1 раз в сутки. Доза препарата Эртапенем Дж у пациентов в возрасте от 3 месяцев до 13 лет составляет 15 мг/кг 2 раза в сутки (но не более 1 г в сутки). Эртапенем Дж можно вводить путем в/в инфузии или в/м инъекции. При в/в инфузии препарата Эртапенем Дж длительность инфузии должна составлять 30 минут.
В/м введение препарата Эртапенем Дж может использоваться как альтернатива в/в инфузии.
Обычная продолжительность терапии препаратом Эртапенем Дж составляет от 3 до 14 дней в зависимости от вида заболевания и вызвавшего его патогенного микроорганизма (микроорганизмов) (см. раздел «Показания к применению»). При наличии клинических показаний допустим переход на последующую адекватную пероральную антимикробную терапию в случае клинического улучшения.
Пациенты с почечной недостаточностью. Эртапенем Дж может применяться для лечения инфекций у взрослых пациентов с почечной недостаточностью. У пациентов с клиренсом креатинина более 30 мл/мин/1,73 м² коррекции режима дозирования не требуется. Взрослые пациенты с выраженной почечной недостаточностью (клиренс креатинина менее или равен 30 мл/мин/1,73 м²), включая тех, кто находится на гемодиализе, должны получать 500 мг в сутки. Нет данных о применении препарата у детей с почечной недостаточностью.
Пациенты, находящиеся на гемодиализе. Взрослым пациентам, находящимся на гемодиализе и получившим рекомендуемую суточную дозу препарата Эртапенем Дж 500 мг в течении 6 часов перед сеансом гемодиализа, рекомендуется дополнительное введение 150 мг препарата после сеанса гемодиализа. Если препарат Эртапенем Дж вводится за 6 часов или ранее до гемодиализа, введения дополнительной дозы не требуется. В настоящее время нет достаточных данных по рекомендации пациентам, подвергающимся перитонеальному диализу или гемофильтрации. Нет данных о применении препарата у детей, находящихся на гемодиализе.
Если известна концентрация креатинина в сыворотке, то для расчета клиренса креатинина можно применять следующие формулы:
Для пациентов с нарушенной функцией печени коррекции дозы не требуется (см. раздел «Фармакологические свойства. Особенности фармакокинетики у отдельных групп пациентов. Пациенты с печеночной недостаточностью»).
Рекомендуемую дозу препарата Эртапенем Дж можно вводить без учета возраста (13 лет и старше) и пола.
Применение у детей. Применение у детей в возрасте младше 3 месяцев не рекомендуется (в связи с недостаточной изученностью эффективности и безопасности).
Применение у пожилых пациентов. В клинических исследованиях эффективность и безопасность препарата Эртапенем Дж у пожилых пациентов (≥65 лет) были сопоставимы с таковыми у более молодых пациентов (<65 лет).
Инструкции по приготовлению растворов
Пациенты в возрасте 13 лет и старше
Приготовление раствора для внутривенной инфузии
Не смешивать и не вводить вместе с другими лекарственными средствами.
Не использовать растворители, содержащие декстрозу (α-D-глюкозу).
Перед введением препарат Эртапенем Дж необходимо растворить, а затем развести.
- Растворите содержимое флакона, содержащего 1 г препарата Эртапенем Дж путем добавления 10 мл одного из следующих растворителей: вода для инъекций, 0,9% раствор натрия хлорида для инъекций или бактериостатическая вода для инъекций.
- Хорошо встряхните флакон до полного растворения препарата и сразу же добавьте раствор из флакона в подготовленные 50 мл 0,9% раствора натрия хлорида для инфузий.
- Инфузия должна быть выполнена в течение 6 часов после растворения препарата Эртапенем Дж.
Приготовление раствора для внутримышечной инъекции
Перед введением препарат Эртапенем Дж необходимо растворить.
- Растворите содержимое флакона, содержащего 1 г препарата Эртапенем Дж, в 3,2 мл 1% или 2% раствора лидокаина для инъекций (без эпинефрина). Хорошо встряхните флакон для растворения содержимого.
- Сразу же наберите в шприц содержимое флакона и введите его глубоко в/м в крупный мышечный массив (например, в ягодичные мышцы или латеральные мышцы бедра).
- Приготовленный раствор дня в/м введения должен быть использован в течение 1 часа после приготовления.
Примечание: приготовленный раствор для в/м инъекций не должен использоваться для в/в инфузий.
Дети в возрасте от 3 месяцев до 13 лет
Приготовление раствора для в/в инфузии
Не смешивать и не вводить вместе с другими лекарственными средствами.
Не использовать растворители, содержащие декстрозу (α-D-глюкозу).
Перед введением препарат Эртапенем Дж необходимо растворить, а затем развести.
- Растворите содержимое флакона, содержащего 1 г препарата Эртапенем Дж, путем добавления 10 мл одного из следующих растворителей: вода для инъекций, 0,9% раствор натрия хлорида для инъекций или бактериостатическая вода для инъекций.
- Хорошо встряхните флакон до полного растворения препарата и сразу же наберите объем раствора, эквивалентный 15 мг/кг веса (но не более 1 г в сутки) и разбавьте в 0,9% растворе натрия хлорида для инфузий до концентрации 20 мг/мл или менее.
- Инфузия должна быть выполнена в течение 6 часов после растворения препарата Эртапенем Дж.
Приготовление раствора для в/м инъекции
Перед введением препарат Эртапенем Дж необходимо растворить.
- Растворите содержимое флакона, содержащего 1 г препарата Эртапенем Дж, в 3,2 мл 1% или 2% раствора лидокаина для инъекций (без эпинефрина). Хорошо встряхните флакон для растворения содержимого.
- Сразу же отберите объем, эквивалентный 15 мг/кг тела (но не более 1 г в сутки) и введите его глубоко внутримышечно в крупный мышечный массив (например, в ягодичные мышцы или латеральные мышцы бедра).
- Приготовленный раствор для в/м введения должен быть использован в течение 1 часа после приготовления.
Приготовленные растворы:
Раствор для инфузий, приготовленный путем немедленного разведения в 0,9% растворе натрия хлорида для инъекций, можно хранить при комнатной температуре (25°С) и использовать в течение 6-ти часов или хранить в течение 24-х часов в холодильнике (5°С) и использовать в течение 4-х часов после извлечения из холодильника.
Растворы препарата Эртапенем Дж нельзя замораживать.
Раствор для в/м инъекций должен быть использован в течение 1 часа после приготовления.
Примечание: приготовленный раствор для в/м инъекции не должен использоваться для в/в инфузий.
Лекарственные препараты для парентерального введения перед использованием нужно подвергать визуальному осмотру для выявления взвешенных частиц или изменений окраски. Цвет растворов препарата Эртапенем Дж варьируется от бесцветного до бледно-желтого (изменение цвета в этих пределах не влияет на активность препарата).
Побочное действие
Взрослые
Нежелательные явления (возможно, вероятно или определенно связанные с применением препарата) были отмечены примерно у 20% пациентов, принимавших эртапенем. В связи с нежелательными явлениями эртапенем отменяли у 1,3% пациентов.
Наиболее частые нежелательные явления, связанные с применением эртапенема при его парентеральном введении, включали диарею (4,8%), местные постинфузионные венозные осложнения (4,5%) и тошноту (2,8%).
Дети от 3 месяцев до 18 лет
Профиль эффективности и безопасности эртапенема у детей был сопоставим с таковым у взрослых пациентов. Нежелательные явления (возможно, вероятно или определенно связанные с применением препарата) были отмечены примерно у 20,8% пациентов, принимавших эртапенем. В связи с нежелательными явлениями эртапенем отменяли у 0,5% пациентов.
Наиболее частые нежелательные явления, связанные с применением эртапенема при его парентеральном применении, включали диарею (5,2%) и боль в месте введения (6,1%). Нежелательные явления, зарегистрированные в ходе лечения пациентов эртапенемом, классифицированы по частоте (часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1 /10000), частота неизвестна).
Таблица 4.
| Взрослые | Дети | |
| Инфекционные и паразитарные заболевания | Нечасто: кандидоз слизистой оболочки полости рта, кандидоз, грибковая инфекция, псевдомембранозный колит, вагинит Редко: пневмония, дерматомикоз, послеоперационная раневая инфекция, инфекция мочевыделительной системы |
|
| Нарушения со стороны крови и лимфатической системы | Редко: нейтропения, тромбоцитопения | |
| Нарушения со стороны иммунной системы | Редко: аллергия Частота неизвестна: анафилаксия, включая анафилактоидные реакции |
|
| Нарушения со стороны обмена веществ и питания | Нечасто: анорексия Редко: гипогликемия |
|
| Нарушения психики | Нечасто: бессонница, спутанность сознания Редко: ажитация, тревожность, депрессия Частота неизвестна: измененное психическое состояние (включая агрессивность, делирий, дезориентацию, изменение психического статуса) |
Частота неизвестна: измененное психическое состояние (включая агрессивность) |
| Нарушения со стороны нервной системы | Часто: головная боль Нечасто: головокружение, сонливость, извращение вкуса, судорожный припадок Редко: тремор, обморок Частота неизвестна: угнетенность сознания, галлюцинации, дискинезия, миоклония, нарушение походки |
Нечасто: головная боль Частота неизвестна: галлюцинации |
| Нарушения со стороны органа зрения | Редко: нарушения со стороны склер | |
| Нарушения со стороны сердца | Часто: синусовая брадикардия Редко: аритмия, тахикардия |
|
| Нарушения со стороны сосудов | Часто: постинфузионные венозные осложнения: флебит/тромбофлебит Нечасто: снижение артериального давления Редко: кровотечение, увеличение артериального давления |
Нечасто: «прилив крови», увеличение артериального давления |
| Нарушения со стороны дыхательной системы, органов грудной клетки и средостения | Нечасто: диспноэ, неприятные ощущения в гортани Редко: заложенность носа, кашель, носовое кровотечение, хрипы, затрудненное дыхание |
|
| Нарушения со стороны желудочно-кишечного тракта | Часто: диарея, тошнота, рвота Нечасто: запор, отрыжка кислым содержимым, ощущение сухости во рту, диспепсия, боль в животе Редко: дисфагия, недержание кала, тазовый перитонит Частота неизвестна: окрашивание зубов |
Часто: диарея Нечасто: обесцвечивание кала, мелена |
| Нарушения со стороны печени и желчевыводящих путей | Редко: холецистит, желтуха, поражения печени | |
| Нарушения со стороны кожи и подкожных тканей | Часто: сыпь, зуд Нечасто: эритема, крапивница Редко: дерматит, шелушение Частота неизвестна: лекарственная сыпь с эозинофилией и системными симптомами (DRESS-синдром) |
Часто: пеленочный дерматит Нечасто: эритема, сыпь, петехия |
| Нарушения со стороны скелетно-мышечной и соединительной ткани | Редко: мышечный спазм, боль в плече Частота неизвестна: мышечная слабость |
|
| Нарушения со стороны почек и мочевыводящих путей | Редко: почечная недостаточность, острая почечная недостаточность | |
| Беременность, послеродовые и перинатальные состояния | Редко: выкидыш | |
| Нарушения со стороны половых органов и молочной железы | Редко: генитальное кровотечение | |
| Общие расстройства и нарушения в месте введения | Нечасто: экстравазация, слабость/утомляемость, лихорадка, отечность, боль в груди Редко: уплотнение в месте введения, недомогание |
Часто: боль в месте введения Нечасто: жжение в месте введения, зуд в месте введения, эритема в месте введения, ощущение тепла в месте введения |
Лабораторные показатели
Взрослые
Наиболее часто наблюдаемыми отклонениями результатов лабораторных анализов, связанными с эртапенемом, были повышение активности АЛТ (аланинаминотрансферазы) (4,6%), ACT (аспартатаминотрансферазы) (4,6%), щелочной фосфатазы (3,8%) и количества тромбоцитов (3,0%).
Дети
Наиболее часто наблюдаемыми отклонениями результатов лабораторных анализов, связанными с эртапенемом, были уменьшение количества нейтрофилов (3,0%), повышение активности АЛТ (2,9%) и ACT (2,8%).
Таблица 5.
| Взрослые | Дети | |
| Биохимические показатели крови | Часто: повышение активности АЛТ, ACT, щелочной фосфатазы Нечасто: повышение концентрации общего, прямого и непрямого билирубина, креатинина, мочевины и глюкозы Редко: уменьшение концентрации бикарбонатов, креатинина, уменьшение содержания калия, повышение активности лактатдегидрогеназы, увеличение содержания фосфора и калия | Часто: повышение активности АЛТ и ACT |
| Общий анализ крови | Часто: увеличение количества тромбоцитов Нечасто: уменьшение количества лейкоцитов. тромбоцитов, сегментоядерных нейтрофилов, снижение гемоглобина и гематокрита, увеличение количества эозинофилов, частичного тромбопластинового времени и протромбинового времени, увеличение количества сегментоядерных нейтрофилов и лейкоцитов Редко: уменьшение количества лимфоцитов, увеличение количества палочкоядерных нейтрофилов, лимфоцитов, метамиелоцитов, моноцитов, миелоцитов, атипичных лимфоцитов | Часто: уменьшение количества нейтрофилов Нечасто: увеличение количества тромбоцитов, частичного тромбопластинового времени и протромбинового времени, снижение гемоглобина |
| Анализ мочи | Нечасто: увеличение количества бактерий в моче, лейкоцитов в моче, эпителиальных клеток в моче, эритроцитов в моче, микоурия Редко: повышение концентрации уробилиногена | |
| Другое | Нечасто: положительная реакция на токсин Clostridium difficile |
Передозировка
Специфической информации по лечению передозировки эртапенема нет. В клинических исследованиях случайное введение до 3 г эртапенема в сутки взрослым не приводило к клинически значимым нежелательным явлениям. В клинических исследованиях у детей однократное в/в введение дозы от 40 мг/кг до максимальной дозы 2 г не вызывало токсических реакций.
В случае передозировки препарата Эртапенем Дж его следует отменить и проводить общее поддерживающее лечение до выведения лекарства почками.
Эртапенем Дж можно удалить из организма путем гемодиализа. Однако информации о применении гемодиализа для лечения передозировки не имеется.
Взаимодействие с другими лекарственными средствами
При применении эртапенема с пробенецидом пробенецид конкурирует за активную канальцевую секрецию и таким образом ингибирует почечную экскрецию эртапенема.
Это ведет к небольшому, но статистически значимому увеличению периода полувыведения (19%) и выраженности системного действия (25%). Коррекции режима дозирования не требуется. Одновременное применение с пробенецидом в целях увеличения периода полувыведения не рекомендуется.
Исследования in vitro показывают, что эртапенем не ингибирует транспорт дигоксина и винбластина, опосредованный Р-гликопротеином, и что эртапенем не является субстратом для этого транспорта. Исследования in vitro микросом печени человека показывают, что эртапенем не ингибирует метаболизм, опосредованный шестью основными изоферментами цитохрома Р450 (CYP) – 1А2, 2С9, 2С19, 2D6, 2Е1 и ЗА4. Взаимодействие с лекарственными средствами, обусловленное ингибированием Р-гликопротеин-опосредованного выведения препаратов или CYP-опосредованного выведения препаратов, маловероятно.
Специальных клинических исследований по взаимодействию с конкретными лекарственными средствами, кроме пробенецида, не проводилось.
Клинические случаи, описанные в литературе, показывают, что одновременное применение карбапенемов, включая эртапенем, с вальпроевой кислотой или дивальпроатом натрия приводит к снижению концентрации вальпроевой кислоты. В результате этого взаимодействия концентрация вальпроевой кислоты может оказаться ниже терапевтического уровня, что увеличивает риск развития судорожного припадка. Хотя механизм взаимодействия неизвестен, данные in vitro и результаты исследований на животных позволяют предположить, что карбапенемы могут ингибировать гидролиз, в результате которого глюкуронидный метаболит вальпроевой кислоты (VPA-g) превращается обратно в вальпроевую кислоту, что приводит к снижению концентрации вальпроевой кислоты в плазме крови (см. раздел «Особые указания»).
Особые указания
Сообщалось о серьезных и летальных анафилактических реакциях у пациентов, получавших лечение бета-лактамными антибиотиками. Эти реакции более вероятны у лиц с повышенной чувствительностью к различным аллергенам в анамнезе (в частности, у лиц с гиперчувствительностью к пенициллину часто развиваются тяжелые реакции гиперчувствительности при лечении другими бета-лактамами). Перед началом лечения препаратом Эртапенем Дж следует тщательно расспросить пациента о предшествующих реакциях гиперчувствительности на другие аллергены, особенно на пенициллины, цефалоспорины и другие бета-лактамы.
При возникновении аллергической реакции на препарат Эртапенем Дж его следует немедленно отменить. Серьезные анафилактические реакции требуют экстренного лечения.
В ходе лечения пациентов эртапенемом зарегистрированы сообщения о судорогах и других побочных реакциях со стороны центральной нервной системы (см. раздел «Побочное действие»). В ходе клинических исследований у взрослых пациентов, принимавших эртапенем (1 г 1 раз в день), судороги, как связанные, так и не связанные с применением препарата, отмечались у 0,5% пациентов в течение курса терапии плюс 14 дней периода наблюдения. Эти явления наиболее часто отмечались у пожилых пациентов, у пациентов с нарушениями ЦНС (например, с поражениями головного мозга или судорогами в анамнезе) и/или у пациентов с нарушенной функцией почек. Необходимо строго придерживаться рекомендуемого режима дозирования, в особенности у пациентов с известной предрасположенностью к судорожной активности. У пациентов с судорожными расстройствами следует продолжать противосудорожную терапию. При возникновении тремора, миоклонии или судорог пациентов следует направить на неврологическое обследование и оценить необходимость уменьшения дозы препарата Эртапенем Дж или отмены препарата.
Увеличение дозы вальпроевой кислоты или дивальпроата натрия может оказаться недостаточным для преодоления последствий взаимодействия. Одновременное применение эртапенема и вальпроевой кислоты/дивальпроата натрия не рекомендуется. Следует рассмотреть возможность лечения инфекций антибиотиками других групп (не карбапенемов) у пациентов, получающих противосудорожную терапию вальпроевой кислотой или дивальпроатом натрия.
При необходимости применения препарата Эртапенем Дж может потребоваться проведение дополнительной противосудорожной терапии (см. раздел «Взаимодействие с другими лекарственными средствами»).
Длительное применение препарата Эртапенем Дж, как и других антибиотиков, может привести к избыточному росту нечувствительных микроорганизмов. Если во время лечения развилась суперинфекция, нужно принять соответствующие меры.
При применении почти всех антибактериальных препаратов, включая эртапенем, возможно развитие псевдомембранозного колита, который по тяжести может варьировать от легкого до опасного для жизни. Важно рассматривать возможность такого диагноза у пациентов, поступающих с диареей после применения антибактериальных препаратов. Следует рассмотреть возможность прекращения терапии препаратом Эртапенем Дж и назначения специфического лечения колита, вызванного Clostridium difficile. Нельзя применять лекарственные средства, тормозящие перистальтику кишечника.
При в/м введении препарата Эртапенем Дж следует соблюдать осторожность, чтобы избежать его случайного введения в кровеносный сосуд (см. раздел «Способ применения и дозы»).
Растворителем для в/м введения препарата Эртапенем Дж является раствор лидокаина (см. инструкцию по медицинскому применению лидокаина).
Влияние на способность управлять транспортными средствами, механизмами
Не проводилось исследований для оценки влияния на способность управлять транспортными средствами и работать с механизмами, однако некоторые нежелательные реакции, наблюдавшиеся при применении препарата эртапенем, такие как головокружение и сонливость, могут влиять на способность управлять транспортными средствами и работать с механизмами (см раздел «Побочное действие»).
Форма выпуска
Лиофилизат для приготовления раствора для внутривенного и внутримышечного введения 1 г.
Для аптек: по 1.0 г эртапенема во флакон прозрачного стекла первого гидролитического класса (USP тип I) вместимостью 20 мл, укупоренный пробкой из бромбутиловой резины, обкатанной алюминиевым кольцом, возможно наличие пластикового колпачка; по 1 флакону вместе с инструкцией по применению в картонную пачку; по 5 флаконов на пластиковый поддон, по 1 поддону вместе с инструкцией по применению в картонную пачку.
Для стационаров: по 1,0 г эртапенема во флакон прозрачного стекла первого гидролитического класса (USP тип I) вместимостью 20 мл, укупоренный пробкой из бромбутиловой резины, обкатанной алюминиевым кольцом, возможно наличие пластикового колпачка; по 25, 50 и 100 флаконов вместе с соответствующим количеством инструкций по применению в коробку картонную.
Условия хранения
Неоткрытые флаконы (до растворения):
Хранить в защищенном от света месте при температуре не выше 25 °С.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Нельзя использовать препарат по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение:
ООО «Джодас Экспоим»
109651, Россия, г. Москва, ул. Перерва, д. 9, стр. 1
Производитель:
Джодас Экспоим Пвт. Лтд.
Комната №2, 42/3, АБ Роуд, Пигдамбер-453 446 М.П. Индия
Производственная площадка:
Налагарх Бадди Роуд, Бадди, Техсил Налагарх, округ Солан (Химачал-Прадеш), 173205, Индия
Jodas Expoim Pvt. Ltd.
Nalagarh Baddi Road, Baddi, Tehsil Nalagarh, Distt. Solan (H.P.) India, 173205, India
За дополнительной информацией и претензиями обращаться по адресу:
ООО «Джодас Экспоим»
109651, Россия, г. Москва, ул. Перерва, д. 9, стр. 1
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Состав
Каждый флакон содержит действующее вещество эртапенем натрия 1,213 г (эквивалентно 1 г эртапенема в виде свободной кислоты).
Вспомогательные вещества: натрия гидрокарбонат 203 мг, натрия гидроксид до pH 7,5. Содержание натрия составляет приблизительно 137 мг (приблизительно 6 мЭкв).
Форма выпуска
Лиофилизат для приготовления раствора для инъекций, 1 г.
По 1 г действующего вещества во флакон из бесцветного стекла вместимостью 15 мл, укупоренный резиновой пробкой, обжатый алюминиевым колпачком с пластиковой крышечкой. По 1 флакону вместе с инструкцией по применению в картонную пачку.
Фармакологическое действие
Антибактериальное.
Фармакологические свойства
Фармакодинамика
Эртапенем — 1-β-метилкарбапенем, бета-лактамный антибиотик длительного действия для парентерального введения, обладающий активностью в отношении широкого спектра грамположительных и грамотрицательных аэробных и анаэробных бактерий.
Бактерицидная активность эртапенема обусловлена ингибированием синтеза клеточной стенки и опосредована его связыванием с пенициллин-связывающими белками (ПСБ). У Escherichia coli он проявляет сильное сродство к ПСБ 1a, 1b, 2, 3, 4 и 5, причем предпочтительно— к ПСБ 2 и 3. Эртапенем обладает значительной устойчивостью к гидролизу бета-лактамазами большинства классов, включая пенициллиназы, цефалоспориназы и бета-лактамазы расширенного спектра, но не металло-бета-лактамазы. Инванз эффективен против большинства штаммов следующих микроорганизмов in vitro и вызываемых ими инфекций в клинических ситуациях:
Аэробные и факультативные анаэробные грамположительные микроорганизмы:
- Staphylococcus aureus (включая штаммы, продуцирующие пенициллиназу, метициллин-резистентные стафилококки устойчивы к препарату Инванз);
- Streptococcus agalactiae;
- Streptococcus pneumoniae;
- Streptococcus pyogenes.
К препарату Инванз устойчивы многие штаммы Enterococcus faecalis и большинство штаммов Enterococcus faecium.
Аэробные и факультативные анаэробные грамотрицательные микроорганизмы:
- Escherichia coli;
- Haemophilus influenzae (включая штаммы, продуцирующие бета-лактамазу);
- Klebsiella pneumoniae;
- Moraxella catarrhalis;
- Proteus mirabilis.
Анаэробные микроорганизмы:
- Bacteroides fragilis и другие виды группы В. fragilis;
- микроорганизмы рода Clostridium (кроме С. difficile);
- микроорганизмы рода Eubacterium;
- микроорганизмы рода Peptostreptococcus;
- Porphyromonas asaccharolytica;
- микроорганизмы рода Prevotella.
Нижеприведенные данные о величинах минимальных подавляющих концентраций (МПК) получены в исследованиях in vitro, однако их клиническая значимость неизвестна:
- Инванз при МПК ≤1 мкг/мл активен против большинства (≥90%) штаммов микроорганизмов рода Streptococcus, включая Streptococcus pneumoniae;
- при концентрации ≤0,5 мкг/мл — против большинства (≥90%) штаммов микроорганизмов рода Haemophilus;
- при концентрации ≤2 мкг/мл — против большинства (≥90%) штаммов других аэробных и факультативных анаэробных микроорганизмов;
- при концентрации ≤4 мкг/мл — против большинства (≥90%) штаммов анаэробных микроорганизмов из приведенного ниже списка.
Однако безопасность и эффективность препарата Инванз при лечении инфекций, вызванных данными микроорганизмами, в клинической практике не была подтверждена в качественных и хорошо контролируемых клинических исследованиях.
Аэробные и факультативные анаэробные грамположительные микроорганизмы:
- микроорганизмы рода Staphylococcus, коагулазонегативные, чувствительные к метициллину (метициллин-резистентные стафилококки устойчивы к препарату Инванз);
- Streptococcus pneumoniae, пенициллин-резистентные;
- Streptococci viridans.
К препарату Инванз устойчивы многие штаммы Enterococcus faecalis и большинство штаммов Enterococcus faecium.
Аэробные и факультативные анаэробные грамотрицательные микроорганизмы:
- Citrobacter freundii;
- Enterobacter aerogenes;
- Enterobacter cloacae;
- Escherichia coli, продуцирующая бета-лактамазы расширенного спектра действия (ESBLs);
- Haemophilus parainfluenzae;
- Klebsiella oxytoca;
- Klebsiella pneumoniae, продуцирующие ESBLs;
- Morganella morganii;
- Proteus vulgaris;
- Serratia marcescens.
Многие штаммы перечисленных выше микроорганизмов, обладающих мультирезистентностью к другим антибиотикам, например, пенициллинам, цефалоспоринам (в том числе III поколения) и аминогликозидам, чувствительны к препарату Инванз.
Анаэробные микроорганизмы:
- микроорганизмы рода Fusobacterium.
Определяемые значения МПК должны быть интерпретированы в соответствии с критериями, указанными в таблице:
| Критерии чувствительности для эртапенема | ||||||
| Метод разведения (МПК в мкг/мл) | Дискодиффузионный метод (диаметр зоны в мм) | |||||
| Микроорганизмы | Чувствит. | Умер. | Резист. | Чувствит. | Умер. | Резист. |
| Аэробы и факультативные анаэробы, кроме Streptococcus spp. и Haemophilus spp. | ≤2 | 4 | ≥8 | ≥19 | 16-18 | ≤15 |
| Streptococcus pneumoniae (только пенициллин-чувствительные, non-meningitis штаммы)b | ≤1c | 2 | ≥4 | — | — | — |
| Streptococcus spp. (только бета-гемолитические)a,d | ≤1c | — | — | — | — | — |
| Haemophilus spp. a | ≤0,5e | — | — | ≥19f | — | — |
| Анаэробы | ≤4g | 8 | ≥16 | — | — | — |
- a Отсутствие в настоящее время данных о резистентных штаммах не дает возможности определить любую категорию иначе как «чувствительную». Если по данным исследования МПК штаммы охарактеризованы не как чувствительные, они должны быть отправлены в лабораторию для дальнейшего исследования.
- b Streptococcus pneumoniae, чувствительные к пенициллину (диаметр зоны 1 мкг оксациллинового диска ≥20 мм), могут считаться чувствительными к эртапенему. Изоляты с диаметром зоны 1 мкг оксациллинового диска ≤19 мм должны тестироваться на чувствительность к эртапенему методом определения МПК.
- c Изоляты Streptococcus pneumoniae, чувствительные к пенициллину (МПК ≤0,06 мкг/мл), и Streptococcus spp. (кроме S. pneumoniae), чувствительные к пенициллину (МПК ≤0,12 мкг/мл), могут считаться чувствительными к эртапенему. Тестирование изолятов с промежуточной чувствительностью к пенициллину или пенициллин-резистентных изолятов на чувствительность к эртапенему не рекомендуется, поскольку надежные критерии интерпретации для эртапенема отсутствуют.
- d Бета-гемолитические Streptococcus spp., чувствительные к пенициллину (диаметр зоны 10 ЕД пенициллинового диска ≥24 мм) могут считаться чувствительными к эртапенему. Изоляты с диаметром зоны 10 ЕД пенициллинового диска ≤24 мм должны тестироваться на чувствительность к эртапенему методом определения МПК. Критерии интерпретации пенициллинового дискодиффузионного метода не применимы для стрептококков группы viridans, которые не следует тестировать в отношении эртапенема.
- e Эти стандарты интерпретации применимы к процедуре микродилюции бульона с использованием среды Haemophilus Test Medium (НТМ), инокулированной суспензией чистой колонии с инкубацией на воздухе при температуре 35 °C в течение 20-24 часов.
- f Эти диаметры зон применимы к тестам с использованием дискодиффузионного метода на НТМ агаре, инокулированном суспензией чистых колоний с инкубацией в 5% СО2 при 35 °C в течение 16-18 часов.
- g Эти стандарты интерпретации применимы только к дилюции агара с использованием агара Brucella с добавлением гемина, витамина К1 и 5% дефибринированной или гемолизированной крови барана, инокулированного суспензией чистой колонии, или 6-24 часовой свежей культуре в обогащенной тиогликолатом среде при инкубации в анаэробном контейнере или камере при 35-37 °C в течение 42- 48 часов.
Фармакокинетика
Всасывание
Эртапенем, растворенный в 1% растворе Лидокаина (без эпинефрина), хорошо абсорбируется после в/м введения в рекомендованной дозе 1 г. Биодоступность составляет приблизительно 92%. После в/м введения 1 г в день максимальная концентрация в плазме (Сmax) достигается приблизительно через 2 часа (Тmax).
Распределение
Эртапенем в значительной степени связывается с белками плазмы крови человека (связь эртапенема с белками уменьшается по мере повышения его концентрации в плазме крови примерно с 95% при концентрации в плазме крови <100 мкг/мл до 85% при концентрации в плазме крови около 300 мкг/мл).
Средние концентрации (мкг/мл) в плазме крови эртапенема после однократной 30-минутной в/в инфузии дозы 1 г или 2 г и в/м введения разовой дозы 1 г здоровым добровольцам представлены в таблице:
| Концентрация эртапенема в плазме у взрослых после введения разовой дозы | |||||||||
| Доза — Способ введения | Средние концентрации в плазме (мкг/мл) | ||||||||
| 0,5 ч | 1 ч | 2 ч | 4 ч | 6 ч | 8 ч | 12 ч | 18 ч | 24 ч | |
| 1 г — в/в* | 155 | 115 | 83 | 48 | 31 | 20 | 9 | 3 | 1 |
| 1 г — в/м | 33 | 53 | 67 | 57 | 40 | 27 | 13 | 4 | 2 |
| 2 г — в/в* | 283 | 202 | 145 | 86 | 58 | 36 | 16 | 5 | 2 |
| * в/в инфузия проводилась при постоянной скорости в течение 30 минут |
Площадь под фармакокинетической кривой «концентрация-время» эртапенема в плазме крови (AUC) у взрослых пациентов увеличивается почти прямо пропорционально дозе в диапазоне доз от 0,5 г до 2 г.
Кумуляции эртапенема у взрослых пациентов после многократного в/в введения в диапазоне доз от 0,5 г до 2 г в день или в/м введения по 1 г в день не наблюдается. Средние концентрации (мкг/мл) в плазме эртапенема у детей представлены в таблице:
|
Концентрация эртапенема в плазме у детей после внутривенного введения разовой дозы* |
||||||||
| Возраст/доза | Средние концентрации в плазме (мкг/мл) | |||||||
| 0,5 ч | 1 ч | 2 ч | 4 ч | 6 ч | 8 ч | 12 ч | 24 ч | |
| 3-23 месяца | ||||||||
| (15 мг/кг)** | 103,8 | 57,3 | 43,6 | 23,7 | 13,5 | 8,2 | 2,5 | — |
| (20 мг/кг)** | 126,8 | 87,6 | 58,7 | 28,4 | — | 12,0 | 3,4 | 0,4 |
| (40 мг/кг)*** | 199,1 | 144,1 | 95,7 | 58,0 | — | 20,2 | 7,7 | 0,6 |
| 2-12 лет | ||||||||
| (15 мг/кг)** | 113,2 | 63,9 | 42,1 | 21,9 | 12,8 | 8,2 | 2,5 | — |
| (20 мг/кг)** | 147,6 | 97,6 | 63,2 | 34,5 | — | 12,3 | 4,9 | 0,5 |
| (40 мг/кг)*** | 241,7 | 152,7 | 96,3 | 55,6 | — | 18,8 | 7,2 | 0,6 |
| 13-17 лет | ||||||||
| (20 мг/кг)** | 170,4 | 98,3 | 67,8 | 40,4 | — | 16,0 | 7,0 | 1,1 |
| (1 г) | 155,9 | 110,9 | 74,8 | — | 24,0 | — | 6,2 | — |
| (40 мг/кг)*** | 255,0 | 188,7 | 127,9 | 76,2 | — | 31,0 | 15,3 | 2,1 |
| * — в/в инфузия проводилась при постоянной скорости в течение 30 минут ** — до максимальной дозы 1 г/сутки *** — до максимальной дозы 2 г/сутки |
Объем распределения эртапенема у взрослых пациентов — около 8 литров (0,11 л/кг), у детей в возрасте от 3 месяцев до 13 лет — 0,2 л/кг и около 0,16 л/кг у детей в возрасте 13-17 лет.
Концентрация эртапенема в грудном молоке у пяти кормящих женщин, определяемая ежедневно в случайных временных точках последовательно в течение 5 дней после последнего внутривенного введения дозы 1 г, составляла в последний день лечения (через 5-14 дней после родов) <0,38 мкг/мл. К 5-му дню после прекращения лечения концентрация эртапенема у 4 женщин была ниже предела обнаружения, а у 1 женщины обнаруживались следовые количества (<0,13 мкг/мл).
Эртапенем не подавляет транспорт дигоксина и винбластина, опосредованный Р-гликопротеином, и сам не является субстратом этого транспорта.
Метаболизм
После в/в инфузии 1 г эртапенема с изотопной меткой источником радиоактивности в плазме является в основном (94%) эртапенем. Основной метаболит эртапенема представляет собой производное с незамкнутым кольцом, образующееся при гидролизе бета-лактамного кольца.
Исследования in vitro микросом печени человека показывают, что эртапенем не ингибирует метаболизм, опосредованный шестью основными изоферментами цитохрома Р450 (CYP)— 1А2, 2С9, 2С19, 2D6, 2Е1 и 3А4.
Выведение
Эртапенем выводится главным образом почками. Среднее время полувыведения в плазме крови у здоровых молодых добровольцев и детей в возрасте 13-17 лет составляет около 4 часов, у детей в возрасте от 3 месяцев до 13 лет — около 2,5 часов. После в/в введения 1 г эртапенема с изотопной меткой здоровым молодым добровольцам около 80% препарата выводится почками, а 10% — через кишечник. Из 80% эртапенема, определяемого в моче, около 38% выделяется в виде неизмененного препарата, а около 37% — в виде метаболита с незамкнутым β-лактамным кольцом.
У здоровых молодых добровольцев, получивших в/в дозу 1 г, средняя концентрация эртапенема в моче в течение 0-2 часов после введения этой дозы превышает 984 мкг/мл, а в течение 12-24 часов после введения этой дозы превышает 52 мкг/мл.
Особенности фармакокинетики у отдельных групп пациентов
Концентрация эртапенема в плазме у мужчин и женщин сопоставима.
Концентрация эртапенема в плазме после в/в введения дозы 1 г и 2 г у пожилых пациентов (≥65 лет) немного выше (приблизительно на 39% и 22% соответственно), чем у более молодых (<65 лет). Коррекции дозы для пожилых пациентов не требуется.
После внутривенного введения препарата в дозе 1 г/сут концентрация эртапенема в плазме крови у детей 13-17 лет и взрослых пациентов сопоставима.
После назначения препарата в дозе 20 мг/кг (до максимальной дозы 1 г) значения фармакокинетических параметров у пациентов в возрасте 13-17 лет в целом были сравнимы с таковыми у здоровых молодых добровольцев. Трое из шести пациентов 13- 17 лет получали дозу менее 1 г. Для оценки фармакокинетических критериев у всех пациентов данной группы полученные показатели были рассчитаны с учетом того, что все пациенты получали дозу препарата 1 г, с допущением линейной зависимости. Результаты сравнения показывают, что фармакокинетический профиль у пациентов 13- 17 лет, получавших эртапенем в дозе 1 г/сут, был сопоставим с таковым у взрослых пациентов. Соотношения (пациенты 13-17 лет / взрослые пациенты) для значений AUC, концентрации в конце введения инфузии и концентрации в середине интервала дозирования составили 0,99, 1,20 и 0,84 соответственно.
Концентрации в плазме крови в середине интервала дозирования после однократного внутривенного введения эртапенема в дозе 15 мг/кг у пациентов в возрасте от 3 месяцев до 13 лет сравнимы с данными концентрациями в середине интервала дозирования после внутривенного введения препарата в дозе 1 г/сут у взрослых. Клиренс эртапенема из плазмы крови (мл/мин/кг) у пациентов в возрасте от 3 месяцев до 13 лет был приблизительно в 2 раза больше в сравнении с таковым у взрослых пациентов. При введении дозы 15 мг/кг значения AUC у пациентов в возрасте от 3 месяцев до 13 лет были сравнимы с данными значениями у молодых здоровых добровольцев, принимавших эртапенем внутривенно в дозе 1 г.
Пациенты с печеночной недостаточностью
Фармакокинетика эртапенема у пациентов с печеночной недостаточностью не изучалась. В связи с небольшой интенсивностью метаболизма препарата в печени можно ожидать, что нарушение ее функции не должно влиять на фармакокинетику эртапенема. Коррекции режима дозирования у пациентов с печеночной недостаточностью не требуется.
Пациенты с почечной недостаточностью
После однократного в/в введения 1 г эртапенема AUC у пациентов с почечной недостаточностью легкой степени (клиренс креатинина Clcr 60-90 мл/мин/1,73 м2) не отличается от таковой у здоровых добровольцев (в возрасте от 25 до 82 лет).
- У пациентов с умеренной почечной недостаточностью (Clcr 31-59 мл/мин/1,73 м2) AUC увеличена приблизительно в 1,5 раза по сравнению со здоровыми добровольцами.
- У пациентов с тяжелой почечной недостаточностью (Clcr 5-30 мл/мин/1,73 м2) AUC увеличена приблизительно в 2,6 раза по сравнению со здоровыми добровольцами.
- У пациентов с терминальной стадией почечной недостаточности (Clcr <10 мл/мин/1,73 м2) AUC увеличена приблизительно в 2,9 раза по сравнению со здоровыми добровольцами.
После однократного в/в введения разовой дозы 1 г эртапенема непосредственно перед сеансом гемодиализа около 30% введенной дозы определяется в диализате.
Данные о применении препарата у детей с почечной недостаточностью отсутствуют. Пациентам с тяжелой и терминальной почечной недостаточностью рекомендуется проводить коррекцию режима дозирования.
Показания к применению
Инванз показан для лечения пациентов с тяжелыми и средней тяжести инфекциями, вызванными чувствительными штаммами микроорганизмов, в том числе для стартовой эмпирической антибактериальной терапии до определения бактериальных возбудителей, при нижеперечисленных инфекциях:
- интраабдоминальные инфекции;
- инфекции кожи и подкожной клетчатки, включая инфекции нижних конечностей при сахарном диабете («диабетическая» стопа);
- внебольничная пневмония;
- инфекции мочевыделительной системы, включая пиелонефрит;
- острые инфекции органов малого таза, включая послеродовый эндомиометрит, септический аборт и пост-хирургические гинекологические инфекции;
- бактериальная септицемия.
Противопоказания
- Повышенная чувствительность к эртапенему или другим компонентам препарата, к другим препаратам класса карбапенемов, повышенная чувствительность (например, анафилактические реакции, тяжелые кожные реакции) на любой другой антибиотик бета-лактамной группы (например, пенициллины или цефалоспорины).
- Инванз не рекомендован для применения у детей в возрасте младше 3 месяцев в связи с недостаточной изученностью эффективности и безопасности.
- При использовании в качестве растворителя Лидокаина внутримышечное введение препарата Инванз противопоказано пациентам с известной гиперчувствительностью к амидным анестетикам местного действия, пациентам с тяжелой артериальной гипотензией или нарушением внутрисердечной проводимости.
Побочные действия
Нежелательные явления (возможно, вероятно или определенно связанные с применением препарата) были отмечены примерно у 20% пациентов, принимавших эртапенем. В связи с нежелательными явлениями эртапенем отменяли у 1,3% пациентов. Наиболее частые нежелательные явления, связанные с применением эртапенема при его парентеральном введении, включали диарею (4,8%), местные постинфузионные венозные осложнения (4,5%) и тошноту (2,8%).
Профиль эффективности и безопасности препарата Инванз у детей был сопоставим с таковым у взрослых пациентов. Нежелательные явления (возможно, вероятно или определенно связанные с применением препарата) были отмечены примерно у 20,8% пациентов, принимавших эртапенем.
В связи с нежелательными явлениями эртапенем отменяли у 0,5% пациентов.
Наиболее частые нежелательные явления, связанные с применением эртапенема при его парентеральном применении, включали диарею (5,2%) и боль в месте введения (6,1%).
Нежелательные явления, зарегистрированные в ходе лечения пациентов препаратом Инванз, классифицированы по частоте:
- часто (≥1/100, <1/10);
- нечасто (≥1/1000, <1/100);
- редко (≥1/10000, <1/1000);
- очень редко (<1/10000),
- частота неизвестна.
| Взрослые | Дети | |
| Инфекционные и паразитарные заболевания |
|
|
| Нарушения со стороны крови и лимфатической системы |
|
|
| Нарушения со стороны иммунной системы |
|
|
| Нарушения со стороны обмена веществ и питания |
|
|
| Нарушения психики |
|
|
| Нарушения со стороны нервной системы |
|
|
| Нарушения со стороны органа зрения |
|
|
| Нарушения со стороны сердца |
|
|
| Нарушения со стороны сосудов |
|
|
| Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
|
|
| Нарушения со стороны желудочно-кишечного тракта |
|
|
| Нарушения со стороны печени и желчевыводящих путей |
|
|
| Нарушения со стороны кожи и подкожных тканей |
|
|
| Нарушения со стороны скелетно-мышечной и соединительной ткани |
|
|
| Нарушения со стороны почек и мочевыводящих путей |
|
|
| Беременность, послеродовые и перинатальные состояния |
|
|
| Нарушения со стороны половых органов и молочной железы |
|
|
| Общие расстройства и нарушения в месте введения |
|
|
Лабораторные показатели
У взрослых наиболее часто наблюдаемыми отклонениями результатов лабораторных анализов, связанными с препаратом Инванз, были повышение активности АЛТ (аланинаминотрансферазы) (4,6%), ACT (аспартатаминотрансферазы) (4,6%), щелочной фосфатазы (3,8%) и количества тромбоцитов (3,0%).
У детей наиболее часто наблюдаемыми отклонениями результатов лабораторных анализов, связанными с препаратом Инванз, были уменьшение количества нейтрофилов (3,0%), повышение активности АЛТ (2,9%) и ACT (2,8%).
| Взрослые | Дети | |
| Химические показатели |
|
|
| Гематология |
|
|
| Анализ мочи |
|
|
| Другое |
|
Способ применения и дозировка
Обычная суточная доза препарата Инванз для пациентов в возрасте 13 лет и старше составляет 1 г, кратность введения — 1 раз в сутки. Доза препарата Инванз у пациентов в возрасте от 3 месяцев до 13 лет составляет 15 мг/кг 2 раза в сутки (но не более 1 г в сутки). Инванз можно вводить путем внутривенной инфузии или внутримышечной инъекции. При внутривенной инфузии препарата Инванз длительность инфузии должна составлять 30 минут.
Внутримышечное введение препарата Инванз может использоваться как альтернатива внутривенной инфузии.
Обычная продолжительность терапии препаратом Инванз составляет от 3 до 14 дней в зависимости от вида заболевания и вызвавшего его патогенного микроорганизма (микроорганизмов). При наличии клинических показаний допустим переход на последующую адекватную пероральную антимикробную терапию в случае клинического улучшения.
Инванз может применяться для лечения инфекций у взрослых пациентов с почечной недостаточностью. У пациентов с клиренсом креатинина более 30 мл/мин/1,73 м2 коррекции режима дозирования не требуется.
Взрослые пациенты с выраженной почечной недостаточностью (клиренс креатинина менее или равен 30 мл/мин/1,73 м2), включая тех, кто находится на гемодиализе, должны получать 500 мг в сутки. Нет данных о применении препарата у детей с почечной недостаточностью.
Взрослым пациентам, находящимся на гемодиализе и получившим рекомендуемую суточную дозу препарата Инванз 500 мг в течение 6 часов перед сеансом гемодиализа, рекомендуется дополнительное введение 150 мг препарата после сеанса гемодиализа. Если препарат Инванз вводится за 6 часов или ранее до гемодиализа, введения дополнительной дозы не требуется. В настоящее время нет достаточных данных по рекомендации пациентам, подвергающимся перитонеальному диализу или гемофильтрации. Нет данных о применении препарата у детей, находящихся на гемодиализе.
Если известна концентрация креатинина в сыворотке, то для расчета клиренса креатинина можно применять следующие формулы:
- Мужчины: [ (вес в кг) х (140 — возраст в годах) ] / [ (72) х креатинин сыворотки (мг/100 мл) ]
- Женщины: (0,85) х (величина, рассчитанная для мужчин)
Для пациентов с нарушенной функцией печени коррекции дозы не требуется.
Рекомендуемую дозу препарата Инванз можно вводить без учета возраста (13 лет и старше) и пола.
Применение у детей в возрасте младше 3 месяцев не рекомендуется (в связи с недостаточной изученностью эффективности и безопасности).
В клинических исследованиях эффективность и безопасность препарата Инванз у пожилых пациентов (≥65 лет) были сопоставимы с таковыми у более молодых пациентов (<65 лет).
Приготовление растворов (от 13 лет и старше)
Приготовление раствора для внутривенной инфузии
Не смешивать и не вводить вместе с другими лекарственными средствами.
Не использовать растворители, содержащие декстрозу (α-D-глюкозу).
Перед введением препарат Инванз необходимо растворить, а затем развести.
- Растворите содержимое 1 г флакона препарата Инванз путем добавления 10 мл одного из следующих растворителей: вода для инъекций, 0,9% раствор натрия хлорида для инъекций или бактериостатическая вода для инъекций.
- Хорошо встряхните флакон до полного растворения препарата и сразу же добавьте раствор из флакона в подготовленные 50 мл 0,9% раствора натрия хлорида для инфузий.
- Инфузия должна быть выполнена в течение 6 часов после растворения препарата Инванз.
Приготовление раствора для внутримышечной инъекции
Перед введением препарат Инванз необходимо растворить.
- Растворите содержимое флакона, содержащего 1 г препарата Инванз, в 3,2 мл 1% или 2% раствора лидокаина для инъекций (без эпинефрина). Хорошо встряхните флакон для растворения содержимого.
- Сразу же наберите в шприц содержимое флакона и введите его глубоко внутримышечно в крупный мышечный массив (например, в ягодичные мышцы или латеральные мышцы бедра).
- Приготовленный раствор для в/м введения должен быть использован в течение 1 часа после приготовления.
Примечание: приготовленный раствор для в/м инъекций не должен использоваться для в/в инфузий.
Приготовление растворов (дети от 3 месяцев до 13 лет)
Приготовление раствора для внутривенной инфузии
Не смешивать и не вводить вместе с другими лекарственными средствами.
Не использовать растворители, содержащие декстрозу (α-D-глюкозу).
Перед введением препарат Инванз необходимо растворить, а затем развести.
- Растворите содержимое 1 г флакона препарата Инванз путем добавления 10 мл одного из следующих растворителей: вода для инъекций, 0,9% раствор натрия хлорида для инъекций или бактериостатическая вода для инъекций.
- Хорошо встряхните флакон до полного растворения препарата и сразу же наберите объем раствора, эквивалентный 15 мг/кг веса (но не более 1 г в сутки) и разбавьте в 0,9% растворе натрия хлорида для инфузий до концентрации 20 мг/мл или менее.
- Инфузия должна быть выполнена в течение 6 часов после растворения препарата Инванз.
Приготовление раствора для внутримышечной инъекции
Перед введением препарат Инванз необходимо растворить.
- Растворите содержимое флакона, содержащего 1 г препарата Инванз, в 3,2 мл 1% или 2% раствора лидокаина для инъекций (без эпинефрина). Хорошо встряхните флакон для растворения содержимого.
- Сразу же отберите объем, эквивалентный 15 мг/кг тела (но не более 1 г в сутки) и введите его глубоко внутримышечно в крупный мышечный массив (например, в ягодичные мышцы или латеральные мышцы бедра).
- Приготовленный раствор для в/м введения должен быть использован в течение 1 часа после приготовления.
Примечание: приготовленный раствор для в/м инъекций не должен использоваться для в/в инфузий.
Лекарственные препараты для парентерального введения перед использованием нужно подвергать визуальному осмотру для выявления взвешенных частиц или изменений окраски. Цвет растворов препарата Инванз варьируется от бесцветного до бледно-желтого (изменение цвета в этих пределах не влияет на активность препарата).
Передозировка
Специфической информации по лечению передозировки препарата Инванз нет. В клинических исследованиях случайное введение до 3 г в сутки взрослым не приводило к клинически значимым нежелательным явлениям. В клинических исследованиях у детей однократное в/в введение дозы от 40 мг/кг до максимальной дозы 2 г не вызывало токсических реакций.
В случае передозировки препарата Инванз его следует отменить и проводить общее поддерживающее лечение до выведения лекарства почками.
Инванз можно удалить из организма путем гемодиализа. Однако информации о применении гемодиализа для лечения передозировки не имеется.
Взаимодействие
При применении эртапенема с пробенецидом пробенецид конкурирует за активную канальцевую секрецию и таким образом ингибирует почечную экскрецию эртапенема. Это ведет к небольшому, но статистически значимому увеличению периода полувыведения (19%) и выраженности системного действия (25%). Коррекции режима дозирования не требуется. Одновременное применение с пробенецидом в целях увеличения периода полувыведения не рекомендуется.
Исследования in vitro показывают, что эртапенем не ингибирует транспорт дигоксина и винбластина, опосредованный Р-гликопротеином, и что эртапенем не является субстратом для этого транспорта. Исследования in vitro микросом печени человека показывают, что эртапенем не ингибирует метаболизм, опосредованный шестью основными изоферментами цитохрома Р450 (CYP)— 1А2, 2С9, 2С19, 2D6, 2Е1 и ЗА4. Взаимодействие с лекарственными средствами, обусловленное ингибированием Р-гликопротеин-опосредованного выведения препаратов или CYP-опосредованного выведения препаратов, маловероятно.
Специальных клинических исследований по взаимодействию с конкретными лекарственными средствами, кроме пробенецида, не проводилось.
Клинические случаи, описанные в литературе, показывают, что одновременное применение карбапенемов, включая эртапенем, с вальпроевой кислотой или дивальпроатом натрия приводит к снижению концентрации вальпроевой кислоты. В результате этого взаимодействия концентрация вальпроевой кислоты может оказаться ниже терапевтического уровня, что увеличивает риск развития судорожного припадка. Хотя механизм взаимодействия неизвестен, данные in vitro и результаты исследований на животных позволяют предположить, что карбапенемы могут ингибировать гидролиз, в результате которого глюкуронидный метаболит вальпроевой кислоты (VPA-g) превращается обратно в вальпроевую кислоту, что приводит к снижению концентрации вальпроевой кислоты в плазме крови.
Условия продажи
Отпускают по рецепту.
Условия хранения
Неоткрытые флаконы (до растворения) хранить при температуре не выше 25 °C.
Раствор для инфузий, приготовленный путем немедленного разведения в 0,9% растворе натрия хлорида для инъекций, можно хранить при комнатной температуре (25 °C) и использовать в течение 6 часов или хранить в течение 24 часов в холодильнике (5 °C) и использовать в течение 4 часов после извлечения из холодильника.
Растворы препарата Инванз нельзя замораживать.
Раствор для в/м инъекций должен быть использован в течение 1 часа после приготовления.
Хранить в недоступном для детей месте.
Срок годности
2 года. Не использовать препарат по истечении срока годности.
Особые указания
Сообщалось о серьезных и летальных анафилактических реакциях у пациентов, получавших лечение бета-лактамными антибиотиками. Эти реакции более вероятны у лиц с повышенной чувствительностью к различным аллергенам в анамнезе (в частности, у лиц с гиперчувствительностью к Пенициллину часто развиваются тяжелые реакции гиперчувствительности при лечении другими бета-лактамами). Перед началом лечения препаратом Инванз следует тщательно расспросить пациента о предшествующих реакциях гиперчувствительности на другие аллергены, особенно на пенициллины, цефалоспорины и другие бета-лактамы.
При возникновении аллергической реакции на препарат Инванз его следует немедленно отменить. Серьезные анафилактические реакции требуют экстренного лечения.
В ходе лечения препаратом Инванз зарегистрированы сообщения о судорогах и других побочных реакциях со стороны центральной нервной системы. В ходе клинических исследований у взрослых пациентов, принимавших Инванз (1 г 1 раз в день), судороги, как связанные, так и не связанные с применением препарата, отмечались у 0,5% пациентов в течение курса терапии плюс 14 дней периода наблюдения. Эти явления наиболее часто отмечались у пожилых пациентов, у пациентов с нарушениями ЦНС (например, с поражениями головного мозга или судорогами в анамнезе) и/или у пациентов с нарушенной функцией почек. Необходимо строго придерживаться рекомендуемого режима дозирования, в особенности у пациентов с известной предрасположенностью к судорожной активности. У пациентов с судорожными расстройствами следует продолжать противосудорожную терапию. При возникновении тремора, миоклонии или судорог пациентов следует направить на неврологическое обследование и оценить необходимость уменьшения дозы препарата Инванз или отмены препарата.
Увеличение дозы вальпроевой кислоты или дивальпроата натрия может оказаться недостаточным для преодоления последствий взаимодействия. Одновременное применение эртапенема и вальпроевой кислоты/дивальпроата натрия не рекомендуется. Следует рассмотреть возможность лечения инфекций антибиотиками других групп (не карбапенемов) у пациентов, получающих противосудорожную терапию вальпроевой кислотой или дивальпроатом натрия.
При необходимости применения препарата Инванз может потребоваться проведение дополнительной противосудорожной терапии.
Длительное применение препарата Инванз, как и других антибиотиков, может привести к избыточному росту нечувствительных микроорганизмов. Если во время лечения развилась суперинфекция, нужно принять соответствующие меры.
При применении почти всех антибактериальных препаратов, включая эртапенем, возможно развитие псевдомембранозного колита, который по тяжести может варьировать от легкого до опасного для жизни. Важно рассматривать возможность такого диагноза у пациентов, поступающих с диареей после применения антибактериальных препаратов. Следует рассмотреть возможность прекращения терапии препаратом Инванз и назначения специфического лечения колита, вызванного Clostridium difficile. Нельзя применять лекарственные средства, тормозящие перистальтику кишечника.
При внутримышечном введении препарата Инванз следует соблюдать осторожность, чтобы избежать его случайного введения в кровеносный сосуд.
Растворителем для внутримышечного введения препарата Инванз является раствор лидокаина.
Не проводилось исследований для оценки влияния на способность управлять транспортными средствами и работать с механизмами, однако некоторые нежелательные реакции, наблюдавшиеся при применении препарата Инванз, такие как головокружение и сонливость, могут влиять на способность управлять транспортными средствами и работать с механизмами.
Аналоги Инванза
Совпадения по коду АТХ 4-го уровня:
К препаратам с аналогичным фармакологическим действием относятся:
- Европенем
- Ластинем
- Мепенам
- Инемплюс
- Меробоцид
- Меромек
- Мероспен
- Препенем
- Ронем
- Тиенам
- Синерпен
При беременности и лактации
Достаточного клинического опыта по применению препарата у беременных женщин не имеется. Инванз следует применять во время беременности, только если возможная польза для матери оправдывает потенциальный риск для плода.
Эртапенем выделяется с грудным молоком. Ввиду возможного неблагоприятного воздействия препарата на плод, в период лактации грудное вскармливание следует прекратить на период применения препарата.
Отзывы об Инванзе
Отзывы о препарате у большинства пациентов положительные. Препарат эффективен при многих инфекционно-воспалительных заболеваниях.
- «… Антибиотик Инванз врач назначил мне после диагноза пиелонефрит. Колола препарат 9 дней. Эффект хороший, исчезли боли в области поясницы, температура нормализовалась, анализы значительно улучшились. Отличный препарат».
Из негативных моментов многие пациенты отмечают его высокую стоимость.
Цена Инванза, где купить
Цена лиофилизата Инванз 1 г для инъекций варьирует в пределах 2500 рублей за упаковку. Купить Инванз в большинстве аптек Москвы и других городах можно без проблем.
- Интернет-аптеки РоссииРоссия
ЛюксФарма* специальное предложение
-
Инванз лиофилизат д/пригот р-ра д/инъекц 1г 20мл фл 1шт
показать еще
Выберите тип аналогов (синонимов), чтобы получить список препаратов.
Аналоги по действующему веществу — препараты, которые содержат одно и то же активное вещество, но выпускаются под разными торговыми наименованиями.
Для того чтобы подобрать полный аналог по действующему веществу, необходимо также выбрать дозировку и лекарственную форму.
Аналоги по фармгруппе — препараты, которые содержат разные действующие вещества, но относятся к одной фармакологической группе и применяются по одинаковым
показаниям.
Аналоги по АТХ — препараты, относящиеся к одному уровню АТХ-классификации.
Информация на сайте Medum.ru – справочная. Содержимое сайта Medum.ru – инструкции, текст, графика, видео, изображения предназначены исключительно для справочных целей. Информация, размещённая на сайте Medum.ru не предназначена для замены профессиональной медицинской консультации, диагностики или лечения. Обязательно обращайтесь к медицинским специалистам и не откладывайте их поиск из-за того, что вы прочитали на сайте Medum.ru. Medum.ru не рекомендует и не одобряет какие-либо лекарственные средства, биологически активные добавки, гомеопатические средства, тесты, врачей, медицинские учреждения, аптеки, отзывы, мнения, комментарии и другую информацию упомянутую на сайте. Внешний вид препаратов (фото и видео) и инструкции могут отличаться от опубликованных и могут зависеть от производителя, упаковки, дозировки, форм выпуска. Обязательно консультируйтесь с медицинскими специалистами.
Medum.ru — справочник лекарственных препаратов. Всё о здоровье, отзывы, мнения, вопросы и ответы, а также другие полезные разделы и сервисы.
Все права защищены. 2016–2023 © ООО «Медум.ру» (Ltd. Medum.ru)
Медум® (Medum®)

