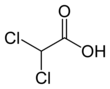
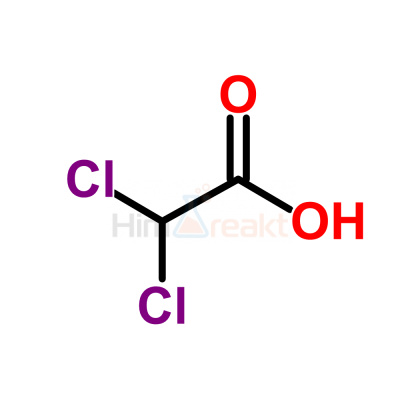
Синонимы: Дихлорэтановая кислота
Брутто-формула C2H2Cl2O2
Квалификация 99%
500 р/кг
Дихлоруксусная кислота CAS 79-43-6
Цена не указана.
+ Владелец? Добавьте оптовую или розничную цены.
г.Санкт-Петербург, Октябрьская наб., д.26, лит.А, пом. 12-Н
07.09.2016
Санкт-Петербург, пр. Обуховской обороны, 101
+7 921 911 25 47
+7 921 911 25 48
Пн-Пт: 10:00-18:00 Сб,Вс: выходной
Молекулярный вес: 128.94
Растворимость в воде, гр/100мл, при 20°C: растворим
Растворимость в других растворителях: смешивается со спиртом, эфиром, этанолом; раств. в ацетоне
Применяется в качестве полупродукта в органическом синтезе. Как саму кислоту, так и её производные используют в производстве косметических и лекарственных средств. Обладает высокой антивирусной и противогрибковой активностью.
Фасовка- пластиковая бочка 250 кг
Опт (от 1 тонны)
|
||
| Имена | ||
|---|---|---|
| Название IUPAC Дихлоруксусная кислота | ||
| Другие названия Дихлорэтановая кислота, бихлоруксусная кислота, DCA, BCA, дихлоруксусная кислота, бихлоруксусная кислота | ||
| Идентификаторы | ||
| Номер CAS |
|
|
| 3D-модель (JSmol ) |
|
|
| Ссылка Beilstein | 1098596 | |
| ChEBI |
|
|
| ChEMBL |
|
|
| ChemSpider |
|
|
| DrugBank |
|
|
| ECHA InfoCard | 100.001.098 |
|
| Номер EC |
|
|
| Справочник Гмелина | 2477 | |
| КЕГГ |
|
|
| МеШ | Дихло роацетат | |
| PubChem CID |
|
|
| номер RTECS |
|
|
| UNII |
|
|
| номер ООН | 1764 | |
| приборная панель CompTox (EPA ) |
|
|
InChI
|
||
| Свойства | ||
| Химическая формула | C2H2Cl2O2 | |
| Молярная масса | 128,94 г · моль | |
| Внешний вид | Бесцветная жидкость | |
| Плотность | 1,5634 г / см (20 ° C) | |
| Температура плавления | от 9 до 11 ° C (от 48 до 52 ° F; От 282 до 284 K) | |
| Температура кипения | 194 ° C (381 ° F; 467 K) | |
| Растворимость в воде | смешивается | |
| Растворимость | смешивается с этанолом, диэтиловый эфир | |
| Кислотность (pK a) | 1,35 | |
| Магнитная восприимчивость (χ) | -58,2 · 10 см / моль | |
| Термохимия | ||
| Стандартная энтальпия. образование (ΔfH298) | -496,3 кДж · моль | |
| Опасности | ||
| Паспорт безопасности | MSDS (jtbaker) | |
| Пиктограммы GHS |   |
|
| Сигнальное слово GHS | Предупреждение | |
| Формулировки опасности GHS | H314, H400 | |
| Меры предосторожности GHS | P260, P264, P273, P280, P301 + 330 + 331, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P310, P321, P363, P391, P405, P501 | |
| NFPA 704 (огненный алмаз) |  1 3 0 1 3 0 |
|
| Родственные соединения | ||
| Родственные хлоруксусные кислоты | Хлоруксусная кислота. Трихлоруксусная кислота | |
| Родственные соединения | Уксусная кислота. Дифторуксусная кислота. | |
| За исключением других Как отмечалось, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | ||
| Ссылки на ink | ||
Дихлоруксусная кислота (DCA ), иногда называемая бихлоруксусной кислотой (BCA ), является химическим соединением с формулой C H Cl. 2COOH. Это кислота, аналог уксусной кислоты, в которой 2 из 3 атомов водорода метильной группы были заменены на атомы хлора. Как и другие хлоруксусные кислоты, он имеет различные практические применения. соли и сложные эфиры дихлоруксусной кислоты называются дихлорацетатами . Соли DCA были изучены как потенциальные лекарственные препараты, поскольку они ингибируют фермент киназу пируватдегидрогеназы.
, хотя предварительные исследования показали, что DCA может замедлять рост некоторых опухолей в исследования на животных и in vitro исследования, по состоянию на 2012 г. недостаточно доказательств, подтверждающих использование DCA для лечения рака.
Содержание
- 1 Химия и встречаемость
- 2 Терапевтическое применение
- 2.1 Местная химиоаблация
- 2.2 Лактацидоз
- 2.3 Рак
- 2.4 Невропатия
- 2.5 Сердечная недостаточность
- 3 См. Также
- 4 Ссылки
- 5 Внешние ссылки
Химия и возникновение
Химический состав дихлоруксусной кислоты типичен для галогенированных органических кислот. Он принадлежит к семейству хлоруксусных кислот. Ион дихлорацетата образуется при смешивании кислоты с водой. Как кислота с pKa 1,35, чистая дихлоруксусная кислота классифицируется как сильная органическая кислота ; он очень разъедает и чрезвычайно разрушает ткани слизистых оболочек и верхних дыхательных путей при вдыхании.
DCA, как было показано, встречается в природа по крайней мере одной водоросли, Asparagopsis taxiformis. Он является следовым продуктом хлорирования питьевой воды и образуется в результате метаболизма различных хлор содержащих лекарств или химических веществ. DCA обычно получают путем восстановления трихлоруксусной кислоты (TCA). DCA получают из хлоралгидрата также реакцией с карбонатом кальция и цианидом натрия в воде с последующим подкислением соляной кислотой. Его также можно получить, пропуская ацетилен через растворы хлорноватистой кислоты.
В качестве лабораторного реагента и DCA, и TCA используются в качестве осадителей для побуждения макромолекул, таких как белки, к осадок из раствора.
Терапевтическое применение
Местная химиоабляция
И DCA, и TCA используются для косметических процедур (например, химический пилинг и удаление татуировок ) и как лекарство для местного применения для химиоаблации бородавок, включая остроконечные кондиломы. Он также может убивать нормальные клетки.
Лактоацидоз
A рандомизированное контролируемое исследование у детей с врожденным лактоацидозом показало, что, хотя DCA хорошо переносится, оно неэффективно для улучшения клинических исходов. Отдельное испытание DCA у детей с MELAS (синдром неадекватной митохондриальной функции, ведущий к лактоацидозу) было прекращено раньше, так как у всех 15 детей, получавших DCA, было значительно нервная токсичность без каких-либо доказательств пользы от лекарства. Рандомизированное контролируемое исследование DCA у взрослых с лактоацидозом показало, что, хотя DCA снижает уровень лактата в крови, он не имеет клинической пользы и не улучшает гемодинамику или выживаемость.
Таким образом, хотя ранний случай отчеты и доклинические данные свидетельствуют о том, что DCA может быть эффективным при лактоацидозе, последующие контролируемые испытания не обнаружили клинической пользы DCA в этих условиях. Кроме того, субъекты клинических испытаний не могли продолжать прием DCA в качестве исследуемого лекарства из-за прогрессирующей токсичности.
Рак
В 2007 году в прессе и в Интернете появились сообщения о том, что и сотрудники Университета Альберты обнаружили, что дихлоруксусная кислота, а точнее ее натриевая соль, дихлорацетат, уменьшал опухоли у крыс и убивал раковые клетки in vitro. История в New Scientist вызвала «беспрецедентный интерес среди читателей», поскольку в ней говорилось о «дешевом и простом лекарстве», которое было «известно как относительно безопасное» и могло убить большинство видов рака. В сопутствующей редакционной статье указывалось, что ни одна фармацевтическая компания не будет заинтересована в одобрении этого соединения для лечения рака, потому что оно непатентовано. Позже в журнале была опубликована статья, в которой подчеркивалась опасность, связанная с повреждением нервов. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США начало применять закон, запрещающий продажу веществ с предположением, что они являются лекарствами от рака, если они не были одобрены FDA.
The американец Общество рака в 2012 году заявило, что «имеющиеся данные не поддерживают использование DCA для лечения рака в настоящее время». Врачи предупредили о потенциальных проблемах, если люди попытаются попробовать DCA вне контролируемого клинического исследования. Одна из проблем, связанных с этим, — получение химического вещества. Один мошенник был приговорен к 33 месяцам тюремного заключения за продажу белого порошка, содержащего крахмал, но не DCA, больным раком.
Единственная контролируемая дозировка in vivo пяти человек, страдающих от глиобластома с DCA не была разработана для проверки его эффективности против рака. Это исследование было направлено скорее на то, чтобы выяснить, можно ли его безопасно вводить в определенной дозировке, не вызывая побочных эффектов (например, невропатия ). Все пять пациентов получали другое лечение во время исследования. Наблюдения in vitro и опухолей, выделенных у этих пяти пациентов, предполагают, что DCA может действовать против раковых клеток путем деполяризации аномальных митохондрий, обнаруженных в раковых клетках глиобластомы, что позволяет митохондриям вызывать апоптоз (гибель клеток).) злокачественных клеток. Работа in vitro с DCA на нейробластомах (которые имеют меньше выявленных митохондриальных аномалий) показала активность против злокачественных недифференцированных клеток. В отчете о клиническом случае 2016 года обсуждается и рассматривается потенциальное применение DCA при злокачественных новообразованиях центральной нервной системы. Исследование 2018 года показало, что DCA может вызвать метаболический переход от гликолиза (эффект Варбурга ) к митохондриальному OXPHOS и увеличить реактивный кислородный стресс влияющие на опухолевые клетки. Эти эффекты не наблюдались в неопухолевых клетках.
Невропатия
Невропатия была проблемой в некоторых клинических испытаниях, когда DCA заставляла их эффективно останавливаться, но обзор BJC 2008 года показал, что это в других исследованиях DCA не встречался. Механизм нейропатии, вызванной DCA, недостаточно изучен. С одной стороны, работа с нервами in vitro позволила предположить механизм нейропатического эффекта DCA; с DCA, показывающим зависимую от дозы и воздействия демиелинизацию нервов (удаление оболочки нерва), причем демиелинизация была частично обратимой со временем после вымывания DCA. С другой стороны, в обзоре BJC за 2008 г. говорится: «Эта нейротоксичность напоминала модель зависимой от длины аксональной сенсомоторной полинейропатии без демиелинизации». Что касается исследования 2006 г., проведенного Kaufman et al.
Сердечная недостаточность
DCA исследовалась как средство лечения постишемического восстановления. Также есть свидетельства того, что DCA улучшает метаболизм за счет стимуляции выработки NADH, но может привести к истощению NADH при нормоксии.
См. Также
- Далапон (дихлорпропионовая кислота)
Ссылки
Внешние ссылки
- Международная карта химической безопасности 0868
- Справочник
- Справочник структурных формул
- д
- Дихлоруксусная кислота
Дихлоруксусная кислота
Cl<|Cl>/`|O|OH
Cl2CHCOOH
H`-C<`|$dots(!B)Cl><|$dots(!T)Cl>`-C<`\O>`/HO
Брутто-формула: C2H2Cl2O2
Молекулярная масса: 128.942
Химический состав
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| C | Углерод (Carbon) | 12.011 | 2 | 18.6% |
| H | Водород (Hydrogen) | 1.008 | 2 | 1.6% |
| Cl | Хлор (Chlorine) | 35.453 | 2 | 55% |
| O | Кислород (Oxygen) | 15.999 | 2 | 24.8% |
Синонимы
- Дихлоруксусная кислота
- 2,2-Dichloroacetic acid
- Acetic acid, dichloro-(CAS)
- DCA
- Dichloroacetic acid(IUPAC)
- Dichloroethanoic acid
Входит в группы
Карбоновые кислоты Хлорорганические соединения
Дихлоруксусная кислота
Артикул: 79-43-6
Производитель: Не указано
Основное описание
Идентификация
- Название
- Дихлоруксусная кислота
- Регистрационный номер CAS
- 79-43-6
- Молекулярная формула
- C2H2Cl2O2
- Молекулярный вес
- 128.94
- InChI
- InChI=1S/C2H2Cl2O2/c3-1(4)2(5)6/h1H,(H,5,6)
- InChIKey
- JXTHNDFMNIQAHM-UHFFFAOYSA-N
- SMILES
- C(C(=O)O)(Cl)Cl
- EINECS
- 201-207-0
Химические и физические свойства
- Плотность
- 1.575
- Точка кипения
- 194°C
- Точка плавления
- 9-11°C
- Температура вспышки
- 75.552°C
- Температура хранения
- 0-6°C
- Показатель преломления
- 1.4653-1.4673
- Растворимость
- Растворяется в воде.
- Стабильность
- Стабильный. Несовместим с сильными окислителями, сильными основаниями, сильными восстановителями. Реагирует с водой. Защищать от влаги. Гигроскопичен.
- Внешний вид
- Прозрачная бесцветная или светло-желтая жидкость.
Риски, безопасность и условия использования
- Указания по безопасности
- S26; S45; S61
- Указания по риску
- R35; R50
- Класс опасности
- 8
- Символы опасности
Классификация химических реактивов
- Чистый («ч.»)
- Дихлоруксусная кислота Ч. Содержание основного компонента 98% и выше (без примесей). Цвет полосы на упаковке — зелёный.
- Чистый для анализа («ч.д.а.», «чда»)
- Дихлоруксусная кислота ЧДА. Содержание основного компонента выше или значительно выше 98%. Примеси не превышают допустимого предела для точных аналитических исследований. Цвет полосы на упаковке — синий.
- Химически чистый («х.ч.», «хч»)
- Дихлоруксусная кислота ХЧ. Содержание основного компонента более 99%. Цвет полосы на упаковке — красный.
- Особо чистый («осч»)
- Дихлоруксусная кислота ОСЧ. Cодержание примесей в таком незначительном количестве, что они не влияют на основные свойства. Цвет полосы на упаковке — жёлтый.
Форма запроса
Чтобы купить дихлоруксусную кислоту, отправьте запрос
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Дихлоруксусная кислота
БИХЛОРАКУСНАЯ КИСЛОТА
ДИХЛОРАКУСНАЯ КИСЛОТА
ДИХЛОРЭТАНОВАЯ КИСЛОТА
Отправить запросТеперь говорите
Подробная информация о продукции
[Имя]
Дихлоруксусная кислота
[CAS]
79-43-6
[Состав]
[Синонимы]
БИХЛОРАКУСНАЯ КИСЛОТА
ДИХЛОРАКУСНАЯ КИСЛОТА
ДИХЛОРЭТАНОВАЯ КИСЛОТА
RARECHEM AL BO 0413
2,2, -дихлорэтановая кислота
2,2-дихлоруксусная кислота
2,2-дихлоруксусная кислота
Уксусная кислота, дихлор-
Acidedichloracetique
Бихлоруксусная кислота
бихлоруксусная кислота
dca (кислота)
Дихлоруксусная кислота
дихлоруксусная кислота
Дихлорэтановая кислота
дихлорэтановая кислота
дихлор
дихлоруксусный
дихлор-уксусная кислота
Киселина дихлороктова
[EINECS (EC #)]
201-207-0
[Молекулярная формула]
C2H2Cl2O2
[Номер в леях]
MFCD00004223
[Молекулярный вес]
128.94
[Файл MOL]
79-43-6 моль
[Появление]
Бесцветная прозрачная жидкость
[Появление]
DCA — коррозионно-агрессивная горючая бесцветная жидкость с резким запахом.
[mp]
9-11 ° C (лит.)
[bp]
194 ° C (лит.)
[плотность ]
1,563 г / мл при 25 ° C (лит.)
[плотность паров ]
4.5 (по сравнению с воздухом)
[давление газа ]
0,19 мм рт. Ст. (20 ° C)
[показатель преломления ]
n20 / D 1.466 (лит.)
[Fp]
GG gt; 230 ° F
[температура хранения. ]
0-6°C
[Стабильность:]
Стабильный. Несовместим с сильными окислителями, сильными основаниями, сильными восстановителями. Реагирует с водой. Беречь от влаги. Гигроскопичен.
[Растворимость воды ]
растворимый
[Чувствительный ]
Гигроскопичен
[Мерк]
14,3050
[BRN]
1098596
[Ссылка на базу данных CAS]
79-43-6 (Справочная база данных CAS)
[Справочник по химии NIST]
Уксусная кислота, дихлор- (79-43-6)
[Система регистрации веществ EPA]
79-43-6 (вещество EPA)
[Коды опасности]
Xn, N, C, Xi, F
[RIDADR]
ООН 1764 8 / PG 2
[WGK Германия]
2
[RTECS]
AG6125000
[F ]
3-10
[HazardClass]
8
[PackingGroup]
II
[Код ТН ВЭД]
29154000
горячая этикетка : дихлоруксусная кислота, Китай, производители, поставщики, завод, в наличии
сопутствующие товары
-
Метил трифторацетат
-
2-бромметил-1,3-диоксолан 4360-63-8
-
Диметилоксалат 553-90-2
-
Метилгидросилоксан, диметилсилоксан, сополимер, трим…
-
Циклогексимид 66-81-9
-
2,2-бис- (4-цианатофенил) пропан 1156-51-0
Запрос
Copyright © Hangzhou Keying Chem Co., Ltd. Все права защищены.
Дихлоруксусная кислота; Dichloroacetic acid
Номер CAS: 79-43-6
Молекулярная формула: C2H2Cl2O2
Молекулярная масса: 128.94
Для покупки товара в нашем интернет-магазине выберите понравившийся товар и добавьте его в корзину. Далее перейдите в Корзину и нажмите на «Оформить заказ» или «Быстрый заказ».
Когда оформляете быстрый заказ, напишите ФИО, телефон и e-mail. Вам перезвонит менеджер и уточнит условия заказа. По результатам разговора вам придет подтверждение оформления товара на почту или через СМС. Теперь останется только ждать доставки и радоваться новой покупке.
Оформление заказа в стандартном режиме выглядит следующим образом. Заполняете полностью форму по последовательным этапам: адрес, способ доставки, оплаты, данные о себе. Советуем в комментарии к заказу написать информацию, которая поможет курьеру вас найти. Нажмите кнопку «Оформить заказ».
Оплачивайте покупки удобным способом при оформлении заказа в интернет-магазине. Оплата возможна банковскими картами VISA, Mastercard, Maestro, Мир, JSB. А также доступна оплата из электронных кошельков.
У нас вы можете воспользоваться стандартными способами доставки:
- Курьерская доставка по Москве в пределах МКАД. Стоимость = 600 рублей. После согласования вашего заказа с менеджером, он передается курьеру по Москве. Специалист предложит выбрать удобное время доставки и уточнит адрес. Осмотрите упаковку на целостность и соответствие указанной комплектации.
- Самовывоз из магазина. Список торговых точек для выбора появится в корзине. Когда заказ будет укомплектован, вам придет уведомление. Для получения заказа обратитесь к сотруднику в кассовой зоне и назовите номер.
- Постамат. Когда заказ поступит на точку, на ваш телефон или e-mail придет уникальный код. Заказ нужно оплатить в терминале постамата. Срок хранения — 3 дня.
- Транспортные компании. Доставка в регионы осуществляется транспортными компаниями на наше усмотрение или по вашему запросу.
| Дихлоруксусная кислота | |
|---|---|
 |
|
 |
|
| Общие | |
| Хим. формула | C2H2Cl2O2 |
| Физические свойства | |
| Молярная масса | 128,94 г/моль |
| Плотность | 1,5634 г/см³ |
| Термические свойства | |
| Т. плав. | 10 °C и 13,5 °C |
| Химические свойства | |
| pKa | 1,479 |
| Классификация | |
| Рег. номер CAS | 79-43-6 |
| PubChem | 6597 |
| Рег. номер EINECS | 201-207-0 |
| SMILES |
ClC(Cl)C(=O)O |
| InChI |
1S/C2H2Cl2O2/c3-1(4)2(5)6/h1H,(H,5,6) JXTHNDFMNIQAHM-UHFFFAOYSA-N |
| RTECS | AG6125000 |
| ChEBI | 36386 |
| ChemSpider | 10771217 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. |
Дихлоруксусная кислота — химическое вещество с формулой Cl2CHCOOH. Производное уксусной кислоты.
Содержание
- 1 Свойства
- 2 Синтез
-
3 Применение
- 3.1 Потенциальная противоопухолевая активность
- 3.2 Нейротоксичность
- 4 Примечания
Свойства
tпл 10,8 °C (по другим данным 9,5 °C, 13,5 °C), tкип 192—194 °C (с разложением). Растворима в воде (2,63г/100г при 20 °C), спирте, ацетоне, диэтиловом эфире. Плотность 1,57 г/см³ (20 °C).
Сильная органическая кислота, pKa (1) = 1,25 (25 °C, вода).
Является весьма сильным коррозионным агентом. При вдыхании разрушает слизистые оболочки носоглотки и верхних дыхательных путей.
Синтез
В лабораторной практике для синтеза дихлоруксусной кислоты и ее амида используются реакции хлоральгидрата с цианидами.
Так, взаимодействие хлоральгидрата с водным растовром цианида натрия в присутствии карбоната кальция ведет к образованию раствора дихлорацетата, из которого дихлоруксусную кислоту выделяют подкислением и дальнейшей экстракцией эфиром, выходы составляют 88–92%:
- CCl3CH(OH)2 + CN—
CHCl2COO—
Реакция эфирного раствора хлоральгидрата с раствором цианидом калия в концентрированном водном растворе аммиака используется как метод синтеза дихлорацетамида, выходы — 65–78%:
- : CCl3CH(OH)2 + KCN + NH3
CHCl2CONH2
Применение
Находит применение в качестве полупродукта в органическом синтезе, как сама кислота, так и её производные используют в производстве косметических и лекарственных средств.
В качестве лекарственного препарата используются исключительно соли ДХА, а не сама кислота — в силу агрессивности этого вещества.
Кроме того, сама дихлоруксусная кислота обладает высокой антивирусной и противогрибковой активностью. Показано, что при применении в качестве лекарственного препарата, по-крайней мере у мышей, в высоких дозах оказывает канцерогенный эффект. При повышенных дозах оказывает обратимые нейротоксичные эффекты, особенно в периферической нервной системе. В умеренных дозах переносится хорошо .
Потенциальная противоопухолевая активность
Соли дихлоруксусной кислоты (дихлорацетаты натрия и калия) в настоящий момент интенсивно изучаются в качестве экспериментальных противоопухолевых средств. В настоящее время ищут способы снижения токсичности этого препарата и исследования его эффективности при лечении некоторых форм рака. Запатентовать его нельзя (препарат считается общественным достоянием; первые попытки использовать ДХА для лечения собак и попытки лечить им лактацидоз у человека относятся ещё к 1864 году; однако по-крайней мере несколько попыток запатентовать метод лечения уже предпринимались) , поэтому исследования ведутся только на деньги государственных и благотворительных фондов, а также частных лиц и на общественные онлайн-пожертвования.
Для раковых клеток характерно повышение гликолиза, потому что для получения энергии они используют анаэробное дыхание, которое протекает в цитозоли (брожение молочной кислоты), а не Окислительное фосфорилирование в митохондриях (Эффект Варбурга), что приводит к гипоксии, которая существует в опухолях и препятствует работе митохондрий. Обычно опасно повреждённые клетки убивают себя путём апоптоза, механизмом самоуничтожения, который вовлекает митохондрии, но этот механизм нарушается в раковых клетках.
Идея исследовать возможность применения ДХА для лечения лактацидоза возникла в связи с тем фактом, что дихлорацетат-ион способен ингибировать киназу пируватдегидрогеназы, тем самым активируя последний фермент — что должно способствовать восстановлению лактата до пирувата и, в конечном счёте, окислению пирувата в митохондриях. Это было подтверждено до-клиническими испытаниями in vitro и на мышах. Однако первые контролируемые клинические исследования (фазы I) на больных врождённым лактацидозом детях показали, что препарат, хотя обычно и хорошо переносится, каких-либо заметных улучшений не вызывает. В отдельных случаях (дети с синдромом MELAS, иначе — митохондриальной энцефаломиопатией) была показана сильная нейротоксичность препарата — снова без каких-либо убедительных признаков пользы лекарства. Исследования препарата после этого продолжились и некоторая его эффективность была показана .
Потенциальное использование ДХА в организме осложнено его плохой биодоступностью и ограниченной способностью проникнуть в его мишени — митохондрии. Результаты первой фазы испытаний были опубликованы в январе 2007 исследователями из университета Альберта, в них определяли действие ДХА на клетки опухолей человека, перевитых мышам, и показали, что ДХА восстанавливает митохондриальную функицию, таким образом, восстанавливает апоптоз и позволяя раковым клеткам самоликвидироваться и уменьшать размеры опухоли.
Эти результаты привлекли широкое внимание средств массовой информации, начинаясь со статьи в New Scientist названной «Дешёвый ‘безопасный’ препарат убивает большинство опухолей». Впоследствии, к американскому Противораковому обществу и другим медицинским организациям был проявлен большой общественный интерес и им задали много вопросов о ДХА. Клинические испытания у лиц с опухолями не были проведены в США и всё ещё не закончены в Канаде, что подчёркивает необходимость осторожно интерпретировать предварительные результаты.
В 2010 году было показано, что при раке толстой кишки применение ДХА ведёт не к активации апоптоза среди раковых клеток, а к его подавлению — что показывает, что по-крайней мере при некоторых типах рака применение ДХА может вести к пагубным последствиям, и что нужны дополнительные исследования, прежде чем можно будет считать препарат безопасным для лечения рака.
Исследования II фазы показали минимальные побочные эффекты препарата, приемлемый уровень безопасности (за исключением случаев наличия у пациентов некоторых дополнительных патологий и некоторых форм рака) и наличие связи с некоторой степенью регресса опухолей — на фоне неэффективности некоторых других форм химиотерапии. В данный момент проходят исследования фазы III (преимущественно, в Канаде).
Нейротоксичность
Вызываемые препаратом нейропаталогии заключаются в нарушении координации, изменении сознания, иногда — в наступлении летаргии. Показано, что лечение с применением ДХА сопровождается развитием тиаминового истощения . В исследованиях на мышах показано, что при совместном введении тиамина нейротоксичность препарата нивелируется. Однако в исследованиях на людях подобная взаимосвязь не обнаружена. Прекращение приёма ДХА может возвращать координацию и сознание в норму — однако могут наблюдаться длительные (месяцы) изменения величин потенциалов действия в нейронах. Также опубликованы исследования, в которых авторы связывают с нейропатологиями обнаруженный повышенный уровень дельта-аминолевулиновой кислоты в моче. Предполагается, что это может быть связано с блокированием образования периферического миелина.
Может оказывать седативный эффект.